腹腔镜下卵巢皮内荷包缝合与表面贯穿缝合两组不同的缝合方法的对比研究
陈文慧 潘敏
卵巢囊肿是女性生殖系统常见的良性疾病,其发病人群主要集中于20~50岁育龄妇女,严重影响患者的健康[1]。对良性卵巢囊肿行剥除术是该病主要治疗方式,伴随妇产科医疗技术的发展,大部分医疗机构已将腹腔镜微创手术作为卵巢囊肿的首选治疗方案[2],但术中不同止血方式对患者卵巢组织均可造成一定程度的损伤。目前临床卵巢囊肿剥除术中常用的止血方法有双极电凝止血法和缝合止血法[3-4]。本次研究针对不同的缝线及缝合止血手术方式,旨在探寻腹腔镜术中恰当的止血方法。现报告如下。
资料与方法
一、一般资料
选取茂名市人民医院妇科2013年1月至2015年12月收治的行腹腔镜卵巢囊肿剥除术的患者80例,其纳入标准为:(1)妇科常规检查与影像学检查证实为单侧卵巢囊肿,肿瘤直径为5.8 cm~12.0 cm,平均直径为(8.3±1.8)cm;(2)治疗前月经规律、无激素应用史;(3)两组患者年龄范围18~42岁,平均年龄为(32±2.5)岁;(4)按照不同的缝合方式分组(图1): A组40例为0/4微乔小针小线卵巢皮质内荷包缝合; B组40例为用0/3微乔大针卵巢皮质贯穿缝合。
二、手术方法
两组患者术前均行常规临床检查,包括:性激素六项、窦卵泡数,年龄35岁以上查AMH(抗苗勒氏管激素)。所有患者均接受腹腔镜卵巢囊肿剥除术,采取头低臀高截石位,行气管插管全身麻醉,依据囊肿体积判定气腹入路位置。行麦氏点、反麦氏点、耻骨联合上左旁开3cm四孔法,建立气腹并控制压力为 10~12mmHg,选取脐上缘中点部位(若卵巢囊肿大于10cm,取脐上2cm)建立穿刺点,进镜;而后依次建立辅助孔,将5mm套管针置入腹腔内。将手术视野良好暴露,若有卵巢囊肿粘连,尽量小心分离表面粘连,不致囊肿破裂,远离卵巢门附近及避开卵巢表面较粗血管,纵向电切卵巢皮质达囊肿壁表面,钝性分离囊肿间隙与卵巢皮质,囊肿体积较大者或剥离过程破裂者先行囊液吸出,而后将囊壁组织完整剥除取出,尽量多保留卵巢正常组织,较大的明显变薄的卵巢切口周围组织给予冷刀剪除,最后缝合卵巢皮质, A组用0/4可吸收微乔线(小针小线)于卵巢皮质中心部始(靠近卵巢门周围)皮内荷包缝合,卵巢切口周围再用同线第2次荷包缝合,收紧打结后恢复正常卵巢外观,注意每次荷包缝合缝线均不穿透卵巢皮质(图2),若囊肿较大保留卵巢皮质较多者行第3次荷包缝合,相反,若囊肿较小,保留的卵巢面渗血不明显,则只行1次荷包缝合卵巢即可; B组用0/3大针吸收微乔线(缝线较粗)8字贯穿缝合卵巢中心部及切口,或连续贯穿缝合卵巢皮质,全线绑扎式贯穿卵巢皮质表面,渗血明显或囊肿较大的卵巢,需8字缝合5~6针。缝合后观察A组卵巢表面未见缝线,B组卵巢表面有明显且较粗缝线及线结(图3)。
三、 观察指标
记录手术时间、出血量、住院天数手术前与手术后3个月对两组患者开展卵巢功能评估,选择雌二醇(E2)、卵泡刺激素(FSH)、黄体生成素(LH)和窦卵泡计数(AFC)作为判断卵巢功能的指标。双侧卵巢窦卵泡数<5表示卵巢储备功能下降,5~20表示卵巢储备功能正常。持续随访过程中记录患者月经减少、闭经、经期延长与月经淋漓不尽等月经异常发生率。追踪术后6个月两组妊娠情况。
四、统计学方法
结 果
两组患者均成功接受腹腔镜下卵巢囊肿剥除术,术中冰冻病理检查提示卵巢良性肿瘤,术后病理类型包括:卵巢单纯性囊肿38例,卵巢畸胎瘤20例,卵巢巧克力囊肿18例及浆液性囊腺瘤4例。
一、观察两组患者手术时间、术中出血量
A组较B组手术时间短、出血量少,差异有统计学意义(P<0.05),住院天数相当(表1)。
二、两组手术前后卵巢激素水平变化情况比较
A组术前E2、FSH、LH和AFC与术后1个月、3个月相比无显著性差异。B组术前E2和AFC与术后相比逐渐减少,FSH、LH和术后相比逐渐增大,有显著性差异。术后1个月和术后3个月A组的E2、FSH和LH均明显高于B组,但AFC少于B组,差异有统计学意义(P<0.05)(表2)。但是两组患者术前和术后1个月和3个月的卵巢功能均处于正常范围之内。
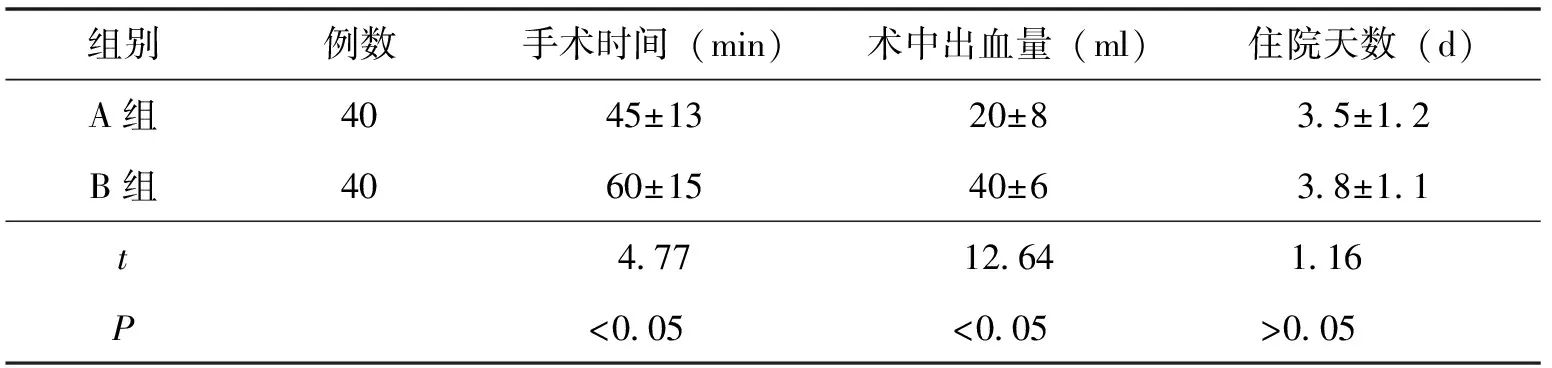
表1 两组患者手术时间、出血量、住院天数比较

表2 两组患者手术前后激素水平变化情况比较
三、术后月经改变情况
术后3个月随访, A组有3例患者月经异常,其中有2例术后第1个月月经周期延迟(35~42d),其后月经周期恢复正常,1例术后第1个月月经量减少约1/3,其后第2、第3个月月经量如常。B组有11例患者月经异常,其中4例术后1个月月经持续时间较长(8~15d),量少;4例月经周期延迟(35~56d不等),1例闭经,3例排卵期少量出血。
四、对照组和观察组患者术后妊娠情况
术后观察组有生育要求者20人,B组有生育要求者21人,此部分患者术前已行输卵管造影检查提示双侧输卵管通畅,或术中行输卵管通液术见双侧输卵管通畅,术前丈夫精液检查均无异常。指导术后2个月始不避孕,术后6个月随访妊娠情况。A组有5例患者自然受孕;B组有仅有1人怀孕。
讨 论
卵巢分为内层的髓质和外层的皮质,皮质是卵巢的主体,含有大小不等的各级发育卵泡、黄体和间质组织[5]。卵巢破坏性因素包括卵巢手术史 (包括输卵管切除、巧克力囊肿剥除术、子宫肌瘤剜除术、 卵巢打孔术等)、放化疗史、盆腔感染等。 其对卵巢的损伤机制可能主要为破坏卵巢血供及损害卵母细胞、 导致卵巢间质纤维化或坏死等[6-7]。近年来,临床研究充分证实腹腔镜手术微创优势明显,有助于患者的早期康复[8]。而众所周知,对于卵巢手术止血方法,缝合方式较电灼方式能更好保护卵巢功能,但缝合方法及缝线选择对卵巢功能的保护是否有区别?因微乔小针较难穿透坚韧的卵巢皮质,既往茂名市人民医院传统用0/3微乔大针卵巢皮质外包扎式贯穿缝合卵巢皮质,恢复完整卵巢外观。本研究A组用小的微乔可吸收线皮内缝合卵巢,不穿透卵巢皮质,即最大限度地不破坏卵巢皮质内的各级卵泡和黄体组织,尽可能保留卵巢皮质功能的完整性;且缝合方法为卵巢皮质内荷包缝合,对于较小卵巢创面,只需要单荷包缝合,线结只有1个或2个,缝线及线结均位于卵巢髓质内或切口缘,不穿透卵巢皮质表面。而B组用较粗的薇乔可吸收线8字贯穿缝合卵巢,全线绑扎式贯穿卵巢皮质表面,卵巢表面有大量缝线及线结,不光通过针的穿刺破坏了卵巢皮质的卵泡,更主要的是粗大的缝线较大范围地压迫了卵巢皮质各级卵泡的血运,以及可吸收线作为异物刺激破坏卵泡的生长发育,且薇乔可吸收缝线的缺点是可能有异物反应和线头排斥反应[9],加大卵巢功能的破坏。本研究结果A组较B组手术时间短、出血量少,差异有统计学意义(P<0.05),但皮内荷包缝合手术难度更高,需较娴熟的腹腔镜下缝合技术。故对于保留卵巢创面大,渗血明显需快速止血者适宜用大针线贯穿快速缝合,而渗血不太明显或术者镜下缝合技术娴熟,则尽可能用小针卵巢皮内缝合 。进一步了解术后卵巢功能,A组术前E2、FSH和LH与术后1个月、3个月相比无显著性差异,B组术前E2、FSH和LH与术后1个月、3个月相比有显著性差异,且月经量减少、周期延长者较多。但是两组患者的卵巢功能检测均在正常范围之内,而且两组患者仅是一侧卵巢囊肿剥除,尚有对侧正常卵巢代偿功能,尚不能说两种不同的缝合方法对卵巢功能有明显影响。而且两组患者术后月经量及周期随有改变,但均能于术后三个月恢复正常,这可能与术后应激状态有关。
总之,腹腔镜卵巢囊肿剥除术中,采用镜下小针小线皮内荷包缝合的方式和传统大针粗线贯穿缝合相比较,两者对卵巢功能的影响均在正常范围之内,但前者对手术时间相对较短,但对手术技巧要求较高,后者手术时间相对较长,但手术技巧要求相对较低,两种方法均可用于卵巢缝合,临床医生可根据自身的手术技巧选择合适的缝合方法。
[1]杨景琦.开腹手术与腹腔镜治疗卵巢囊肿蒂扭转的临床效果探索分析[J].中国伤残医学,2015,23(11):83-84.
[2]彭洁,张丽娜,朱维培.三种手术方法治疗卵巢囊肿的临床分析 [J].腹腔镜外科杂志,2015,20(6):412-415.
[3]吴淑玲,彭小莲,康惠超,等.腹腔镜下卵巢囊肿剥除术pk刀电凝与缝合止血方法对卵巢功能的影响[J].中国妇幼保健,2011,26(23):3640-3641.
[4]周芳.腹腔镜卵巢囊肿剔除术后早期注射缓释醋酸亮丙瑞林的临床疗效[J].临床医学,2014,8(6):96-97.
[5]谢幸,苟文丽,林仲秋,等.妇产科学[M].8版.北京:人民卫生出版社,2014:8.
[6]杨瑶,张平,刘红.腹腔镜双侧卵巢子宫内膜异位囊肿剔除 术对卵巢储备功能及生育的影响 [J].中国妇幼保健,2015,30(13):2116-2117.
[7]肖晓娟,张晓平.腹腔镜手术致卵巢损伤的危险因素分析 [J].吉林医学, 2015,36(9):1823.
[8]黄智,刘任袜.腹腔镜和开腹胆囊切除术对患者肝功能及C反 应蛋白水平的影响[J].医学综述,2012,18(22):3867-3868.
[9]孙铁莉.妇科腹部皮肤纵切口缝线选择的探讨[J].中国实用医药,2015,10(26):85.

