煅烧水滑石对硝态氮的吸附性能研究
蒋钦凤,喻杏元,艾玉明,邱喜,何欣,陈金毅
(武汉工程大学化学与环境工程学院,湖北 武汉 430073)
煅烧水滑石对硝态氮的吸附性能研究
蒋钦凤,喻杏元,艾玉明,邱喜,何欣,陈金毅
(武汉工程大学化学与环境工程学院,湖北 武汉 430073)
摘要:通过共沉淀法和煅烧法制备不同煅烧温度的水滑石,并对其进行XRD、FT-IR及BET表征.结果表明,煅烧水滑石后使水滑石的特征峰消失,层状结构塌陷,并生成了镁铝复合氧化物,比表面积增加,平均孔径减少.将水滑石进行硝态氮的吸附性能研究,结果表明,煅烧450 ℃水滑石除硝态氮效果优于其他煅烧温度下的水滑石,对10 mg/L的硝态氮吸附240 min后平衡浓度低于1 mg/L.最后,研究水滑石对硝态氮的吸附动力学与吸附等温线,结果表明准二级动力学模型和Langmuir吸附等温线能较好地描述硝态氮在水滑石上的吸附行为,吸附过程分为快速吸附阶段和慢速吸附阶段,水滑石对硝态氮的吸附过程主要为化学吸附,偏向于单分子层的吸附过程,但也不能排除多分子层吸附的存在.
关键词:水滑石;煅烧;硝态氮;吸附
0引言
随着我国工农业的发展,国内很多地区的水中氮含量大大超出饮用水的标准,氮的增加导致水华的爆发[1-2],水华爆发对于环境以及人类健康都有着极大危害[3];因此,减少氮的含量对控制水华爆发具有重要的现实意义.
在常见的除氮方法中,粘土矿物具有来源广泛、价格低廉、环境友好等优点成为研究热点[4-5].而水华环境下的硝态氮主要以阴离子的形式存在,因此需要找到阴离子型粘土矿物作为吸附材料.然而大多数天然粘土矿物表面带有负电荷,对阳离子具有较好的吸附效果,要想实现对阴离子型污染物的吸附去除,需要对其进行改性,从而增加成本和造成二次污染[6].水滑石[7]是为数不多的表面带正电荷、层间含有阴离子的粘土矿物,不需要改性就可以对阴离子型污染物具有较好的吸附性能.
水滑石(hydrotalcite,简称 LDH)是典型的表面带正电荷的粘土矿物材料,具有独特的层状结构和性能,其层板上阳离子具有同晶取代性,层间阴离子具有可交换性,结构特性独特、组成及结构可调,有独特的“记忆效应”,以及合成简单、成本低廉、耐高温、耐辐射、无二次污染、易再生等优点,使其作为典型的正电性吸附剂在污水治理方面已经取得了较大的进展.大量研究表明,水滑石对无机阴离子(如硝酸盐、亚硝酸盐)[8-9]、复杂阴离子团(如亚砷酸盐)[10]和有机阴离子(如腐殖酸)[11]等都有良好的吸附性能,是一种非常具有发展前景的正电性吸附剂;因此利用水滑石作为表面带正电性的粘土矿物材料对去除表面带负电的硝态氮的研究具有可行性.本文中以表面带负电性的硝态氮为代表,探究煅烧温度、不同浓度对水滑石吸附硝态氮的影响,并对实验数据进行吸附动力学和吸附等温线分析,得出重要的吸附参数,探讨吸附机理,为水滑石用于水华的处理提供依据.
1实验部分
1.1药品与仪器氯化镁(MgCl2·6H2O)、氯化铝(A1Cl3·6H2O)、碳酸钠(Na2CO3)、氢氧化钠(NaOH)、盐酸(HCl)、硝酸钾(KNO3)等均为分析纯,购自国药集团化学试剂有限公司.
FA-N型电子天平(上海民桥精密科学仪器有限公司);TU-1901型分光光度计(北京普析通用仪器有限责任公司),PHS-3C型精密PH计(上海精密科学仪器有限公司);GZXGF-9053A型鼓风干燥箱(上海玺恒实业有限公司);SRJX-4-13马弗炉(天津市中环实验电炉有限公司).

1.3实验方法在锥形瓶中加入一定量的硝酸盐氮标准液,配成一定浓度的硝态氮溶液200 mL,并取样测定硝态氮的初始浓度,向其中加入0.2 g水滑石,放入摇床开始计时,设置温度25 ℃、转速250 r/min,10、30、60、90、120、240 min后取样进行测定硝态氮浓度.硝态氮的测定方法按《水质 硝酸盐氮的测定 紫外分光光度法(试行)》(HJ/T346-2007)[12]测定.
1.4吸附动力学
1) 准一级动力学[13]:描述吸附过程是否是物理吸附;适合早期快速吸附过程,选用时间越短,回归的相关系数越高;
lg(qe-qt)=lgqe-k1t/2.303
(1)
其中qe为平衡吸附量,mg/g;qt为t时刻吸附量,mg/g;k1为准一级反应速率常数,min-1.
2) 准二级动力学:假设吸附位点的占有率与剩余的吸附位点数目成正比,它指出吸附动力学是由化学反应控制的,选用吸附时间越长,吸附量越接近平衡吸附量;
t/qt=1/(k2qe2)+t/qe
(2)
其中,k2为准二级反应速率常数,g/(mg·min).
3) 粒内扩散模型线性方程如下:
qt=kpt1/2+c
(3)
其中,kp为粒内扩散速率常数,μg/g·min0.5;c为截距.
1.5吸附等温线
1) Langmuir吸附又称“单分子吸附理论”,它假定固体吸附剂表面上均匀地分布着具有吸附能力的吸附位,并且吸附是单分子层的.Langmuir 吸附等温式如下:
Ce/qe=Ce/Q0+1/Q0b
(4)
其中Ce平衡浓度,mg/L;Q0理论单层最大吸附量,mg/g;b为Langmuir模型常数,L/mg;C0初始浓度,mg/L.
Langmuir等温吸附模型式中,可以用以下参数来分析水滑石吸附硝态氮的效果:
RL=1/(1+bC0)
(5)
其中RL等温吸附参数;C0为硝态氮初始浓度.当吸附等温参数RL<1时,代表材料有很好的吸附效果.
2) Freundlich等温吸附模型吸附出现在不均匀的表面时,
lnqe=lnkf+lnCe/n
(6)
Kf为Freundlich模型常数,L/mg;n为Freundlich模型常数;以lnqe对lnCe作图,由直线的斜率和截距确定Kf和n的值.当n>1时,有利于吸附;n<1时,不利于吸附.
2结果和讨论
2.1水滑石的表征
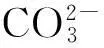

图1 不同煅烧温度水滑石的XRD图
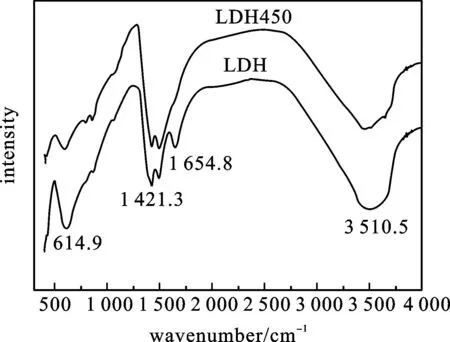
图2 不同煅烧温度水滑石的FT-IR图

2.1.3BET为探究煅烧对水滑石比表面积的影响,对未煅烧、煅烧450 ℃的水滑石进行了BET分析.从表1中可以看出,煅烧水滑石比未煅烧水滑石具有更大的比表面积和更小的平均粒径;原因是水滑石经过煅烧后,层板结构塌陷,失去大部分的层间碳酸根和水分子;煅烧水滑石比表面积的增加使水滑石对硝态氮具有更高的吸附能力,这也与上述实验数据和XRD结果一致.因此,煅烧水滑石可作为一种更高效的吸附剂处理水体中的硝态氮.

表1 水滑石的比表面积与平均粒径一览表
2.2煅烧温度对水滑石吸附硝态氮的影响通过上述分析可知,煅烧对水滑石的结构具有很大的影响,未煅烧的水滑石具有良好的层状结构,而水滑石在煅烧后层板塌陷,具有“结构记忆效应”,即可通过吸附阴离子恢复水滑石的层状结构[15],因此,为了研究煅烧温度对水滑石对吸附硝态氮的影响,选择了LDH、LDH300、LDH400、LDH450、LDH500、LDH600进行除硝态氮对比.由图3可以看出,LDH450吸附硝态氮90 min即可达到平衡,且平衡浓度低于0.1 mg/L,LDH400吸附240 min后硝态氮浓度也低于0.5 mg/L,而LDH吸附240 min后硝态氮浓度仍为5.7 mg/L以上,LDH300、LDH500、LDH600吸附效率随着吸附时间的增长,硝态氮浓度慢慢降低,在吸附240 min后,LDH500的硝态氮浓度低于2.0 mg/L,LDH300的硝态氮浓度低于3.0 mg/L,LDH600的硝态氮浓度低于4.0 mg/L.从结果分析,LDH和LDH300的水滑石结构未破坏或者未完全破坏,而经过400 ℃或更高温度煅烧后的水滑石结构完全破坏并形成了镁铝复合氧化物,利用水滑石特有的记忆效应进行吸附,因而在450 ℃左右的水滑石即可达到较高的吸附效果,而随着温度的升高,水滑石内部生成了其他的镁铝氧化物的复合衍生物,影响了吸附效果率,因而导致其对硝态氮吸附效果的降低,所以本实验选用LDH450进行硝态氮的吸附实验.
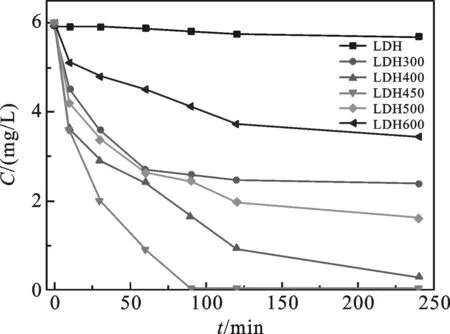
图3 煅烧温度对水滑石吸附硝态氮的影
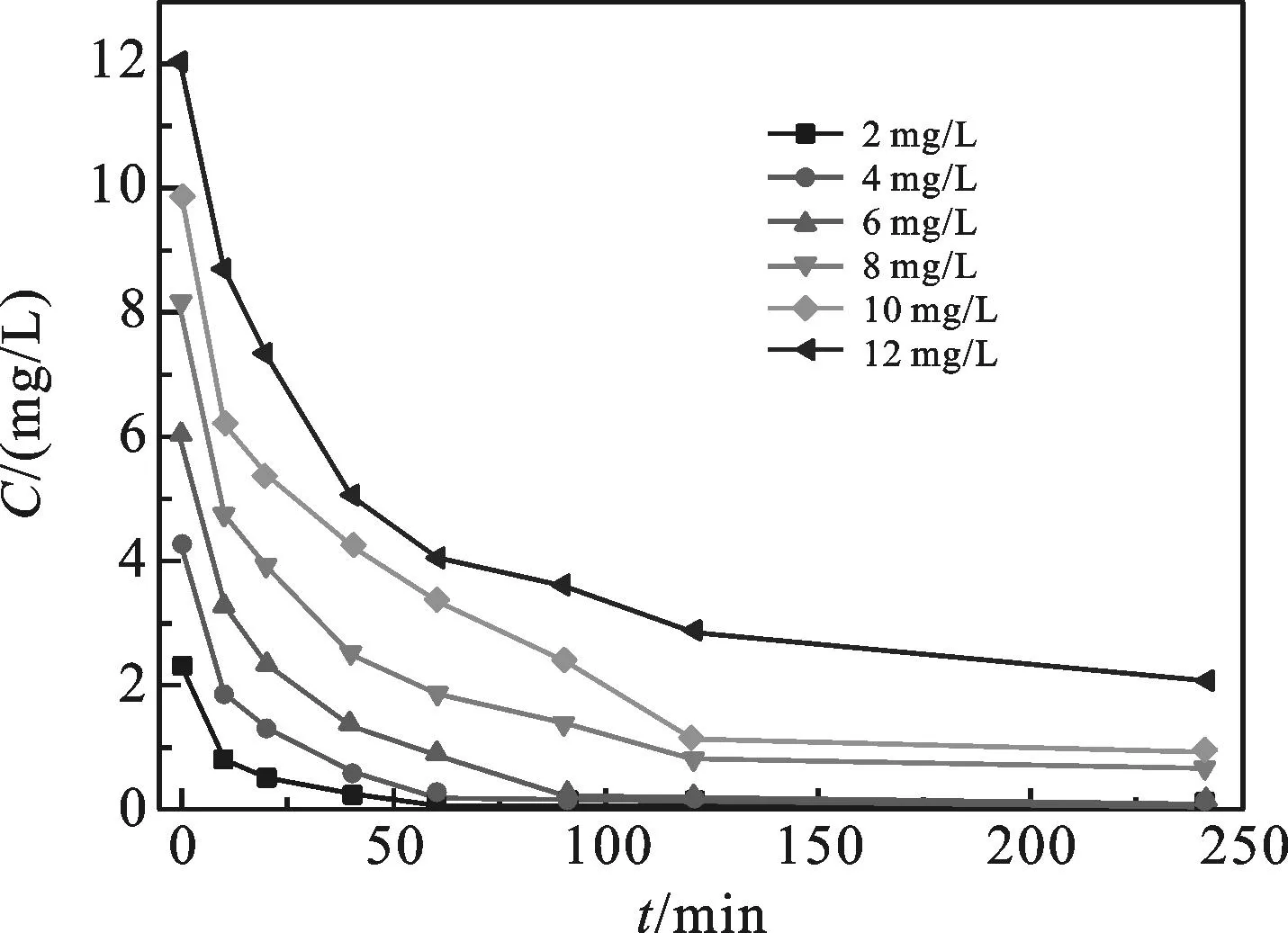
图4 硝态氮浓度对水滑石吸附硝态氮的影
2.3硝态氮浓度对水滑石吸附硝态氮的影响为探究不同硝态氮浓度对水滑石吸附硝态氮的影响,并考虑实际水体中水华爆发时硝态氮的浓度,选择了硝态氮浓度为2、4、6、8、10、12 mg/L作为研究对象.从图4可以看出,随着吸附时间的增长,硝态氮浓度逐渐降低,2 mg/L和4 mg/L的硝态氮吸附60 min后即可达到平衡,而随着硝态氮浓度的增加,水滑石吸附逐渐达到饱和,导致溶液中剩余硝态氮浓度相对较大,但8 mg/L和10 mg/L硝态氮的吸附240 min后平衡浓度仍低于1 mg/L,达到地表水环境质量标准(GB3838—2002)中的Ⅲ类水标准要求,12 mg/L硝态氮的吸附240 min后平衡浓度低于2 mg/L,也满足地表水环境质量标准中的Ⅴ类水标准要求.

图5 准一级动力学模型


图6 准二级动力学模
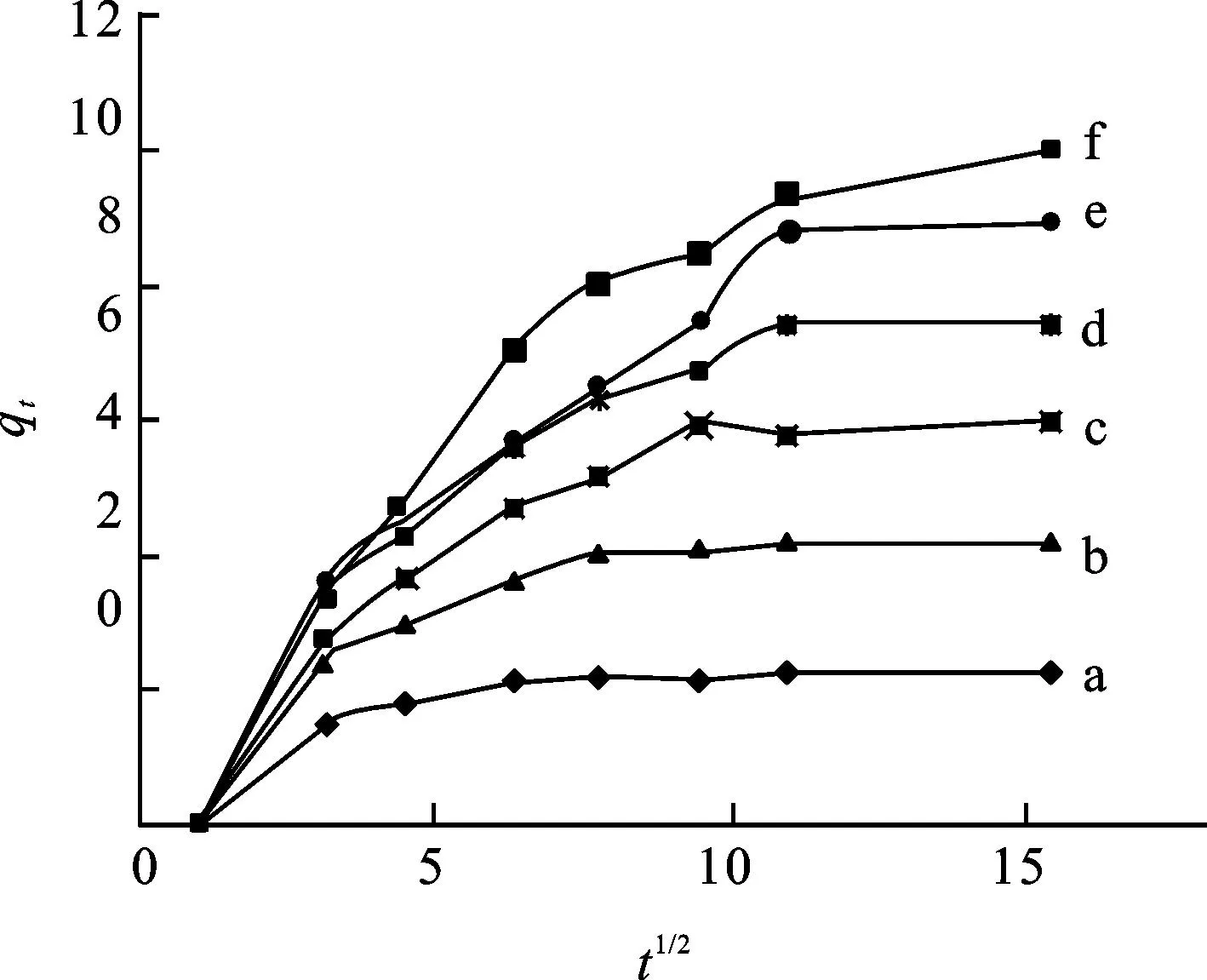
图7 粒内扩散模

C0/(mg/L)qe(exp)准一级动力学参数qe(cal)K1R2准二级动力学参数qe(cal)K2R222.3061.0670.01290.90052.3410.09790.999344.2221.5590.01560.96194.3230.04220.998865.9422.0840.01770.89226.1920.01770.996187.4662.3270.01440.94437.8000.01150.9953108.9132.5820.01170.90299.4610.00600.98591210.0072.4710.00870.967610.5710.00550.9907
2.5吸附等温线分析利用Langmuir吸附等温线方程和Freundlich吸附等温线方程,分别以Ce/qe-Ce和lnqe-lnCe作图,并进行线性拟合,得到拟合曲线如图8和图9所示,并从斜率和截距计算相关参数,具体见表3;从表中的数据可以看出,水滑石对硝态氮的吸附更符合Langmuir吸附等温线模型,其线性相关系数R2=0.989 0,而用Freundlich等温线模型拟合得到的线性相关系数R2=0.927 5.由此,可以推测,水滑石对硝态氮的吸附更偏向于单分子层的吸附过程,但也不能排除多分子层吸附的存在.吸附等温参数RL<1表明吸附效果较好.通过Langmuir等温线模型计算得出水滑石对硝态氮的理论单层最大吸附量Q0为10.183 mg/g.

图8 Langmuir吸附等温
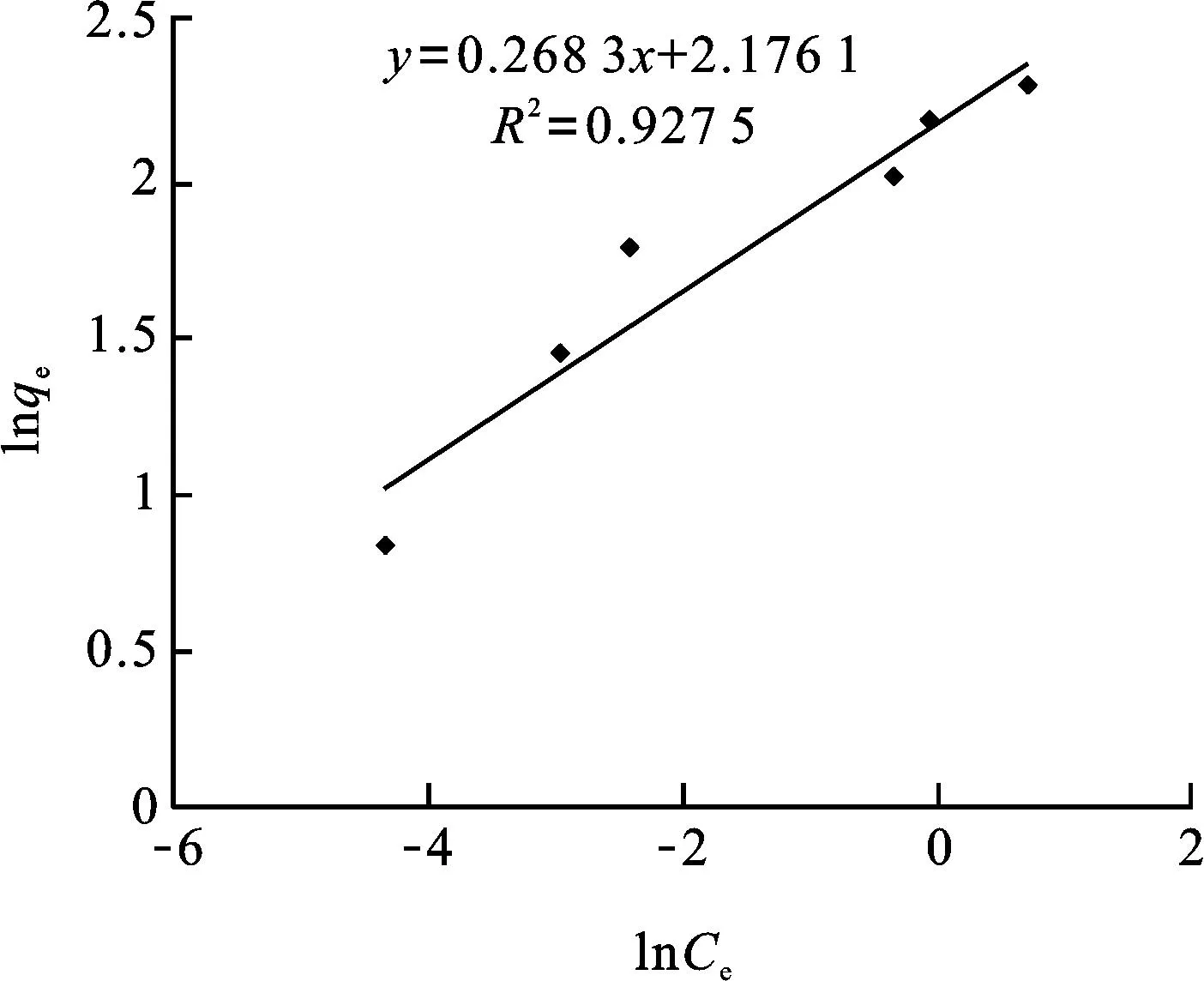
图9 Freundlich吸附等温

isothermR2KfnRLQ0bLangmuir0.9890——<110.1839.723Freundlich0.92758.8093.727———
3总结
1) 通过共沉淀法制备不同煅烧温度的水滑石,并对其进行XRD、FT-IR及BET表征,结果表明,未煅烧的水滑石具有良好的层状结构,在煅烧后水滑石失去了层板间的结晶水和大部分碳酸根,层状结构塌陷,具有“结构记忆效应”,并生成了镁铝复合氧化物,煅烧水滑石比表面积增加,平均孔径减少.
2) 研究不同煅烧温度的水滑石及不同硝态氮浓度对吸附硝态氮的影响,结果表明,煅烧温度为450 ℃的水滑石除硝态氮效果优于其它煅烧温度下的水滑石,8 mg/L和10 mg/L硝态氮的吸附240 min后平衡浓度低于1 mg/L,达到地表水环境质量标准中的Ⅲ类水标准要求,12 mg/L硝态氮的吸附240 min后平衡浓度低于2 mg/L,也满足Ⅴ类水标准要求..
3) 研究了水滑石对硝态氮的吸附动力学与吸附等温线,并对吸附机理及吸附容量进行初步讨论与计算,表明水滑石对硝态氮的吸附更好地符合准二级动力学模型和Langmuir吸附等温线,吸附分为两个阶段,吸附过程主要为化学吸附,更偏向于单分子层的吸附过程,但也不能排除多分子层吸附的存在,理论单层最大吸附量Q0为10.183 mg/g.
4参考文献
[1] Xie L Q,Xie P,Li S X,et al.The low TN:TP ratio,a cause or a result of microcystis blooms[J].Water Research,2003,37(9):2073-2080.
[2] Havens K E,James R T,East T L,et al.N:P ratios,light limitation,and cyanobacterial dominance in a subtropical lake impacted by non-point source nutrient pollution[J].Environmental Pollution,2003,122:379-390.
[3] Anderson D M.Approaches to monitoring,control and management of harmful algal blooms (HABs)[J].Ocean and Coastal Management,2009,52:342-347.
[4] Liany D L Miranda,Carlos R Bellato,Maurício P F Fontes,et al.Preparation and evaluation of hydrotalcite-iron oxide magnetic organocomposit intercalated with surfactants for cationic methylene blue dye removal[J].Chemical Engineering Journal,2014,254:88-97.
[5] Kang Dongjuan,Yu Xiaolin,Tong Shengrui,et al.Performance and mechanism of Mg/Fe layered double hydroxides for fluoride and arsenate removal from aqueous solution[J].Chemical Engineering Journal,2013,228:731-740.
[6] Liu Guofeng,Fan Chengxin,Zhong Jicheng,et al.Using hexadecyl trimethyl ammonium bromide (CTAB) modified clays to clean the Microcystis aeruginosablooms in Lake Taihu,China[J].Harmful Algae,2010,9:413-418.
[7] Yang Yiqiong,Gao Naiyun,Chu Wenhai,et al.Adsorption of perchlorate from aqueous solution by the calcination product of Mg/(Al-Fe) hydrotalcite-like compounds[J].Journal of Hazardous Materials,2012,209-210:318-325.
[8] Wang Dongjin,Liu Huijuan,Liu Ruiping,et al.Adsorption of nitrate and nitrite from aqueous solution onto calcined (Mg-Al) hydrotalcite of different Mg/Al ratio[J].Chemical Engineering Journal,2012,195-196:241-247.
[9] Mahamudur Islam,Rajkishore Patel.Nitrate sorption by thermally activated Mg/Al chloride hydrotalcite-like compound[J].Journal of Hazardous Materials,2009,169:524-531.
[10] Caporale A G,Pigna M,Azam S M G G,et al.Effect of competing ligands on the sorption/desorption of arsenite on/from Mg-Fe layered double hydroxides (Mg-Fe-LDH)[J].Chemical Engineering Journal,2013,225:704-709.
[11] Zhang Guochen,Wu Tao,Li Yujiang,et al.Sorption of humic acid to organo layered double hydroxides in aqueous solution[J].Chemical Engineering Journal,2012,191:306-313.
[12] 国家环境保护总局.HJ/T 346-2007.水质硝酸盐氮的测定:紫外分光光度法(试行)[S].北京:中国环境科学出版社,2007.
[13] Wang Tiangang,Cheng Zihong,Wang Baodong,et al.The influence of vanadate in calcined Mg/Al hydrotalcite synthesis on adsorption of vanadium (V) from aqueous solution[J].Chemical Engineering Journal,2012,181-182:182-188.
[14] Xiao Lili,Ma Wei,Han Mei,et al.The influence of ferric iron in calcinednano-Mg/Al hydrotalcite on adsorption of Cr (VI) from aqueous solution[J].Journal of Hazardous Materials,2011,186:690-698.
[15] 王莉娟.镁铝水滑石及其煅烧产物吸附溶液中重金属阴离子的研究[D].长沙:中南大学,2012.
(责任编辑胡小洋)
Adsorption capacity of nitrate by calcination layered double hydroxide
JIANG Qinfeng, YU Xinyuan,AI Yuming,QIU Xi,HE Xin, CHEN Jinyi
(School of Chemistry and Environmental Engineering,Wuhan Institute of Technology,Wuhan 430073,China)
Abstract:Layered double hydroxide(LDH)were synthesized by co-precipitation method and its calcination products (LDH450) was prepared by heating LDH at 450 ℃.The materials were characterized by X-ray diffraction (XRD),Fourier transform infrared spectroscopy (FT-IR) and Brunauer-Emmett-Teller(BET).Results indicate that the characteristic peaks (003) and (006) of LDH450 disappeared,a mixed oxide Mg(Al)O was formed,and the BET SSA of LDH450 increased,and the average pore size reduced.The adsorption capacity of hydrotalcite was studied.Results indicate that nitrate adsorption by LDH450 was superior to the others.When initial concentrations of nitrate was 10 mg/L,the adsorption reaction reached a balance in 240 min,and the equilibrium concentration was less than 1 mg/L.Finally,the adsorption kinetics and adsorption isotherm showed that the Pseudo-second-order kinetic model and Langmuir isotherm model could be used to describe nitrate adsorption satisfactorily.Adsorption process divided into two stages,included fast stage and slow stage,and mainly chemical adsorption,the adsorption process in favor of a single molecular layer,but can not exclude the presence of multiple molecular layer adsorption.
Key words:layered double hydroxide;heating nitrate;adsorption
中图分类号:X524
文献标志码:A
DOI:10.3969/j.issn.1000-2375.2016.03.006
文章编号:1000-2375(2016)03-0201-07
作者简介:蒋钦凤(1989-),女,硕士生;陈金毅,通信作者,教授,E-mail:jychwit@163.com
基金项目:国家自然科学基金(51374157)、教育部新世纪优秀人才计划项目(NCET-12-0713)、湖北省自然科学基金(2013CFA106)和武汉工程大学研究生教育创新基金(CX2014111)资助
收稿日期:2016-01-02

