基于酚类特征图谱的人参质量表征关联分析研究
陈唯 杨元 张芳 李焕娟 孔静 申立峰 王亚利 谭立 赵博 刘璐 张元元 姜艳艳 石任兵
100102 北京中医药大学中药学院国家中医药管理局中药经典名方有效物质发现重点实验室[陈唯(硕士研究生)、杨元(硕士研究生)、张芳(硕士研究生)、李焕娟(硕士研究生)、孔静(硕士研究生)、王亚利(硕士研究生)、谭立(硕士研究生)、赵博(硕士研究生)、刘璐(硕士研究生)、张元元(硕士研究生)、姜艳艳、石任兵];首都医科大学中医药学院[申立峰(硕士研究生)];北京市教委中药质量控制技术工程中心(姜艳艳、石任兵)
·论著·
基于酚类特征图谱的人参质量表征关联分析研究
陈唯杨元张芳李焕娟孔静申立峰王亚利谭立赵博刘璐张元元姜艳艳石任兵
100102北京中医药大学中药学院国家中医药管理局中药经典名方有效物质发现重点实验室[陈唯(硕士研究生)、杨元(硕士研究生)、张芳(硕士研究生)、李焕娟(硕士研究生)、孔静(硕士研究生)、王亚利(硕士研究生)、谭立(硕士研究生)、赵博(硕士研究生)、刘璐(硕士研究生)、张元元(硕士研究生)、姜艳艳、石任兵];首都医科大学中医药学院[申立峰(硕士研究生)];北京市教委中药质量控制技术工程中心(姜艳艳、石任兵)
【摘要】目的建立基于酚类特征图谱的人参质量表征关联分析方法与评价模式,为有效精准地评价人参质量奠定基础。方法运用HPLC-PDA法表征人参酚类特征图谱中13个特征峰及其所属化学类型,对16批人参饮片进行质的表征;建立HPLC同时测定对羟基苯甲酸、阿魏酸、槲皮素、山奈酚、异鼠李素含量的方法,并表征酚类成分和指标;建立可见分光光度法测定人参饮片中总酚的含量,基于酚类成分及其和指标与总酚的含量对16批人参饮片进行量的表征;对人参中各酚类成分及其和指标与总酚含量的关联性、质量表征规律进行分析,并基于参比饮片(批号16)对16批人参质与量的表征结果进行关联性分析。结果16批人参酚类特征图谱中均含有13个特征峰,其中酚酸类10个,黄酮类3个;得出酚类有效指标性成分与总酚含量的相关系数范围及各成分含量分布规律,并得出各批次人参饮片中各成分含量与参比饮片比较的总体含量变化趋势及关联度。结论所建立的基于酚类特征图谱的人参质量表征关联分析模式,为关注人参质量整体关联性与应用有效性及有效精准地评价人参饮片质量奠定基础。
【关键词】人参;特征图谱;质量评价;关联分析;酚酸类指标;黄酮类指标;总酚
人参为五加科植物人参PanaxginsengC.A.Mey.的干燥根和根茎,具有大补元气,复脉固脱,补脾益肺,生津养血,安神益智等功效,其化学成分包括皂苷、多糖、挥发油、有机酸及其酯、蛋白质、甾醇及其苷、生物碱、黄酮、木质素、无机元素以及维生素等[1-2]。银荷方为课题组拟定的临床经验方,基于药物体系导向,在对其药学-药效质量表征关联分析研究中,笔者发现组方药味人参中酚类成分(主要为酚酸类和黄酮类成分)为银荷方活血止血药物体系架构组成之一。因此,本文对基于酚类特征图谱的人参质量表征关联分析研究进行报道。
2015版《中华人民共和国药典》(一部)以人参皂苷Rg1与人参皂苷Re的总含量以及人参皂苷Rb1的含量规定指标作为人参的质量标准[3]。目前文献报道中,已有对人参中山奈酚和总黄酮含量测定的研究[4-5],但未见人参中酚酸类成分的报道,笔者在人参中发现对羟基苯甲酸和阿魏酸及酚酸类的存在,并通过酸水解后发现人参黄酮类成分的三个黄酮苷元槲皮素、山奈酚、异鼠李素,进而建立HPLC同时测定人参中酚类对羟基苯甲酸、阿魏酸、槲皮素、山奈酚、异鼠李素含量的方法,并以阿魏酸为质量表征标尺,通过主要酚酸类成分峰面积和表征主要酚酸类成分的含量,以水解后槲皮素、山奈酚、异鼠李素含量和表征黄酮类成分含量;以酚酸类含量和与黄酮类含量和的加和表征酚类含量和;并且建立可见分光光度法测定人参中总酚的含量。诚然对药物质量的控制不仅仅只考量指标性成分,还应表征特性有效指标性成分及其有关类型总含量,更应关注相对含量及其相对比值表征,同时结合特征图谱关注质量表征的完整性[6-7]。本研究以此为切入点,运用课题组建立的基于药物体系的中药质量评价模式[8-18],对基于酚类特征图谱的人参质量表征关联分析研究,即基于酚类特征图谱,关注特征峰化学类型及其关联性,并对人参饮片中对羟基苯甲酸、阿魏酸、主要酚酸类含量和、槲皮素、山奈酚、异鼠李素、黄酮类含量和、酚类含量和、总酚的含量及其相对比值进行质量表征,且与经过药效验证的参比饮片(批号16)进行关联度分析比较,并对人参中各酚类成分及其和指标与总酚含量的关联性、质量表征规律进行分析,以期为提高人参饮片质量控制的精准性奠定基础[19-21]。
1材料
1.1仪器
Waters XbridgeTMC18色谱柱(4.6 mm×250 mm,5 μm);Waters e2695高效液相色谱仪;Empower Pro软件系统;2998PDA检测器;METTLER-AE240型电子分析天平(北京赛多利斯仪器有限公司);KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司);TU-1810型紫外-可见分光光度计(北京普析通用仪器有限公司)。
1.2试剂与药物
对羟基苯甲酸(批号:yy91251,纯度≥98%)购自上海源叶生物科技有限公司;阿魏酸(批号:121002,纯度≥98%)购自北京方程生物科技有限公司;槲皮素(批号:111672-200702,纯度≥98%)购自中国药品生物制品检定所;山奈酚(批号:140708,纯度≥98%)购自成都普菲德生物技术有限公司;异鼠李素(批号:YY110860,纯度≥98%)购自上海源叶生物科技有限公司;聚酰胺树脂(30~60目,柱层析用)购自浙江省台州市路桥四甲生化塑料厂;乙腈(色谱级,Fisher Scientific公司);甲醇(分析纯,北京化工厂); 盐酸(分析纯,北京化工厂); 磷酸(分析纯,北京化学试剂公司);娃哈哈纯净水(杭州娃哈哈集团有限公司);其余试剂均为分析纯。
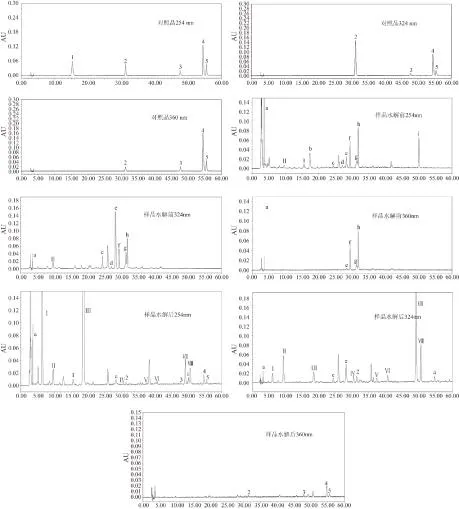
注:峰1对羟基苯甲酸;峰2阿魏酸;峰3槲皮素;峰4山奈酚;峰5异鼠李素;峰Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅵ、Ⅶ、Ⅷ为未知酚酸类;峰a、b、c、d、e、i为未知成分;峰f、h为黄酮苷;峰g为阿魏酸和峰Ⅳ及黄酮类混合峰
图1对照品及人参供试品水解前后的HPLC谱图
16批人参饮片:购自北京市、浙江杭州市、广东省深圳市、湖北省武汉市各药店。经北京中医药大学刘春生教授鉴定,均为正品。饮片标本现存于北京中医药大学中药学院中药化学系。
2方法与结果
2.1人参指标性酚类成分含量测定方法
2.1.1色谱条件Waters C18色谱柱,流动相乙腈(A)-0.2%磷酸水(B),洗脱梯度(0~10分钟,7%A;10~32分钟,7%~19.5% A;32~60分钟,19.5%~38% A),流速1.0 mL/min,柱温25℃,检测波长:对羟基苯甲酸(254 nm);阿魏酸(324 nm);槲皮素、山奈酚、异鼠李素均为360 nm,进样量30 μL。
上述色谱条件下,对照品及人参样品水解前后的HPLC谱图见图1,水解后对羟基苯甲酸(254 nm)、阿魏酸(324 nm)、槲皮素(360 nm)、山奈酚(360 nm)、异鼠李素(360 nm)及各酚酸类特征峰(324 nm)在各自检测波长下与其他色谱峰分离度良好。
2.1.2对照品溶液的制备方法分别取上述5种对照品适量,精密称取,加入甲醇制成对羟基苯甲酸、阿魏酸、槲皮素、山奈酚、异鼠李素的浓度分别为0.01376 mg/mL、 0.0095 mg/mL、 0.01672 mg/mL、 0.051 mg/mL、 0.01688 mg/mL的混合对照品溶液。
2.1.3供试品溶液的制备方法取人参饮片粉碎,过四号筛,称取约2 g,置于具塞锥形瓶中,精密加入100 mL 70%甲醇,加热回流提取2次,每次2小时,合并提取液,浓缩至无醇味,加水分散至50 mL,用已经处理过的30~60目聚酰胺树脂湿法装柱,树脂体积为25 mL,水洗0.5 BV,然后甲醇洗脱,收集甲醇洗脱液,蒸干溶剂,再加入甲醇-25%盐酸溶液(4∶1)混合溶液5 mL,加热回流40分钟,放冷,加甲醇定容至5 mL容量瓶内,即得酸水解后供试品溶液。
2.1.4人参指标性酚类成分含量测定方法学考察将“2.1.2”项下混合对照品溶液进样1 μL、2 μL、5 μL、10 μL、15 μL、20 μL、25 μL、30 μL,以进样量(μg)为横坐标,峰面积为纵坐标绘制标准曲线,计算线性回归方程及相关系数得出对羟基苯甲酸:Y=8833298.65X+6158.66(r=0.9999),线性范围0.01376~0.3440 μg;阿魏酸:Y=4157762.01X-12679.53(r=0.9999),线性范围0.0095~0.2850 μg;槲皮素:Y=3003601.61X-31893.96(r=0.9999),线性范围0.01672~0.5016 μg;山奈酚:Y=3925859.81X-118060.23(r=0.9999),线性范围0.05100~1.5300 μg;异鼠李素:Y=3021260.71X-28782.89(r=0.9999),线性范围0.01688~0.5064 μg。该方法精密度、重复性、稳定性、加样回收率均合格。
2.2人参总酚含量测定方法
2.2.1对照品溶液的制备方法精密称取一定量的阿魏酸对照品,置于10 mL容量瓶内,用70%甲醇定容至10 mL,制得阿魏酸对照品的浓度为0.201 mg/mL。
2.2.2供试品溶液的制备方法取人参饮片粉碎,过四号筛,称取约0.1 g,加70%甲醇25 mL,称定重量,超声(功率500 W,频率40 KHz)提取1小时,再次称定重量,用70%甲醇补足损失的重量,即得供试品溶液。
2.2.3显色方法精密吸取供试品溶液适量,置于25 mL棕色容量瓶中,加70%甲醇至5mL,随行空白,再依次加入0.3%十二烷基硫酸钠溶液2.0 mL,0.6%三氯化铁-0.9%铁氰化钾(1∶1)混合溶液1.0 mL,暗处放置5分钟,用 0.1 mol/L盐酸定容至25 mL刻度线,摇匀后于暗处静置30分钟,于768 nm波长处测定吸光度值[22]。
2.2.4人参总酚含量测定方法学考察精密吸取“2.2.1”项下的阿魏酸对照品0.03 mL、0.06 mL、0.09 mL、0.11 mL、0.14 mL、0.17 mL、0.20 mL、0.23 mL、0.26 mL、0.29 mL,按照“2.2.3”项下的方法进行显色。以对照品质量为横坐标,吸光度值为纵坐标绘制标准曲线,并进行线性回归分析,计算回归方程为:Y=17.98X-0.0324(r=0.9989),线性范围0.00603~0.00603 mg。且该方法精密度、重复性、稳定性、加样回收率均合格。
2.3人参质的表征及其关联性分析
2.3.1基于酚类特征成分的质的表征取16批不同批号的人参饮片,按“2.1.3”项下方法制备供试品溶液,每批平行制备3份,进样,得到16批人参饮片酚类特征图谱(254 nm),见图2。
2.3.2基于酚类特征成分的质的表征关联分析对酚类特征色谱图中的各特征成分进行相关性分析,选择阿魏酸为基准峰,计算其他酚类特征成分的相对保留时间,结果见表1。
2.4人参量的表征及其关联性分析
2.4.1基于各酚类成分及其和指标与总酚含量的质量表征取16批人参饮片,按“2.1.3”项下方法制备供试品溶液,每批平行制备 3 份,按照“2.1.1”项下色谱条件进样,分别测定酸水解后人参饮片中对羟基苯甲酸、阿魏酸、槲皮素、山奈酚、异鼠李素的含量;以阿魏酸为质量表征标尺,通过主要酚酸类成分峰面积和表征主要酚酸类成分的含量;以水解后槲皮素、山奈酚、异鼠李素含量和表征黄酮类成分含量;以酚酸类含量和与黄酮类含量和的加和表征酚类含量和;按“2.2.2”项下方法制备供试品溶液,每批平行制备3份,按照“2.2.3”项下显色方法,测定总酚的含量。对16批人参饮片的含量进行质量表征,结果见表2。

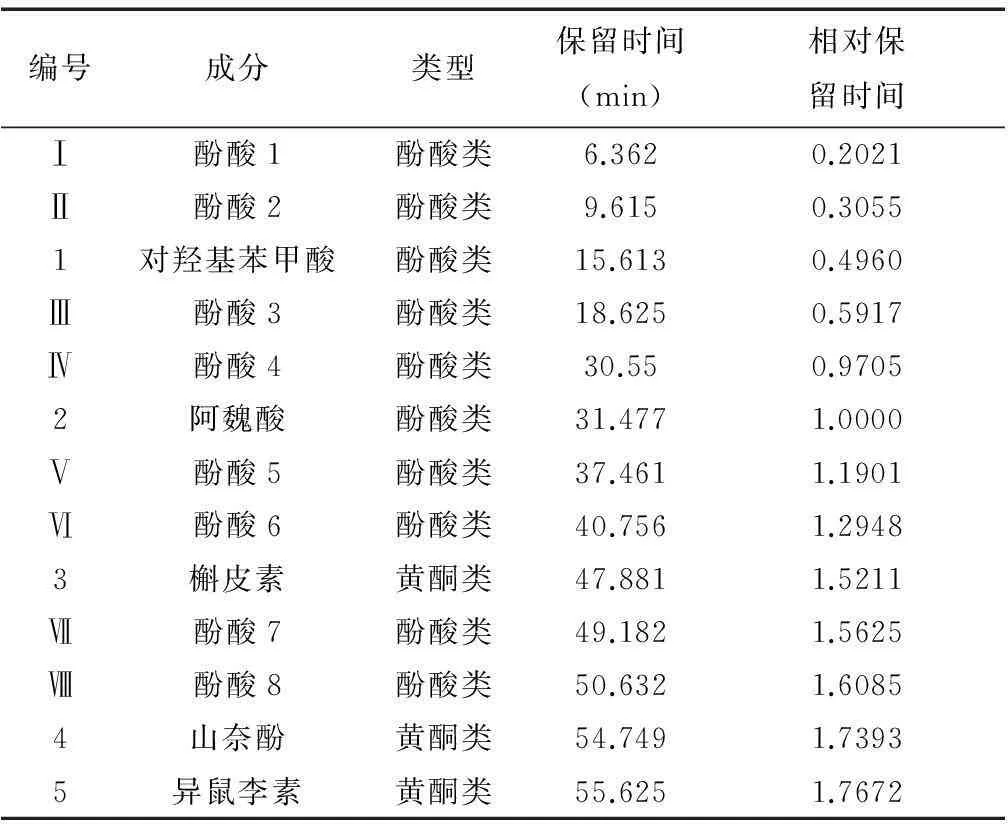
图2 16批人参饮片HPLC酚类特征图谱
2.4.2基于各酚类成分及其和指标与总酚含量相对比值的质量表征以阿魏酸的含量为参比,将16批人参饮片各酚类成分及其和指标与总酚含量相对于阿魏酸的比值予以表征,结果见表3;将各酚类成分及其和指标与总酚含量换算成同一数量级(即将对羟基苯甲酸、槲皮素、异鼠李素同时扩大1000倍;将阿魏酸、山奈酚、黄酮类含量和同时扩大100倍;将酚酸类含量和、酚类含量和同时扩大10倍),然后绘制各酚类成分及其和指标与总酚含量相对于阿魏酸的比值变化图,见图3。
2.5人参质量表征关联分析
2.5.1各酚类成分及其和指标与总酚含量的关联性分析基于“2.4.1”项下表2,将各酚类成分及其和指标与总酚含量换算成同一数量级,然后绘制各酚类成分及其和指标与总酚在不同批次间的含量变化趋势图,见图4。

表2 16批人参饮片各酚类成分及其和指标与总酚含量质量表征(%, n=3)

表3 16批人参饮片各酚类成分及其和指标与总酚含量相对于阿魏酸的比值

图3 16批人参饮片各酚类成分及其和指标
结合表2和图4进行分析,可知阿魏酸、酚酸类含量和、山奈酚、黄酮类含量和、酚类含量和与总酚含量变化趋势一致,当以阿魏酸为参比时,各酚类成分及其和指标与总酚含量相对于阿魏酸的比值范围分别为0.18~0.72、38.96~53.49、0.064~0.25、1.37~2.06、0.075~0.27、1.54~2.49、40.75~55.94、165.22~332.57,即阿魏酸与总酚含量的相关系数范围为165.22~332.57;结合表3和图3进行分析,其中60%批次对羟基苯甲酸与阿魏酸比值在0.43左右;60%批次酚酸类含量和与阿魏酸比值在36.14左右;60%批次槲皮素与阿魏酸比值在0.14左右;60%批次山奈酚与阿魏酸比值在1.61左右;60%批次异鼠李素与阿魏酸比值在0.15左右;60%批次黄酮类含量和与阿魏酸比值在1.84左右;60%批次酚类含量和与阿魏酸比值在45.23左右;60%批次总酚与阿魏酸比值在274.18左右。
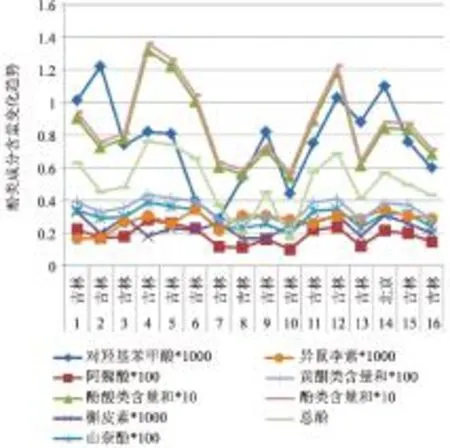
图4 16批人参饮片各酚类成分及其和
2.5.2各酚类成分及其和指标与总酚质量表征分布规律分析基于“2.5.1”项下关联性分析结果,绘制16批人参饮片中阿魏酸、酚酸类含量和、山奈酚、黄酮类含量和、酚类含量和、总酚(均换算成同一数量级)的含量分布规律图,见图5。

图5 16批人参饮片各酚类成分及其和指标
结合表2和图5进行分析,批号4、5、12、6、1为前30%的优质饮片,其酚酸类含量和不得低于0.09037%,酚类含量和不得低于0.09428%,总酚含量不得低于0.6308%;批号4、5、12、6、1、11、14、15、3、2为前60%的良好饮片,其酚酸类含量和不得低于0.07235%,酚类含量和不得低于0.07566%,总酚含量不得低于0.4563%;批号4、5、12、6、1、11、14、15、3、2、9、16、13、7、8为前90%的普通饮片,其酚酸类含量和不得低于0.05599%,酚类含量和不得低于0.05880%,总酚含量不得低于0.2005%,且由此可知经过药效验证的批号16为质量普通的人参饮片。
2.5.3基于与参比饮片(批号16)各酚类成分及其和指标与总酚含量相对比值的质量表征关联分析基于“2.4.1”项下表2,以批号16为参比,计算其它批号饮片中各酚类成分及其和指标、总酚含量与参比饮片相应成分含量的相对比值,进行16批人参饮片质量表征关联分析,见图6。
结合表2和图6进行分析,可知在16批人参饮片中,各酚类成分及其和指标与总酚含量的差异较大,并计算最高比值与最低比值的比,以反映各饮片中酚类成分及其和指标与总酚含量的差异。对羟基苯甲酸含量最大比值与最小比值之比为4.21,含量从高到低排序为:2>14>12>1>13>9>4>5>15>11>3>16>8>10>6>7;阿魏酸最大比值与最小比值之比为2.77,含量从高到低排序为:4>5>12>6>1>11>14>15>3>2>9>16>13>7>8>10;酚酸类含量和最大值与最小值之比为2.41,含量从高到低排序为:4>5>12>6>1>11>14>15>3>2>9>16>13>7>8>10;槲皮素最大值与最小值之比为1.94,含量从高到低排序为:1>12>14>3>11>7>15>10>5>6>2>16>4>13>8>9;山奈酚含量最大值与最小值之比为1.98,含量从高到低排序为:4>5>12>6>1>11>14>15>3>2>9>16>13>7>8>10;异鼠李素含量最大值与最小值之比为2.06,含量从高到低排序为:6>14>8>12>4>15>9>16>13>10>3>5>11>7>2>1;黄酮类含量和最大值与最小值之比为1.75,含量从高到低排序为4>5>12>6>1>11>14>15>3>2>9>16>13>7>8>10;酚类含量和最大值与最小值之比为2.38,含量从高到低排序为4>5>12>6>1>11>14>15>3>2>9>16>13>7>8>10;总酚含量最大值与最小值之比为4.52,含量从高到低排序为:4>5>12>6>1>11>14>15>3>2>9>16>13>7>8>10。
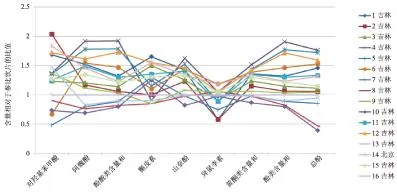
图6 16批人参饮片与参比饮片相应成分含量的相对比值
综合分析以上各酚类成分及其和指标与总酚含量的差异,得出总酚(4.52倍)>对羟基苯甲酸(4.21倍)>阿魏酸(2.77倍)>酚酸类含量和(2.41倍)>酚类含量和(2.38倍)>异鼠李素(2.06倍)>山奈酚(1.98倍)>槲皮素(1.94倍)>黄酮类含量和(1.75倍)。基于各酚类成分及其和指标与总酚含量进行综合考量,发现批号1、3、4、5、6、11、12、14、15中各酚类成分及其和指标与总酚含量总体高于参比饮片,批号2、9与参比饮片接近。
2.5.4基于与参比饮片(批号16)各酚类成分及其和指标与总酚含量相对比值的比值质量表征关联分析基于“2.4.2”项下表3,以批号16为参比,将16批人参饮片中各酚类成分及其和指标与总酚含量相对比值与参比饮片对应成分含量相对比值的比值进行关联分析,见表4、图7。
图7中不同颜色的矩形条代表各饮片中各酚类成分及其和指标与总酚含量相对比值与参比饮片对应成分含量相对比值的比值,矩形条长短与参比饮片相同颜色的矩形条长短越相近,代表该饮片各酚类成分及其和指标与总酚含量比值与参比饮片越接近,即质量表征关联密切。由图6可看出,批号3、4、5、6、7、8、9、11、15与参比饮片的关联度较高。与参比饮片质量表征关联密切。以参比饮片为基准,其他样品与其相对比值的比值差值的绝对值之和,即为非关联系数;非关联系数与各酚类成分及其和指标与总酚数目和的比值,即为非关联度,进而得到关联度,以反映饮片质量之间的关联性,见表4。由表4可知,关联度由高到低排序为16(0/100%)>15(9.44/90.56%)>6(13.11/86.89%)>11(14.78/85.22%)>3(14.67%/85.33%)>5(16.22/83.78%)>7(17.67/82.33%)=9(17.67/82.33%)>8(19.78/80.22%)>4(20.44/79.56)>10(27.33%/72.67%)>12(28.22/71.78%)>13(37.33/62.67%)>1(41.56/58.44%)>14(45.22/54.78%)>2(58.89/41.11%),即批号3、4、5、6、7、8、9、11、15与参比饮片的关联度较高。
3讨论
3.1样品处理方式的选择
本文报道旨在同一色谱条件下同时测定人参中酚酸类和黄酮类成分的含量,人参样品在富集水解前可以检测到对羟基苯甲酸、阿魏酸及其他酚酸类成分的存在,但是难以检测到黄酮类成分,故通过聚酰胺树脂进行富集,富集后可以检测到黄酮苷的存在,但是考虑到测定单个指标性成分的含量难以全面对人参中黄酮类成分进行质量控制,故采用酸水解方式,将人参中黄酮苷类成分转化成相应的苷元成分,即槲皮素、山奈酚、异鼠李素,以其含量和表征以槲皮素、山奈酚、异鼠李素为苷元的黄酮类成分的含量,更加准确和全面。
3.2水解前后主要酚酸类及主要黄酮类成分的变化
由于254 nm处色谱图较其他波长处基线平稳,分离度良好,且出峰多,故以此波长处色谱图为例讨论人参饮片水解前后色谱峰变化。由图1可知,未知峰中峰a、e、i水解后峰面积显著减小;峰b、c、d、f、h水解后消失,其中峰f、h经PDA分析推测为黄酮苷;峰g经PDA以及结合水解后相应保留时间处色谱峰分析推测,该峰为峰Ⅳ、峰2(阿魏酸)及黄酮苷的混合峰;峰Ⅰ、Ⅲ、Ⅴ、Ⅵ、Ⅶ、Ⅷ均为水解后产生,峰Ⅱ水解后峰面积有所增加,经PDA分析推测峰Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅵ、Ⅶ、Ⅷ均为酚酸类成分。已知峰中峰1(对羟基苯甲酸)水解前后无明显变化;峰3(槲皮素)、峰4(山奈酚)、峰5(异鼠李素)均为水解后产生,故推断水解前人参中黄酮类成分主要以槲皮素、山奈酚、异鼠李素的苷类形式存在,而在水解后转化为相应的苷元。

表4 16批人参饮片关联度表征
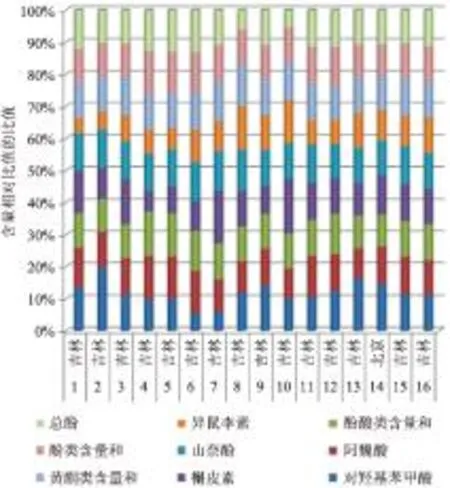
图7 16批人参饮片与参比饮片相应
本文在自然药学观相关理论的指导下,基于药物体系导向研究发现人参酚类(主要为酚酸类和黄酮类)及其特征指标性成分(对羟基苯甲酸、阿魏酸、槲皮素、山奈酚、异鼠李素),建立基于酚类特征图谱的人参质量表征关联分析方法,对16批人参的质量进行表征,得出酚类有效指标性成分与总酚含量的相关系数范围及各成分的含量分布规律,并基于参比饮片进行质量关联度分析比较,得出各批次人参饮片中各成分含量与参比饮片比较的总体含量变化趋势及关联度。本文研究的基于酚类特征图谱的人参质量表征关联分析方法综合考量了人参应用有效性及质量关联性,为有效精准地评价人参质量奠定基础。
参考文献
[1]黎阳,张铁军,刘素香,等.人参化学成分和药理研究进展[J].中草药,2009,40(1):164-166.
[2]姜林.浅谈人参的药理作用及应用研究[J].中国药物经济学,2012,(3):373-374.
[3]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:8-9.
[4]张儒,张变玲,赵勇,等.人参根中黄酮类化合物提取及其抗氧化性研究[J].中成药,2012,34(10):1896,1900.
[5]张儒,张变玲,谢涛,等.聚酰胺法富集人参根总黄酮工艺研究[J]. 湖南工程学院学报,2015,25(1):58-61.
[6]石任兵,王永炎.基于自然药学观药物体系的中药药物创新相关性思考[J].环球中医药,2015,8(3):257-259.
[7]石任兵,王永炎.基于自然药学观药物体系的中药药物本质相关性思考[J].北京中医药大学学报,2015,38(3):149-151.
[8]左胜,孙雅姝,石任兵,等.基于药物体系的藁本质量评价研究[J].北京中医药大学学报,2014,37(7):481-485.
[9]李焕娟,张璐,石任兵,等.基于药物体系质量评价模式的远志质量表征关联分析研究[J].北京中医药大学学报,2014,37(12):834-840.
[10]张璐,李焕娟,石任兵,等.基于药物体系质量评价模式的石菖蒲质量表征关联分析研究[J].环球中医药,2015,8(3):274-280.
[11]孙雅姝,张璐,潘婷,等.基于药物体系质量评价模式的白芷质量表征关联分析研究[J].环球中医药,2015,8(3):266-272.
[12]温静,唐雪阳,石任兵,等.基于药物体系质量评价模式的丹参质量表征关联分析研究[J].中华中医药学刊,2015,33(4):843,846.
[13]潘婷,黄亚婷,石任兵,等.基于药物体系质量评价模式的柴胡质量表征关联分析研究[J].世界中医药,2015,10(4):577-582.
[14]唐雪阳,安 琪,石任兵,等.基于药物体系的紫苏子特征图谱质量表征关联分析研究[J].北京中医药大学学报,2015,38(4):241-246.
[15]许舒娅,李 钢,石任兵,等.基于药物体系的栀子特征图谱质量表征关联分析[J].北京中医药大学学报,2015,38(7):473-480.
[16]黄亚婷,潘婷,石任兵,等.基于药物体系的肉桂特征图谱质量表征关联分析研究[J].北京中医药大学学报,2015,38(5):344-350.
[17]卢广英,赵丽敏,石任兵,等.基于药物体系的生地黄的质量评价研究[J].世界中医药,2015,10(5):765-771.
[18]李钢,许舒娅,石任兵,等.基于药物体系质量评价模式的蒲黄质量表征关联分析研究[J].北京中医药大学学报,2015,10(6):393-399.
[19]石任兵,王永炎,吕松涛.中药药物质量精准预期的相关性思考[J].中国中药杂志,2015,40 (17):3343-3346.
[20]石任兵,王永炎.自然药学观的相关性思考[J].北京中医药大学学报,2012,35(4):221-225.
[21]石任兵,王永炎,姜艳艳,等.论中药化学发展近况[J].北京中医药大学报,2012,35(3):163-169.
[22]李焕娟.基于药物体系的开心散药物制备工艺与系统质量表征研究[D].北京:北京中医药大学,2015.
(本文编辑: 董历华)
Quality characterization and correlation analysis based on phenolic characteristic spectrum of Panax ginseng
CHENWei,YANGYuan,ZHANGFang,etal.
KeyUnitofExploringEffectiveSubstancesofClassicalandFamousFormulasofStateAdministrationofTraditionalChineseMedicine,SchoolofChinesePharmacy,BeijingUniversityofChineseMedicine,Beijing100102,China
【Abstract】ObjectiveBased on phenolic constituents to establish the quality characterization and correlation analysis method of Panax ginseng, and to lay the foundation for evaluating the quality of ginseng. MethodsHPLC-PDA method was used to characterize the 13 kinds of characteristic peaks and their chemical type of Panax ginseng, the quality of 16 batches of ginseng slices was characterized. The HPLC method was established to simultaneous detect the content of p-hydroxybenzoic acid, ferulic acid, quercetin, kaempferol and isorhamnetin, the content of the phenolics indicators were characterized, and visible spectrophotometry was established to detect the content of total phenols in Panax ginseng. The 16 batches of Panax ginseng’s content of phenolic components, relevant indicators and total phenolic was characterized. And analysis the regularity of the relevance and quality characterization of each phenolic components and its indicators of ginseng with the total phenolic content, then correlatively analysis the results of quantity and quality of 16 batches of Panax ginseng based on reference piece(No.16). Results In the 16 batch of phenolic compounds, 13 characteristic peaks were found, including 10 phenolic acids and 3 flavonoids; The correlation coefficient range and the distribution law of the content of the total phenolic content and the effective index of phenols were found, and the change trend and correlation degree of the total content and the reference compound in each batch of ginseng were found. ConclusionThe quality characterization and correlation analysis method of characteristic spectrum of Panax ginseng is based on phenolic constituents, it lays the foundation for the overall quality relevance and effective applicationand effective and accurate evaluation of the quality of ginseng pieces.
【Key words】Panax ginseng;Characteristic spectrum;Quality evaluation;Correlation analysis;Phenolic acids indicators;Flavonoids indicators;Total phenol
(收稿日期:2016-01-13)
Corresponding author:SHI Ren-bing, E-mail: shirb@126.com
【中图分类号】R284
【文献标识码】A
doi:10.3969/j.issn.1674-1749.2016.04.009
作者简介:陈唯(1990- ),女,2013级在读硕士研究生。研究方向:中药(复方)有效物质基础研究与药物创新。 E-mail:chenwei1507@126.com通讯作者: 石任兵(1957- ),博士,教授,博士生导师。研究方向:中药(复方)有效物质基础研究与药物创新。E-mail:shirb@126.com
基金项目:国家“十二五”科技支撑计划(2012BAI29B06);北京中医药大学创新团队资助项目(2011-CXTD-12)

