尿毒症继发甲旁亢对心脏结构的影响
王继伟 张凌
【摘要】 目的 研究尿毒症继发甲状旁腺功能亢进(甲旁亢)对心脏结构的影响。方法 选取45例中日友好医院接受甲状旁腺切除术(PTX)手术治疗的尿毒症继发甲旁亢患者, 为组1;选取60例台湾高雄长庚医院进行腹膜透析的尿毒症继发甲旁亢患者, 为组2。对两组的各项资料进行比较, 分析尿毒症继发甲旁亢对心脏结构的影响。结果 两组患者例数及平均年龄比较, 差异无统计学意义(P>0.05);两组患者平均透析龄、平均甲状旁腺激素(iPTH)、血钙、血磷和Ca-P乘积比较, 差异均有统计学意义(P<0.05);两组患者左心房直径(LA)、射血分数(EF)比较, 差异有统计学意义(P<0.05)。结论 尿毒症继发甲旁亢对患者左室射血分数和左心房直径的影响可造成对心脏结构的影响。iPTH 升高与透析龄、血钙、血磷和Ca-P乘积呈正相关;对左心室收缩末期容积、舒张末期容积、主动脉根直径、室间隔厚度无明显影响。
【关键词】 尿毒症;继发;甲状旁腺功能亢进;甲状旁腺激素;左室射血分数;左心房直径
1 资料与方法
1. 1 一般资料 选取2009~2012年中日友好医院接受PTX手术治疗的患者45例, 为组1。选取2005~2013年台湾高雄长庚医院进行腹膜透析的患者60例, 为组2。收集术前心脏多普勒超声检查, 记录患者的基础信息:性别、年龄、透析龄;透析前化验:血钙、血磷、iPTH等。记录患者的基础信息和心脏多普勒超声检查结果及同期的化验, 包括:血钙、血磷、血浆白蛋白、iPTH等。其中包含有PTX术后的患者15例。iPTH均≤800 pg/ml。
1. 2 方法 使用Philips iE 33彩色多普勒超声仪所有患者数据连续测量3次, 取其平均值。常规超声心动图M 型测量主动脉根直径(AoR)、室间隔厚度(IVSd)、左心室舒张末期内径(LVIDd)、左心室收缩末期内径(LVIDs)等。
1. 3 观察指标 比较两组患者例数、年龄、透析龄、iPTH值和Ca-P乘积及两组心脏彩色多普勒的结果。
1. 4 统计学方法 采用SPSS17.0统计学软件对数据进行统计分析。计量资料以均数±标准差( x-±s)表示, 采用t检验;计数资料以率(%)表示, 采用χ2检验。P<0.05表示差异具有统计学意义。
2 结果
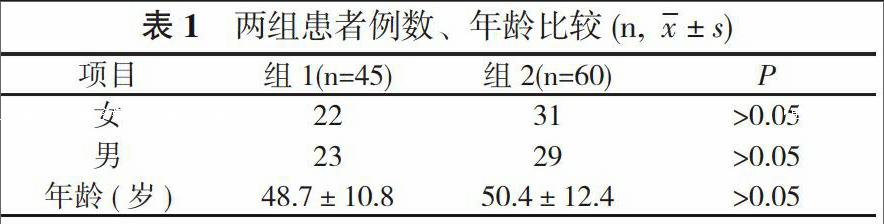
2. 1 两组患者例数及平均年龄比较 组1中男23例、女22例, 年龄30~77岁, 平均年龄(48.7±10.8)岁, 透析龄(105.2±49.6)个月。患者的iPTH均≥800 pg/ml;组2中男29例、女31例, 年龄28~77岁, 平均年龄(50.4±12.4)岁, 透析龄(33.0±13.1)个月。包含有PTX术后患者15例, iPTH均<800 pg/ml。两组患者例数及平均年龄比较, 差异无统计学意义(P>0.05)。见表1。
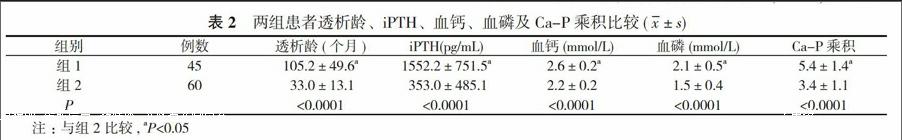
2. 2 两组各项检测结果比较 两组患者透析龄、iPTH、血钙、血磷和Ca-P乘积比较, 差异均有统计学意义(P<0.05)。见表2。
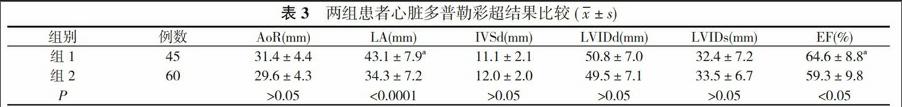
2. 3 两组心脏彩色多普勒结果比较 两组患者LA、EF比较, 差异有统计学意义(P<0.05)。见表3。
3 讨论
组1选取中日友好医院的患者均行PTX手术, iPTH> 800 pg/ml为诊断难治性甲状旁腺功能亢进的诊断标准之一。此类患者通常透析时间较长, 合并严重的钙磷代谢异常, 有研究发现许多年轻的透析患者可出现很严重的血管钙化[1, 2]。因此冠状动脉钙化是危及血液透析患者生命安全的重要因素[3, 4]。发生血管钙化的机制目前尚不是很清楚, 但高磷、高钙磷乘积及继发甲状旁腺功能亢进可能是血管钙化的主要原因。心血管钙化是多因素参与的主动调节过程, 钙化促进因素与钙化抑制因素不平衡的结果[5]。继发甲状旁腺功能亢进时, 过高的iPTH水平可增加胞浆中钙离子的水平, 引起转移性钙化。
组2腹膜透析患者在透析龄、血钙、血磷、Ca-P乘积、iPTH水平方面与组1比较, 差异有统计学意义(P<0.05)。台湾健全的医疗体系使患者在慢性肾脏病(CKD)早起即开始全方面的干预和治疗, 使得患者能够早期对合并症有计划的治疗, 透析进入的时间选择上要相对更早, 同时腹膜透析对残余肾功能的保护相对于血液透析更好。残余肾功能对于钙磷代谢和继发甲状旁腺功能亢进的进展起到推迟和保护作用。两组患者LA、EF比较, 差异有统计学意义(P<0.05)。
两组血钙、血磷、Ca-P乘积和iPTH水平方面均存在较大差异(P<0.05)。但在心脏多普勒的超声检查方面研究结果显示重度继发甲旁亢患者和没有合并甲旁亢的患者的左室射血分数和左心房直径是有显著差异的。
有研究结果显示尿毒症心脏瓣膜钙化的特点为:①主动脉瓣受累多于二尖瓣;②瓣环多于瓣叶;③主动脉无冠瓣环钙化多于左和右冠瓣环钙化;④二尖瓣后瓣环钙化多于前瓣环钙化 这些特点似乎与老年性瓣膜钙化一致。即主动脉瓣承受较大血流压力, 钙盐更易在此沉积。老年性瓣膜钙化常常累及瓣环和二尖瓣后瓣环。有研究表明左心房壁薄是尿毒症瓣膜钙化所致反流最先累及的地方, 而左心室壁厚, 代偿性好, 故短时间内其结构和射血分数难以改变。但由于短期内左心房可受影响, 因此不能忽视尿毒症瓣膜钙化对心脏的影响。但对于尿毒症患者继发甲状旁腺功能亢进造成的心血管钙化, 心室重构的机制尚不清楚, 仍需继续探讨。
参考文献
[1] Chan WK, Lee KW, But WM, et al. Vascular calcification in a young patient with end-stage renal disease. Hong Kong Med J, 2013, 19(2):178-181.
[2] Imai N, Nagasawa M, Kimura K. Severe calcification of the arteries. Intern Med, 2012, 51(11):1445.
[3] Nakamura SI, Ishibashi-Ueda H, Niizuma S, et al. Coronary calcification in patients with chronic kidney disease and coronary artery disease. Clin J Am Soc Nephrol, 2009, 4(12):1892-1900.
[4] Patel AA, Budoff MJ. Screening for heart disease: C-reactive protein versus coronary artery calcium. Expert Rev Cardiovasc Ther, 2010, 8(1):125-131.
[5] Cozzolino MI, Mazzaferro S, Pugliese F, et al. Vascular calcification and uremia: what do we know? Am J Nephrol, 2008, 28(2):339-346.
[收稿日期:2015-12-03]

