显微手术治疗颅内动脉瘤破裂后脑血管痉挛发生的影响因素
程宇宏
【摘要】 目的 分析显微手术治疗颅内动脉瘤破裂后脑血管痉挛发生的影响因素。方法 100例行显微手术治疗的颅内动脉瘤破裂患者, 对其临床资料进行回顾性分析, 对影响脑血管痉挛发生的因素进行分析。结果 吸烟、年龄≤50岁、出血次数≥2次的脑血管痉挛发生率显著增加, 差异有统计学意义(P<0.05);术前Fisher分级≥Ⅲ级、Hunt-Hess分级≥Ⅲ级患者的脑血管痉挛发生率显著高于Ⅰ~Ⅱ级患者, 差异有统计学意义(P<0.05)。影响患者术后血管痉挛发生的影响因素包括吸烟、年龄≤50岁、术前Hunt-Hess分级≥Ⅲ级、Fisher分级≥Ⅲ级以及出血≥2次。结论 影响显微手术治疗颅内动脉瘤破裂后脑血管痉挛发生的因素包括吸烟、年龄≤50岁、出血次数≥2次、术前Hunt-Hess分级≥Ⅲ级、Fisher分级≥Ⅲ级。
【关键词】 显微手术;颅内动脉瘤破裂;脑血管痉挛;影响因素
临床中在对颅内动脉瘤破裂进行治疗时, 首选方法为显微手术夹闭, 但是临床医务人员应关注术后的脑血管痉挛发生情况。脑血管痉挛会引起延迟性缺血性神经功能障碍, 增加动脉瘤患者的死亡率和致残率[1]。本研究主要分析了显微手术治疗颅内动脉瘤破裂后脑血管痉挛发生的影响因素, 现总结如下。
1 资料与方法
1. 1 一般资料 选取2013年1月~2015年1月本院收治的100例行显微手术治疗的颅内动脉瘤破裂患者, 全部患者均于术前经过CT血管造影(CTA)或者全脑数字血管减影确诊。患者中男43例, 女57例;年龄20~74岁, 平均年龄(54.2±14.1)岁;合并糖尿病的患者41例, 合并高血压的患者51例。Hunt-Hess分级为:Ⅰ级13例, Ⅱ级22例, Ⅲ级34例, Ⅳ级23例, V级8例。
1. 2 方法 CT血管造影或者全脑数字血管减影检查发现, 全部100例患者中存在动脉瘤112个, 前、后交通动脉瘤个数分别为35个和32个, 大脑前、中、后动脉瘤个数分别为15个、19个和11个。CT Fisher分级为:Ⅰ级15例, Ⅱ级30例, Ⅲ级38例, Ⅳ级17例。回顾性分析全部患者的临床治疗, 详细询问患者的年龄、吸烟情况、合并症、术前Hunt-Hess分级、Fisher分级等情况, 并记录。
1. 3 术后脑血管痉挛的诊断标准 ①临床诊断:术后患者意识状态恶化, 存在颅内压增高情况和新局灶定位体征, 对患者进行临床检查可知患者并没有新的神经缺损症状或者其他因素导致的原有症状加重, 则为脑血管痉挛;②经过CTA或者磁共振血管造影(MRA)或者脑血管造影检查证实为脑血管痉挛;③经颅多普勒(TCD)血流指标诊断标准:患者大脑中动脉血流的流速峰值>200 cm/s和(或)平均流速>120 cm/s。
1. 4 统计学方法 采用SPSS19.0统计学软件处理数据。计数资料以率(%)表示, 采用χ2检验。P<0.05表示差异有统计学意义。
2 结果
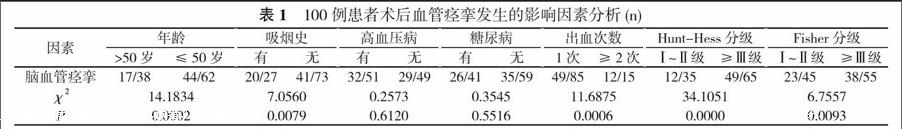
吸烟、年龄≤50岁、出血次数≥2次的脑血管痉挛发生率显著增加, 差异有统计学意义(P<0.05);术前Fisher分级≥Ⅲ级、Hunt-Hess分级≥Ⅲ级患者的脑血管痉挛发生率显著高于Ⅰ~Ⅱ级患者, 差异有统计学意义(P<0.05)。影响患者术后血管痉挛发生的影响因素包括吸烟、年龄≤50岁、术前Hunt-Hess分级≥Ⅲ级、Fisher分级≥Ⅲ级以及出血≥2次。见表1。
3 小结
脑血管痉挛的发生过程比较复杂, 临床研究, 蛛网膜下腔血凝块会引起脑血管痉挛, 蛛网膜下腔血管的大小和部位会直接决定脑血管痉挛的严重程度和部位[2]。Fisher分级直接反映了动脉瘤蛛网膜下腔出血的分布和出血量, 是反映脑血管痉挛和蛛网膜下腔积血量的主要指标[3, 4]。
综上所述, 影响显微手术治疗颅内动脉瘤破裂后脑血管痉挛发生的因素包括吸烟、年龄≤50岁、出血次数≥2次、术前Hunt-Hess分级≥Ⅲ级以及Fisher分级≥Ⅲ级。
参考文献
[1] 李金坤, 孙晓娟, 吴洪涛.颅内动脉瘤破裂的患者预后影响因素分析.中华老年心脑血管病杂志, 2015, 17(6):613-615.
[2] 唐志鹏.颅内动脉瘤破裂术后脑血管痉挛影响因素分析.中国现代医生, 2014, 52(7):46-47.
[3] 马荣耀, 朱帅, 李柯.颅内动脉瘤破裂栓塞治疗后症状性脑血管痉挛的发生及影响因素分析.中华神经医学杂志, 2011, 10(9): 945-947.
[4] 王刚, 冯文峰, 张国忠, 等. 3T磁共振血管造影在颅内动脉瘤弹簧圈栓塞术后随访价值的汇总分析. 国际脑血管病杂志, 2012, 20(1):42-47.
[收稿日期:2015-12-15]

