血糖参考测量实验室能力验证*
血糖参考测量实验室能力验证*
全灿1,李红梅1,徐蓓1,吴佳佳1,史光华2,吕京2,陈宝荣3
(1.中国计量科学研究院,北京 100029;2.中国合格评定国家认可委员会,北京 100062;
3.北京航天总医院检验科,北京 100076)
本论文在质检公益性行业科研专项项目的资助下,建立同位素稀释质谱技术开展国际比对,研制血清葡萄糖国家标准物质,并应用于参考测量实验室的血糖能力评估,验证我国参考测量实验室血糖测量能力,为参考测量程序提供可溯源性,报道如下。
1计划概述
1.1项目简介葡萄糖是人体内新陈代谢的重要物质,是人体能量的主要来源之一。血糖浓度测定、口服糖耐量试验是临床诊断糖尿病的重要指标[1]。人血清葡萄糖的常规测定方法主要包括葡萄糖氧化酶法和己糖激酶法。葡萄糖氧化酶法操作简便,性能较好,广泛用于临床,但是此方法线性范围较窄,抗干扰能力稍差;己糖激酶方法性能优于前者,但由于价格偏高,临床应用受到限制;干化学法快速简便,主要用于急诊[2]。参考测量程序:亦称参考方法,是经过充分研究的测量程序,给出的量值测量不确定度适合其预期用途,主要用于评价测量相同被测量的其他测量程序[3]。血清葡萄糖测定的一级参考测量程序是同位素稀释质谱法(IDMS),二级参考测量程序是己糖激酶分光光度法[4]。《血清葡萄糖测定参考方法》WS/T 350-2011是由卫生部临床检验标准专业委员会提出改采用由国际检验医学溯源联合委员会(JCTLM)批准的《CDC人血清葡萄糖己糖激酶参考方法(分光光度法)》,并参考ISO15193:2009《体外诊断器具-生物源样品中量的测定-参考测定程序的表述》适当增加内容[5]。
1.2参加实验室本次选用中国计量科学研究院实验室建立的同位素稀释质谱法作为参考值的确定方法。中国计量科学研究院建立的同位素稀释质谱法参加了CCQM的血糖国际比对CCQM K11.1和K11.2[6]。本次能力验证得到了国家科技基础性专项项目(2011FY130100)的支持。共10家来自北京、上海、广东、四川、浙江、吉林共5省的10家血糖参考实验室参加了本次能力验证项目,包括医院、临床检验、医疗器械及民营实验室等。每个参加实验室被赋予唯一的实验室代码,能力验证相关报告均按代码标识参加实验室。
2能力验证
2.1方案设计依据CNAS-CL03:2006《能力验证提供者认可规则》[7]设计本次能力验证。
2.1.1样品制备及浓度水平本次PT样品为健康人血清样品和添加样本,依据CNAS-CL03:2006《能力验证提供者认可规则》。本次能力验证样品为血清中葡萄糖基体标准物质样品,按照一级标准物质技术规范(JJG1006-94)[8]进行制备。每家机构将获得2个浓度水平的样品,各浓度样品量不少于10瓶,每瓶约0.5 mL。样品基质为人体血清。浓度1,量值在5~7 mmol/L;浓度2,量值在12~15 mmol/L范围。
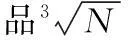
2.1.3样品储存、运输和分发每家实验室发给随机配对抽取的两个浓度水平的样品,与能力验证实施指南、样品确认单、实验室代码编号和测量结果总结表等,采用现场或特快专递的方式发给各参加实验室。样品长期保存需-80 ℃,干冰运输,以物流方式将样品发送至各参加技术机构。当样品到达后,参加者应立即核查运输包装是否有损坏、干冰是否还有剩余、样品是否保持低温状态。如果情况正常,则填写接收交接单,并发送邮件或传真至组织单位。如果在传送过程中有意外情况发生,应及时通报组织单位,由组织单位按意外情况进行处理。
2.1.4能力验证方法本次能力验证,参加实验室可选用:(1)WS/T 350——《人血清葡萄糖己糖激酶参考方法(分光光度法)》;(2)《同位素稀释质谱法(GC ID/MS 或LC/ID/MS/MS) 测定血清葡萄糖》的1种或者两种。参加实验室在收到样品后,根据检验方法进行检测,最后报告血糖的测量结果。
2.2统计评价方法能力验证统计方法取决于实验结果的总体分布,通过统计验证实验室的数据分布,以确定合适的统计方法。
2.2.1数据准备在对实验结果进行统计分析之前,应确保数据是正确、合理的。输入并检查所有数据结果(必要时经过转换),制作显示结果分布的数据直方图,以检验正态性假设。通过数据直方图检查结果是否连续和对称。
2.2.2总计统计量完成了数据准备,就可以用总计统计量来描述结果,包括结果数、中位值、标准四分位数间距(IQR)、稳健的变异系数(CV)、最小值、最大值和极差等统计量[10-11]。结果数是从一个特定检测中得到的结果总数,符号为N。

3血糖能力验证结果及统计评价
3.1样品A血糖能力验证结果见表1、图1(见《国际检验医学杂志》网站主页“论文附件”)。
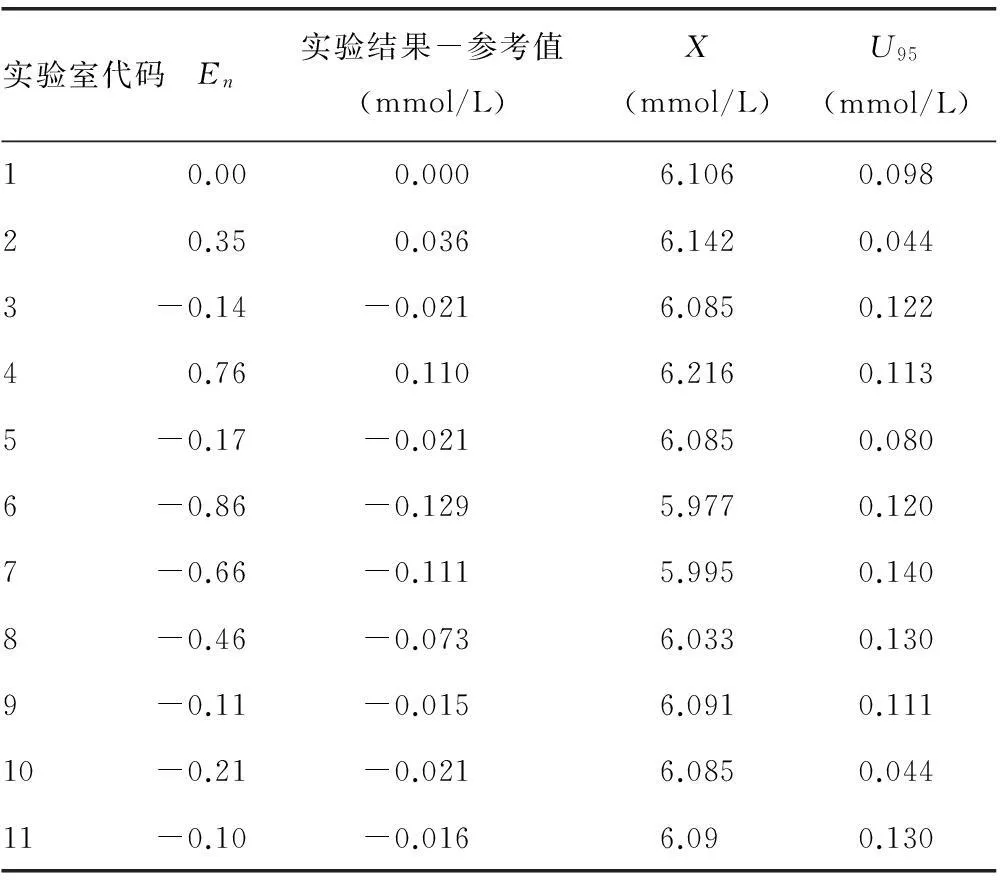
表1 样品A的能力验证结果
3.2样品B血糖能力验证结果见表2、图2(见《国际检验医学杂志》网站主页“论文附件”)。
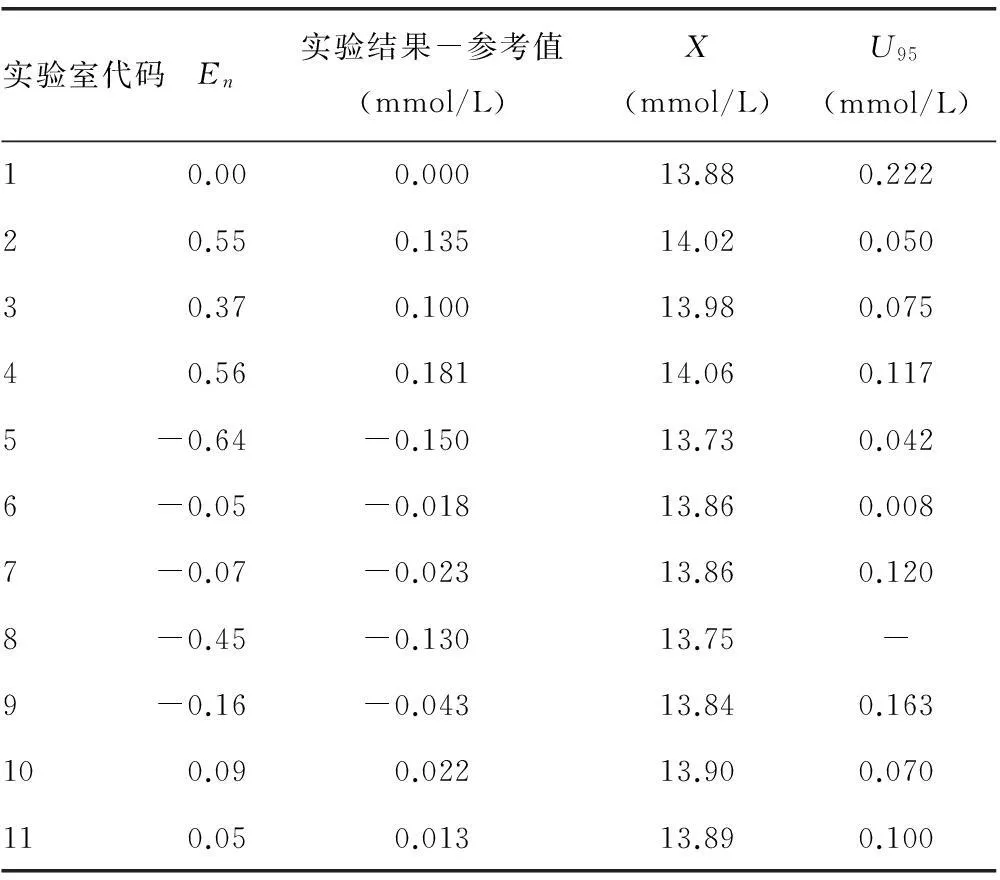
表2 样品B的能力验证结果
-:无数据。
3.3图形显示在最终报告中应有结果的图示及其相关的不确定度。图3、4(见《国际检验医学杂志》网站主页“论文附件”)分布显示了在表1、2中的结果。每个参加实验室的值和参考值用菱形◆表示。实验室值向上和向下延伸的线段代表实验室报告的不确定度。
4技术分析
4.1不同参考测量程序的比较绝大部分参加实验室采用第一法:WS/T350-2011血清葡萄糖测定参考方法,该方法采用在己糖激酶催化下,葡萄糖和三磷酸腺苷(ATP)磷
酸化反应,生成葡萄糖-6-磷酸与ADP。葡萄糖-6-磷酸催化脱氢,生成6-磷酸葡萄糖酸,同时NAD还原成NADH。通过紫外可见分光光度计检测吸光度;只有2号实验室采用同位素稀释气相色谱质谱法(ID-GC/MS),对应的前处理方法为衍生化,先后和盐酸羟胺、醋酐反应,得到糖腈乙酰酯衍生物。利用IDGCMS具有更小的不确定度。
4.2不确定度评定部分参考实验室尚未掌握不确定度评定,没有依据《测量不确定度要求的实施指南》[14]开展不确定度评定,对A类、B类、样品称量、前处理、定值等不确定度分量不能正确分析和评定,对线性拟合不确定评定基本没有考虑。
参考文献
[1]Quan C.Establishment of the purity values of carbohydrate certified reference materials using quantitative nuclear magnetic resonance and mass balance approach[J].Food Chem,2014,153(1):378-386.
[2]Weissman M,Klein B.Evaluation of glucose determinations in untreated serum samples[J].Clin Chem,1958,4(5):420-422.
[3]International Organization for Standardization.ISO 17025 General requirements for the competence of testing and calibration laboratories[S].2nd ed.Switzerland:ISO,2005.
[4]Jones GR,Jackson C.The Joint Committee for Traceability in Laboratory Medicine (JCTLM) - its history and operation[J].Clinica Chimica Acta,2016,453(30):86-94.
[5]孙慧颖,邵燕,胡滨,等.7种血清葡萄糖常规检测系统测量结果的正确度评价[J].临床检验杂志,2013,31 (7):542-544.
[6]丁兆婷,全灿,金君素,等.气相色谱-质谱法测定人血清中葡萄糖含量[J].北京化工大学学报:自然科学版,2010,37(2):109-112.
[7]中国合格评定国家认可委员会.CNAS-CL03 能力验证计划者认可准则[S].北京:中国合格评定国家认可委员会,2006.
[8]国家标准物质研究中心.JJG1006 一级标准物质技术规范[S].北京:国家标准物质研究中心,1994.
[9]中国合格评定国家认可委员会.CNAS-GL03 能力验证样品均匀性和稳定性评价指南[S].北京:中国合格评定国家认可委员会,2006.
[10]臧慕文,柯瑞华.成分分析中的数理统计集不确定度评定概要[M].北京:中国质检出版社,2012.
[11]全浩,韩永志.标准物质及其应用技术[M].2版.北京:化学工业出版社,1993.
[12]中国合格评定国家认可委员会.CNAS-RL02能力验证规则[S].北京:中国合格评定国家认可委员会,2010.
[13]中国合格评定国家认可委员会.CNAS-GL02能力验证结果的统计处理和能力评价指南[S].北京:中国合格评定国家认可委员会,2006.
[14]中国合格评定国家认可委员会.CNAS-GL05测量不确定度要求的实施指南[S].北京:中国合格评定国家认可委员会,2011.

血清肿瘤标志物PSA检测助力前列腺癌有效管理
日前,在北京举办的肿瘤标志物大师班交流会上,西班牙巴塞罗那临床医院生化实验室癌症研究中心主任Rafael Molina教授就PSA的研究发展、医学价值及其对前列腺癌管理的应用进行了深入探讨。
WHO 1999年发布的PSA校准方法(WHO 96/670)将截断(cut-off)值定为3.1 ng/mL,一般超过10 ng/mL考虑罹患前列腺癌的可能。但血清PSA浓度在前列腺增生和前列腺炎中均有升高,前列腺良性疾病与前列腺癌在2~10 ng/mL时有交叉,存在很高比例的假阴性和假阳性结果。若假阴性出现在2~4 ng/mL,可导致15%癌症漏检;假阳性在4~10 ng/mL出现时,被认为是判断前列腺癌的灰区,65%良性疾病被错判为癌症。此时,可通过结合fPSA计算游离前列腺指数(%fPSA),提高检出率。在tPSA水平为4~10 ng/mL的患者中,以%fPSA为标准可减少35%不必要的活检,检出敏感性达94%。
Molina教授介绍了一项覆盖欧洲八个国家、入组50~74岁男性人群的欧洲前列腺癌随机筛查研究(ERSPC),结果发现,随访至第9年时,核心年龄段定期筛查组与对照组的前列腺癌死亡率之比为0.85;随访至第11年时,比值为0.78。近期,在《柳叶刀》杂志上公布的13年随访结果显示,55~69岁男性中,PSA筛查使前列腺癌死亡率下降了21%,且与随访9年和11年结果相比,获益呈增长趋势。
PSA筛查也存在潜在伤害,包括过度诊断和随之而来的过度治疗。Molina教授表示:“筛查前,建议医生和患者讨论检测项目的选择、益处和可能的副作用,以便患者根据情况做出自己的选择,对有早期诊断要求的人群不应拒绝进行PSA筛查。”
由于tPSA检测方法多样,不同厂商试剂、不同检测方法之间差异水平达10%~40%。为提高PSA检测特异性,临床医生需结合年龄特异性参考范围、PSA抗原密度(PSA/D)、速率(PSAV)、游离与总PSA比(f/t)、外周带PSA(PSA-TZD)检测等附加指标综合判断。虽然当前不同PSA检测方法之间差异仍较大,但随着诊断技术改进,PSA检测精准度正在不断提高。罗氏诊断Elecsys®PSA和fPSA检测拥有WHO标准溯源,只需一管血,18分钟就能为临床提供准确结果和高医学价值信息,为患者长期随访提供可靠依据,有助于实现前列腺癌高效管理。
(收稿日期:2015-09-24)
DOI:10.3969/j.issn.1673-4130.2016.04.068
文献标识码:B
文章编号:1673-4130(2016)04-0571-03
基金项目:质检公益性行业科研专项项目(201410234);质检公益性行业科研专项项目(201210066);国家科技基础性专项项目(2011FY130100)。
·检验科与实验室管理·

