ELISA检测血清EV71-IgM诊断手足口病价值的Meta分析*
·论著·
ELISA检测血清EV71-IgM诊断手足口病价值的Meta分析*
郑华珍1,2,刘新光1,2,3,赵炜1,2△
(1.广东医学院衰老研究所,广东东莞523808;2.广东省医学分子诊断重点实验室,广东东莞523808;
3.广东医学院生物化学与分子生物学研究所,广东东莞523808)
摘要:目的系统评价酶联免疫吸附试验(ELISA)检测血清肠道病毒71型IgM抗体(EV71-IgM)诊断手足口病(HFMD)的价值。方法检索PubMed、Embase、Web of Science、Cochrane、维普、万方、中国知网以及中国医学生物文献数据库中有关用ELISA检测EV71-IgM诊断HFMD的文献,检索时限从建库至2015年1月。对符合纳入标准的文献进行资料提取、方法学质量评价,采用Meta-disc 1.4软件进行Meta分析。结果共纳入文献8篇,合计4 126例,其中HFMD患者1 484例,非HFMD患者2 642例。Meta分析结果显示,各研究间存在非阈值效应引起的异质性,合并灵敏度、特异度和诊断比值比分别为84%、90%、28.77;拟合综合受试者特征曲线(SROC)下面积为0.906 8。结论ELISA检测血清EV71-IgM诊断HFMD有较高的诊断价值,但因纳入研究存在一些方法学缺陷,该结论尚需进一步开展高质量的诊断性试验来进行验证。
关键词:肠道病毒71型;手足口病;酶联免疫吸附试验;Meta分析
肠道病毒71型(EV71)是人类肠道病毒的一种,为单股正链RNA病毒,是引起手足口病(HFMD)的主要病原体之一。近年来,EV71流行日益严重,且相对于柯萨奇病毒感染患者,EV71感染患者更容易出现脑膜炎、脑炎、脑脊髓炎及肺水肿等并发症[1]。细胞培养分离病毒是EV71感染诊断的“金标准”,该方法特异度高,但灵敏度低,鉴定时间长,不适合临床大规模检测;反转录聚合酶链反应(RT-PCR)和荧光定量聚合酶链反应(FQ-PCR)是EV71临床实验室诊断的主要方法,其特异度和灵敏度高,但成本较高,样品处理较复杂;免疫学检查操作简单,不需要特殊仪器,被广泛应用于初筛试验,但准确性较低[2]。ELISA检测血清EV71-IgM是辅助诊断HFMD的常见免疫学方法,为了进一步系统地评价该方法诊断HFMD的准确性,本研究全面收集相关文献进行Meta分析,以期为该方法在临床诊断应用中提供更可靠的证据。
1资料与方法
1.1一般资料计算机检索PubMed、Embase、Web of Science、Cochrane、维普数据库、万方数据库、中国知网以及中国医学生物文献数据库,全面收集有关ELISA检测EV71感染的诊断性试验。检索时限均为建库至2015年1月。英文检索词包括“enterovirus 71”,“enterovirus type 71”,“EV71”,“hand,foot and mouth disease”,“HFMD”,“enzyme-linked immunosorbent assay”,“ELISA”。中文检索词包括“肠道病毒71型”、“手足口病”、“酶联免疫吸附试验”、“ELISA”。
1.2纳入标准(1)研究类型为公开发表的关于EV71感染准确性的诊断性试验研究;(2)诊断金标准为细胞培养分离病毒或FQ-PCR;(3)检测方法是ELISA法;(4)评价指标为血清中EV71-IgM水平;(5)各研究中可以提取到完整的四格表数值。
1.3排除标准(1)非EV71感染研究;(2)无法获取四格表信息;(3)研究例数少于20例;(4)非临床诊断研究试验、会议摘要及综述等文献;(5)同一作者重复发表的文献。
1.4文献筛选、数据提取和质量评价由两位研究者按照上述纳入和排除标准独立筛选文献,提取资料。提取资料内容包括第一作者、发表时间、试剂来源、样品总数、真阳性值、假阳性值、真阴性值、假阴性值等。用诊断试验质量评价工具QUADAS[3]对筛选出来的文献进行质量评价。评价内容是每项条目按“是”、“否”、“不清楚”进行评价,评价为“是”得1分,“否”为0分,“不清楚”得0.5分,进而算出每篇文献得分,如有分歧则通过第三方介入协商解决。
1.5统计学处理采用Meta Disc 1.4软件进行数据分析。先合并分析各研究间是否存在阈值效应引起的异质性。若有阈值效应,数据合并的最佳方式是拟合综合受试者特征曲线(SROC)并计算曲线下面积(AUC)或应用Q*指数(Q*)。若无阈值效应,则进一步判断是否存在非阈值效应所引起的异质性,并采用固定(无异质性时)或随机效应模型(有异质性时)计算其合并灵敏度(SEN)、特异度(SPE)、阳性似然比(PLR)、阴性似然比(NLR)和诊断比值比(DOR),绘制SROC曲线,并计算AUC和Q*。
2结果
2.1文献检索结果初筛选出相关文献共365篇,其中英文文献118篇、中文文献247篇,排除综述、重复发表、不符合纳入标准文献后,最终纳入8篇文献,英文文献1篇,中文文献7篇。
2.2纳入研究的基本特征与方法质量评价8项研究发表于2004~2014年,共4 126例,各项研究的基本特征见表1。8项研究均未提及检测结果的观察是否采用盲法,亦未报告难以解释的结果,纳入研究的详细QUADAS质量评价结果见表2(见《国际检验医学杂志》网站主页“论文附件”)。
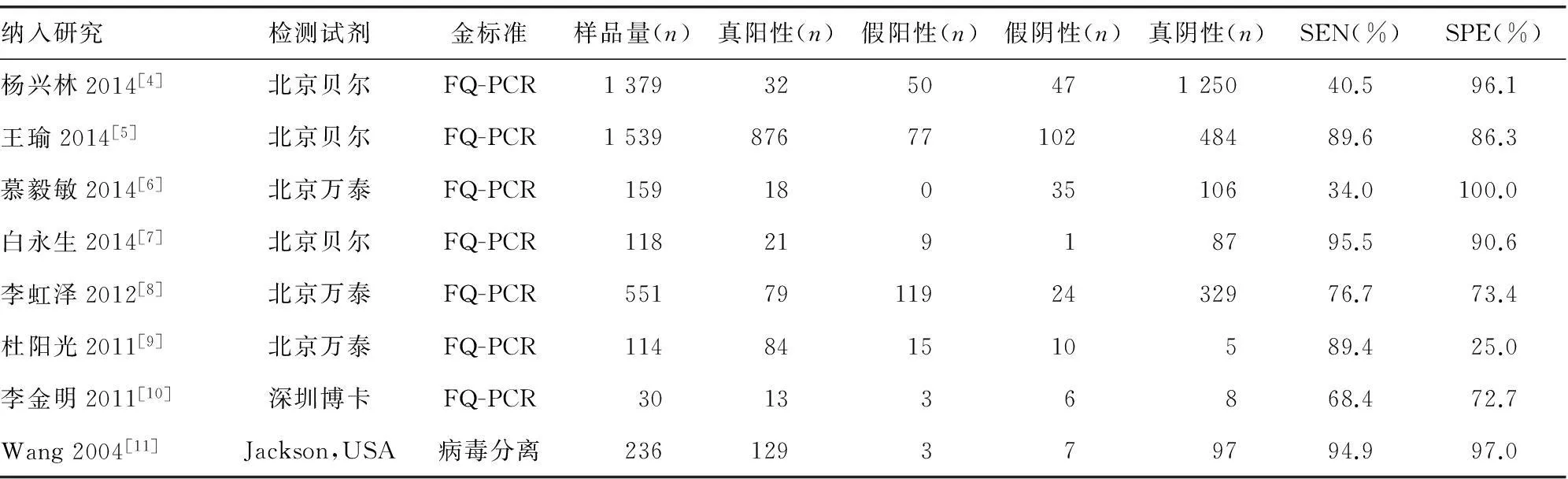
表1 纳入研究的基本特征
2.3异质性检验
2.3.1阈值效应本研究通过SROC曲线平面图检验阈值效应,结果显示不呈“肩臂状”分布,提示不存在阈值效应。进一步计算灵敏度对数与(1-特异度)对数的Spearman相关系数为0.143,P=0.736,亦表明各研究间不存在阈值效应。
2.3.2非阈值效应本研究通过DOR探讨非阈值效应引起的异质性,DOR的Cochran-Q检验结果为I2=91.3%,Cochran-Q=80.34,P=0.000 0,表明存在非阈值效应引起的异质性,故Meta分析模型选用随机效应模型。
2.4Meta分析结果
2.4.1合并统计量采用Meta Disc 1.4软件随机效应模型Meta分析结果显示SEN合=0.84[95%CI(0.82~0.86)];SPE合=0.90[95%CI(0.88~0.91)];PLR合=6.14[95%CI(2.93~12.87)];NLR合=0.25[95%CI(0.12~0.53)];DOR合=28.77[95%CI(10.91~75.84)]。
2.4.2SROC曲线分析用Meta Disc 1.4软件绘制SROC曲线,结果显示:AUCSROC=0.906 8(SE=0.042 6),Q*=0.838 6(SE=0.046 6)。
2.4.3异质性来源分析由于存在非阈值效应引起的异质性,现按ELISA试剂盒生产厂家和研究样品量进行亚组分析,从而分析异质性的可能来源。试剂盒主要来源于北京贝尔生物制品有限公司和北京万泰生物药业股份有限公司,且使用这两家试剂盒的研究各有3项。另外,对研究样品量进行分析,8项研究中有4项样品量小于或等于200例,4项样品量大于200例。采用随机效应模型进行亚组分析,结果见表3。

表3 生产厂家与样品量的亚组分析
3讨论
EV71感染是全球性的重大公共卫生问题,不同地区EV71的流行差异很大,我国是EV71感染最为严重的地区之一[12]。因此,判断EV71感染对HFMD的早期诊断和防治具有重要意义。血清EV71-IgM是EV71感染的早期诊断指标之一,在感染后第1~2天即可出现,并且随着病程的延长阳性检出率不断增加[13-14]。商品化试剂盒一般采用ELISA捕获法对EV71-IgM进行检测。
本文全面检索了有关使用ELISA检测EV71-IgM诊断HFMD的研究,最终纳入8项研究。按照QUADAS对各文献进行质量评估,结果显示纳入文献为中高质量,结果较可信。通过Meta Disc 1.4软件描绘SROC曲线平面图和计算Spearman相关系数可知纳入研究间不存在阈值效应。但对其他来源的异质性进行检验,发现存在异质性。因此,采用随机效应模型合并效应量以减少异质性影响。
本研究结果显示采用ELISA检测血清EV71-IgM诊断HFMD的合并灵敏度和特异度都较高,为84%和90%。表明采用ELISA检测EV71-IgM有84%的把握度将HFMD患者检测出来,漏诊率为16%。这除了试剂盒本身方法学的不足,操作技术等原因导致假阴性外,还有可能因为存在其他肠道病毒的多重感染出现交叉反应,而降低EV71-IgM水平[15]。所以,对于临床症状明显而检测结果为阴性者,应联合检测其他相关项目。另外,该试验能将90%的非EV71感染患者分辨出来,10%的非EV71感染患者可能误诊为患病。流行病学研究认为,阳性似然比大于10有肯定诊断的价值,阴性似然比小于0.1有否定价值。本研究中合并阳性似然比为6.14,表明检测EV71-IgM阳性则患HFMD的可能性是不患HFMD的6.14倍;合并阴性似然比为0.25,提示EV71-IgM阴性疑似病例不能排除感染EV71的可能。合并DOR为28.77,说明用ELISA检测EV71-IgM诊断HFMD的效果较好。
SROC曲线不仅能反映诊断试验的特异度和灵敏度,而且还能对某一诊断试性验进行全面的评价。AUC是用于评判诊断性试验的准确性,取值在0.9以上时表示诊断准确性较高[16]。本研究绘制了SROC曲线,并得出其AUC为0.906 8,表明用ELISA检测EV71-IgM诊断HFMD的准确性较好。
本研究对使用不同厂家试剂盒的研究进行Meta分析,发现北京贝尔试剂盒的检测灵敏度和特异度均高于北京万泰试剂盒。提示两试剂盒可能存在方法学异质性,这可能是因为包被的抗体来源、包被工艺、标记酶等不同。另外,发现样品量大于200例研究的检测合并灵敏度高于样品量小于或等于200例的,对特异度则无影响。这可能是因为不同样本量下阳性检出率明显不一致,样本量越大,其阳性检出率越高,故诊断效能高。
此外,还有一些因素可能导致本研究的异质性。如同样使用北京贝尔公司的试剂盒,杨兴林等[4]和王瑜[5]的研究中检测灵敏度和特异度分别为40%、96%和89%、86%,说明不同实验室间的操作技术、实验仪器等可能存在差异。各研究中纳入的研究对象间的差异也是导致异质性的一个重要原因。本研究纳入文献[9]同时选择临床确诊患者和健康人为研究对象,文献[4,10-11]以临床疑似患者为研究对象,而文献[5-8]是以临床确诊患者为研究对象。另外,本Meta分析中的各项研究检测时未说明是否采用盲法,因此会增加检测偏倚的可能性。
综上所述,ELISA检测血清EV71-IgM诊断手足口病有较高的诊断价值,可用于手足口病的辅助诊断。但由于纳入研究存在一些方法学缺陷,本结论仍需要进一步开展高质量的诊断性试验来进行验证。
参考文献
[1]Ho M.Enterovirus 71:the virus,its infections and outbreaks[J].Microbiol Immunol Infect,2000,33(4):205-216.
[2]田燕,陆志刚,梁洁.手足口病检测方法的研究进展[J].现代预防医学,2011,38(15):3058-3059.
[3]Whiting PF,Weswood ME,Rutjes AW,et al.QUADAS评价:一种用于诊断性研究的质量评价工具(修订版)[J].中国循证医学杂志,2007,7(7):531-536.
[4]杨兴林,熊金凤,李丽,等.荧光聚合酶链式反应与酶联免疫吸附法筛查肠道病毒71型病原感染的比较研究[J].华西医学,2014,29(7):1309-1312.
[5]王瑜.联合检测手足口病肠道病毒71型RNA及IgM结果分析[J].医药论坛杂志,2014,35(9):31-32.
[6]慕毅敏,代岩石,孙伟,等.肠道病毒71型手足口病病毒3种检测技术比较研究[J].中国卫生工程学,2014,13(3):232-234.
[7]白永生,郭林池,杨安宁,等.病毒性脑炎患者脑脊液肠道病毒和EV71检测与分析[J].宁夏医学杂志,2014,36(9):784-787.
[8]李虹泽,项杰.武汉地区2011年553例手足口病患儿EV71-IgM ELISA法和EV71 RNA RT-PCR法检测结果分析[J].临床肺科杂志,2012,17(9):1726-1727.
[9]杜阳光,杨晋川,晏嘉璐,等.血清中EV71型IgM抗体检测对手足口病诊断的意义[J].中华全科医学,2011,9(10):1574-1575.
[10]李金明,熊德琴,齐晓彤,等.实时荧光定量PCR在手足口病病原体检测中的应用[J].实验与检验医学,2011,29(2):129-130.
[11]Wang SY,Lin TL,Chen HY,et al.Early and rapid detection of enterovirus 71 infection by an IgM-capture ELISA[J].J Virol Methods,2004,119(1):37-43.
[12]Wang Y,Feng Z,Yang Y,et al.Hand,foot,and mouth disease in China:patterns of spread and transmissibility[J].Epidemiology,2011,22(6):781-792.
[13]Xu F,Yan Q,Wang H,et al.Performance of detecting IgM antibodies against enterovirus 71 for early diagnosis[J].PLoS One,2010,5(6):11388.
[14]Tsao KC,Chan EC,Chang LY,et al.Responses of IgM for enterovirus 71 infection[J].J Med Virol,2002,68(4):574-580.
[15]Lin Y,Wen K,Pan Y,et al.Cross-reactivity of anti-EV71 IgM and neutralizing antibody in series sera of patients infected with Enterovirus 71 and Coxsackievirus A 16[J].J Immunoass Immunoch,2011,32(3):233-243.
[16]Mitchell MD.Validation of the summary ROC for diagnostic test meta-analysis:a monte carlo simulation[J].Academic radiology,2003,10(1):25-31.
Value of EV71-IgM tested by enzyme-linked immunosorbent assay in diagnosis of hand,foot and mouth disease:a meta-analysis*
ZhengHuazhen1,2,LiuXinguang1,2,3,ZhaoWei1,2△
(1.InstituteofAgingResearch,GuangdongMedicalCollege,Dongguan,Guangdong523808,China;2.KeyLaboratoryforMedicalMolecularDiagnosticsofGuangdongProvince,Dongguan,Guangdong523808,China;3.InstituteofBiochemistryandMolecularBiology,GuangdongMedicalCollege,Dongguan,Guangdong523808,China)
Abstract:ObjectiveTo systematically review the diagnostic value of EV71-IgM tested by enzyme-linked immunosorbent assay (ELISA) in patients with Hand,Foot and Mouth Disease(HFMD).MethodsSuch databases as PubMed,Embase,Web of Science,Cochrane,VIP,Wan Fang Data,CNKI,and CBM were searched for studies about the diagnostic value of EV71-IgM tested by ELISA in patients with HFMD from inception to January,2015.We screened literature according to inclusion criteria,extracted data,and assessed methodological quality of included studies.Meta-analysis was conducted using Meta-Disc 1.4 software.ResultsA total of eight studies were included,involving a total of 4 126 clinical samples,1 484 of which with EV71 and 2 642 of which with non-EV71.The results of meta-analysis showed that heterogeneity was found in these studies,excepting for threshold effect and the pooled sensitivity,specificity,diagnostic odds ratio(DOR)and the area under the SROC curve was 84%,90%,28.77 and 0.906 8,respectively.ConclusionEV71-IgM tested by ELISA has certain value in the diagnosis of patients with HFMD.But due to some poor methodological qualities of the included studies,the above conclusion should be verified by conducting high quality diagnostic tests.
Key words:Enterovirus 71;hand,foot and mouth disease;enzyme-linked immunosorbent assay;Meta analysis
(收稿日期:2015-10-22)
DOI:10.3969/j.issn.1673-4130.2016.04.005
文献标识码:A
文章编号:1673-4130(2016)04-0444-03
基金项目:国家自然科学基金资助项目(81170327);东莞市医疗卫生单位科技计划一般项目(2012108102022);广东医学院建博科技创新团队资助项目(STIF201102)。
作者简介:郑华珍,女,在读研究生,主要从事临床检验诊断学研究。△通讯作者,E-mail:davidzhao1999@foxmail.com。

