玻璃体腔注射康柏西普联合复合式小梁切除术治疗新生血管性青光眼临床观察
周林,周岚
(淮安市第二人民医院徐州医学院附属淮安医院眼科,江苏 淮安 223002)
玻璃体腔注射康柏西普联合复合式小梁切除术治疗新生血管性青光眼临床观察
周林,周岚
(淮安市第二人民医院徐州医学院附属淮安医院眼科,江苏 淮安 223002)
目的 观察玻璃体腔注射康柏西普(Conbercept)联合复合式小梁切除术治疗新生血管性青光眼(NVG)的临床疗效。方法选取2014年1~12月在徐州医学院附属淮安医院眼科病区住院并确诊为NVG的22例(22眼)患者,行玻璃体腔注射康柏西普(0.50 mg/0.05 ml),8~14 d后行复合式小梁切除术。观察玻璃体腔注射康柏西普后虹膜新生血管消退的时间,眼压的变化以及复合式小梁切除术后视力和眼压的变化。术后随访3~15个月。结果玻璃体腔注射康柏西普后,17只眼虹膜新生血管1周内完全消退,5只眼2周内完全消退。注药前平均眼压(41.53±3.37)mmHg,注药后1周平均眼压(40.12±2.13)mmHg,与注药前比较眼压变化差异无统计学意义(P>0.05)。复合式小梁切除术后1周眼压(11.43±1.68)mmHg,术后1个月眼压(12.15±1.46)mmHg,术后3个月眼压(12.81±1.56)mmHg,最后一次随访眼压(12.03±2.31)mmHg,与术前比较差异均有统计学意义(P<0.05)。术后最佳矫正视力>0.1者4眼,视力0.01~0.1者15眼,与术前视力比较,差异有统计学意义(P<0.05)。结论玻璃体腔注射康柏西普联合复合式小梁切除术能有效地控制眼压,保护视功能。
新生血管性青光眼;玻璃体腔注射;康柏西普;复合小梁切除术;疗效
新生血管性青光眼(Neovascular glaucoma,NVG)是一种继发于广泛性视网膜缺血,如视网膜静脉阻塞、糖尿病性视网膜病变等之后的难治性青光眼,其临床特点是在原发性眼病基础上虹膜出现新生血管,疾病前期由于纤维血管膜封闭了房水外流通道,后期由于纤维血管膜收缩牵拉,使房角关闭,引起眼压升高和剧烈疼痛[1]。与血管形成有关的因子众多,其中血管内皮生长因子(Vascular endothelial growth factor,VEGF)能引起毛细血管通透性增加,诱导体内新生血管的生成,在新生血管形成过程中起关键性作用。本病治疗困难,常规滤过性手术常常失败,术前全视网膜光凝术或冷凝术使新生血管退化,或术中、术后应用抗代谢药可提高手术成功率。房水引流装置或阀门植入手术近年也用于治疗新生血管性青光眼。目前抗VEGF药物治疗新生血管性青光眼成为时下研究热门,我们采用玻璃体腔注射康柏西普(Conbercept)联合复合式小梁切除术并术后及时行全视网膜光凝(Panretinal photocoagulation,PRP)治疗新生血管性青光眼,能有效地减少新生血管的活动性,降低新生血管的渗透性,促使虹膜和房角新生血管消退,有效地控制眼压,取得良好的临床效果。
1 资料与方法
1.1 一般资料 收集2014年1~12月在徐州医学院附属淮安医院眼科病区住院并确诊为NVG的患者22例(22眼),Ⅱ期15眼,Ⅲ期7眼,其中男性12例(12眼),女性10例(10眼);年龄46~72岁,平均(57.13±10.21)岁,其中9例为视网膜静脉阻塞,13例为糖尿病视网膜病变;视力:光感眼前3眼、指数/眼前8眼、0.02~0.1有9眼、>0.1有2眼;术前眼压:(41.53±3.37)mmHg (1 mmHg=0.133 kPa)。术前予以局部及全身降眼压药物均不能控制眼压。
1.2 临床分期 依据发病机制和病程发展进行分期[2]:I期(青光眼前期即虹膜红变期)、Ⅱ期(开角型青光眼期)及Ⅲ期(闭角型青光眼期)。
1.3 方法 选择NVGⅡ期及Ⅲ期的患者,予以玻璃体腔内注射康柏西普联合复合式小梁切除术,术后常规予以全视网膜光凝术,观察术后眼压下降和新生血管消退的情况。(1)玻璃体腔康柏西普注射:抽取康柏西普(商品名Conbercept,成都康弘生物科技有限公司生产)质量浓度10 g/L,0.50 mg/0.05 ml,30G针头距角巩缘3.5 mm倾斜缓慢刺入巩膜,针尖朝向眼球中心(避免伤及晶状体),小心缓慢推完药液。(2)复合式小梁切除术:玻璃体腔注射康柏西普7~14 d后,虹膜及房角新生血管完全消退,行复合式小梁切除术。术中0.04%丝裂霉素棉片置于巩膜瓣下4 min,用生理盐水冲洗干净。(3)全视网膜光凝术:小梁切除术后1周有视网膜缺血现象的患者均行全视网膜光凝术。全视网膜光凝治疗的前界为赤道部或超出赤道部,后界呈卵圆形,距视乳头缘鼻侧500µm,距黄斑中心上方,颞侧及下方各3 000µm,要避开后极部。光凝斑之间相隔一个光凝间隙。常规的全视网膜光凝需要500µm的光凝斑1 000~1 600个,分2~4次完成,以减少光凝副作用。
1.4 观察指标 患者术后眼压、视力、虹膜新生血管消退的情况、滤过泡形态及手术并发症。
1.5 统计学方法 应用SPSS17.0统计软件进行数据分析,计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 眼压 注药后1周眼压与注药前眼压比较,差异无统计学意义(P>0.05)。复合式小梁切除术后1周眼压、术后1个月眼压、术后3个月眼压、末次随访时眼压各组较术前眼压比较,差异均有统计学意义(P<0.05),见表1。
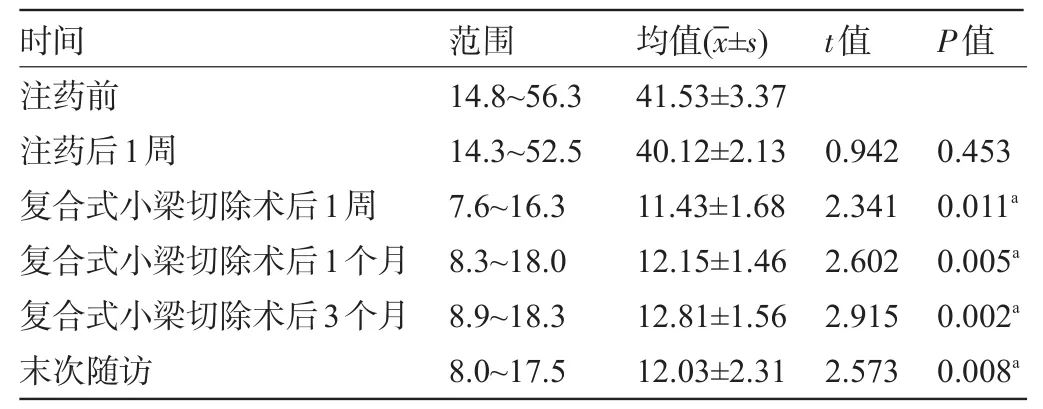
表1 不同时间点眼压的比较(n=12,mmHg)
2.2 视力 术后末次随访时最佳矫正视力>0.1者4眼,视力0.01~0.1者15眼,与术前视力比较,差异均有统计学意义(χ2=6.738,P<0.05),见表2。

表2 NVG术前及术后视力分布情况[眼数(%)]
2.3 虹膜新生血管 玻璃体腔注射康柏西普后,虹膜新生血管1周内完全消退为17只眼,2周内完全消退为5只眼。复合式小梁切除术后3~15个月随访期间未见虹膜新生血管复发。
2.4 术中术后并发症及滤过泡形态 本组病例22眼玻璃体腔注射康柏西普后,有5眼发生结膜下出血,于注射后3~7 d自行吸收,3眼眼内压过高而行前房穿刺。所有病例复合式小梁切除术均顺利完成,术后2眼出现浅前房,1周内恢复正常。术后7眼有前房炎症反应,治疗3~5 d后消失。术后Ⅰ型功能滤过泡10眼,Ⅱ型功能滤过泡12眼。
3 讨论
NVG的病因主要有视网膜静脉阻塞、糖尿病视网膜病变及其他疾病,各约占1/3[3]。血管形成的刺激因子与抑制因子的平衡控制正常和病理性血管(新生血管)形成的关键。VEGF是目前已知最直接作用于眼内的新生血管形成因子[4],促进内皮细胞迁移增生,细胞外基质变性促血管生成,血管通透性增加,上调细胞间粘附分子-1和内皮型一氧化氮合酶表达,破坏血-视网膜屏障,加重缺血缺氧导致新生血管形成[5]。贝伐单抗(Avastin)、兰尼单抗(Lucentis)、康柏西普(Conbercept)等抗VEGF药物均被临床相继应用,以控制眼内新生血管形成。临床上Avastin与Lucentis结构、作用类似,能够结合VEGF-A所有异构体的,而Conbercept优于两者,其VEGF trap是一种完全人源化、可溶性的VEGF受体,不但作用为诱饵受体能结合VEGF-A的所有异构体,同时还能结合VEGF-B和胎盘生长因子,作用靶标更完全,治疗效果更好。临床上经玻璃体腔内注射Conbercept可用于治疗多种眼底新生血管疾病,包括湿性年龄相关性黄斑变性(Age-related macular degeneration,AMD)、糖尿病黄斑水肿(Diabetic macular edema,DME)、病理性近视(Pathological myopia,PM)、视网膜静脉阻塞(Retinal vein occlusion,RVO)等。徐瑜玲[6]报道,糖尿病黄斑水肿患者14只眼接受玻璃体腔注射Conbercept及视网膜激光光凝联合治疗,能更有效地减轻黄斑水肿,提高视力,减少并发症。毕燃等[7]报道,16例(16眼)接受玻璃体腔内注射康柏西普治疗的视网膜静脉阻塞黄斑水肿患者,观察治疗后2周、4周、6周平均最佳矫正视力均有不同程度提高,FFA显示黄斑区荧光素渗漏明显减少,即黄斑水肿明显消退。OCT图像显示黄斑中心凹视网膜厚度明显变薄,与治疗前相比差异有统计学意义(P<0.05)。本文我们对22例(22只眼)新生血管性青光眼行玻璃体腔注射Conbercept 0.50 mg/0.05 ml,17只眼虹膜新生血管1周内完全消退,5只眼2周内完全消退。
如何根据不同的病情选择合适的治疗方案,尚无明确、统一的方案。陶绍武等[8]研究指出对于NVG I期的患者单用抗VEGF药物可通过新生血管的消退而达到降低眼压的目的。然而,对于NVGⅡ期以及Ⅲ期的患者,由于其虹膜面及房角广泛的新生血管膜使得单用抗VEGF治疗难以达到预期目标。近年来的研究多倾向于通过抗VEGF药物联合小梁切除术或者引流阀植入术来探讨NVG的治疗新途径。应用抗VEGF类药物能提高滤过手术的成功率[9],其原因:(1)抗VEGF药物促使NVG的虹膜面及房角新生血管消退,减少术中术后的前房出血的风险,为后期手术及治疗创造良好条件。(2)抗VEGF药物可以有效抑制术后炎症反应从而减少术后滤过道的阻塞和滤过泡的纤维化包裹,有研究表明VEGF对于肌成纤维细胞转化TGF-β1/Smad/Snail信号通道有潜在的影响[10],因此,抑制VEGF可有效减少小梁切除术后结膜下纤维化,提高手术成功率。(3)抗VEGF药物可通过拮抗作用抑制新生血管生成、减低血管通透性以及调控血-视网膜屏障的通透性,进而促进视网膜内渗液吸收,改善视网膜病变,提高患者的视功能[11]。在本组病例中22只眼玻璃体腔注射Conbercept 7~14 d后,虹膜及房角新生血管完全消退,行复合式小梁切除术,术中应用丝裂霉素C减少了术后瘢痕形成,为房水排出建立了良好的引流通道,术后滤过泡形成良好,角膜恢复透明。由于视网膜缺氧和毛细血管无灌注是虹膜新生血管形成的根源,一旦发现视网膜有缺血现象时就应考虑作全视网膜光凝术。激光封闭新生血管及供养血管,破坏新生血管区、减轻视网膜耗氧量,并促进视网膜出血水肿及渗出的吸收,停止释放血管内皮生长因子[12],从源头治疗预防虹膜新生血管的发生。本组病例22只眼复合式小梁切除术后1周眼压、术后1个月眼压、术后3个月眼压、末次随访时眼压各组较术前眼压比较,差异均有统计学意义。末次随访时最佳矫正视力>0.1者4眼,视力0.01~0.1者15眼,与术前视力比较,差异有统计学意义(P<0.05)。复合式小梁切除术后3~15个月随访期间未见虹膜新生血管复发。
综上所述,抗VEGF治疗是NVG治疗的关键环节,本研究采用玻璃体腔注射康柏西普联合复合式小梁切除术治疗新生血管性青光眼,术后及时行全视网膜光凝,可以减少虹膜新生血管,使患者有效控制眼压的同时获得更好的视功能,临床疗效满意,值得推广应用。但由于本研究病例数较少,其长期的安全性和有效性均待进一步的研究和探讨。
[1]于湛,刘国军,邸霞.玻璃体腔注射Bevicazumab联合玻璃体切除视网膜及睫状体光凝治疗新生血管性青光眼[J].中国实用眼科杂志, 2011,29(12):1272-1274.
[2]李美玉.青光眼学[M].北京:人民卫生出版社,2004:444.
[3]葛坚,崔浩.眼科学[M].北京:人民卫生出版社,2002:159.
[4]Zhang XL,Wen L,Chen YJ,et al.Vascular endothelial growth factor up-regulates the expression of intracellular adhesion molecule-1 in retinal endothelial cells via reactive oxygen species,but not nitric oxide[J].Chin Med J(Engl),2009,122(3):338-343.
[5]朱丹,金子夜.重视糖尿病视网膜病变相关细胞因子的研究[J/ CD].中华眼科医学杂志(电子版),2014,4(4):1-3.
[6]徐瑜玲,段幸亭,曾祥冰,等.康柏西普联合激光光凝治疗糖尿病性黄斑水肿的疗效[J].中国激光医学杂志,2014,10(23):308-309.
[7]毕燃,贾彩华,于越,等.康柏西普治疗视网膜静脉阻塞黄斑水肿的临床观察[J].赤峰学院学报(自然科学版),2014,12(30):71-73.
[8]陶绍武,李惠,李静,等.新生血管性青光眼治疗时机的临床研究[J].国际眼科杂志,2013,13(3):519-521.
[9]Eid TM,Radwan A,el-Manawy W,et al.intravitreal bevacizumab and aqueous shunting surgery For neovascular glaucoma:safety and efficacy[J].Can J Ophthalmol,2009,44(4):451-456.
[10]Park HY,Kim JH,Park CK.VEGF induces TGF-β1expression and myofibroblast transformation after glaucoma surgery[J].Am J Pathol,2013,182(6):2147-2154.
[11]陆诗林.比较眼底激光单用和联合雷珠单抗治疗糖尿病性视网膜病变的疗效观察[J].中国实用医药,2014,9(1):165-166.
[12]郑纯,李学喜,陈佳娜.玻璃体腔注射雷珠单抗联合23G玻璃体切除治疗新生血管性青光眼疗效观察[J].海南医学,2015,26(21): 3154-3156.
Clinical observation of intravitreous injection of Conbercept combined with complex trabeculectomy in the treatment for neovascular glaucoma.
ZHOU Lin,ZHOU Lan.Department of Ophthalmology,Huai'an Second People's Hospital,Huai'an Hospital Affiliated to Xuzhou Medical College,Huai'an 223002,Jiangsu,CHINA
ObjectiveTo observe the effect of intravitreous injection of Conbercept combined with complex trabeculectomy on neovascular glaucoma(NVG).MethodsTwenty-two eyes of 22 patients with NVG in our hospital were treated with intravitreous injection of Conbercept(0.50 mg/0.05 ml)and then complex trabeculectomy 8~14 days later.The regression of iris neovascularization and changes in intraocular pressure(IOP)were observed after injection.Best corrected visual acuity and changes in IOP were observed after complex trabeculectomy.Patients were followed-up for 3~15 months after operation.ResultsAfter injection of Conbercept,iris neovascularization completely regressed within 1 week in 17 eyes and within 2 weeks in 5 eyes.The average IOP was(41.53±3.37)mmHg before injection and (40.12±2.13)mmHg in a week after injection,showing no statistically significant difference(P>0.05).The IOP at 1 week, 1 month,3 months after complex trabeculectomy were(11.43±1.68)mmHg,(12.15±1.46)mmHg,(12.81±1.56)mmHg, and(12.03±2.31)mmHg in the last follow-up visit,showing statistically significant difference compared with those before trabeculectomy(P<0.05).After surgery,the best-corrected visual acuity was>0.1 in 4 eyes,0.01~0.1 in 15 eyes, which showed statistically significant difference with the visual acuity before surgery(P<0.05).ConclusionIntravitreous injection of Conbercept combined with complex trabeculectomy can effectively control the IOP and preserve the visual function in patients with neovascular glaucoma.
Neovascular glaucoma;Intravitreal injection;Conbercept;Complex trabeculectomy;Effect
R775.3
A
1003—6350(2016)04—0591—03
10.3969/j.issn.1003-6350.2016.04.026
2015-06-13)
周林。E-mail:zhoulin770624@sina.com

