SD大鼠不同小肠段对血糖控制作用的基础研究
艾小明,杨念印,李胜春,郭绍红,叶宜芬
(南京明基医院普外科南京医科大学附属医院,江苏 南京 210019)
SD大鼠不同小肠段对血糖控制作用的基础研究
艾小明,杨念印,李胜春,郭绍红,叶宜芬
(南京明基医院普外科南京医科大学附属医院,江苏 南京 210019)
目的 探讨正常SD大鼠不同小肠段对血糖控制改变的影响和可能机制。方法将20只SD大鼠按数字表随机分为A、B、C三组,其中A组6只,B组和C组各7只。测各大鼠体质量及尾部静脉血空腹血糖。手术探查小肠全长度,并将其分为三等分,用7b丝线结扎每段肠管的两端,保留正常的肠系膜血液循环。A组向近侧段小肠腔内注射葡萄糖,B组向中间段小肠腔内注射葡萄糖,C组向远侧段小肠腔内注射葡萄糖(注射量均为1 mg/kg,生理盐水稀释至1 ml)。分别测定注射葡萄糖后2 min、15 min、45 min、75 min、120 min尾部静脉血血糖。结果手术过程中有3只大鼠死亡,A组1只死于失血量过多,B组1只死于麻醉药物中毒(麻醉药物注入血管),C组1只大鼠死于空气栓塞,手术存活率为85%。三组SD大鼠空腹血糖相互比较差异均无统计学意义[(7.85±1.26)mmol/L vs (7.76±2.19)mmol/L vs(7.83±1.82)mmol/L,P>0.05]。术后2 min B组与A组血糖比较差异均无统计学意义[(9.90±1.51)mmol/L vs(10.56±1.47)mmol/L,P>0.05];而C组[(7.78±1.56)mmol/L]明显低于A组和B组,差异均有统计学意义(P<0.05)。术后15 min、45 min、75 min、120 min血糖比较,B组均低于A组,C组均低于A组和B组,差异均有统计学意义(P<0.05)。结论通过向不同段SD大鼠小肠注射葡萄糖的研究结果发现,近段小肠控制血糖效果最差,中间段小肠次之,远段小肠效果最好。从本实验的结果中可以看出,越是靠近末端的小肠,越是有控制血糖水平的能力。不同肠段对血糖控制的作用机制可能与胃肠道激素分泌有关,尚有待进一步的研究。
SD大鼠;小肠;血糖;控制
目前关于胃肠道重建手术治疗2型糖尿病(Type 2 diabetes mellitus,T2DM)的研究已经成为国际上研究的热点,胃肠转流术(GBP)对肥胖型T2DM的治疗作用在国内外已经得到了广泛证实[1-2]。尽管目前关于手术治疗T2DM的机制尚未完全明确,但近端小肠(十二指肠与近端空肠)和远端小肠(特别是末端回肠)的作用已经成为研究的热点,由此产生了前肠学说和后肠学说这两种学说,并且都认为小肠在T2DM的发病过程中扮演极其重要的角色[3]。既然研究一致认为GBP治疗T2DM的机制-可能与手术改变了胃肠生理通道、进而影响到食物生理流向有关,那么理论上,在这一过程中整个小肠的任何部位的肠段都有可能是参与血糖调控的关键部位。本研究选用正常SD大鼠作为研究对象,旨在探讨大鼠不同小肠段在注入葡萄糖后血糖的动态变化,进而推测其调节血糖的机理,并为进一步进行糖尿病大鼠模型的动物实验研究奠定下基础。
1 材料与方法
1.1 实验动物和主要材料 SPF级6周龄的SD大鼠20只(北京维通利华实验动物技术有限公司),雌雄各半,体重130~160 g。OneTouch®SelectSimple™血糖仪(美国强生公司)。AEL-200型电子分析天平(日本LIBROR公司)。丙泊酚(意大利阿斯利康制药有限公司),氯胺酮(江苏恒瑞医药股份有限公司),50%葡萄糖、生理盐水(中国大冢制药有限公司)。实验动物基础饲料(北京维通利华实验动物技术有限公司)。基础饲料适应性喂养1周,饮用直饮水。手术器械由南京明基医院实验室提供。
1.2 实验方法
1.2.1 分组 将20只SD大鼠分为三组,其中A组6只,B组及C组各7只,雌雄随意分配。
1.2.2 术前准备 手术前禁食12 h、不限饮水。分别测各组大鼠体质量及尾部静脉血空腹血糖。
1.2.3 分段结扎肠管 以丙泊酚(100 mg/kg)+氯胺酮(50 mg/kg)腹腔内注射麻醉。麻醉成功后大鼠取仰卧位,常规0.5%碘伏消毒后取上腹部正中切口,长约4 cm。进腹后探查全小肠长度,并将其均分为三等分,并用7b丝线靠近肠壁结扎每段肠管的两端,保证肠腔内注射的液体不会流出注射段肠腔,保留正常的肠系膜血液循环。
1.2.4 肠腔注射葡萄糖 向小肠腔内注射葡萄糖液体:注射量:1 mg/kg(用50%的葡萄糖配置,生理盐水稀释至1 ml)。A组向近侧段小肠腔内注射,B组向中间段小肠腔内注射,C组向远侧段小肠腔内注射。
1.2.5 测定血糖 分别测定各组大鼠注射葡萄糖后2 min、15 min、45 min、75 min、120 min尾部静脉血血糖。最后将全部大鼠按脊椎脱臼法处死。
1.3 统计学方法 应用SPSS17.0统计软件包对数据进行分析,计量资料符合正态分布,以均数±标准差(±s)表示,三组比较采用单因素方差分析,两两比较采用LSD,以P<0.05为差异有统计学意义。
2 结 果
2.1 手术成功率及大鼠存活情况 手术过程中有3只大鼠死亡,A组1只死于失血量过多,B组1只死于麻醉药物中毒(麻醉药物注入血管),C组1只大鼠死于空气栓塞,手术存活率为85%。
2.2 三组大鼠血糖值变化 三组SD大鼠手术前后血糖水平变化见表1和图1。三组SD大鼠空腹血糖相互比较差异均无统计学意义(P>0.05)。术后2 min B组与A组血糖比较差异均无统计学意义(P>0.05);而C组明显低于A组和B组,差异均有统计学意义(P<0.05)。术后15 min、45 min、75 min、120 min血糖比较,B组均低于A组,C组均低于A组和B组,差异均有统计学意义(P<0.05)。
表1 SD大鼠手术前后血糖水平变化(±s,mmol/L)
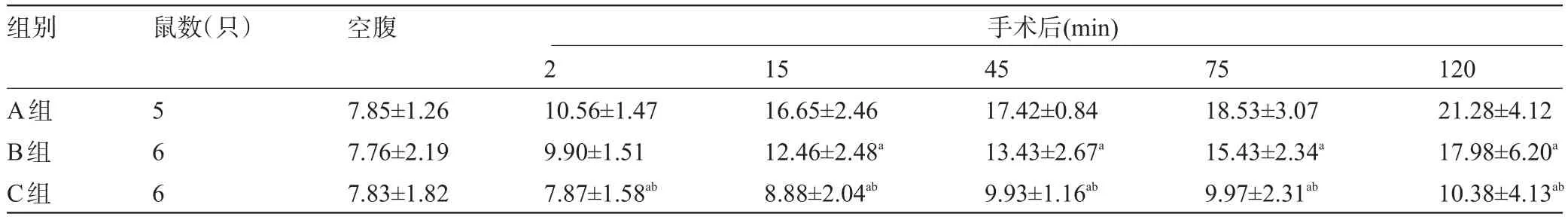
表1 SD大鼠手术前后血糖水平变化(±s,mmol/L)
注:与A组比较,aP<0.05;与B组比较,bP<0.05。
组别 鼠数(只) 空腹手术后(min) A组B组C组5 6 6 7.85±1.26 7.76±2.19 7.83±1.82 2 10.56±1.47 9.90±1.51 7.87±1.58ab15 16.65±2.46 12.46±2.48a8.88±2.04ab45 17.42±0.84 13.43±2.67a9.93±1.16ab75 18.53±3.07 15.43±2.34a9.97±2.31ab120 21.28±4.12 17.98±6.20a10.38±4.13ab
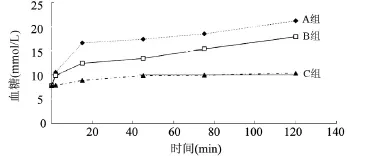
图1 SD大鼠手术前后血糖水平变化
3 讨 论
T2DM的发病机制是由于体内胰岛素激素相对不足,或周围组织对胰岛素敏感性下降而引起的血糖升高。传统的糖尿病治疗方法,主要包括饮食控制、运动、口服降糖药物、胰岛素治疗等,但传统手段并不能保证使患者血糖恢复正常,也不能避免糖尿病所致的各种严重并发症及病情的进一步加重,长期会加重患者的经济负担、降低生活质量。GBP从20世纪80年代开始应用于合并肥胖症的T2DM患者,开辟了T2DM治疗的一个新的领域,已成为胃肠外科研究的热点。Müller-stich等[4]研究发现,GBP不仅使T2DM患者的血糖水平降低,而且使肥胖症和糖耐量受损患者得以改善、避免其进展为T2DM,同时还使T2DM患者的并发症发生率和病死率降低。在美国2009年糖尿病防治指南中,已经明确将GBP手术列入治疗2型糖尿病标准[5]。中华医学会糖尿病学分会及中华医学会外科学分会也在2011年对手术治疗糖尿病达成专家共识[1]。由此可见,共识与声明已经明确了“糖尿病外科治疗”的重要意义。
T2DM外科手术治疗的机制目前尚不完全明确,可能与手术通过消化道重建对胃肠道激素分泌的影响,以及由此产生的胰岛素分泌或敏感性的改变相关[6]。科学家们已开始将术后降低血糖的机制转向了胃肠道激素的作用[7]。GBP术后,食物的消化部位从原来的十二指肠、近端空肠直接转移到了远端空肠和回肠,使肠道激素的分泌发生了改变。关于GBP治疗T2DM的机制,形成了多种假设和学说,但绝大多数都是在消化道改道和重建的基础上提出来的。大多数的学者认为,在胃肠道的黏膜上广泛分布有大量的内分泌细胞、并分泌各种胃肠道激素,GBP术后胃肠道激素的改变,被认为是GBP治疗T2DM的最主要机制[8]。GBP术后,食物自小胃囊直接排入远端小肠,未经过充分消化的食糜过早的到达末段回肠。肠道在营养物质特别是各种碳水化合物的刺激下,通过释放多种内分泌激素和递质来促使胰岛素的分泌和释放,且肠道摄取葡萄糖所产生的B细胞分泌胰岛素的反应、会比静脉注射葡萄糖能产生更高的效果,这种胃肠道激素与胰岛素分泌之间的关系、也就是胃肠道与胰腺内分泌之间的关系,被称之为“肠-胰岛轴(Enteroinsular axis)”。Rubino等[9]设想,人的肠道中可能存在分泌肠促胰岛素(Incretin)和抗-肠促胰岛素(Anti-incretin)的部位,且这二部位同时存在。Anti-incretin的分泌部位主要分布在十二指肠与近段空肠,它的分泌能对抗胰岛素活性、产生胰岛素抵抗,而并不是直接抑制胰岛素的分泌和合成[10]。GBP术后食物绕过了十二指肠和近段空肠,避免了对Anti-incretin分泌部位的刺激。这一机制通过减少十二指肠与近段空肠分泌Anti-incretin(如抑胃肽),减少对胰岛素合成和分泌的抑制,增强胰岛素的敏感性,就形成了前肠学说(Foregut hypothesis)。再者,也可能由于未充分消化的食物过早地到达末段回肠,这一机制通过刺激、诱导末段回肠分泌和合成Incretin(如胰高血糖素样肽-l),促进胰岛素的合成和分泌,增强外周组织对胰岛素的敏感性,达到使血糖下降、甚至恢复正常的作用,就形成了后肠学说(Hindgut hypothesis)。研究证明,外科手术(如GBP)是可以治愈糖尿病的,所以有学者认为,2型糖尿病可能就是一种小肠外科的疾病[3,11]。
从本研究中可以看出,总体上B组对血糖控制效果优于A组,而C组对血糖控制效果不仅优于A组,而且优于B组。本实验研究说明,从血糖上升速度和程度方面来看,近段小肠控制效果最差,中间段小肠次之,远段小肠效果最好。中段小肠与远段小肠在注射葡萄糖120 min时,血糖最高值也没能到达近端小肠的数值。末段小肠注射葡萄糖后,血糖上升缓慢,且不超过11 mmol/L。从本实验的结果中可以看出,越是靠近末端的小肠,越是有控制血糖水平的能力。虽然肠道吸收功能的差异有可能是这种现象的原因,但是吸收功能的差异,不能很好解释为什么实验终点120 min时,血糖水平仍有差异。所以我们推测这些差异更可能与胃肠道激素分泌的影响密切相关。这项实验的结果可以作为转流手术能够有效治疗Ⅱ型糖尿病的理论基础之一。也就是行GBP术后,食物不经过近段、中段小肠,食物仅仅通过末段小肠,其结果就能控制血糖上升的速度与高限。
与糖尿病有关的胃肠道激素,目前研究较多、较深入的主要有肠抑胃肽(Gastric inhibitory peptide,GIP,又称葡萄糖依赖性促胰岛素释放肽)、胰高血糖素样肽-l(Glucagon-like peptide 1,GLP-1)等。GIP由十二指肠和近端空肠肠壁上之K细胞受食物中的脂肪、碳水化合物刺激后所分泌[12],是43个氨基酸所组成的直链肽,属于胰泌素和胰高血糖素家族。一般生理状态下,当血液中的血糖≥6.0 mmol/L时,GIP能刺激胰岛素的合成和分泌,能抑制胃的蠕动和排空;而在T2DM的病理状态下,由于体内存在异常活化的肠-胰岛轴,能使GIP水平增高,体内会产生过多的胰岛素,继而就产生了胰岛素抵抗。而GBP术后食物绕过了近端小肠,减少了对十二指肠和近端空肠肠壁上的K细胞刺激,GIP的释放也相应大大减少,解除了胰岛素的抵抗,从而T2DM得以获得治愈。Flatt[6]通过研究显示,GBP术后近端小肠释放的GIP减少。
研究显示,GLP-1可能是肠-胰岛轴中控制T2DM最重要的作用靶点和最核心的介导因子[13]。GLP-1是由胰高血糖素原基因表达,由回肠末端及结肠肠壁上的L细胞分泌的多肽链序列,是人体内的一种肠源性激素。进食后,食物进入肠腔后能直接刺激GLP-1的释放[14]。GLP-1的分泌也可能受到胃肠道内分泌和神经机制等的调控。GLP-1的主要作用表现在以下几个方面:①通过腺苷酸环化酶作用于胰岛B细胞,促进胰岛素基因的转录,增加葡萄糖浓度依赖性的胰岛素的合成和分泌,减少餐后血糖的波动。研究显示,体内持续性低剂量注射GLP-1,可以促使胰岛B细胞对葡萄糖的反应恢复到正常水平[15];②通过诱导胰岛B细胞增殖与分化,抑制胰岛B细胞的凋亡,增加胰岛B细胞数量;③既可以葡萄糖浓度依赖性地作用于胰岛B细胞、促进胰岛素的分泌,还可以作用于胰岛A细胞、强烈抑制胰高血糖素的分泌[16];④具有保护胰岛B细胞的作用,改善胰岛B细胞功能,从而减轻胰岛素抵抗;⑤餐后引起GLP-1的分泌,还可作用于中枢神经系统(特别是下丘脑),从而使人体产生饱胀感和食欲下降,起到了终止摄食信号的作用。GLP-1通过降低食欲,有助于减轻体重[17];⑥能延迟胃排空,进而减缓食物消化,降低餐后血糖。目前已有实验证明在GBP术后胰岛素的分泌增加和GLP-1水平升高相关[18]。有大量研究显示,GBP术后的餐后GLP-1分泌水平明显上升[19]。
构成“肠-胰岛轴”的成员,除了胰岛素、GIP、GLP-1外,还包括胃饥饿素(Ghrelin)、人多肽YY (Peptide YY,PYY)、缩胆囊素(Cholecystokinin,CCK)、瘦素(Leptin)、脂联素(Adiponectin/ADPN)以及胰岛素样生长因子-1(Insulin-like growth factor 1,IGF-1)等。此外,多种炎症介质,包括肿瘤坏死因-α(TNF-α)、白细胞介素-1β(IL-1β)、白细胞介素-6(IL-6)和C-反应蛋白(CRP)等,亦可能参与了血糖调控、胰岛素抵抗[20],在糖尿病的发病过程中起到了重要作用。近年来已有学者提出糖尿病可能属于炎症性疾病。研究表明GBP术后患者IL-6、CRP、TNF-α水平均有不同程度的降低,脂肪组织内的巨噬细胞浸润减少,胰岛素抵抗得以改善[21]。总之,其调控过程是极其错综复杂的。
本实验的缺陷是:(1)选择的大鼠不是糖尿病大鼠;(2)是动物实验;(3)没有对大鼠血液中胃肠道激素的变化及胰岛素的变化进行测定。所以目前还不能直接将本实验结果推断成人体的实际情况。这些都是我们今后需要进一步研究的内容,以期为外科手术治疗T2DM提供更多的基础理论支持。
[1]中华医学会糖尿病学分会,中华医学会外科学分会.手术治疗糖尿病专家共识[J].中国实用外科杂志,2011,31(5):367-370.
[2]Buchwald H,Oien DM.Metabolic/bariatric surgery Worldwide 2011 [J].Obes Surg,2013,23(4):427-436.
[3]Rubino F.Is type 2 diabetes an operable intestinal disease?Aprovocative yet reasonable hypothesis[J].Diabetes Care,2008,31(Suppl 2): S290-296.
[4]Müller-Stich BP,Fischer L,Kenngott HG,et a1.Gastric bypass leads to improvement of diabetic neuropathy independent of glucose normalization-results of a prospective cohort study(DiaSurg 1 study) [J].Ann Surg,2013,258(5):760-765.
[5]林允信,许昌泰.胃旁路手术治疗2型糖尿病研究现状述[J].医学综述,2011,17(6):902-905.
[6]Flatt PR.Effective surgical treatment of obesity may be mediated by ablation of the lipogenic gut hormone gastric inhibitory polypeptide (GIP):evidence and clinical opportunity for development of new obesity-diabetes drugs[J].Diab Vasc Dis Res,2007,4(2):151-153.
[7]Lee WJ,Lee YC,Ser KH,et a1.Improvement of insulin resistance after obesity surgery:a comparison of gastric banding and bypass procedures[J].Obes Surg,2008,18(9):11l9-1125.
[8]Lawson ML,Kirk S,Mitchell T,et al.One-year outcomes of Roux-en-Y gastric bypass for morbidly obese adolescents:a multicenter study from the Pediatric Bariatric Study Group[J].J Pediatr Surg,2006,4l(1):137-143.
[9] Rubino F,Marescaux J.Effect of duodenal-jejunal exclusion in a non-obese animal model of type 2 diabetes:a new perspective for an old disease[J].Ann Surg,2004,239(1):1-11.
[10]Pories WJ.Diabetes:the evolution of a new paradigm[J].Ann Surg, 2004,239(1):12-13.
[11]Laferrère B,Swerdlow N,Bawa B,et a1.Rise of oxyntomodulin in response to oral glucose after gastric bypass surgery in patients with type 2 diabetes[J].J Clin Endocrinol Metab,2010,95(8):4072-4076.
[12]Powers KA,Rehrig ST,Jones DB.Financial impact of obesity and bariatric surgery[J].Med Clin NorthAm,2007,91(3):321-338.
[13]Stearns AT,Balakrishnan A,Rhoads DB,et al.Rapid upregulation of sodium-glucose transporter GLT-1 in response to intestinal sweet taste stimulation[J].Ann Surg,2010,251(5):865-871.
[14]王晓兢,武晓泓.营养物质刺激肠道L细胞分泌GLP-1的机制[J].国际内分泌代谢杂志,201l,31(5):324-326.
[15]Kjems LL,Holst JJ,Vølund A,et a1.The influence of GLP-1 on glucose-stimulated insulin secretion:effects on beta-cell sensitivity in type 2 and nondiabetic subjects[J].Diabetes,2003,52(2):380-386.
[16]徐键,王勇,刘源,等.胃转流术治疗2型糖尿病的研究进展[J].中华内分泌外科杂志,2010,4(2):132-134.
[17]郑志坚,史逸华.腹腔镜胃转流术治疗2型糖尿病与胰高血糖素样肽-1[J].中国微创外科杂志,2012,12(5):463-465.
[18]Laferrère B,Heshka S,Wang K,et a1.Incretin levels and effect are markedly enhanced 1 month after Roux-en-Y gastric bypass surgery in obese patients with type 2 diabetes[J].Diabetes Care,2007,30(7): 1709-1716.
[19]Laferrère B,Teixeira J,McGinty J,et a1.Effect of weight loss by gastric bypass surgery versus hypocaloric diet on glucose and incretin levels in patients with type 2 diabetes[J].J Clin Endocrinol Metab, 2008,93(7):2479-2485.
[20]Monte SV,Caruana JA,Ghanim H,et a1.Reduction in endo-toxemia, oxidative and inflammatory stress,and insulin resistance after Roux-en-Y gastric bypass surgery in patients with morbid obesity and type 2 diabetes mellitus[J].Surgery,2012,151(4):587-593.
[21]Viana EC,Araujo-Dasilio KL,Miguel GP,et al.Gastric bypass and sleeve gastrectomy:the same impact on IL-6 and TNF-α.Prospective clinical trial[J].Obes Surg,2013,23(8):1252-1261.
Effect of different segments of small intestine on blood glucose control in Sprague-Dawley rats.
AI Xiao-ming, YANG Nian-yin,LI Sheng-chun,GUO Shao-hong,YE Yi-fen.Department of General Surgery,BenQ Medical Center,the Affiliated Hospital of Nanjing Medical University,Nanjing 210019,Jiangsu,CHINA
ObjectiveTo evaluate the effect and possible mechanisms of different segments of small intestine on blood glucose control in Sprague-Dawley(SD)rats.MethodsTwenty SD rats were randomly divided into three groups based on a random number table:group A(n=6),group B(n=7),and group C(n=7).The body weight and the values of fasting plasma glucose(FPG)were measured.All the rats underwent an operation,and the whole length of small intestine was separated into three segments averagely(proximal,middle,and distal segment),with each segment ligated at the ends by 7b silk suture.In group A,B,C,50%glucose(at the dose of 1 mg/kg,adding normal saline to 1 ml)was injected into enteric cavity of proximal segment,middle segment,distal segment,respectively.The values of blood glucose were tested at 2 min,15 min,45 min,75 min and 120 min after operation.ResultsThree rats died during the operation, with one in group A died of excessive blood loss,one in group B of toxicity of local anesthetics,and one in group C of air embolism.The survival rate of the operation for the rats was 85%.There were no significant differences in the values of FPG among the three groups[(7.85±1.26)mmol/L vs(7.76±2.19)mmol/L vs(7.83±1.82)mmol/L,P>0.05].At 2 min after operation,the values of blood glucose showed no significant differences between group A and B[(9.90±1.51)mmol/L vs (10.56±1.47)mmol/L,P>0.05],but the values of group C[(7.78±1.56)mmol/L]were significantly lower than those of group A and group B(P<0.05).Furthermore,at 15 min,45 min,75 min,120 min after operation,values of blood glucose of group B were significantly lower than those of group A,and the values of group C were significantly lower than those of group A and group B(P<0.05).ConclusionEffect of proximal segment of small intestine on blood glucose control was the worst after injection of glucose,followed by middle segment,and the effect of distal segment was the best, which indicates that the more close to distal small intestine,the better effect could be achieved on blood glucose control. The possible mechanisms of different segments of small intestine on blood glucose control in SD rats may be associated with gastrointestinal hormone secretion.
Sprague-Dawley(SD)rat;Small intestine;Blood glucose;Control
R-332
A
1003—6350(2016)04—0520—04
2015-10-09)

