14例尿毒症透析患者冠脉搭桥手术临床分析
刘伟,曹建军,胡小平,王宏宇,陈浩D
(1.湖北医药学院附属东风医院心胸大血管外科,湖北 十堰 442008;2武汉大学人民医院心血管外科,湖北 武汉 434000)
14例尿毒症透析患者冠脉搭桥手术临床分析
刘伟1,曹建军1,胡小平2,王宏宇1,陈浩1D
(1.湖北医药学院附属东风医院心胸大血管外科,湖北 十堰 442008;2武汉大学人民医院心血管外科,湖北 武汉 434000)
目的 探讨尿毒症透析患者合并冠心病的外科治疗方法及其治疗效果。方法2009年1月至2014年12月东风汽车公司总医院心胸大血管外科对14例尿毒症透析合并冠心病患者实施冠状动脉旁路移植术(CABG)。尿毒症透析患者中慢性肾功能衰竭13例,急性肾功能衰竭1例,合并室壁瘤1例;3例采用非体外循环心脏不停跳冠脉旁路移植术(OPCABG),11例采用体外循环下冠状动脉旁路移植术(CCABG),前降支均采用左乳内动脉(LIMA)作为桥血管,移植血管1~4支;同期行室壁瘤折叠术1例。比较术前、术后2周及术后一年患者的左心室舒张末期内径(LVEDD)、左室射血分数(LVEF)、NYHA心功能分级、血肌酐(Cre)、血尿素氮浓度(BUN)等指标,并评价手术治疗效果。结果所有患者均手术成功,术后2例出现重症感染。14例患者术后随访1~3年,1例于术后27个月因重症感染死亡。未见其他并发症和死亡病例。术后2周,患者NYHA心功能分级为Ⅱ级(M=Ⅱ),LVEF、LVEDD、Cre、BUN等指标与术前比较差异均无统计学意义(P>0.05)。术后1年,患者NYHA心功能分级为Ⅰ级(M=Ⅰ),较术后2周显著改善(P<0.05);LVEF为(55.74±7.84)%、LVEDD为(50.21±5.28)mm,较术前的(51.23±6.46)%和(56.73±6.33)mm均改善(P<0.05),而Cre、BUN等指标与术前比较差异均无统计学意义(P>0.05)。结论尿毒症透析患者合并冠心病行CABG风险较大,经过严格的术前评估、充分的冠状动脉再血管化,并加强围手术期管理,可取得满意疗效。
冠心病;尿毒症;透析;冠状动脉旁路移植术
维持性血液透析(Maintenance hemodialysis,MHD)是尿毒症患者有效治疗的方法之一,随着透析技术的不断进步,维持性血液透析患者的生存时间、生活质量得以不断提高。然而,长期血液透析患者易出现心血管转移性钙化,特别是冠状动脉钙化的几率明显升高[1],合并冠心病的概率高达40%~70%[2],冠状动脉钙化引起心肌缺血,可导致心律失常、心功能衰竭甚至猝死,严重影响患者预后,其5年生存率明显下降[3]。尿毒症透析患者合并冠心病后采取冠状动脉旁路移植术(CABG),可改善预后[4]。2009年1月至2014年12月,东风总医院心胸大血管外科共对14例尿毒症透析合并冠心病患者实施CABG,取得了满意的效果,报道如下:
1 资料与方法
1.1 一般资料 2009年1月至2014年12月我科共收治14例尿毒症透析合并冠心病患者,其中男性10例,女性4例;体重43~82 kg,平均(56.4±12.3)kg;年龄43~72岁,平均(58.6±6.3)岁;所有患者均表现出典型胸痛症状。14例患者中,慢性肾功能衰竭13例[均长期规律透析,每周2~3次,术前维持性透析时间为14~143个月,平均(63±17.2)个月,急性肾功能衰竭1例(每日透析一次);合并先天性多囊肾病2例,糖尿病肾病4例,肾移植术后移植肾衰竭2例,高血压肾病6例;10例通过动静脉瘘穿刺透析,2例通过长期透析导管透析,2例通过股静脉临时置管透析。非ST段抬高型心肌梗死(NSTEMI)3例,心梗距手术时间为(12.2±4.2)d;ST段抬高型心肌梗死(STEMI)1例合并左心室室壁瘤形成,心梗距手术时间为32 d;不稳定型心绞痛10例。术前心功能分级(NYHA分级)为Ⅱ级3例,Ⅲ级9例,Ⅳ级2例,平均为Ⅲ级(M=Ⅲ)。术前均完善血常规、肝肾功能电解质、凝血功能、心脏超声、冠状动脉造影等检查,并评估患者心肺功能。术前冠脉造影显示前降支单支病变2例,冠脉2支病变3例,冠脉多支病变8例,其中合并左主干病变1例,均存在不同程度冠状动脉钙化。术前一周内心脏彩超检查,左室射血分数(LVEF)为40%~57%,平均(51.23±6.46)%;术前左室舒张末直径为(LVEDD)mm,平均(56.73±6.33)mm。术前1 d外周静脉血检查,血红蛋白为(83.4~94.5)g/L,平均(87.8±3.96)g/L;血小板为(75.3~238.4)×109/L,平均(143.5±53.2)×109/L;血钾浓度为(3.5~5.6)mmol/L,平均(4.48±0.98)mmol/L;血肌酐(Creatinine,Cre)浓度为157~690 μmol/L,平均(461±72.6)μmol/L;血尿素氮(BUN)浓度为6.3~19.6 mmol/L,平均(11.4±5.74)mmol/L。
1.2 手术方法 所有患者均行气管插管静脉复合麻醉,常规游离左乳内动脉(LIMA),移植血管多于1支者取大隐静脉(SV)备用。(1)行体外循环下冠状动脉旁路移植术(CCABG)11例:胸骨正中切口开胸,仔细探查心脏及冠状动脉情况,全身肝素化后(肝素剂量为3 mg/kg)常规经升主动脉、右心耳分别插管建立体外循环;主动脉阻断后经根部顺行灌注冷血心脏停跳液,在心脏停搏下用7-0 Prolene线连续缝合完成全部远端各吻合口。近端口吻合采取部分钳夹,升主动脉用6-0 Prolene线连续缝合完成。开放升主动脉,心脏复跳后,检查桥血管通畅情况及吻合口周围有无渗血,各项指标正常,撤机,鱼精蛋白中和肝素,彻底止血后关胸。(2)行非体外循环下冠状动脉旁路移植术(OPCABG)3例:切口及探查同体外循环下手术,在左心室侧面和后下方缝合心包壁层牵引线,拉紧固定后悬吊抬高心脏,充分暴露拟搭桥的前降支、钝缘支、后降支和左室后支等靶血管。全身肝素化(1 mg/kg)后以心脏稳定器固定心脏局部。远端吻合口用7-0 prolene单根双头线连续缝合,侧侧吻合采用菱形吻合(桥的长轴垂直于冠脉切口,端侧吻合则长轴平行)。吻合时局部吹CO2显露,并采用分流栓技术。近端口吻合时,钳夹升主动脉侧壁,将动脉收缩压控制在90~100 mmHg(1 mmHg=0.133 kPa),用6-0 Prolene线吻合。检查桥血管通畅情况及吻合口周围有无渗血。鱼精蛋白中和肝素。彻底止血后关胸。(3)体外循环下“三明治”法室壁瘤折叠术1例:瘤体直径约3 cm,剪取长约4 cm毛毡片2条,沿左心室长轴将毡条置于瘤体外缘,于瘤壁外正常心肌组织处进针,以2-0 Prolene线第一层连续水平褥式缝合夹闭瘤体,第二层行简单连续缝合加固。
1.3 观察指标 术前1周内心脏彩超测量左室射血分数(LVEF)、左室舒张末期直径(LVEDD);评估心功能分级;术前1 d外周静脉血检查血红蛋白、钾离子、Cre、BUN及血小板计数指标,术后当天每2 h复查上述指标一次。术后2周复查上述指标;术后随访,注意观察患者有无心衰、心绞痛症状,术后一年复查心脏彩超评估LVEF、LVEDD,评价心功能分级,复查Cre、BUN等指标。
1.4 统计学方法 应用SPSS20.0统计软件进行数据分析,计量资料呈正态分布以均数±标准差(±s)表示,相关变量采用t检验,呈非正态分布采用中位数(M)表示,进行非参数检验;计数资料采用例(%)表示,组间比较采用χ2检验,以P<0.05表示差异有统计学意义。
2 结 果
2.1 手术情况 所有患者手术均获成功。前降支均采用左乳内动脉作为桥血管,移植血管1~4支(M=3)。体外循环手术组体外循环时间(93±17.5)min,主动脉阻断时间(60.2±13.3)min。
2.2 术后并发症及处理 术后血胸2例(1例为静脉桥分支结扎线脱落;1例为术前血小板低,术后胸骨后渗血),术后出现重症感染2例,给予敏感抗生素治疗后治愈;1例移植肾衰竭患者术后长期发热,给予停用药物他克莫司,并以亚胺培南西司他丁钠、万古霉素及卡泊芬净联合静脉滴注后控制;术后房颤8例,给予减慢透析时超滤速率、减少超滤量及药物对症治疗后好转。术后常规口服拜阿司匹林、波立维抗血小板治疗。术后脱离呼吸机时间为(17.4±6.1)h,ICU滞留时间为(49.3±13.6)h。
2.3 术后透析情况 术后进行床旁透析,首次透析距手术结束时间(12.5±3.2)h,5例患者术后8 h内进行首次床旁透析,最短时间为术后2 h透析。术后8 h后透析患者其术后48 h引流量为(635±143.9)ml,较术后8 h内透析患者(928±162.7)ml明显减少(P<0.05)。术后5 d内每日透析一次,5 d后根据病情改为每2 d透析一次。
2.4 术后随访情况 术后14例患者定期随访1~3年,平均(35.3±11.6)个月。1例于术后27个月因重症感染死亡。术后2周、术后1年分别复查心脏彩超。术后2周患者LVEF、LVEDD较术前无明显改善(P≥0.05);术后1年患者LVEF、LVEDD较术前明显改善(P<0.05)。心功能分级术后2周(M=Ⅱ)、术后1年(M=I),较术前(M=3)明显改善。血肌酐、尿素氮指标术后2周、术后1年与术前相比较差异无统计学意义,见表1。
表1 各时间点心功能、肾功能相关指标比较(±s,n=14)
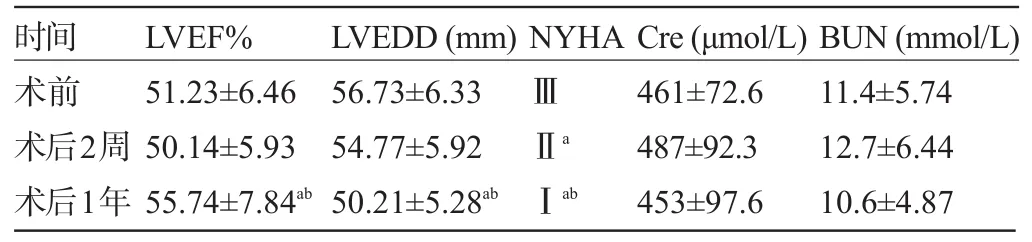
表1 各时间点心功能、肾功能相关指标比较(±s,n=14)
注:与术前比较,aP<0.05;与术后2周比较,bP<0.05。
时间LVEF%LVEDD(mm)NYHA Cre(μmol/L)BUN(mmol/L)术前术后2周术后1年51.23±6.46 50.14±5.93 55.74±7.84ab56.73±6.33 54.77±5.92 50.21±5.28abⅢⅡaⅠab 461±72.6 487±92.3 453±97.6 11.4±5.74 12.7±6.44 10.6±4.87
3 讨 论
尿毒症患者由于维持性血液透析、肾移植技术的开展得以延长生存时间,但由于同时合并糖尿病及转移性钙化使得MHD患者冠心病发病概率高达40%~70%[2]。心血管疾病(Cardiovascular disease,CVD)如高血压、高血脂等是MHD患者的主要死亡原因[5]。血管钙化是MHD患者死亡的重要预测指标[6-8]。
与普通冠心病患者一样,冠脉介入治疗、冠脉搭桥手术是严重冠脉病变血运重建的有效手段。冠脉搭桥的手术适应证对于重症患者与普通患者并无差异,但由于维持性血液透析患者长期处于慢性炎症状态,基础疾病多,心肺储备功能下降,术前一般状况相对差(包括轻度贫血、血小板减少、低蛋白血症、体质差、长期疾病所致焦虑等精神状态等),术后自动容量调节功能缺乏,手术风险大,特别是在异体肾移植状态患者中[9]。但术前病情的全面评估、手术适应证的把握、严格的围手术期管理均有助于提高手术成功率及改善预后[4]。本组病例中患者经冠脉搭桥手术后心功能明显改善,生活质量显著提高,取得了满意效果。而围手术期的管理是手术成功的关键,按照术前准备、术中管理、术后管理总结相关经验。
除常规CABG术前准备外,还应强化术前透析。充分透析、预防和减少尿毒症患者心血管并发症的发生是改善患者生存率和生活质量的重要措施[10]。术前2~3 d每日连续规律透析,利于减轻容量负荷,改善心肺功能,特别是对于心功能衰竭患者。同时,通过透析尽可能把血钾浓度调整到正常偏低的水平,使得术中、术后有更好的血钾浓度贮备空间;特别是在OPCABG患者中更为重要,可避免术中心律失常,减少术中紧急透析等情况。对于血小板低及未停抗血小板药的患者应备血小板,于术中或术后及时输入。肾衰患者多合并有贫血,术前血红蛋白多在90 g/L左右,术前无需处理,待术中复查后进一步处理。术前3 d停用促红细胞生成素,避免术中血液黏稠。术前血小板明显稍低的患者术前补充血小板有增加术前心梗风险,应该停机后复查血小板,如血小板低于50×109/L应及时补充,以减少出血的风险。
狭窄的冠状动脉充分再血管化、左心室功能恢复是改善冠心病患者预后的关键[11-12]。本组均选用LIMA与前降支搭桥,合并有室壁瘤者积极处理以恢复左心室功能。对于需行多支血管桥患者,倾向于选择CCABG,有以下优点:(1)可使再血管化更充分,获得更好的远期预后[13];(2)长期肾功能衰竭患者,心脏负荷重,心脏扩大,非体外循环搭桥移动心脏过程中易出现心律失常、循环不稳定,有心跳骤停可能,而体外循环可减少上述风险;(3)通过体外循环可调节术中血钾浓度、容量,对麻醉要求相对偏低。本组3例患者术前透析后血钾控制在4.0 mmo/L以下,且血管桥为1~2支,故采用OPCABG。体外循环过程中应根据血红蛋白水平、红细胞比容预充红细胞及血浆,不预充含钾液体,术中全程超滤,调整容量平衡及血钾浓度;体外循环停机时,保持血红蛋白在90 g/L左右,血钾浓度尽可能调整到正常偏低的水平,中心静脉压(CVP)维持在3~5 cmH2O(1 cmH2O=0.098 kPa),给术后早期补液留有空间。体外循环停机后,麻醉医师在能维持血压、心率稳定的基础上做到“尽量少输液体,尽量输入胶体,避免输入库存血”,不能按照常规的思维以CVP评估补液量。
术后透析是手术后康复的关键。患者术后的血容量及血钾浓度的调整完全依赖透析。但透析会造成体温下降及凝血因子消耗,增加出血风险。本组术后8 h内透析患者在术后48 h的引流量明显高于8 h后透析患者;2例患者在术后2 h、3 h进行首次透析,其引流量明显偏多。因此术后首次透析的时间应尽可能延后。通过手术中体外循环超滤、术中严格的液体管理,术后首次透析大多可在8 h后进行。对血钾偏高的患者则应尽早透析,以免诱发心跳骤停。尿毒症患者对高钾血症耐受较高,通常当血钾达6.0 mmol/L或明显容量负荷过重时进行透析。术后5 d每日透析一次,尽量减轻前负荷,减少心肺部并发症。5 d后根据病情改为每2 d透析一次并适时调整,本组1例患者每日透析持续5 d后改为隔日透析后,咳嗽咳痰,胸片表现为心影增大、肺淤血,改为每日透析后症状很快缓解。
肾衰患者由于水钠潴留、肺淤血、免疫力低下等原因,容易并发房颤、肺部感染甚至脓毒血症。透析是预防的重要措施,同时应用广谱抗菌素,尽早脱离呼吸机可减少交叉感染。本组病例术后出现重症感染2例,给予敏感抗生素治疗后治愈;1例移植肾衰竭患者术后长期发热,考虑长期服用抗排斥药物及透析管感染,给予停用他克莫司,并亚胺培南西司他丁钠、万古霉素及卡泊芬净联合静脉滴注后控制;术后房颤8例,给予减慢透析时超滤速率、减少超滤量及药物对症治疗后好转。
尿毒症透析患者合并冠心病行冠脉搭桥的手术风险较大,但经过全面的术前评估、严格的手术适应证把握、充分的冠状动脉再血管化,加强围手术期管理,可改善患者生存质量,延长存活时间,取得满意的疗效。
[1]杨艳,董莘,敖国昆,等.尿毒症与非尿毒症患者胸部CT心血管钙化的对照研究[J].中国医学装备,2015,12(2):62-64.
[2]Goodman WG,Goldin J,Kuizon BD,et al.Coronary-artery calcification in young adults with end-stage renal disease who are undergoing dialysis[J].N Engl J Med,2000,342(20):1478-1483.
[3]Chiu YW,Jiwakanon S,Lukowsky L,et al.An update on the comparisons of mortality outcomes of hemodialysis and peritoneal dialysis patients[J].Semin Nephrol,2011,31(2):152-158
[4]Gelsomino S,Da CP,Frassani R,et al.Coronary artery bypass grafting in patients with dialysis-dependent renal failure:ten-year results [J].Ital Heart J,2001,2(5):379-383
[5]徐丰博,孙懿,王银娜,等.维持性血液透析患者冠状动脉钙化的相关因素分析[J].首都医科大学学报,2015,36(4):630-633.
[6]Chen Z,Chen X,Xie J,et al.Fibroblast growth factor 23 is a predictor of aortic artery calcification in maintenance hemodialysis patients [J].Ren Fail,2013,35(5):660-666.
[7]Moldovan D,Moldovan I,Rusu C,et al.FGF-23,vascular calcification,and cardiovascular diseases in chronic hemodialysis patients[J]. Int Urol Nephrol,2014,46(1):121-128.
[8]Kidney Disease:Improving Global Outcomes(KDIGO)CKD-MBD Work Group.KDIGO clinical practice guideline for the diagnosis, evaluation,prevention,and treatment of chronic kidney disease-mineral and bone disorder[J].Kidney Int Suppl,2009,113:S1-130.
[9]吴新莲,唐盛,闭闵,等.血液透析滤过改善尿毒症患者心脏功能的疗效观察与护理[J].海南医学,2010,21(19):140-141.
[10]de Souza DD,Gerola LR,Hossne NJ,et al.Myocardial revascularization in renal transplant patients[J].Arq Bras Cardiol,2002,79(5): 476-483.
[11]Takagi H,Watanabe T,Mizuno Y,et al.A meta-analysis of adjusted risk estimates for survival from observational studies of complete versus incomplete revascularization in patients with multivessel disease undergoing coronary artery bypass grafting[J].Interact Cardiovasc Thorac Surg,2014,18(5):679-682.
[12]Raza S,Sabik JR,Masabni K,et al.Surgical revascularization techniques that minimize surgical risk and maximize late survival after coronary artery bypass grafting in patients with diabetes mellitus[J]. J Thorac Cardiovasc Surg,2014,148(4):1257-1264,1264-1266
[13]Takagi H,Umemoto T.Worse long-term survival after off-pump than on-pump coronary artery bypass grafting[J].J Thorac Cardiovasc Surg,2014,148(5):1820-1829.
Clinical analysis of coronary artery bypass grafting in uremic patients during hemodialytic treatment.
LIU Wei1, CAO Jian-jun1,HU Xiao-ping2,WANG Hong-yu1,CHEN Hao1.1.Department of Cardiothoracic Surgery,Dongfeng General Hospital,Hubei University of Medicine,Shiyan 442008,Hubei,CHINA;2.Department of Cardiovascular Surgery, Renmin Hospital of Wuhan University,Wuhan 434000,Hubei,CHINA
ObjectiveTo investigate the surgical treatment methods for uremic patients with coronary heart disease(CHD)on maintenance hemodialysis.MethodsFourteen patients with uremia and CHD on maintenance hemodialysis were operated with coronary artery bypass grafting(CABG)from January 2009 to December 2014 in Dongfeng General Hospital.Among the 14 patients,there were 13 patients of chronic renal failure,1 patient of acute renal failure, with one patient complicating ventricular aneurysm.Three patients were treated with off-pump CABG(OPCAB),and 11 patients were treated with conventional CABG(CCABG),all using left internal mammary artery(LIMA)as grafts and with 1~4 graft vessels.One patients received placation for ventricular aneurysm.The left ventricular end-diastolic diameter(LVEDD),left ventricular ejection fraction(LVEF),New York Heart Association(NYHA)heart function classification,Serum creatinine(Cre)and blood urea nitrogen(BUN)were compared in all patients before operation,2 weeks after operation and 1 year after operation.The curative effects of surgical treatment were evaluated.ResultsAll the 14 patients were successfully operated,and 2 patients obtained severe postoperative infection after operation.During the follow-up of 1~3 years,one patient died of severe infection 27 months after operation,and the rest all developed well.Two weeks after operation,NYHA heart function classification wasⅡ (M=Ⅱ),and the levels of LVEF,LVEDD,Cre, BUN showed no significant difference compared with the levels before operation(P≥0.05).One year after operation, NYHA heart function classification wasⅠ(M=Ⅰ),which were significantly improved than that of two weeks after operation.LVEF and LVEDD one year after operation were significantly improved compared with those before operation[(55.74±7.84)%vs(51.23±6.46)%,(50.21±5.28)mm vs(56.73±6.33)mm,P<0.05],while Cre and BUN showed no significant difference between one year after operation and before operation(P≥0.05).ConclusionThere is ahigh risk for patients with uremia and CHD on maintenance hemodialysis to accept CABG.Rigorous preoperative evaluation,adequate coronary revascularization and perioperative period management should be performed to achieve a satisfactory efficacy.
Coronary heart disease;Uremia;Hemodialysis;Coronary artery bypass graft
R692.5
A
1003—6350(2016)04—0567—04
10.3969/j.issn.1003-6350.2016.04.018
2015-08-18)
中央高校基本科研业务费专项资金项目青年教师资助项目(编号:2042014kf0117);湖北省十堰市科技局指导项目(编号:ZD 2012035]
陈浩。E-mail:xwkchen@163.com

