超高效液相色谱-串联四级杆质谱法测定中药材(饮片)中非法添加6种水溶性红色素通用方法的研究*
徐昱婷,张学博,苏 静,龚 瑞,徐 刚,沙禕炜**
(1. 闸北区卫生和计划生育委员会 上海 200070;2.上海市崇明食品药品检验所 上海 202150;3. 上海食品药品包装材料测试所 上海 201203)
超高效液相色谱-串联四级杆质谱法测定中药材(饮片)中非法添加6种水溶性红色素通用方法的研究*
徐昱婷1,张学博2,苏 静2,龚 瑞3,徐 刚2,沙禕炜2**
(1. 闸北区卫生和计划生育委员会 上海 200070;2.上海市崇明食品药品检验所 上海 202150;3. 上海食品药品包装材料测试所 上海 201203)
目的:建立快速筛查及确证中药材(饮片)中非法添加6种水溶性红色素(日落黄、苋菜红、胭脂红、赤藓红、新品红、酸性红73)的超高效液相色谱-串联四级杆质谱的通用方法。方法:中药材(饮片)经溶剂提取后,采用超高效液相色谱法分离,以乙腈和5 mmol·L-1乙酸铵溶液为流动相,进行梯度洗脱,采用多反应监测模式,筛查中药材(饮片)中非法添加的6种水溶性红色素,并进行确证。结果:超高效液相色谱-串联四级杆质谱可在4 min内快速筛选并确证是否含有非法添加的6种水溶性红色素。结论:该方法具有简便快捷、灵敏度高、结果准确的特点,适用于中药材(饮片)中非法添加6种水溶性红色素的筛查和确证工作。
超高效液相色谱-串联质谱 色素 中药材(饮片) 非法添加
近年来,在药品检验工作中发现有不法分子将假、劣药材染色后冒充正品,颜料染色伪制的常用药材、贵细中药材(饮片),外观性状酷似正品,隐蔽性大,不易辨别。如果缺乏相关的药材知识和严格的监管制度,这些假冒伪劣中药材会在临床应用,这将扰乱药材市场,严重影响中药材的临床合理、安全、有效用药,甚至危及患者的生命。若染色药材经进一步加热炮制,如蒲黄炒炭、黄芩酒炒等,其中的化工染料又可能因受热分解产生新的有害物质。这会给患者用药安全带来潜在威胁,给患者家庭造成重大经济损失。因此,必须随时随地予以严厉打击,依法检查和处理假冒伪劣中药材[1,2]。
目前,中国中药材(饮片)现行标准中,对于此类染色现象的相关标准较少,国内外对于中药材(饮片)中非法添加色素检测方法的相关研究报道文献较少,而检测多组分色素或色素系列的方法更为罕见。在检测中药材(饮片)非法添加色素的研究工作中,检测方法开始向仪器化和自动化发展,目前色素测定多采用薄层色谱法[3,4]、液相色谱法[5-9]和气相色谱-质谱法[10],而液相色谱-质谱法[11-14]则主要用于食品检测,且食品中色素检测方法[15]较为多样和通用。虽然,《中国药典》2015年版第四部有9303色素测定法指导原则[16],但覆盖面和通用性尚需完善。
由于不法分子贪图利益,中药尤其是中药材(饮片)非法添加色素的状况愈演愈烈。因此,建立系统的中药材(饮片)多组分色素的检测方法工作迫在眉睫。
为解决以上问题,本研究采用超高效液相色谱-串联四级杆质谱法测定法,建立了一种快速筛查和确证中药材(饮片)中非法添加6种水溶性红色素的通用方法。
1 实验部分
1.1 仪器、药品与试剂
ACQUITY UPLC超高效液相色谱系统(美国Waters公司);Waters BEH C18色谱柱(50 mm×2.1 mm,1.7 μm);TQD三重四级杆质谱仪(美国Waters公司);0.2 μm针式滤器(上海安谱公司)。
乙腈、甲醇(德国Merck公司,色谱纯);纯净水(中国娃哈哈公司);其余试剂均为分析纯;日落黄、苋菜红、胭脂红、赤藓红、酸性红73、新品红标准品(购自中国药品生物制品检定所);朱砂、紫苏梗、乌梅、五味子、枸杞子、鸡血藤、丁香、红花、玫瑰花、丹参(均为市售商品药材)。
1.2 色谱条件
色谱柱:Waters ACQUITY UPLC BEH C18柱(50 mm×2.1 mm,1.7 μm),流速:0.2 mL·min-1, 柱温:25℃, 进样量:10 μL,样品室温度:20 ℃,流动相:采用5 mmol·L-1乙酸铵溶液(A)-乙腈(B),梯度洗脱条件见表1。

表1 流动相梯度洗脱表
1.3 质谱条件
离子化模式:电喷雾离子源(ESI),正离子模式(ESI+);扫描方式:多反应监测(Multiple Reaction Monitoring,MRM);毛细管电压:3.5 kV,去溶剂气温度400℃,离子源温度:120℃,用于定性的离子对及锥孔电压和碰撞能量参数[17]见表2。
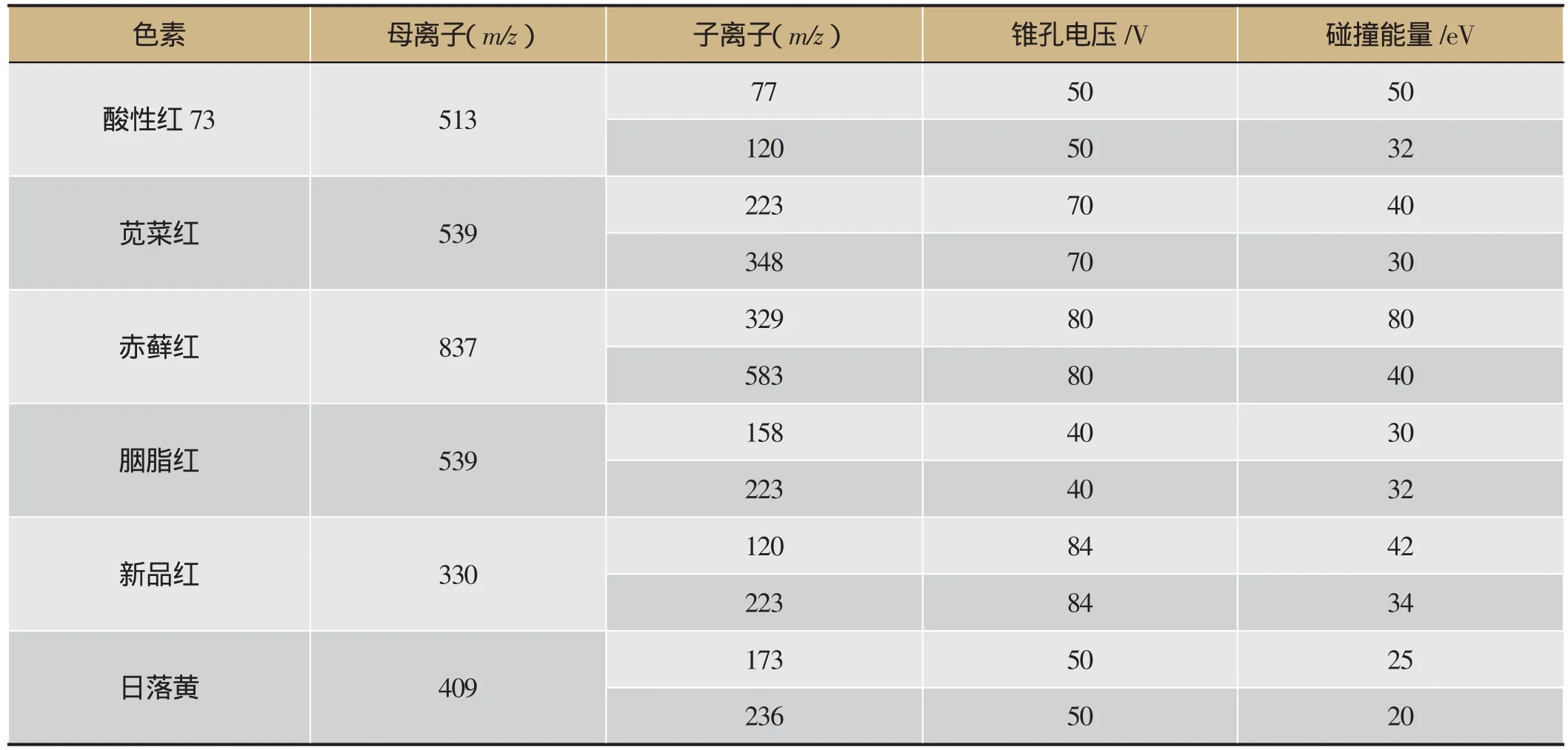
表2 六种色素质谱MRM多反应监测其他条件
1.4 标准储备液和工作液的配制
精密称取适量的各色素标准品,用70%乙醇溶解并定容至10 mL,配制出1 mg·mL-1标准储备液,于-20℃下保存。精密量取各色素标准储备液200 μL,用水定容至100 mL,作为混合标准工作液,于4℃下保存。
1.5 样品前处理
1.5.1 阳性样品制备
取已知不含任何色素的丁香和鸡血藤,将标准混合溶液按0.4 mg·g-1比例,定量喷洒加入中药材(饮片)中,挥干溶剂,置烘箱中50℃干燥4 h,作为阳性样品。
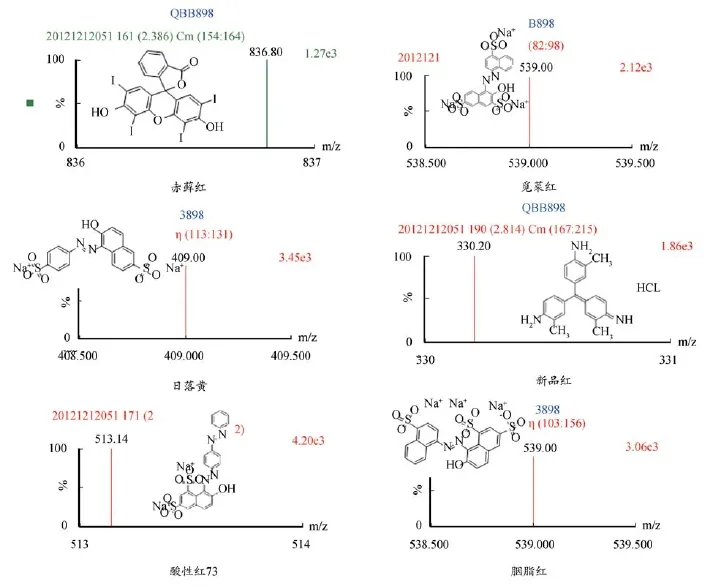
图1 6种色素一级质谱图及结构式
1.5.2 供试品溶液制备
称取中药材(饮片)或阳性样品2 g,加70%乙醇20 mL,超声提取20 min,取上清液离心,精密量取1 mL,用水定容至20 mL,过0.20 μm聚醚砜微孔滤膜后,作为供试品溶液。
2 结果
分别取朱砂、紫苏梗、乌梅、五味子、枸杞子、鸡血藤、丁香、红花、玫瑰花、丹参等药材共计13批样品,其中红花3批,按上述实验条件进行测定。由实验结果表明,朱砂、紫苏梗、乌梅、五味子、鸡血藤、丁香、玫瑰花、丹参及一批红花中均未检出含有色素,有两批红花中含有日落黄和胭脂红(《中国药典》2015年版未收载的色素[16])。
该方法将超高效液相色谱的高速、高分离度与串联四级杆质谱的高选择性、高灵敏度相结合,具有通用性强、选择性好、灵敏度高、便捷省时的优点。本研究建立了中药材(饮片)中日落黄、苋菜红、胭脂红、赤藓红、酸性红73、新品红的UPLC-ESI-MS/MS检测的方法,方法快速、简单、灵敏,抗干扰能力强,定性准确,一次提取和进样即可完成多成分色素的筛查,也适用于中药材(饮片)中这6种红色素的确证,其检测结果也为中药材(饮片)监督检查提供确切、有效的科学法律依据,可用于中药材(饮片)日常监督检测工作。
3 讨论
3.1 样品处理方法的优化
3.1.1 提取方法
日落黄、苋菜红、胭脂红、赤藓红、酸性红73、新品红均为水溶性色素,极性较大,各色素均在水、70%乙醇中有较好的溶解性,为了获得较高的提取效率,通过实验比较,选择70%乙醇作为提取溶剂。为了减少操作步骤及提高提取效率,采用超声提取方式对样品进行提取。考察了不同提取时间和和提取次数的提取效果,最终确定最佳的样品处理条件。
3.1.2 过滤器的选择
由于中药材(饮片)成分较复杂,经70%乙醇提取后,可能存在一些杂质。本实验选择亚微米粒径的色谱柱,这些杂质的存在容易堵塞液相色谱柱,也有可能污染质谱。为了净化样品,避免损失仪器,样品需通过0.20 μm微孔滤膜进行净化。实验室常用样品过滤器有尼龙66(Nylon)、聚醚砜(PES)、聚偏氟乙醚(PVDF)、混合纤维素(MCE)等。本实验考查了各种针式滤器对样品的吸附作用。实验结果表明,尼龙66、混合纤维素等常用针式滤器对样品明显的吸附作用。因此本实验采用聚醚砜(PES)针式滤器对样品进行净化。
3.2 色谱条件的优化
3.2.1 色谱柱的选择
本实验采用1.7 μm粒径色谱柱与传统5 μm粒径的色谱柱相比,分析时间大大减小,柱效大大提高,同时显著提高了样品分析的通量。
3.2.2 流动相的选择
通过实验分别考察了有机相溶剂(甲醇和乙腈)与不同种类挥发性缓冲液组成的流动相体系,如甲醇(或乙腈)-5mmol·L-1甲酸铵溶液、甲醇(或乙腈)-5mmol·L-1乙酸铵溶液、甲醇(或乙腈)-0.1%甲酸溶液等、结果表明,以乙腈 -5mmol·L-1乙酸铵溶液作为流动相时色谱峰形、分离效果和质谱信号相应最佳。通过比较不同乙酸铵缓冲液离子强度的影响,分别考察了浓度2 -10 mmol·L-1乙酸铵溶液,结果表明5mmol·L-1乙酸铵为最佳添加量。通过梯度洗脱方式,各色素能得到有效分离。

图3 空白溶剂总离子流图
3.3 质谱条件的优化
本实验所检测的色素为偶氮类、蒽醌类和三芳基甲烷类色素。在ESI+和ESI-离子化模式下,对各色素进行全扫描,选择适当的电离方式和子离子。结果表明,日落黄、新品红、苋菜红、胭脂红、酸性红73、赤藓红在ESI+电离模式下均具有较高的丰度。苋菜红、胭脂红、日落黄、赤藓红为含钠色素,母离子为[(M-nNa)+(n+1)H]+,新品红为含氯色素,母离子为[M-Cl+H]+。在确定各色素准分子离子后,对二级质谱进行分析,对子离子进行优化选择,确定定量离子和定性离子。通过优化毛细管电压、一级锥孔电压、二级锥孔电压、萃取锥孔电压、碰撞能量、质谱分辨率等质谱参数,使每种色素的特征碎片离子的强度达到最大。
由于苋菜红和胭脂红为同分异构体,母离子均为539,均有子离子223,因此在苋菜红和胭脂红在232子离子处有响应,但是苋菜红和胭脂红出峰时间不同,可明显区分苋菜红和胭脂红,出峰顺序依次为苋菜红、胭脂红。
3.4 UPLC-ESI-MS/MS优点
本实验方法为发挥UPLC的最大优势,同时选用亚微米小颗粒填料色谱柱,提高了样品分离度、样品通量和灵敏度。0.2 mL·min-1的流速更适合质谱电喷雾化的要求,减少溶剂对结果的影响,所用溶剂也大大减少,减少了检验成本,与此同时,实验产生废液也大大降低。
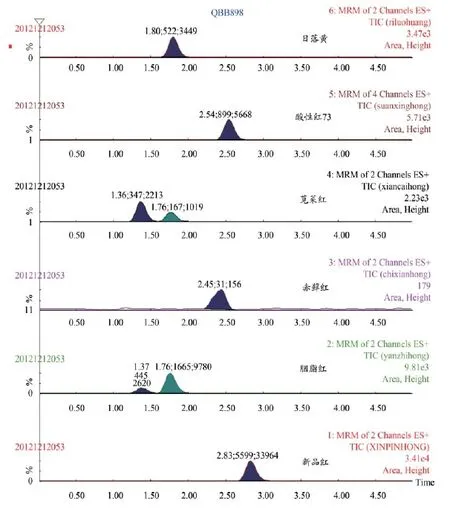
图4 丁香阳性样品总离子流图
3.5 方法专属性
在本实验条件下分别称取朱砂(矿物类)、紫苏梗(全草类)、乌梅(果实类)、五味子(果实类)、枸杞子(果实类)、鸡血藤(藤茎类)、丁香(花类)、红花(花类)、玫瑰花(花类)、丹参(根茎类)药材按“1.5.2 供试品溶液制备”项下方法制备供试品溶液进行测定,结果表明,这5类10种中药材在相应色素色谱峰位置均不干扰色素的测定。实验还考察了溶剂对实验结果的影响,由实验结果表明,溶剂水和70%乙醇对色素测定均不干扰。
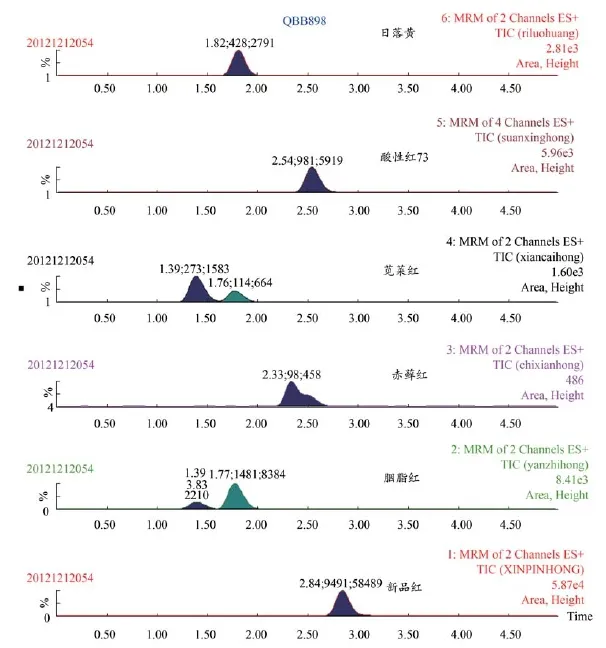
图5 鸡血藤阳性样品总离子流图
1 吴云燕,孙雪妮.中药饮片染色现象不容忽视.中草药,2001,32(8): 752-753.
2 饶伟文,蒋玲,赵纯玉,等.几种染色掺假中药的化工染料鉴定.药物分析杂志,2007,27(11): 1742-1745.
3 胡青,孙健.张甦,等. 中药中48 种非法染色色素的TLC法检测.中国医药工业杂志,2015,46(7): 695-700.
4 刘艳,张勤,吕志刚,等. 红花中非法添加色素的薄层色谱快速鉴别法.中国实验方剂学杂志,2014,20(18): 95-98.
5 李启艳,朱日然,孙萍,等. HPLC-DAD 法检测染红中药材中20种非法添加色素.医药导报,2015,34(5): 655-657.
6 郑娟,邹耀华. HPLC-PDA 法检测蒲黄和黄连中十种非法添加色素.中国卫生检验杂志,2011,21(5): 1078-1082.
7 邹耀华,殷红妹,郭怡飚,等. HPLC-PDA法检测西红花和红花中十一种非法添加色素.中国卫生检验杂志,2010,20(11): 2724-2725.
8 汪建君,陈惠玲. HPLC-PDA 法检测正天丸和正天胶囊中6 种非法添加色素.药物评价研究,2013,36(1): 51-53.
9 金竹昳,陈旭,戴小峰,等.利用HPLC 建立对比筛选法测定红花中色素金橙Ⅱ.天然产物研究与开发,2013,36(3): 384-387,402.
10 苏小川. 调味品中苏丹红违禁色素的GC-MS分析测定. 广西科学院学报,2006,22(S1): 459-462.
11 吕东明,丁云连,詹晟,等. 超高效液相色谱/ 四极杆-飞行时间质谱法检测22 种禁用和限用合成色素.现代仪器与医疗,2013,19(2): 52-56.
12 侯建波,谢文,李杰,等. 液相色谱-串联质谱法测定虾肉中7种非食用色素的残留量.理化检验-化学分册,2015,51(11): 1541-1546.
13 杨熙,吴惠勤,黄芳,等. 高效液相色谱-串联质谱法同时测定粉条中6 种人工合成色素. 分析试验室,2015,34(6): 672-676.
14 陈晓红,李小平,赵永纲,等. 固相萃取超快速液相色谱-串联质谱同时测定熟肉制品中常用人工合成色素. 卫生研究,2015,44(4): 636-640.
15 肖义夫,廖百森.食品中非食用色素及其检测方法研究进展. 现代预防医学,2008,35(16): 3159-3160.
16 国家药典委员会. 中国药典(四部). 北京: 中国医药科技出版社,2015: 404-406.
17 董鲁艳,刘颖,张加余,等. 超高效液相色谱一质谱/质谱联用法快速测定苦碟子注射液中两种倍半萜内酯类成分的含量. 世界科学技术一中医药现代化,2014,16(12): 2671-2675.
General Approaches to Determining Six Water-Soluble Red Pigments Illegally Added in Crude Drug (Prepare Slices) by UPLC-ESI-MS / MS
Xu Yuting1,Zhang Xuebo2,Su Jing2,Gong Rui3,Xu Gang2,Sha Yiwei2
(1. Shanghai Zhabei District Health and Family Planning Commission,Shanghai 200070,China; 2. Shanghai Chongming Institute for Food and Drug Control,Shanghai 202150,China; 3. Shanghai Food and Drug Packaging Material Control Center,Shanghai 201203,China)
The study aimed to establish a general method for the rapid screening and confirmation of the six water-soluble red pigments,sunset yellow,amaranth,carmine,erythrosine,new fuchsin and acid red 73,using UPLC-ESI-MS/MS. The six water-soluble red pigments were illegally added into crude drug or prepare slices. After extracting the samples through bysolvent extraction,the UPLC-ESI-MS / MS method was adopted using a gradient elution with the mobile phase of acetonitrile and ammonium acetate solution (5 mmoL·L-1). The MRM mode was performed to screen and quantitatively confirm the six red pigments added illegally. The results showed that UPLC-ESI-MS / MS method rapidly screened and confirmed whether the illegal six red pigments had been added into the crude drug or prepare slices within 4 minutes. In conclusion,the UPLC-ESI-MS / MS method was accurate and suitable for screening and confirming water-soluble red pigments in crude drug or prepare slices featuring simple,sensitivity and accuracy.
UPLC-ESI-MS/MS,pigment,crude drug (prepare slices), illegally additives
10.11842/wst.2016.05.031
R2
A
(责任编辑:马雅静,责任译审:朱黎婷)
2015-12-08
修回日期:2015-12-25
* 上海市食品药品监督管理局科技攻关课题(2011JY2-06);中药材(饮片)中非法添加红色类色素的快速检测法及确证方法的建立,负责人:沙禕炜,苏静。
** 通讯作者:沙禕炜,在职研究生,主管中药师,主要研究方向:中药、食品(含保健食品)和化妆品检验分析及质量管理工作。

