清瘟败毒散的质量标准提升研究
潘春晖,杨红玉,张 煊,,任园琴,彭晓凤,刘 涛,*
(1.四川德成动物保健品有限公司,德阳618100;2.成都大学药学与生物工程学院,成都610106)
清瘟败毒散的质量标准提升研究
潘春晖1,杨红玉1,张 煊1,2,任园琴2,彭晓凤2,刘 涛1,2*
(1.四川德成动物保健品有限公司,德阳618100;2.成都大学药学与生物工程学院,成都610106)
摘 要:为完善清瘟败毒散的质量标准,采用薄层色谱鉴别清瘟败毒散中的黄连、地黄、栀子、连翘、知母、淡竹叶;采用HPLC法测定清瘟败毒散中的栀子苷含量,色谱条件为:ODS C18色谱柱(4.6mm ID×250mm,5μm),乙腈-水(13∶87)为流动相,检测波长为238nm。研究结果表明,在建立的薄层色谱鉴别结果中,在与对照药材色谱相对应的位置上,供试品色谱显示相同颜色的斑点,且阴性样品无干扰;栀子苷在0.062~0.370μg范围内具有良好的线性关系,其回归方程为y=1 789.1x-14.296,R2=0.99984,平均回收率为99.60%,RSD为0.76%。本方法简单、准确、重复性好,能更好地控制清瘟败毒散的质量,可作为清瘟败毒散的质量标准。
关键词:清瘟败毒散;质量标准;薄层色谱;测定
清瘟败毒饮是清代著名温病学家余师愚所创制的名方[1],治一切火热,表里俱盛,狂躁烦心,口干咽痛,大热干呕,错语不眠,吐血衄血,热盛发斑[2],载于其所著的《疫疹一得》一书中,现收录于《中华人民共和国兽药典》2010年版二部。本药由石膏、地黄、水牛角、黄连等14味药材组成,是“白虎汤”、“黄连解毒汤”和“犀角地黄汤”3方加减化裁而得[3]。清瘟败毒散由清瘟败毒饮改剂型而来,具有泻火解毒,凉血的功效,在兽药临床上主要用于治疗热毒发斑,高热神昏[4],在临床上有着较好的疗效,被收载于2010年版《中华人民共和国兽药典》二部,其现有法定质量标准简单,仅有显微鉴别和黄连的薄层鉴别,无含量测定项,该标准很难控制其产品质量,不能保证产品临床疗效。为了提升清瘟败毒散的质量标准,保证产品的安全性、有效性与质量可控性,本试验对其进行了研究。
1 材料与方法
1.1仪器与试剂
FA2004分析电子天平购自上海良平仪器仪表有限公司;DZF-6050型真空干燥箱购自北京中兴伟业仪器有限公司;P230II型高效液相色谱仪测定系统购自大连伊力特分析仪器有限公司。正丁醇、冰乙酸、甲醇、乙酸乙酯、三氯甲烷、氨水、硫酸、香兰素、丙酮、甲酸、二甲苯均为分析纯均购自成都市科龙化工试剂厂;清瘟败毒散购自四川德成动物保健品有限公司;石膏、地黄、水牛角、黄连、栀子、牡丹皮、黄芩、赤芍、玄参、知母、连翘、桔梗、甘草、淡竹叶对照药材均购自中国食品药品检定研究院。
1.2薄层鉴别
1.2.1黄连的薄层鉴别 参照文献[5-7]报道的方法,取清瘟败毒散2g,加甲醇25mL,超声30min,滤过,滤液蒸干,残渣加甲醇2mL使其溶解,作为供试品溶液;取黄连对照药材0.25g,按清瘟败毒散处方(除去黄连药材),同法制成对照药材溶液和阴性样品溶液。分别吸取供试品溶液、对照药材溶液与阴性样品溶液,点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(10∶1∶2)为展开剂,展开、取出、晾干,置紫外光灯(365.5nm)下检视。
1.2.2地黄的薄层鉴别 参照文献[8-10]报道的方法,取清瘟败毒散2g,加甲醇25mL,超声处理30min,滤过,滤液蒸干,残渣加水10mL使其溶解,采用乙酸乙酯振摇提取2次,每次10mL,合并乙酸乙酯液,蒸干,残渣加甲醇2mL溶解,作为供试品溶液;取地黄对照药材1g,按清瘟败毒散处方(除去地黄药材),同法制成对照药材溶液和阴性样品溶液。分别吸取供试品溶液、对照药材溶液与阴性样品溶液,点于同一硅胶G薄层板上,以三氯甲烷-甲醇-氨水(14∶1∶0.1)为展开剂,展开、取出、晾干,喷以5%香草醛硫酸溶液,在105℃下,加热至斑点清晰。
1.2.3栀子的薄层鉴别 参照文献[11-13]报道的方法,取本品粉末2g,加50%甲醇25mL,超声处理40min,滤过,滤液蒸干,加甲醇2mL溶解,作为供试品溶液。另取栀子对照药材0.5g、按清瘟败毒散处方(除去栀子药材),同法制成对照药材溶液和阴性样品溶液。再取栀子苷对照品,加甲醇制成每1mL含4mg的溶液,作为对照品溶液。照薄层色谱法(附录ⅥB)试验,吸取上述4种溶液,分别点于同一硅胶G薄层板上,以乙酸乙酯-丙酮-甲酸-水(5∶5∶1∶1)为展开剂,展开、取出、晾干。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的黄色斑点;再喷以10%硫酸乙醇溶液,在110℃加热至斑点显色清晰。
1.2.4连翘的薄层鉴别 参照文献[14-16]报道的方法,取清瘟败毒散2g,加甲醇10mL,超声处理30min,过滤,取滤液作为供试品溶液;取连翘对照药材1g、按清瘟败毒散处方(除去连翘药材),同法制成对照药材溶液和阴性样品溶液。吸取供试品溶液、对照药材溶液和阴性样品溶液,点于同一硅胶G薄层板上,以三氯甲烷-甲醇(5∶1)为展开剂,展开、取出、晾干,喷以10%的硫酸乙醇溶液,在105℃下加热至斑点清晰。
1.2.5淡竹叶的薄层鉴别 参照文献[17]报道的方法,取清瘟败毒散2g,加甲醇10mL超声处理30min,过滤,滤液蒸干,加甲醇2mL溶解,作为供试品溶液;取淡竹叶0.5g、按清瘟败毒散处方(除去淡竹叶药材),同法制成对照药材溶液和阴性样品溶液。分别吸取供试品溶液、对照药材溶液、阴性样品溶液,点于同一硅胶G薄层板上,以二甲苯-乙酸乙酯-丙酮-甲酸-水(2.2∶4.8∶2.5∶0.8∶1.5)为展开剂,展开,取出,晾干,置紫外光灯(365.5nm)下检视。
1.2.6知母的薄层鉴别 参照文献[18-19]报道的方法,取本品粉末2g,加30%丙酮10mL,超声处理20min,取上清液作为供试品溶液。另取知母对照药材0.2g、按清瘟败毒散处方(除去知母药材),同法制成对照药材溶液和阴性样品溶液。照薄层色谱法(附录ⅥB)试验,吸取上述3种溶液,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(4∶1∶5)的上层溶液为展开剂,展开、取出、晾干,置紫外光灯(365.5nm)下视检。
1.3清瘟败毒散中栀子苷的含量测定
1.3.1色谱条件的筛选 参考2015版《中华人民共和国药典》一部[11]栀子项下栀子苷含量测定方法,色谱柱为(C18 4.6mm ID×250mm,5μm);流速为1.0mL/min;检测波长为238nm;柱温为室温;进样体积为10μL;以分离度R为指标,考察流动相。
1.3.2供试品溶液制备方法研究
1.3.2.1提取方式 取2份清瘟败毒散各2.0g,精密称定,精密移取25mL甲醇加入,称定重量,分别超声(功率100W,频率40kHz)提取与加热回流提取30min,放冷至室温,补足减失重量,过滤,取续滤液作为供试品,按照2.2.1项下色谱条件测其含量。
1.3.2.2提取溶媒种类 取清瘟败毒散2.0g、3份,精密称定,置具塞锥形瓶中,分别精密移取25mL水、无水乙醇,甲醇加入,称定重量,超声处理30min,放冷至室温,补足减失重量,过滤,取续滤液作为供试品,按照2.2.1项下色谱条件测其含量。
1.3.2.3溶媒浓度 取4份清瘟败毒散各2.0g,精密称定,置具塞锥形瓶中,分别精密移取25mL 25%、50%、75%、100%的甲醇加入,称定重量,超声处理30min,放冷至室温,补足减失重量,过滤,取续滤液作为供试品,按照2.2.1项下色谱条件测其含量。
1.3.2.4溶媒用量 取4份清瘟败毒散各2.0g,精密称定,置具塞锥形瓶中,分别精密移取75%的甲醇10、25、50、100mL加入,称定重量,超声处理30min,放冷至室温,补足减失重量,过滤,取续滤液作为供试品,按照2.2.1项下色谱条件测其含量。
1.3.2.5提取时间 取4份清瘟败毒散各2.0g,精密称定,置具塞锥形瓶中,精密移取50mL 75%的甲醇加入,称定重量,分别超声处理15、30、45、60min,放冷至室温,补足减失重量,过滤,取续滤液作为供试品,按照2.2.1项下色谱条件测其含量。
1.3.3对照品溶液、对照药材溶液与阴性样品溶液的制备 精密称取栀子苷对照品适量,加甲醇制成每1mL含0.0309mg的溶液,作为对照品溶液;取栀子对照药材0.1g、清瘟败毒散处方(除栀子药材),按供试品溶液的制备方法,同法制得对照药材溶液与阴性样品溶液。
1.3.4栀子苷的方法学研究
1.3.4.1专属性 取对照品溶液、供试品溶液、阴性样品溶液在2.2.1所确定的色谱条件下进样分析。
1.3.4.2线性关系 使用自动进样器分别吸取栀子苷对照品(0.0309mg/mL)2、4、6、8、10、12μL,按2.2.1的色谱条件进样分析。
1.3.4.3精密度 使用自动进样器吸取栀子苷对照品(0.0309mg/mL)10μL,按2.2.1的色谱条件连续进样6次,根据峰面积计算RSD值。
1.3.4.4稳定性 取清瘟败毒散2.0g,精密称定,精密移取50mL 75%的甲醇,超声提取30min,放冷至室温,补足减失重量,滤过,取续滤液作为供试品溶液。按2.2.1的色谱条件于0、2、4、6、8、10h分别进样。根据栀子苷的峰面积计算RSD值。
1.3.4.5重复性 取清瘟败毒散2.0g、6份,精密称定,置具塞锥形瓶中,精密移取50mL 75%的甲醇加入,称定重量,超声处理30min,放冷至室温,补足减失重量,过滤,取续滤液作为供试品。按2.2.1的色谱条件分别进样,根据栀子苷的含量计算RSD值。
1.3.4.6加样回收率试验 取已知含量的清瘟败毒散1.0g、6份,精密称定,置具塞锥形瓶中,精密移取50mL 75%的甲醇和2.6mL栀子苷对照品(0.2732mg/mL),称定重量,超声处理30min,放冷至室温,补足减失重量,过滤,取续滤液作为供试品。按2.2.1的色谱条件分别进样,根据峰面积测定栀子苷含量,计算回收率、平均加样回收率及RSD值。
2 结果与分析
2.1薄层鉴别
清瘟败毒散组方中黄连、地黄、栀子、连翘、淡竹叶及知母的薄层鉴别,与对照药材色谱相对应的位置,供试品色谱显示相同颜色的斑点,且阴性样品无干扰结果(图1~6)。
2.2清瘟败毒散中栀子苷的含量测定
2.2.1色谱条件的筛选 以乙腈-水(15∶85)为流动相,结果显示供试品色谱中栀子苷与后一峰的分离度R=0.86<1.5,达不到分离要求;以乙腈-水(13∶87)为流动相,结果显示供试品色谱中栀子苷与后一峰的分离度R=1.61>1.5,满足分离要求。故后续试验栀子色谱条件:苷色谱柱为(C18 4.6mm ID×250mm,5μm);流速为1.0mL/min;检测波长为238nm;柱温为室温;进样体积为10μL;流动相为乙腈-水(13∶87)。
2.2.2供试品溶液制备方法研究
2.2.2.1提取方式 超声与加热回流提取两种提取方式所得栀子苷含量均为0.070%。超声简便,且节约时间。
2.2.2.2提取溶媒种类 25mL水、无水乙醇,甲醇超声提取30min,所得栀子苷含量分别为0.032%、0.047%、0.061%。

图1 黄连的薄层鉴别Fig.1 The TLC identification ofCoptis

图2 地黄的薄层鉴别Fig.2 The TLC identification ofRadixRehmanniae

图3 栀子的薄层鉴别Fig.3 The TLC identification ofGardenia
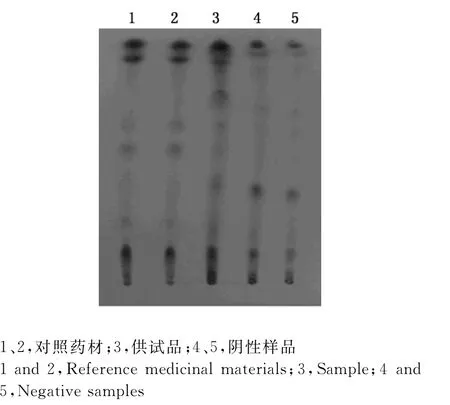
图4 连翘的薄层鉴别Fig.4 The TLC identification ofForsythia

图5 淡竹叶的薄层鉴别Fig.5 The TLC identification ofLophatherumgracileBrongn

图6 知母的薄层鉴别Fig.6 The TLC identification ofRhizomaanemarrhenae
2.2.2.3溶媒浓度 25mL 25%、50%、75%、100%的甲醇超声提取30min,所得栀子苷含量分别为0.060%、0.063%、0.066%、0.063%。
2.2.2.4溶媒用量 10、25、50、100mL 75%的甲醇超声提取30min,所得栀子苷含量分别为0.0586%、0.0537%、0.0625%、0.0590%。
2.2.2.5提取时间 50mL 75%的甲醇超声处理15、30、45、60min,所得栀子苷含量分别为0.0606%、0.0628%、0.0629%、0.0633%,当提取时间达到30min后,栀子苷含量基本不再增加。
2.2.3供试品溶液的制备 经上述考察,供试品溶液的制备方法为:取清瘟败毒散2.0g,精密称定,精密移取50mL 75%的甲醇,超声提取30min,放冷至室温,补足减失重量,滤过,取续滤液,即得。
2.2.4栀子苷的方法学研究
2.2.4.1专属性 供试品色谱图在与栀子苷对照品色谱图主峰相应的保留时间处有峰,且阴性样品色谱图在与栀子苷对照品色谱图主峰相应的保留时间处无峰,即阴性无干扰(图7~9)。
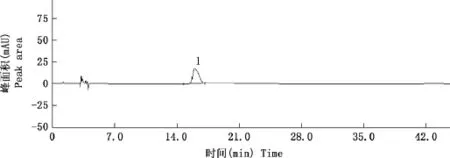
图7 栀子苷对照品色谱Fig.7 The control chromatogram ofGardenin
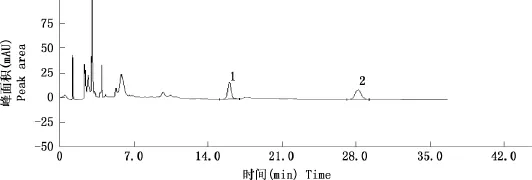
图8 供试品色谱图Fig.8 The chromatography of samples

图9 阴性样品色谱图Fig.9 The chromatography of negative samples
2.2.4.2线性关系 以栀子苷进样量(μg)为横坐标,峰面积(mAU)为纵坐标,计算回归方程为y=1789.1x-14.296,R2=0.99984,表明栀子苷在0.062~0.370μg范围内具有良好的线性关系。
2.2.4.3精密度 按2.2.1的色谱条件连续进样6次,峰面积分别为596.262、593.426、592.462、591.343、588.809、591.483mAU,根据峰面积计算RSD值为0.292%。
2.2.4.4稳定性 按2.2.1的色谱条件于0、2、4、6、8、10h进样,峰面积分别为920.199、923.574、925.085、920.760、925.430、918.162。根据栀子苷的峰面积计算RSD值为0.335%。
2.2.4.5重复性 按2.2.1的色谱条件测定6份样品的栀子苷含量分别为0.0711%、0.0716%、0.0715%、0.0706%、0.0620%、0.0613%,根据栀子苷的含量计算RSD值为1.098%。
2.2.4.6加样回收率试验 按2.2.1的色谱条件进样,根据峰面积测定栀子苷含量,计算回收率分别为98.42%、99.11%、100.52%、100.12%、99.92%、99.51%,平均加样回收率为99.60%,RSD值为0.76%。
3 讨 论
清瘟败毒散中栀子的薄层鉴别,供试品的点样量较少时,供试品色谱与栀子对照药材色谱在相同位置上有一个草绿色斑点,但供试品色谱与栀子苷对照品色谱在相应的位置上无斑点;供试品点样量增加后,草绿色斑点消失,栀子苷对应的斑点显现,这可能是因为清瘟败毒散中栀子苷含量低,随着点样量的增加,栀子苷对应的斑点显现出来,草绿色斑点却被其他成分的斑点覆盖。
清瘟败毒散作为中兽药大复方制剂,组成成分复杂,本试验曾对清瘟败毒散组方中的牡丹皮、玄参、桔梗等进行薄层定性鉴别,都因阴性干扰严重,专属不强等原因无法建立其鉴别方法。
黄有霖等[5]研究表明黄连鉴别的展开剂正丁醇-冰醋酸-水(7∶1∶2),发现亮黄色斑点相互重叠,分离度不好;曾试验2015版《中国药典》一部连翘项下薄层鉴别的展开剂三氯甲烷-甲醇(8∶1),发现展开速度太慢,展开效果不理想;照2015版《中国药典》一部项下栀子苷的含量测定方法,也不能直接用于清瘟败毒散中栀子苷的含量测定。不能直接将已有法定标准或文献报道的单味药材鉴别与含量测定方法,照搬作为中药复方中药材的鉴别方法。复方中药的的成分更加复杂,成分之间的相互干扰更加严重。
清瘟败毒散现有法定标准虽有性状及显微鉴别,但缺乏专属性;仅有黄连的薄层鉴别,但处方中有14味药材,远远不能控制产品质量;缺乏定量指标,不符合现代复方中药的质量控制模式。本研究有利于提升清瘟败毒散的质量标准。
4 结 论
本试验采用薄层色谱鉴别清瘟败毒散中的黄连、地黄、栀子、连翘、知母、淡竹叶;采用HPLC法测定清瘟败毒散中的栀子苷含量。薄层色谱鉴别中,在与对照药材色谱相对应的位置上,供试品色谱显示相同颜色的斑点,且阴性样品无干扰;栀子苷在0.062~0.370μg范围内具有良好的线性关系,其回归方程为y=1789.1x-14.296,R2=0.99984,平均回收率为99.60%,RSD为0.76%。本方法简单、准确、重复性好,能更好地控制清瘟败毒散的质量,可作为清瘟败毒散的质量标准。
参考文献:
[1] 付建忠.余霜生平及其《疫疹一得》考[J].安徽中医药大学学报,2014,33(4):13-15.
[2] 刘桐序.小议清瘟败毒饮[J].现代中医临床,2015,22(2):50-53.
[3] 王文远,杨 进.余师愚《疫疹一得》治疫思想探析[J].老林中医药,2011,31(6):449-501.
[4] 国家兽药典委员会.中华人民共和国兽药典(二部)[M].北京:中国农业出版社,2010.
[5] 黄有霖,潘 馨.成方中黄连、黄柏的薄层鉴别的研究[J].海峡药学,2003,15(2):36-37.
[6] 李正国,孙兆伟,刘琳琳.栀子金银花丸中黄连、黄柏的薄层鉴别方法研究[J].中国药事,2010,24(11):1122-1123.
[7] 李铁刚,李钰婷,武小赟,等.黄连及其炮制品薄层鉴别方法的研究[J].时珍国医国药,2011,22(3):677-679.
[8] 张 涛,马园园,王小英,等.清热解毒软胶囊地黄、麦冬博层色谱鉴别[J].亚太传统医药,2014,10(18):12-13.
[9] 刘 瑛,徐银伍.地黄及其炮制品薄层鉴别方法的改进[J].时珍国医国药,2005,16(8):765.
[10] 邓如伟,冉 兰,李 颖,等.杞菊地黄颗粒中六味药材的薄层色谱鉴别[J].华西药学杂志,2005,20(3):266-267.
[11] 国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015.
[12] 苏云艳,宁东兴.四季三黄片中栀子薄层鉴别研究[J].亚太传统医药,2015,11(7):38-39.
[13] 张学兰,徐 萍,李慧芬.焦栀子的薄层鉴别与有效成分含量控制方法研究[J].辽宁中医杂志,2011,38(2):335-337.
[14] 张秋玲,黄志豪,伍柏坚,等.消炎解毒丸质量标准的研究[J].广东药学院学报,2014,30(5):599-603.
[15] 梁朝锋,韩晓珂,祁 俊.芩玄清咽胶囊的质量标准研究[J].现代中药研究与实践,2014,28(6):68-70.
[16] 周 欢,王小平,白吉庆.连翘薄层鉴别方法的改进[J].中国现代医药,2015,17(4):338-340.
[17] 宋秋烨.淡竹叶生药学研究[D].南京:南京中医药大学,2007.
[18] 马宏达,崔英宇,何 静,等.小儿退热镇惊口服液的质量标准研究[J].解放军药学学报,2015,31(3):228-234.
[19] 唐靖雯,潘 梅.抗病毒咀嚼片的质量标准研究[J].中国药房,2015,26(24):3420-3422.
(责任编辑 秦 彤)
中图分类号:S854.5
文献标识码:A
文章编号:1671-7236(2016)12-3170-07
doi:10.16431/j.cnki.1671-7236.2016.12.013
收稿日期:2016-03-10
基金项目:四川省千人计划支持项目(川特聘第332号)
作者简介:潘春晖(1974-),男,四川达州人,学士,高级兽医师,主要从事兽药研究开发,E-mail:892086915@qq.com
通信作者:*刘 涛(1976-),男,四川南充人,博士,研究员级高级工程师,主要从事中药新药研究及成药质量再评价研究工作,E-mail:liutao0578@sina.com
Research on the Promotion of Qingwenbaidu Powder Quality Standard
PAN Chun-hui1,YANG Hong-yu1,ZHANG Xuan1,2,REN Yuan-qin2,PENG Xiao-feng2,LIU Tao1,2*
(1.SichuanDechengAnimalHealthProductsCo.,Ltd.,Deyang618100,China;2.PharmaceuticalandBiologicalEngineeringCollege,ChengduUniversity,Chengdu610106,China)
Abstract:To improve the quality standard of Qingwenbaidu powder,TLC was used to qualitative identity ofCoptis,RadixRehmanniae,Gardenia,Forsythia,RhizomaAnemarrhenaandLophatherumgracileBrongn in Qingwenbaidu powder.The content of gardenin was determined by HPLC.Stationary phase were performed on ODS C18column(4.6mm ID×250mm,5μm)and the mobile phase was acetonitrile and water(13∶87),the detection wavelength was 238nm.The results showed that in the relative position of the chromatography of the control medicinal material,the chromatogram of the test sample showed the same color spots,and the negative sample had no interference.There was a good linear relationship(R2=0.9999)when the garden in range of 0.062to 0.370μg.Its regression equation was y=1 789.1x-14.296and R2=0.99984.The average recovery was 99.60%and RSD was 0.76%.This method was simple,accurate and reproducible,which could better control the quality of the Qingwenbaidu powder,and could be used as the quality standard of Qingwenbaidu powder.
Key words:Qingwenbaidu powder;quality standard;TLC;determination

