HPLC-PDA联合UPLC-Q/TOF法确证硫酸卡那霉素注射液中的非法添加物
董玲玲,曹莹, 于晓辉,王静文,万仁玲,顾进华*
(1中国兽医药品监察所 北京 100081;2 上海市兽药饲料检测所 上海 201103 )
HPLC-PDA联合UPLC-Q/TOF法确证硫酸卡那霉素注射液中的非法添加物
董玲玲1,曹莹2, 于晓辉1,王静文1,万仁玲1,顾进华1*
(1中国兽医药品监察所 北京 100081;2 上海市兽药饲料检测所 上海 201103 )
确证1批硫酸卡那霉素注射液中的非法添加物。在对该批样品进行非法添加物常规筛查时发现其含有未知色谱峰,且紫外光谱具有特征性,但与现有的紫外光谱库进行比对,无法确定该未知物的结构。结合UPLC-Q-TOF法给出的未知物的分子量信息推导出疑似添加物,再用HPLC-PDA和UPLC-Q/TOF两种方法进行验证,最终确证非法添加物。结果显示该批样品中的非法添加物为尼可刹米。通过检查该批样品中的非法添加物,总结出确证非法添加物的一般模式,从而为兽药处方外非法添加物的筛查与确证提供思路。
尼可刹米;非法添加
随着国家对农产品质量安全的日益重视,农业部对兽药处方外非法添加的监管与打击力度也不断加大,近年来发布了大量公告作为兽药处方外非法添加物检查的检验依据,比较常见的是采用HPLC-PDA法,也有UPLC-MS方法[1-3]。但判断兽药制剂中是否存在非法添加,添加了何种药物,一直以来都是工作中的难点。目前,本团队已建立了非法添加的常见化学药物紫外光谱数据库,能够提供紫外光谱图与保留时间等信息,是兽药处方外非法添加物常规筛查的重要依据,但其存在一定的局限性,对于未收入光谱库的化合物会有漏查的风险。UPLC-Q-TOF MS法能提供精确分子量,在化合物确证方面应用广泛[4-5],但由于其昂贵的成本,较高的技术壁垒,再加上二级质谱数据庞大的信息量和易受分子量较小的化合物干扰的特点,该方法目前在兽药处方外非法添加物的筛查领域应用尚处于初级探索阶段。本团队建立了部分化学药物的一级质谱数据库,用于非法添加物的初筛。近日,在1批监督抽检样品硫酸卡那霉素注射液中的处方外非法添加物检查中,发现添加物,通过一级质谱库筛查,并结合紫外光谱特征,最终锁定疑似添加物,再用HPLC-PDA法联合UPLC-Q-TOF MS法进行双重确证。通过检查该批样品中的非法添加物,总结出确证非法添加物的一般模式,以期为兽药处方外非法添加物的筛查与确证开辟出新的思路。
1 仪器与试药
高效液相色谱仪(Waters e2695-2996),配二极管阵列检测器(PDA);超高效液相色谱仪(Waters ACQUITY UPLC)-四极杆/飞行时间质谱仪(Q/TOF MS,Waters Synapt HDMS);XS205分析天平(Mettler Toledo);资生堂®C18 4.6 mm×250 mm,5 μm;ACQUITY HSS T3色谱柱(1.7 μm,100 mm×2.1 mm)。甲醇为色谱纯,购自Merck公司。尼可刹米,购自ACROS公司,纯度99.9%,批号:A0344236。硫酸卡那霉素注射液为2016年度监督抽检样品,批号20140101。
2 方法
2.1 溶液的制备
2.1.1 供试品溶液 取供试品1.0 mL,置100 mL量瓶中,加水稀释至刻度,摇匀;取1.0 mL,置10 mL量瓶中,加流动相稀释至刻度,摇匀,即得UPLC-PDA初筛用供试品溶液;用乙腈-0.1%甲酸(10∶90)将上述溶液稀释10倍,作为UPLC-Q/TOF MS初筛用供试品溶液;未知物HPLC-PDA验证用供试品溶液同初筛,未知物UPLC-Q/TOF MS验证用供试品溶液同UPLC-Q/TOF MS初筛。
2.1.2 对照品溶液 取尼可刹米对照品,加流动相使溶解并稀释制成5 μg/mL的溶液,作为HPLC-PDA验证用对照品溶液;用乙腈-0.1%甲酸(10∶90)将上述溶液稀释成50 ng/mL的溶液,作为UPLC-Q/TOF MS验证用对照品溶液。
2.2 试验条件
2.2.1 硫酸卡那霉素注射液 HPLC-PDA初筛:采用ACQUITY HSS T3色谱柱(1.7 μm,100 mm×2.1 mm)色谱柱,以甲醇(含0.01 mol/L醋酸铵)-0.01 mol/L醋酸铵为流动相,梯度洗脱(0~0.25 min,保持2%A;0.25~12.25 min,由2%A线性变化为99%A;12.25~13.0 min,由99%A线性变化为2%A,13.0~17.0 min,保持2%A),流速0.25 mL/min。UPLC-PDA初筛采集波长范围为210~400 nm。
2.2.2 硫酸卡那霉素注射液 UPLC-Q/TOF MS初筛:采用ACQUITY HSS T3(1.7 μm,100 mm×2.1 mm)色谱柱,流动相A为含0.1%甲酸的乙腈,B为0.1%甲酸,梯度洗脱(0~5 min,由20%A线性变化为95%A;5.0~6.0 min,由95%A线性变化为20%A);流速0.45 mL/min;Q/TOF MS采用电喷雾正离子源(ESI+),毛细管电压3.0 kV,电离源温度110 ℃,锥孔电压为35 V,数据采集质量范围为50~1000 Da,二级质谱(MS/MS)碰撞电压为25 eV;采用甲酸钠溶液进行精确质量校正,并用亮氨酸-脑啡肽溶液([M+H]+,m/z556.2 Da)进行实时质量锁定。2.2.3 非法添加物HPLC-PDA验证 采用资生堂C18( 4.6 mm×250 mm,5 μm)色谱柱。以水- 甲醇(70∶30)为流动相;流速1.0 mL/min。采集波长范围为200~400 nm;记录263 nm波长处的色谱图。
2.2.4 非法添加物UPLC-Q/TOF MS验证 色谱柱及流动相同2.2.2项,流动相A:流动相B(20:80);流速0.4 mL/min;Q/TOF MS参数同初筛,数据采集质量范围为50~800 Da。
3 结果与分析
3.1 非法添加物的发现和初步分析 在非法添加物常规筛查中发现有1批硫酸卡那霉素注射液有一未知色谱峰(tR=6.7 min)见图1,且紫外光谱具有特征性,最大吸收波长为264.0 nm(图2)。将该光谱图与已建立的非法添加物光谱图库进行比对,没有查到疑似添加物。
遂对该批供试品进行UPLC-Q/TOF MS初筛,采用电喷雾正离子源模式(ESI+),全扫描范围(100~1000 Da),采集得到供试品的一级质谱(MS)信息;在TIC图(图3)中,除卡那霉素峰(tR=0.41 min)外,还发现了另一明显的色谱峰(tR=1.73 min)。从质谱图(图4)中看出强度最高的m/z值为179.11 Da,将该值在已建立的一级质谱数据库中进行查找,查到疑似添加物6种,具体信息见表1。
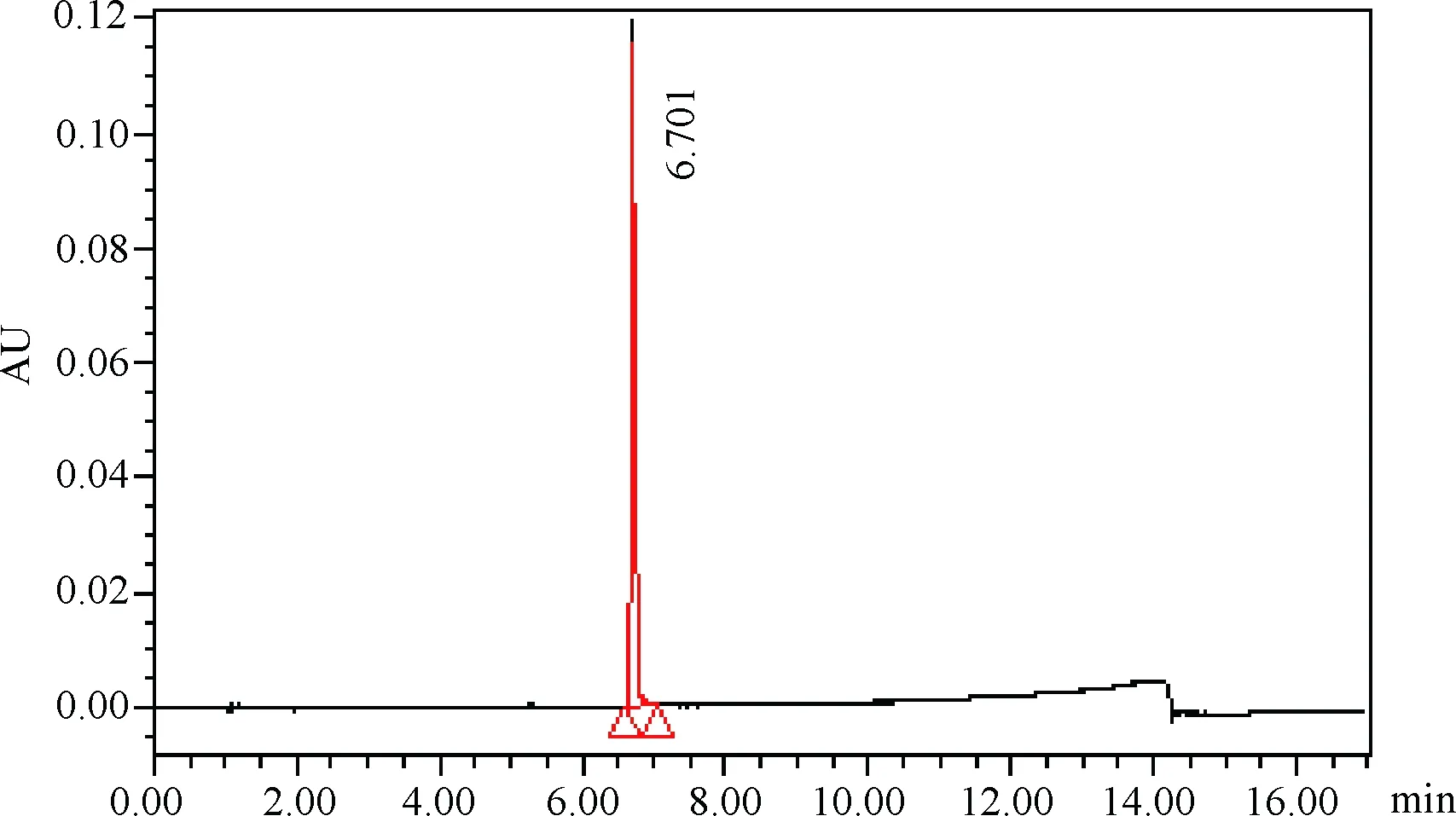
图1 供试品色谱图

图2 未知峰紫外光谱图

图3 供试品总离子流图

图4 供试品质谱图

编号化合物分子式峰类型m/z/Da紫外光谱吸收波长/nm∗类别∗1无水葡萄糖C6H12O6[M-H]-179.0556无营养药2阿司匹林C9H8O4[M-H]-179.0344276解热镇痛、非甾体抗炎药3氨茶碱C7H8N4O2[M-H]-179.0569275平滑肌松弛药;利尿药4茶碱C7H8N4O2[M-H]-179.0569271平滑肌松弛药5丙硫异烟胺C9H12N2S[M-H]-179.0643291抗结核病药6尼可刹米C10H14N2O[M+H]+179.1184263中枢兴奋药
*参见《中华人民共和国药典》2015年版二部
UPLC-Q/TOF MS初筛时所用流动相含有0.1%甲酸,更易形成 [M+H]+峰,且未知峰的紫外光谱图中最大吸收波长为264 nm,考虑到以上两点,怀疑添加物为尼可刹米。尼可刹米结构式见图5,为酰胺类化合物,易发生酰胺键的断裂,丢失N,N-二乙基碎片,形成二级碎片(C6H6NO+),m/z108,进一步佐证了猜想。继而对添加物利用HPLC-PDA法和UPLC-Q/TOF MS法进行验证。
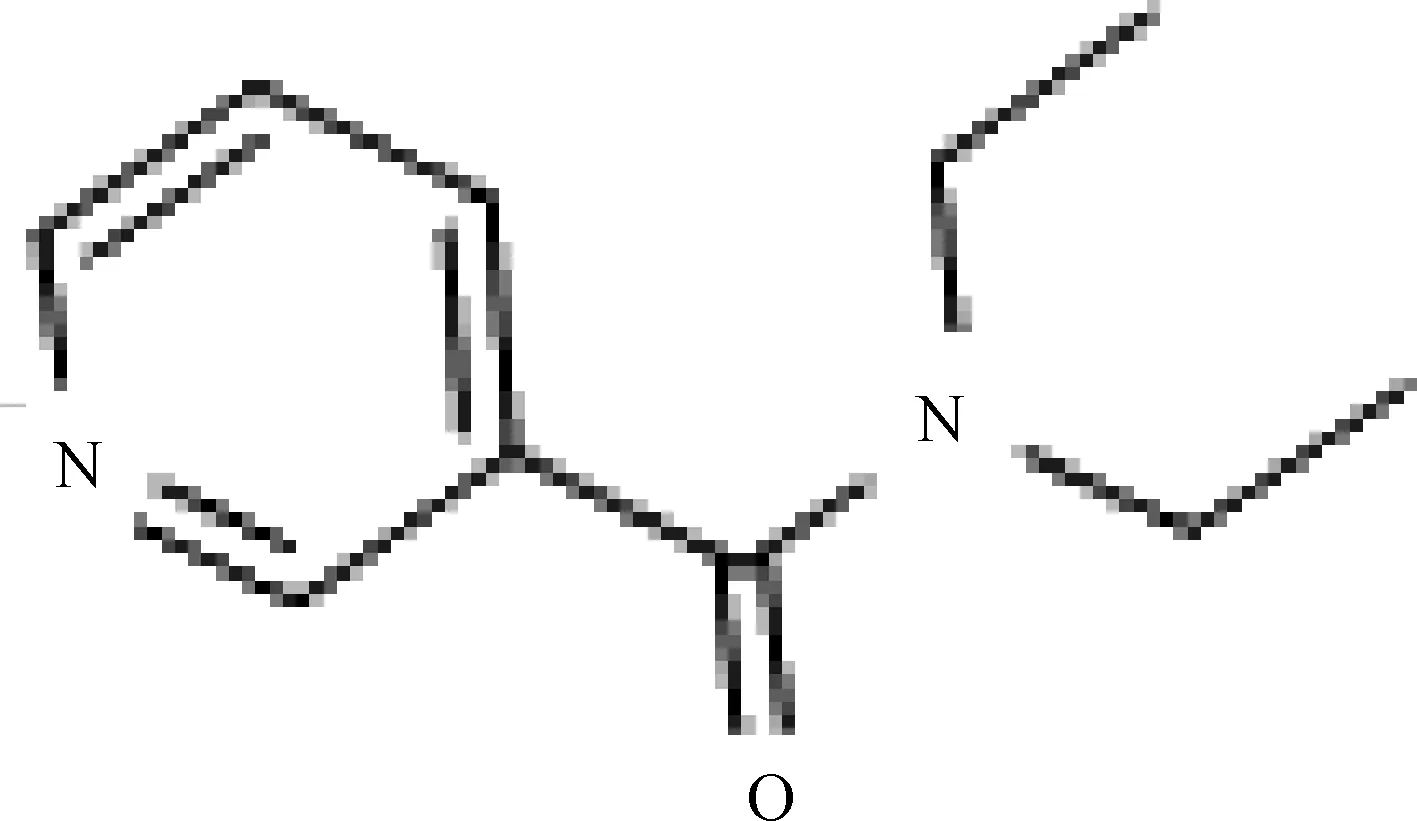
图5 尼可刹米结构式
3.2 添加物验证3.2.1 HPLC-PDA 与对照品保留时间及紫
外光谱进行比对,以及不同浓度本底添加试验峰纯度检查和光谱相似度检查的方式对供试品中的未知物进行验证。供试品在该试验条件下检出1个未知色谱峰,其与该条件下尼可刹米对照品的保留时间一致,紫外光谱相似;同时,不同浓度(取对照品溶液与供试品溶液按1∶4、1∶1、4∶1 的比例混合)的本底添加试验峰纯度检查结果显示:添加前后,供试品色谱图相应位置上色谱峰的纯度角度小于纯度阈值,为单一物质峰;光谱相似度检查结果显示:添加前后,供试品色谱图相应位置上色谱峰的光谱匹配角度小于匹配阈值,与对照品的光谱相似。保留时间、紫外光谱验证结果及峰纯度检查、光谱相似度检查结果见表2、表3。

表2 保留时间、紫外光谱验证结果表

表3 峰纯度检查与光谱相似度检查结果表
3.2.2 UPLC-Q/TOF MS 采用UPLC-Q/TOF MS 验证试验条件,提取供试品与对照品在[M+H]+m/z179.01 Da的质谱图,采取与对照品保留时间、准分子离子峰及碎片峰比对的方式对供试品中的非法添加物进行进一步验证。在相同试验条件下,添加物的保留时间、准分子离子峰及碎片离子峰与尼可刹米对照品完全一致,进一步证明添加物为尼可刹米。结果见表4。
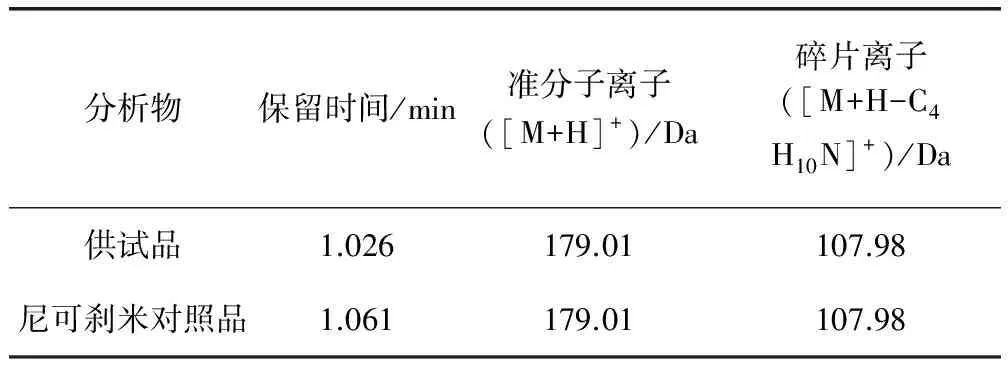
表4 UPLC-Q-TOF MS法验证结果
4 讨论
4.1 确证非法添加物的一般模式 此次非法添加物的检查过程中将UPLC-Q-TOF法和HPLC-PDA法结合起来,相互佐证,最大限度的提供非法添加物的信息,为非法添加物的确证提供了双重保险。据此次尼可刹米的发现与确证过程,总结出兽药非法添加物确证的一般模式:若供试品中发现添加物,采用HPLC-PDA法进行初筛,将所得添加物的紫外光谱图与已建立的数据库进行匹配,若匹配成功,找到疑似添加物,用HPLC-PDA法对添加物进行确证;若匹配不成功,用UPLC-Q-TOF法采集添加物质谱信息,分析准分子离子峰并与已建立的一级质谱数据库进行匹配,同时根据所给出的质谱信息推导结构特征,找到疑似添加物,再建立UPLC-Q-TOF法或HPLC-PDA法对添加物进行确证。
4.2 非法添加物筛查的合理性分析 在非法添加物筛查时不仅要依靠技术手段,也要讲究“合情合理”。尼可刹米在兽医临床中用于解救呼吸中枢抑制,用于各种原因引起的呼吸中枢抑制,如中枢抑制药中毒,疾病引起的中枢性呼吸抑制,新生仔畜窒息或加速麻醉动物的苏醒等。硫酸卡那霉素为氨基糖苷类广谱抗菌药,临床上用于治疗败血症及泌尿道、呼吸道感染,也用于猪气喘病[6]。从两者的临床应用可以看出,在硫酸卡那霉素注射液中添加尼可刹米,是为了在治疗呼吸道感染、气喘病的同时兴奋呼吸中枢,达到增强疗效的目的;再者,尼可刹米合成简单,价格低廉,这符合不良商家的利益诉求,因此存在添加的可能性。一切非法添加都不是盲目的,对目的性的分析看似不相干,实际很重要,这在确证非法添加物的时候可以帮助排除因之前检测样品的残留而造成“假阳性”的结果。对非法添加物的筛查既要符合技术层面的推理也要符合逻辑规律。
5 展望
目前,兽药制剂中非法添加物的筛查主要基于紫外光谱数据库和质谱数据库,库容量的大小直接影响到能否成功锁定疑似添加物,若添加物信息未被收入数据库中,则需要进一步借助质谱或核磁共振等波谱解析手段推导添加物的结构,这将极大的增加筛查的难度。因此,笔者认为应该不断扩充两个数据库,增加库容量;同时,筛查目标不能仅囿于药物,应将防腐剂、增溶剂、稳定剂等常用添加剂的信息也扩充到数据库里,避免假阳性结果。
[1] 中华人民共和国农业部公告第1848 号.黄芪多糖注射液中非法添加解热镇痛类、抗病毒类、抗生素类、喹诺酮类等11 种化学药物(物质)检查方法和肥猪散、健胃散、银翘散等中兽药散剂中非法添加氟喹诺酮类化学药物(物质)检查方法[S].
[2] 中华人民共和国农业部公告第2508号. 注射用青霉素钾(钠)中非法添加解热镇痛药物检查方法等11 个兽药非法添加化学药物(物质)检查方法[S].
[3] 中华人民共和国农业部公告第2320号. 鱼腥草注射液中非法添加林可霉素检查方法、鱼腥草注射液中非法添加水杨酸氧氟沙星检查方法和中药散剂中非法添加金刚烷胺和金刚乙胺检查方法等3项检查方法标准[S].
[4] Ren Q, Wang Y L, Wang M L,etal. Screening and identification of the metabolites in rat urine and feces after oral administration of Lycopus lucidus Turcz extract by UHPLC-Q-TOF-MS mass spectrometry [J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2016,1027 (8):64-73.
[5] 蓝芳,张毅,岳振峰,等.液相色谱-四极杆/飞行时间质谱快速筛查饲料中36种违禁药物[J].分析测试学报,2012,31(12):1471-1478.
[6] 中国兽药典委员会.兽药使用指南化学药品卷[M]. 北京: 中国农业出版社,2010: 31.
(编辑:侯向辉)
Identification of Compound Illegally Adulterated in One Batch of Kanamycin Sulfate Injection by UPLC-Q/TOF MS and HPLC-PDA Method
DONG Ling-ling1, CAO Ying2, YU Xiao-hui1, WANG Jin-wen1, WAN Ren-ling1, GU Jin-hua1*
(1.ChinaInstituteofVeterinaryDrugControl,Beijing100081,China; 2.ShanghaiMunicipalVeterinaryDrugsandFeedstuffControlInstitute,Shanghai201103,China)
To identify the unknown adulterated compound in one batch of kanamycin sulfate injection in the common screening course,an unknown compound was observed with characteristic UV spectra, and couldn’t confirm its structure.The target compound was deduced with the information provided by UPLC-Q/TOF MS and HPLC-PDA,and finally validated by the two methods above.Results showed that the unknown adulterated compound in this sample was identified as nikethamide.A model of the unknown compound identification was generalized through the progress of deduction and validation described above,which provided a reference for the future inspection of adulteration in veterinary drugs.
nikethamide; illegal drug adulteration
“十二五”科技支撑计划(2015BAD11B03-4)
董玲玲,硕士研究生,从事兽医药品检验工作。
顾进华。E-mail:gujinhua@ivdc.org.cn
2016-06-12
A
1002-1280 (2016) 08-0015-05
S859.83

