右旋糖酐40氯化钠注射液沉淀物形成的影响因素及控制措施
·工业药学·
右旋糖酐40氯化钠注射液沉淀物形成的影响因素及控制措施
许文东1,2,张雪梅2,秦文明2
(1.山东大学,山东 济南 250014;2.山东齐都药业有限公司,山东 淄博 255400)
摘要:目的分析右旋糖酐40氯化钠注射液沉淀物的来源,查找影响因素,并提出控制措施。方法通过分析产品中沉淀物的性质及其产生的因素,并结合试验及生产经验,确定控制措施。结果右旋糖酐40氯化钠注射液沉淀物为右旋糖酐40结晶析出;产品的原料药质量、运输和储存条件对右旋糖酐40氯化钠注射液沉淀物产生有直接的关系。结论通过提高原料质量及保证运输和储存条件等可减少析出结晶,并修订药品说明书明确结晶的处理方式。
关键词:右旋糖酐40氯化钠注射液;析出;结晶;因素;控制措施
作者简介:许文东,男,工程师,研究方向:制药工程,E-mail:853120365@qq.com
中图分类号:R927.11文献标识码:A
The factors affecting and control measures of Dextran 40 Sodium Chloride Injection precipitate
XUWen-dong1,2,ZHANGXue-mei2,QINWen-ming2
(1.ShandongUniversity,Jinan250014,China;2.ShandongQiduPharmaceutical
Co.,Ltd.,Zibo255400,China)
Abstract:ObjectiveTo analyze the precipitate source of Dextran 40 Sodium Chloride Injection and find the factors affecting,propose control measures.MethodsBy analyzing the factors in the nature of the product precipitate,and combined test,production experience,to determine the control measures.ResultsDextran 40 Sodium Chloride Injection precipitate was crystallized dextran 40;API product quality,transport and storage conditions on the Dextran 40 Sodium Chloride Injection precipitate had a direct relationship.ConclusionBy improving the quality of API and to ensure that transport and storage conditions can reduce precipitation crystallization,and revise the package insert to identify the approach of crystal clear.
Key words:Dextran 40 Sodium Chloride Injection;Precipitation;Crystallization;Factors;Control measures
右旋糖酐40氯化钠注射液在临床上使用广泛,适应于各种原因引起的休克、血栓性疾病、肢体再生和血管外科手术等[1]。该产品主要原料右旋糖酐40是蔗糖经肠膜状明串珠菌LM-1226发酵后生成的高分子葡萄糖聚合物,平均相对分子质量为4 000[2]。右旋糖酐40氯化钠注射液在生产和贮存过程中个别产品会出现乳白色片状沉淀物,造成产品可见异物检查不合格,影响临床使用,同时会使医务人员和患者对药品质量产生疑惑。因此,研究分析右旋糖酐40氯化钠注射液中沉淀物的来源及影响因素,并提出控制措施是十分有必要的。我们通过对沉淀物进行分析确定了沉淀物就是右旋糖酐40结晶析出,提高原料药的质量及确保运输和储存条件等可减少析出结晶,提高产品质量。
1仪器与试药
SPD-20A型高效液相色谱仪(日本岛津公司);IRPrestige-21红外分光光度计(日本岛津公司);右旋糖酐40(山东金洋药业有限公司,批号:140640);氯化钠(中盐宏博集团云梦云虹制药有限公司,批号:20140429)。
2方法与结果
2.1右旋糖酐40氯化钠注射液中沉淀物鉴别实验取数瓶存在沉淀物的右旋糖酐40氯化钠注射液,使用微孔滤膜进行过滤,将过滤后的沉淀物物使用注射用水冲洗3遍,然后烘干,对烘干样品进行红外鉴别,同时取右旋糖酐40原料进行对比试验,红外光谱见图1和图2。
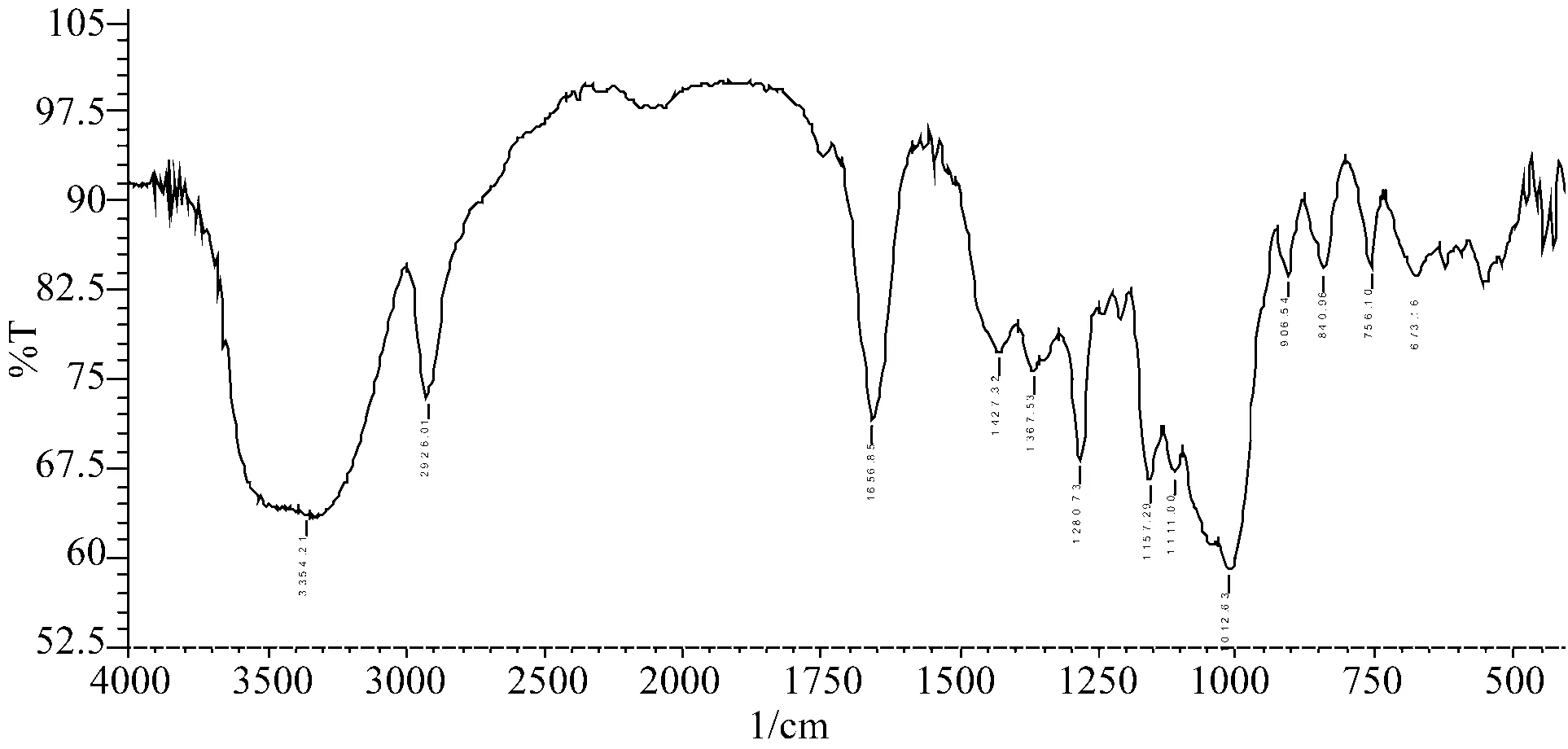
图1 右旋糖酐40氯化钠注射液中沉淀物的红外色谱图
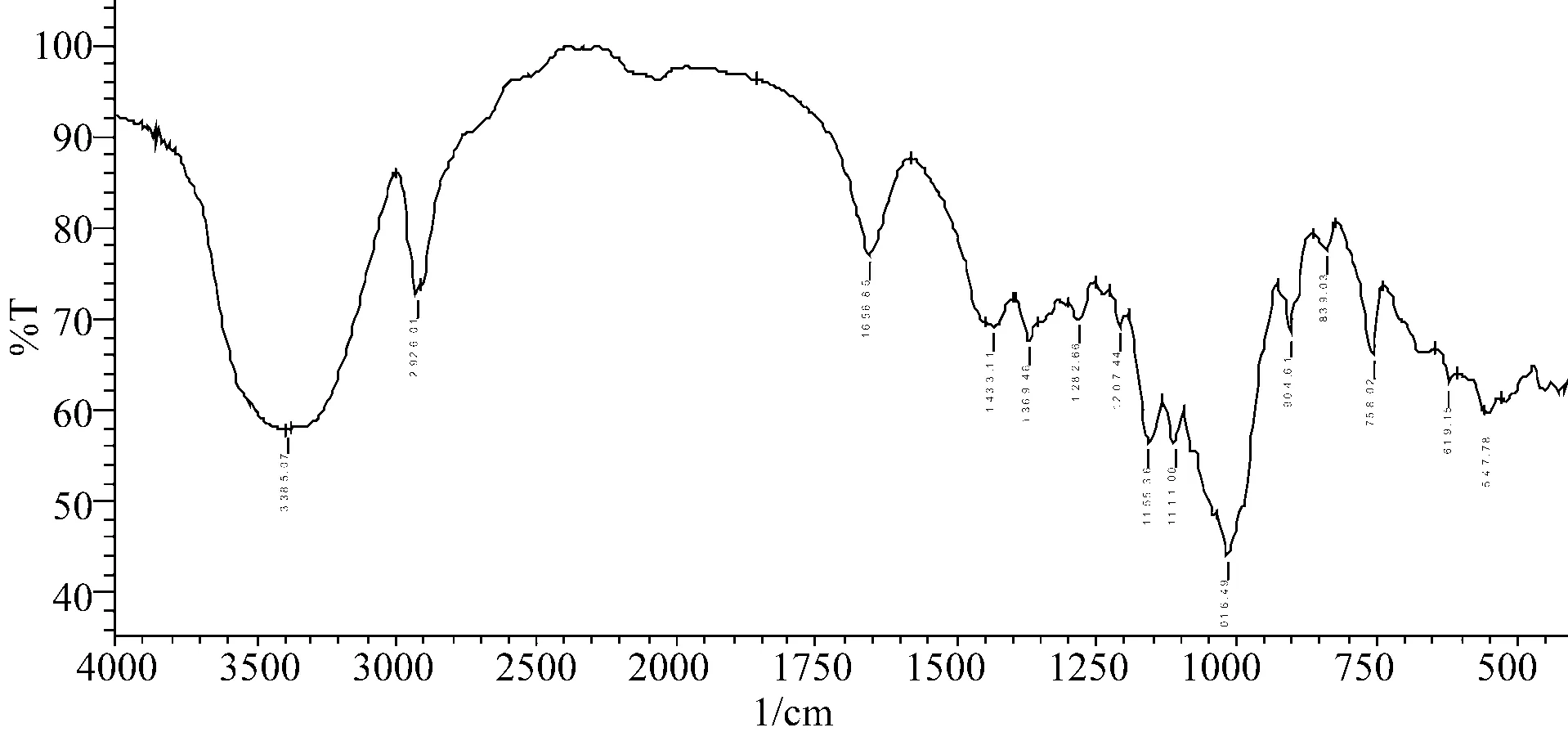
图2 右旋糖酐40原料药的红外色谱图
结果分析:右旋糖酐40氯化钠注射液中沉淀物与右旋糖酐40原料药红外色谱特征峰基本一致,试验证明沉淀物即为右旋糖酐40,与国内、国外相关研究结论一致。结晶析出产生的主要原因是分子间氢键的作用。右旋糖酐40分子中含有较多的羟基,右旋糖酐40分子之间、右旋糖酐40分子与水分子之间,都有强烈的亲和力,如果右旋糖酐分子之间的亲和力大于右旋糖酐40分子与水分子之间的亲和力,右旋糖酐40就以氢键的方式结合,形成沉淀物[3]。
2.2影响右旋糖酐40氯化钠注射液沉淀物产生的试验有关文献报道[4],右旋糖酐40氯化钠注射液的储存温度对结晶析出有影响。《中国药典》2010年版储存条件规定:储存条件应为25 ℃以下[5]。我们各取20瓶产品选择4种条件进行试验。条件一:夏季将样品放置在室外,经昼夜温度变化(最高39 ℃,最低17 ℃)60 d;条件二:将样品放置在阴凉库内(温度低于20 ℃);条件三:将样品放置在烘箱中40 ℃ 60 d;条件四:进行冻融试验(-10 ℃冷冻12 h,45 ℃放置12 h)。对以上个条件进行观察,具体结果见表1。
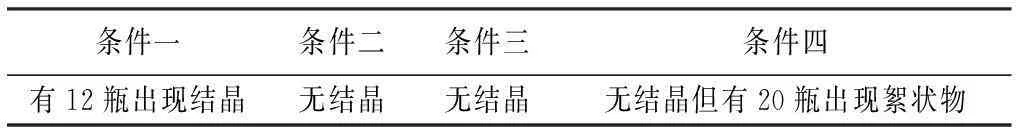
表1 右旋糖酐40氯化钠注射液储存实验结果
从以上试验结果可以看出:试验条件一产品中有结晶析出,试验条件四产品中有絮状物产生,以上两个条件均是温度变化较大的条件。右旋糖酐40氯化钠注射液在温度变化较大的环境中不稳定,产品在夏季昼夜温差大时易结晶析出,同时通过冻融试验发现该产品冻融后可见异物不合格。该产品的储存条件应为25 ℃以下且温差不得波动过大。储存条件是影响右旋糖酐40氯化钠注射液结晶析出的一个因素。
2.3右旋糖酐40原料对结晶的影响乙醇沉淀法是工业上对右旋糖酐进行分级精制的传统方法,但所得产品分子量分布很宽[6],通过与原料供应商沟通,他们采用同样的精制方法。为确定原料分子量分布对沉淀物的影响选择使用3批分子量分布不同的原料生产产品进行对比试验,夏季分别将右旋糖酐40样品放置在室外,经昼夜温度变化60 d,试验结果见表2。
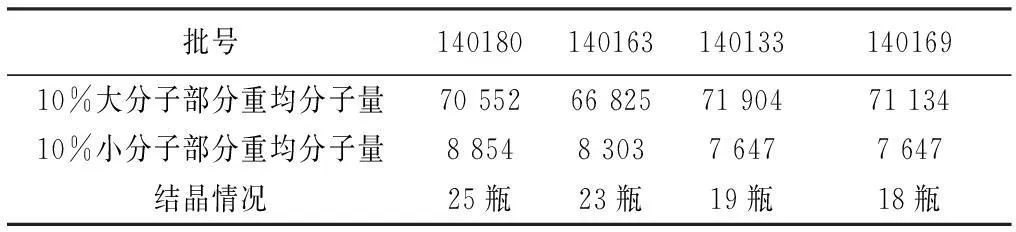
表2 右旋糖酐40氯化钠注射液分子量分布试验实验结果
结果分析,右旋糖酐40分子量的分布对结晶析出有一定影响,10%小分子部分重均分子量高的结晶析出小。右旋糖酐40分子量的分布范围应严格控制[7],分子量的分布是影响右旋糖酐40氯化钠注射液结晶析出的一个因素。
2.4右旋糖酐40氯化钠注射液结晶溶解试验通过试验发现产品析出的结晶再次溶解困难,需水浴煮沸30 min方可溶解,或在121 ℃ 8 min灭菌的条件下也可溶解,溶解后药液回复澄清。取溶解后药液进行检测,发现结晶复溶后的注射液所有指标均与结晶前一致。
3讨论
3.1右旋糖酐40氯化钠注射液中沉淀物为结晶析出,为了方便临床的使用,建议将该产品的结晶析出现象在药品说明书中加以标注,并对复溶的方法条件加以说明。
3.2右旋糖酐40氯化钠注射液结晶析出受温度波动影响大,建议产品在运输及储存过程中严格控制温度,减少波动,同时防止产品结冻。
3.3右旋糖酐40是经发酵后生成的高分子葡萄糖聚合物[8],发酵的温度及精制处理所得分子量分布的情况均影响产品的质量。故实际生产过程中一定要关注原料药的质量。
参考文献:
[1]王发,王嫦鹤,张秉华,等.HPLC法检查右旋糖酐40氯化钠注射液中5-羟甲基糠醛的限量[J].西北药学杂志,2011,26(6):410-411.
[2]杨贤,葛卫红.右旋糖酐40氯化钠注射液致过敏性休克1例[J].临床荟萃,2013,28(12):1404.
[3]薛忠良.右旋糖酐注射液的结晶沉淀物问题探讨[J].中国药业,2000,9(9):37.
[4]雷琨.右旋糖酐40注射液质量与安全相关性的研究[D].西安:陕西中医学院,2013.
[5]国家药典委员会.中国人民共和国药典2010年版(二部)[S].北京:中国医药科技出版社,2010:921.
[6]陈山,郭祀远,杨晓泉.采用分级超滤法精制右旋糖酐[J].食品与发酵工业,2004,30(6):42-45.
[7]冯燕,李洁.影响右旋糖酐40氯化钠注射液质量的主要因素及改进措施[J].齐鲁药事,2011,30(7):422-423.
[8]支兴蕾,李存玉,李红阳,等.右旋糖酐40中细菌内毒素超滤去除工艺[J].医药导报,2014,33(7):922-925.

