/ZrO2制备及其对双戊烯催化脱氢的影响
梁慧明,卢泽湘,沈权辉,郑梅琴,郑德勇,3
(1.福建农林大学材料工程学院;2.福建农林大学金山学院;3.福建农林大学茶叶科技与经济研究所,福建福州350002)
对伞花烃(1-甲基-4-异丙基苯)是一种重要的有机合成中间体,可用来合成多种多环麝香型香料、药物、除草剂和杀菌剂等[1].目前对伞花烃多以甲苯为原料,采用气相法或液相法合成,但存在产物选择性较差、副产物分离困难的缺点[2].国内外开展了以蒎烯为原料合成对伞花烃的研究,但产物收率普遍较低[3-6].双戊烯,学名1-甲基(1-甲基乙烯基)环己烯,是松节油合成松油醇和樟脑等的副产物,可经过脱氢芳环化后生成对伞花烃[7-9].二氧化硅负载 Pd/C[10]、二氧化硅负载 Pd[11]、海泡石分别负载 Ni、Fe、Mn[12]、二氧化硅与氧化铝的混合物[13]等催化剂对双戊烯均具有较好的催化脱氢作用,但这些催化剂主要应用于气相反应,对设备的要求较高.固体酸催化剂对烷烃的酯化、异构化、烯烃异构、芳香化合物烷基化等反应具有很高的催化活性,具有可重复使用、污染小和腐蚀性小等优点,是一种环境友好型催化剂.本文制备了/ZrO2固体酸的催化剂,并表征其主要结构特性,将其应用于双戊烯液相催化制备对伞花烃,考察了催化剂制备、反应条件对其催化性能的影响.
1 材料与方法
1.1 主要试剂与原料
双戊烯(≥95%)由上海晶纯实业有限公司提供;乙腈(≥99.9%)由德国默克集团有限公司提供;ZrOCl2·8H2O、硫酸、正丁胺、氨水与硝酸银均为AR级试剂,由上海国药集团提供.
将60 mL 0.25 mol·L-1ZrOCl2水溶液注入250 mL三口烧瓶,在剧烈搅拌中缓慢滴加浓氨水至pH值为9.5,产生ZrO(OH)2·nH2O白色沉淀.室温静置12 h,抽滤,去离子水洗涤至滤液中无Cl-(用0.1 mol·L-1的AgNO3溶液检验),将沉淀物于105℃烘干12 h,研磨,过筛(100目).将15 mL H2SO4浸渍液加到1 g ZrO(OH)2粉末中,均匀混合,浸渍18 h,过滤除去多余浸渍液,滤渣于105℃烘干12 h.在马弗炉中焙烧3 h,干燥器中自然冷却,即获得白色固体粉末/ZrO2固体酸催化剂.
1.3 催化剂性能评价
向装有回流冷凝器、温度计的50 mL三口烧瓶中,加入一定量的原料和催化剂,通入N2保护,在一定的温度下搅拌反应,定时取样.样品经过滤后,采用美国安捷伦公司生产的7890A-5975C气质联用仪(GCMS)分析.HP-5MS 毛细管色谱柱规格:30 m×0.25 mm×0.25 μm.以氦气(99.999%)作为载气,流速 1 mL·min-1,进样量 0.1 μL,分流比 60 ∶1,汽化室温度 250 ℃.程序升温:起始温度为 60 ℃,以 5 ℃·min-1升温至90℃,保持2 min;以15℃·min-1升温至280℃,保持10 min.质谱条件:电离方式为EI,电子能量70 eV,离子源230℃,四极杆150℃,MS接口温度280℃.扫描范围为10-320 m·z-1,采用全扫描方式,溶剂延迟3 min.双戊烯的转化率和脱氢产物对伞花烃的选择性分别按式(1)、式(2)计算.

式中,MD1表示原料中双戊烯的相对质量分数;MD2表示反应产物中双戊烯的相对质量分数;MO表示反应产物中对伞花烃的相对质量分数.
1.4 测试与表征
采用日本Rigaku公司MiniFlex型X射线衍射仪测定样品的晶相结构,采用Cu靶射线,管电压30 kV,管电流 15 mA,扫描步长 0.02°,衍射范围 20°-70°(2θ),扫描速率 8°·min-1.采用美国 Thermo Scientific 公司生产的Nicolet380型傅里叶变换红外光谱仪表征样品红外吸收特征,KBr压片制样,扫描范围为400-4000 cm-1,步长4 cm-1.采用德国NETZSCH公司生产的STA499热分析仪来分析样品的热性质,载气O2(99.999%)流速为10 mL·min-1,升温范围25-800℃,升温速率为10℃·min-1.催化剂的酸量用正丁胺电位滴定法测定[14]:50 mg 催化剂加入到 50 mL 乙腈(纯度 99.9%)中,搅拌 3 h,然后用 0.05 mol·L-1正丁胺的乙腈溶液滴定,电位变化用Thermo Orion4 STAR型pH计测定.一般认为,初始电极电位值E表示酸强度,曲线达到拐点所对应的横坐标值表示催化剂酸性位总数.
2 结果与分析
2.1 XRD表征和FT-IR表征
对ZrO2固体粉末(600℃焙烧)与不同温度焙烧所得的/ZrO2固体酸的XRD谱图图1Ⅰ和红外谱图图1Ⅱ进行分析.
由图1Ⅰ中的f谱图可知,经600℃焙烧制备的ZrO2以单斜晶相衍射峰为主,分别在2θ=30°、50°和60°出现较弱的四方晶相衍射峰,说明其主要存在单斜晶相结构,含有少量四方晶相结构.由图1Ⅰ中的a谱图可知,经400℃焙烧制备的/ZrO2固体酸仅在2θ=30°附近出现一个较弱的ZrO2非晶衍射包,表明400℃焙烧的固体酸中的ZrO2为无定形态.比较图1Ⅰ中的a-e谱图可知,当焙烧温度由400℃上升到700℃时,2θ=30°、50°和60°处的四方晶相衍射峰越发尖锐,并出现小的单斜晶相衍射峰,说明随着焙烧温度的提高,ZrO2逐渐从无定形态向四方晶相转化,并向单斜晶相转化.焙烧温度为800℃时,在2θ=27.791°和31.118°处出现较强的单斜晶相衍射峰,ZrO2中四方晶相结构已大部分转变为单斜晶相结构,与纯的ZrO2的衍射峰(图1Ⅰ中的f谱图)类似.表明的引入抑制了ZrO2的四方晶相向单斜晶相的转变,提高了ZrO2的晶相转变温度.由于四方晶相的ZrO2为亚稳态,能与S=O键的电子云发生相互重叠,形成共价键结合,使得基团不易流失[15],而单斜晶相则为热稳定晶相,不易与结合.因此,四方晶相的ZrO2有助于形成/ZrO2固体超强酸结构.由图1Ⅰ中的f谱图可知,焙烧温度为700℃时,ZrO2在2θ=30°、50°和 60°四方晶相衍射峰最强,较易结合形成固体酸结构,说明此时制备的/ZrO2固体酸结构最稳定.

图1 不同焙烧温度的/ZrO2和ZrO2样品的表征Fig.1 The characterization of /ZrO2and ZrO2samples calcined at different temperatures
2.2 热重分析
对于不同温度焙烧制得的催化剂,采用热分析仪进行热分析,得到DTG曲线(图1Ⅲ和DSC曲线(图1Ⅳ).由图1Ⅲ可知,不同焙烧温度的/ZrO2固体酸均存在2个快速失重区,即拐点约为80℃的低温失重区和拐点约为650℃的高温失重区.25-200℃低温失重区主要是由催化剂表面的吸附水脱附所致.随着焙烧温度的提高,图1Ⅲ中80℃时失重峰强度逐渐减弱,图1Ⅳ中80℃的吸热峰强度也逐渐减弱,表明焙烧温度越高,催化剂表面越不易吸附水.650-800℃高温失重区主要是样品表面硫组分的脱附和ZrO2晶相转变所致.在图1Ⅳ的DSC曲线中出现了相应的宽放热峰强度在300℃左右且随着焙烧温度的提高逐渐减弱.比较纯ZrO2样品,在该处也有一个较强的放热峰,但放热的同时没有发现明显的质量变化,可知此放热峰是ZrO2的晶型转变所致[20].200-650℃则是一个相对恒重区,主要失去的是样品中少量键合的硫,说明样品/ZrO2在这个温度区间较稳定,这与XRD、IR分析结果相一致.
2.3 催化剂的酸性测定
图2是空气气氛焙烧的不同焙烧温度制备的催化剂和N2气氛焙烧的不同H2SO4浸渍液制备的催化剂的滴定曲线.由图2可以得到催化剂的酸量,Ei大小与酸性质的关系可以分为以下几类[15]:Ei>100 mV(很强的酸);0<Ei<100 mV(强酸);-100<Ei<0 mV(弱酸)和 Ei<-100 mV(很弱的酸).由表 1 可知:当焙烧温度为400-700℃时/ZrO2固体酸酸强度均很高;在600℃焙烧温度下,ZrO2固体在负载后,无论是酸强度还是总酸量都有显著的提高,分别由原来的147.3 mV和0.064 mmol·g-1提高至 393.0 mV和0.076 mmol·g-1,其中在600℃焙烧的/ZrO2酸强度最大,为393.0 mV;随着焙烧温度的提高,酸强度呈现先增加后减少的变化趋势;而总酸量则逐渐降低,由0.193 mmol·g-1降至0.065 mmol·g-1,但700℃焙烧的/ZrO2总酸量明显高于600℃焙烧的/ZrO2,这与XRD分析结果相一致.因此,700℃焙烧的/ZrO2总酸量高于600℃焙烧的/ZrO2.由表1还可知,当浸渍液H2SO4浓度为0.05-1 mol·L-1时,随着浸渍液H2SO4浓度的提高/ZrO2固体酸酸酸强度和总酸量均逐渐提高,分别由原来的 288.7 mV 和 0.067 mmol·g-1提高至 391.0 mV 和 0.077 mmol·g-1.

图2 催化剂电位滴定曲线Fig.2 Potentiometric titration curves of the catalysts
表1 不同焙烧温度的/ZrO2和ZrO2样品的酸性Table 1 The acidity data of /ZrO2and ZrO2samples calcined at different temperatures

表1 不同焙烧温度的/ZrO2和ZrO2样品的酸性Table 1 The acidity data of /ZrO2and ZrO2samples calcined at different temperatures
催化剂 酸强度(Ei)/mV 总酸量/(mmol·g-1)SO2-4/ZrO2-400 ℃ -空气 201.9 0.193 SO2-4/ZrO2-500 ℃ -空气 219.0 0.186 SO2-4/ZrO2-600 ℃ -空气 393.0 0.076 SO2-4/ZrO2-700 ℃ -空气 161.9 0.099 SO2-4/ZrO2-800 ℃ -空气 63.9 0.065 ZrO2-600 ℃ -空气 147.3 0.064 SO2-288.7 0.067 SO2-4/ZrO2-0.05 mol·L-1-N2 295.9 0.068 SO2-4/ZrO2-0.1 mol·L-1-N2 311.6 0.069 SO2-4/ZrO2-0.25 mol·L-1-N2 360.8 0.076 SO2-4/ZrO2-0.5 mol·L-1-N24/ZrO2-1 mol·L-1-N2 391.0 0.077
2.4 催化剂焙烧温度对催化活性的影响
用1.0 mol·L-1H2SO4浸渍ZrO(OH)2粉末,采用不同焙烧温度制备/ZrO2固体酸,焙烧气氛为空气.在催化剂用量(质量分数)2%、反应温度130℃和反应时间0.5 h的条件下,考察催化剂焙烧温度对双戊烯合成对伞花烃的影响.由图3a可知,焙烧温度由400℃提高到500℃时,双戊烯的转化率由89.76%提高到100%,而对伞花烃的选择性由12.45%快速上升至24.86%.在焙烧温度由500℃提高到700℃时,双戊烯的转化率均为100%,对伞花烃的选择性则缓慢增大,在700℃时达到最大值,为28.94%.但焙烧温度升至800℃时,双戊烯的转化率与对伞花烃的选择性均降为零.结合XRD和酸量的分析结果可知,焙烧温度在700℃内,随着焙烧温度的提高,ZrO2逐渐从无定形态转变为四方晶相与单斜晶相,使得/ZrO2固体酸的酸强度先增强后降低.焙烧温度为400-600℃时,固体酸的酸强度逐渐增大,催化剂活性逐渐提高,均有利于双戊烯的转化与对伞花烃的生成.但此时,催化剂的活性与酸量均较大,反而促进了副反应的发生,不利于对伞花烃的生成;700℃焙烧的/ZrO2酸强度与总酸量均较小,更有利于对伞花烃的生成;而800℃焙烧的/ZrO2中的ZrO2已大部分转化为单斜晶相/ZrO2中的大量流失,使其酸强度与总酸量均较低,催化剂失去催化活性.
2.5 H2SO4浸渍液浓度对催化活性的影响
采用不同浓度的H2SO4浸渍ZrO(OH)2粉末,经700℃焙烧制备/ZrO2固体酸,焙烧气氛为N2.在催化剂用量(质量分数)2%、反应温度170℃和反应时间0.5 h的条件下,考察催化剂H2SO4浸渍液浓度对双戊烯合成对伞花烃的影响.由图3b可知,H2SO4浸渍液浓度为0.05-0.1 mol·L-1时制备固体酸催化剂,双戊烯的转化率达到100%,对伞花烃的选择性由29.85%上升到33.25%.浸渍液H2SO4浓度为0.1-1.0 mol·L-1时制备固体酸,双戊烯的转化率达到100%,而对伞花烃的选择性降为27.06%.这是由于在H2SO4浸渍液浓度较低时,固体酸催化剂表面的含量低,使得/ZrO2固体酸的总酸量和酸强度较低,催化剂中活性中心的数目较少,不利于副反应的发生,有利于对伞花烃选择性的提高.而随着H2SO4浸渍液浓度的提高/ZrO2固体酸的酸强度和酸性逐渐增强,催化剂中活性中心的数目逐渐增加,副反应也增多,对伞花烃的选择性逐渐下降.当H2SO4浓度过高时,固体酸催化剂表面形成的硫酸盐覆盖了活性中心,使酸性降低,导致/ZrO2固体酸催化活性下降,使得对伞花烃的选择性下降.
2.6 反应温度对催化活性的影响
1.0 mol·L-1H2SO4浸渍ZrO(OH)2粉末,经600℃焙烧制备/ZrO2固体酸,在反应时间0.5 h和催化剂用量(质量分数)2%的条件下,考察反应温度对双戊烯合成对伞花烃的影响,结果见图3c.由图3c可知:当反应温度为100-170℃时,双戊烯的转化率基本不变,均达到100%;在反应温度为100-130℃时,对伞花烃的选择性由19.54%迅速上升至26.78%;当反应温度为130-170℃时,对伞花烃的选择性则缓慢上升;当反应温度为170℃时,对伞花烃的选择性达到最大值(28.75%).由于双戊烯脱氢制备对伞花烃的反应是一个热效应比较显著的吸热反应[3],因此,提高反应温度有利于对伞花烃的生成.
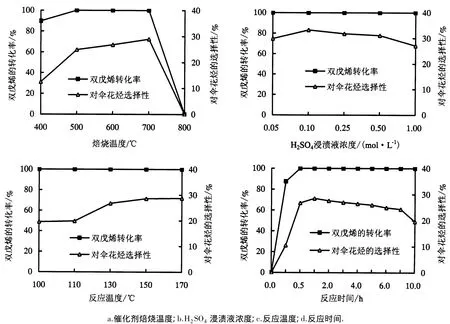
图3 各因素对双戊烯脱氢反应的影响Fig.3 Effects of each factor on dipentene dehydrogenation
2.7 反应时间对催化活性的影响
用1.0 mol·L-1H2SO4浸渍ZrO(OH)2粉末,经600℃焙烧制/ZrO2固体酸.在反应温度130℃和催化剂用量(质量分数)2%的条件下,考察反应时间对双戊烯合成对伞花烃的影响.从图3d可知,反应时间为0-0.5 h时,双戊烯的转化率迅速达到100%,而对伞花烃的选择性迅速升至26.78%.反应时间为0.5-1 h时,对伞花烃的选择性则缓慢上升,在1 h时,达到最大值(28.51%).反应时间为1-10 h时,对伞花烃的选择性随着反应时间的增加而逐渐降低,最终降至19.58%.
2.8 反应产物的化学组成
用0.1 mol·L-1H2SO4浸渍 ZrO(OH)2粉末,经700℃焙烧制备/ZrO2固体酸.在反应温度170℃、催化剂用量(质量分数)2%和反应时间1 h的条件下,反应产物通过GC-MS分析鉴定,结果表明产物多达80种.确定了选择性大于1.0%、匹配度在90%以上的成分6个,结果如表2所示.由表2可知,主产物为对伞花烃,副产物主要为3-对孟烯和对薄荷烯,其它成分均较少.此时,双戊烯转化率达100%,对伞花烃选择性为33.39%,说明/ZrO2固体酸可应用于双戊烯催化脱氢制备对伞花烃.
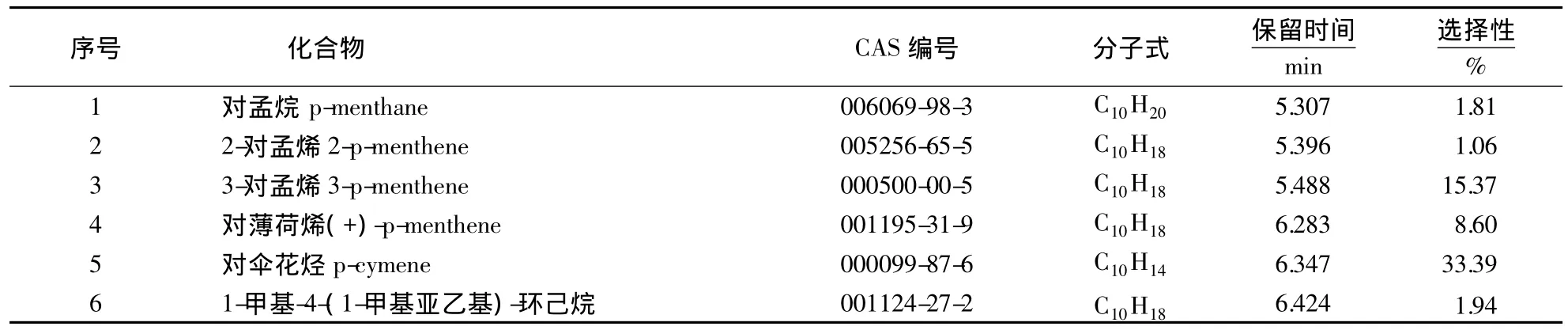
表2 反应产物GC-MS分析结果Table 2 GC-MS analysis result of reaction product
3 小结
[1]张秋格,毕良武,赵振东,等.对伞花烃的制备与应用研究进展[J].现代化工,2008,28(S2):401-406.
[2]翟卢琼,陈小鹏,王琳琳,等.酸改性膨润土负载ZnCl2催化松节油直接异构——歧化反应研究[J].高校化学工程学报,2011,25(1):68-70.
[3]ROBERGE D M,BUHL D,NIEDERER J P M,et al.Catalytic aspects in the transformation of pinenes to p-cymene[J].Applied Catalysis A:General,2001,215(1):111-124.
[4]王廖杀.由α-蒎烯制取对伞花烃液相反应条件的确定及催化剂的选择[J].化学世界,2001,42(3):131-133.
[5]李凝.以松节油为原料合成对异丙基甲苯[J].精细化工,2002,19(8):477-478.
[6]AJAIKUMAR S,GOLETS M,LARSSON W,et al.Effective dispersion of Au and Au-M(M=Co,Ni,Cu and Zn)bimetallic nanoparticles over TiO2grafted SBA-15:their catalytic activity on dehydroisomerization of α-pinene[J].Microporous and Mesoporous Materials,2013,173:99-111.
[7]王兰英,郭海福,闫鹏,等.工业双戊烯催化脱氢合成对伞花烃[J].精细石油化工,2008,25(6):18-21.
[8]杜俊明.负载型M/SBA15催化剂在双戊烯脱氢裂解与N2O催化分解中的应用研究[D].上海:复旦大学,2008.
[9]张秋格.工业双戊烯催化脱氢及对伞花烃定向氧化研究[D].北京:中国林业科学研究院,2010.
[10]BUHL D,ROBERGE D M,HÖLDERICH W F.Production of p-cymene from α-limonene over silica supported Pd/C catalysts[J].Applied Catalysis A:General,1999,188(1-2):287-299.
[11]BUHL D,ROBERGE D M,HÖLDERICH W F.Production of p-cymene from α-limonene over silica supported Pd catalysts[J].Applied Catalysis A:General,1999,188(1):287-299.
[12]MARTIN-LUENGO M A,YATES M,ROJO E S,et al.Sustainable p-cymene and hydrogen from limonene[J].Applied Catalysis A:General,2010,387(1):141-146.
[13]MARTIN-LUENGO M A,YATES M,DOMINGO M J M,et al.Synthesis of p-cymene from limonene,a renewable feedstock[J].Applied Catalysis B:Environmental,2008,81(3):218-224.
[14]PIZZIO L R,VÁZQUEZ P G,CÁCERES C V,et al.Supported Keggin type heteropolycompounds for ecofriendly reactions[J].Applied Catalysis A:General,2003,256(1):125-109.
[15]YANG X,JENTOFT F C,JENTOFT R E,et al.Sulfated zireonia with ordered mesopores as an active catalyst for nbutane isomerization[J].Catalysis Letters,2002,81(1):25-41.
[17]闫鹏,郭海福,舒华,等.固体超强酸/SnO2-Al2O3[J].化学研究与应用,2006,18(6):639-640.
[18]苏孟兴,刘宏儒,李敏,等.固体超强酸/SnO2的表征及其催化水解反应性能[J].中国油脂,2013,38(8):69-70.
[19]张汉辉,江凤玲,杨融生,等.红外辐射材料的制备与光谱研究[J].光谱学与光谱分析,2000,20(6):761-764.
[20]刘源,钟炳,彭少逸.超细二氧化锆的差示扫描热法分析及物相表征[J].工业催化,1998,6(1):55-59.

