碱性离子液体催化合成碳酸甲乙酯
刘 勇,刘 涛,陈蔚萍
(河南大学 化学化工学院,河南 开封 475004)
碳酸甲乙酯(EMC)是一种重要的不对称碳酸酯,在医药、农药、溶剂等方面用途广泛,尤其作为锂电池非水溶液电解质的溶剂可提高电池的能量密度和放电容量[1-3].EMC的合成方法主要有光气法、氧化羰化法和酯交换法,其中以碳酸二甲酯(DMC)和碳酸二乙酯(DEC)为原料酯交换合成EMC是一种极具应用前景的生产工艺,因为该工艺可避免DMC和乙醇酯交换反应产生共沸物,后续分离困难等缺点[4-5],产物选择性高,反应原料及产物都可用作锂电池电解液,反应体系不需分离.目前报道的催化剂主要集中于金属氧化物[6]、有机金属[7]催化剂、分子筛[8]催化剂等方面,但都存在着催化剂制备复杂,反应时间长,产品收率不高等问题,因此开发一种高效的催化剂非常必要.
碱性离子液体不仅具有常规离子液体的物理化学性能,而且还具有碱性,有望成为一类新型的碱性催化剂而引起人们的广泛关注[9-12].本文作者采用1-丁基-3-甲基咪唑阳离子与羧酸根阴离子合成羧酸类碱性离子液体,通过DMC和DEC酯交换合成EMC的反应,考察了催化剂类型、反应时间、反应温度、催化剂用量及反应物配比等工艺条件对酯交换反应的影响,确定了适宜的反应条件.
1 实验部分
1.1 试剂
DMC、N-甲基咪唑、DEC、溴代正丁烷、甲酸、乙酸、丙酸、丁酸、NaOH均为市售分析纯试剂;氯型717阴离子交换树脂:淡黄色透明球状颗粒,颗粒度0.3~1.20mm,粒径0.4~0.7mm,含水量40%~50%,交换容量≥3mmol/g,国药集团化学试剂有限公司.
1.2 碱性离子液体的制备
将N-甲基咪唑和溴代正丁烷以物质的量之比1∶1.1依次加入250mL的三口烧瓶中,在N2保护下70℃反应24h,冷却至室温,得淡黄色油状液体,用乙酸乙酯洗涤3次后,将洗涤后的产物80℃真空干燥24h,即得到淡黄色离子液体[Bmim]Br.
用上述所制[Bmim]Br配制成水溶液,通过装有阴离子交换树脂的柱子进行离子交换得到[Bmim]OH,接下来用等物质的量的丁酸进行中和,旋转蒸发除去水分,得到的离子液体用乙醚洗涤,最后在70℃的真空条件下干燥48h,即得到1-丁基-3-甲基咪唑丁酸盐([C4mim][CH3(CH2)2COO]).其他三种碱性离子液体1-丁基-3甲基咪唑甲酸盐([C4mim][HCOO])、1-丁基-3甲基咪唑乙酸盐([C4mim][CH3COO])及1-丁基-3甲基咪唑丙酸盐([C4mim][CH3CH2COO])以同样的方法进行制备.
1.3 碳酸甲乙酯合成
由DMC与DEC酯交换合成EMC反应方程式如下:
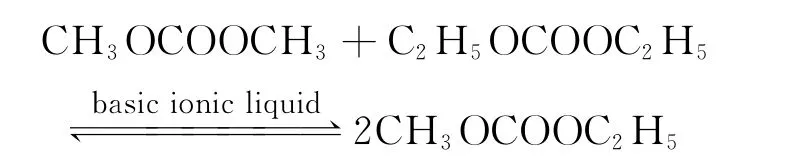
合成EMC的实验采用250mL三口烧瓶为反应器,装有冷凝器、温度计、取样口.反应在恒温水浴中进行.首先往反应器加入一定量的DMC与碱性离子液体,打开搅拌器,等加热到设定的温度后,迅速加入一定配比的DEC,反应5h后进行取样分析.
1.4 产物的分析与表征
采用岛津公司GC-17A型气相色谱仪分析试样的组成.色谱分析条件为:N2为载气,FID检测器,DB-1毛细管柱(30m×0.539mm×1.50μm),进样口温度为280℃,检测器温度为300℃,采用程序升温,柱温初温90℃,升温速率为15℃/min,终温180℃,色谱分析定量分析采用校正的面积归一化法.Bruker DPX-400型核磁共振仪,DMSO-d6为溶剂,TMS为内标,四种碱性离子液体的1H NMR数据如下:
[C4mim][HCOO]δ:9.45(1H,s,NCHN),8.57(1H,s,HCOO),7.81(1H,s,NCH),7.74(1H,s,NCH),4.18(2H,t,NCH2),3.86(3H,s,NCH3),1.76(2H,m,CH2),1.25(2H,m,CH2),0.90(3H,t,but-CH3);[C4mim][CH3COO]δ:9.73(s,1H,NCHN),7.82(t,1H,NCH),7.75(t,1H,NCHN),4.18(t,2H,NCH2),3.87(s,3H,NCH2),1.76(2H,m,CH2),1.54(3H,s,CH3CO2),1.24(2H,m,CH2),0.90(t,3H,but-CH3);[C4mim][CH3CH2COO]δ:9.64(s,1H,NCHN),7.81(s,1H,NCH),7.74(s,1H,NCHN),4.18(t,2H,NCH2),3.87(s,3H,NCH3),1.78(m,2H,CH2),1.25(m,2H,CH2),0.90(t,3H,ethyl-CH3),0.86(t,3H,but-CH3);[C4mim][CH3(CH2)2COO]δ:9.77(1H,s,NCHN),7.82(1H,s,NCHN),7.75(1H,s,NCHN),4.18(2H,t,NCH2),3.87(3H,s,NCH3),1.77(m,2H,CH2),1.39(m,2H,CH2),1.24(m,2H,CH2),0.90(t,3H,propyl-CH3),0.79(t,3H,but-CH3).
2 结果与讨论
2.1 碱性离子液体催化剂的筛选
分别 以[C4mim][HCOO]、[C4mim][CH3COO]、[C4mim][CH3CH2COO]、[C4mim][CH3(CH2)2COO]及NaOH为催化剂,当反应温度为90℃,催化剂的量6%(占反应物总质量百分数),n(DMC)∶n(DEC)=1∶1,反应时间为5h时,考察了5种催化剂的催化性能,结果如表1所示.
由表1可以看出,在相同的反应条件下,以[C4mim][CH3(CH2)2COO]为催化剂时DEC的转化率明显优于其他3种碱性离子液体,这是由于[C4mim][CH3(CH2)2COO]的碱性较强,导致其催化活性也较高.虽然NaOH碱性最强,但在反应体系中几乎不溶解,其催化活性较低.因此,本实验选用[C4mim][CH3(CH2)2COO]作为该酯交换反应的催化剂.
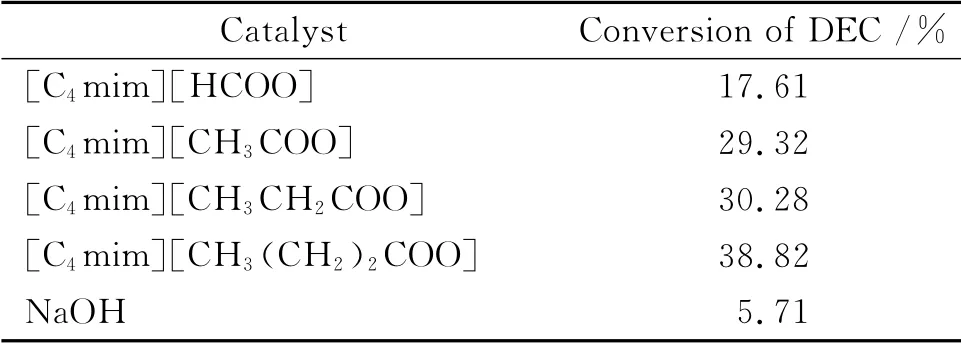
表1 不同催化剂对DEC转化率的影响Table 1 Effect of the different catalysts on the conversion of DEC
2.2 反应时间的影响
当以[C4mim][CH3(CH2)2COO]为催化剂,反应温度为90℃,催化剂量为6%(占反应物总质量百分数),n(DMC)∶n(DEC)=1∶1时,考察反应时间对酯交换反应的影响,结果如图1所示.由图1可以看出,随着反应时间的延长,DEC转化率逐渐增加,当反应达到5h时,碳酸二乙酯转化率高达38%,进一步延长反应时间,DEC的转化率基本不变,因此适宜的反应时间为5h左右.
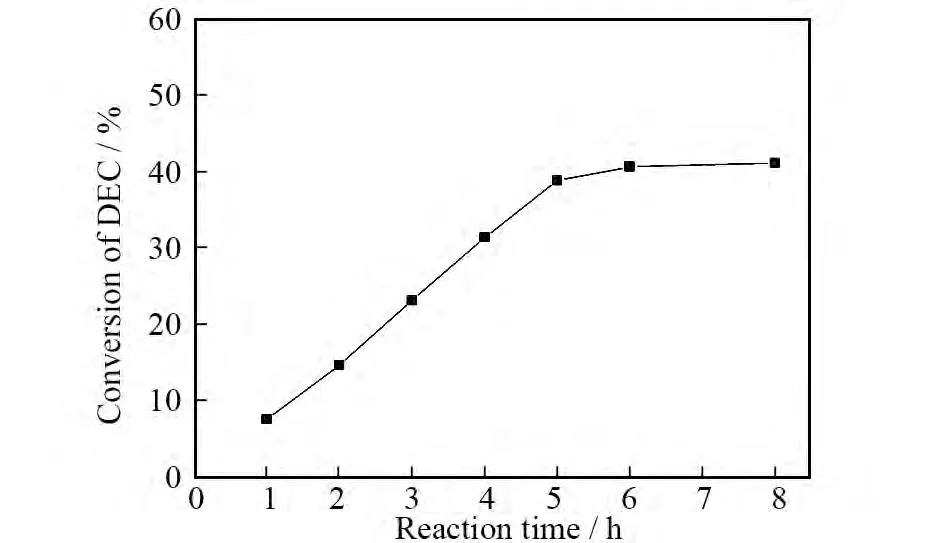
图1 反应时间对DEC转化率的影响Fig.1 Effect of the reaction time on the conversion of DEC
2.3 反应温度的影响
以[C4mim][CH3(CH2)2COO]为 催化剂,在n(DMC)∶n(DEC)=1∶1,催化剂量6%(占反应物总质量百分数),反应时间为5h时,考察反应温度对酯交换反应的影响,结果见图2.由图2可以看出,DEC的转化率随着反应温度的升高而增加,这可能由于增加反应温度,有利于增加反应物分子之间的有效碰撞,降低反应能垒,从而提高了转化率.但反应温度高于90℃时,DEC转化率增加缓慢,当温度为100℃时,DEC转化率开始下降,这可能是由于温度过高造成原料的挥发(DMC沸点为90.1℃)而导致DEC转化率降低,因此适宜的反应温度为90℃.
2.4 催化剂用量的影响
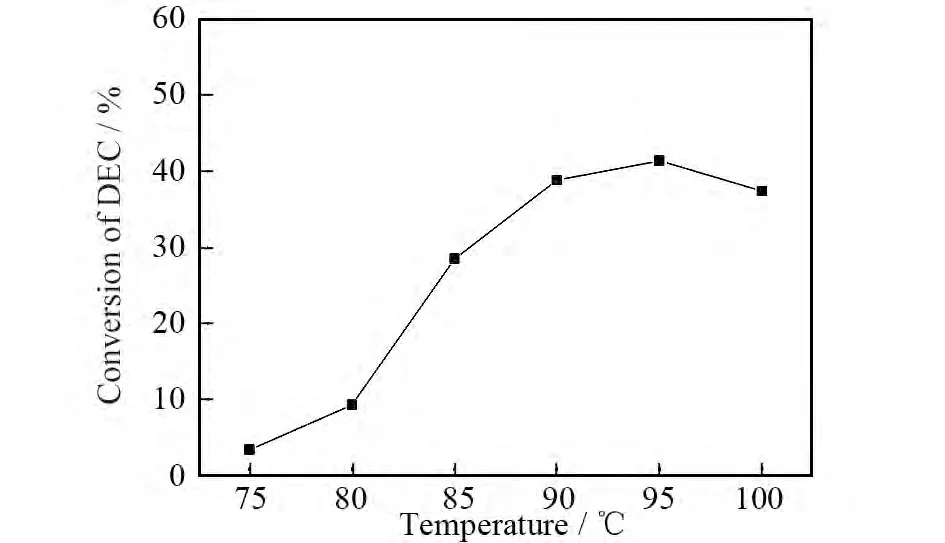
图2 反应温度对DEC转化率的影响Fig.2 Effect of the reaction temperature on the conversion of DEC
以[C4mim][CH3(CH2)2COO]为催化剂,反应温度为90℃,n(DMC)∶n(DEC)=1∶1,反应时间为5h,考察催化剂用量对酯交换反应的影响,结果如图3所示.由图3可以看出,DEC的转化率随着催化剂用量的增加而升高,到达反应平衡的时间缩短,这可能由于催化剂用量越大,碱性活性中心越多,从而促进反应的进行.但催化剂的用量高于6%时,DEC的转化率没有明显变化,因此适宜的催化剂用量为6%.
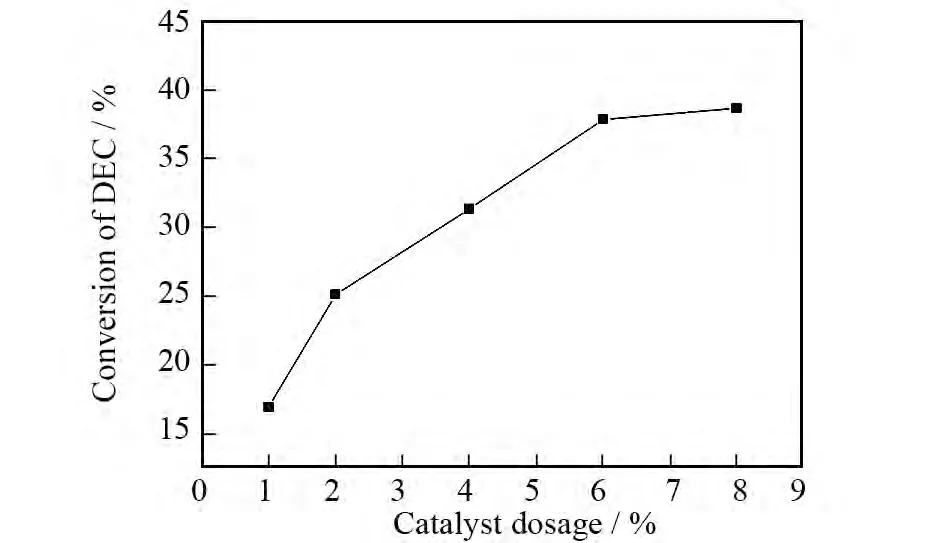
图3 催化剂量对DEC转化率的影响Fig.3 Effect of the catalyst dosage on the conversion of DEC
2.5 反应物配比的影响
以[C4mim][CH3(CH2)2COO]为催化剂,反应温度为90℃,催化剂量6%(占反应物总质量百分数),反应时间5h,考察了反应物配比对酯交换反应的影响,实验结果如图4所示.由图4可以看出,随着DMC量的增大,DEC的转化率不断提高(从1∶2到1.5∶1).这是由于DMC与DEC酯交换反应是一个可逆反应,当增加一种反应物浓度,反应向产物方向移动,从而导致DEC转化率增加.当DMC的量进一步增加时,DEC的转化率开始降低,这是由于过多的DMC同时会稀释反应物DEC的浓度,因此适宜的配比为n(DMC)∶n(DEC)=1.5∶1.
2.6 催化剂的重复使用
在反应温度为90℃,催化剂量6%(占反应物总质量百分数),n(DMC)∶n(DEC)=1.5∶1,反应时间5h条件下,对[C4mim][CH3(CH2)2COO]催化剂进行重复使用,DEC转化率结果如图5所示.由图5可看出,催化剂经过重复利用5次后,DEC转化率虽略有降低,DEC的转化率仍有较高的催化活性,表明[C4mim][CH3(CH2)2COO]对DMC和DEC酯交换反应具有良好的稳定性.
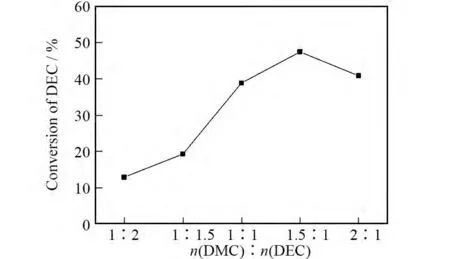
图4 原料配比对DEC转化率的影响Fig.4 Effect of n(DMC)∶n(DEC)on the conversion of DEC

图5 [C4mim][CH3(CH2)2COO]的重复使用Fig.5 Repeated use of[C4mim][CH3(CH2)2COO]
3 结论
碱性离子液体催化DMC与DEC酯交换合成EMC,其中[C4mim][CH3(CH2)2COO]的催化活性最高.[C4mim][CH3(CH2)2COO]催化合成EMC的最佳条件为:温度90℃、催化剂用量6%(占反应物总质量百分数)、n(DMC)∶n(DEC)=1.5∶1,反应时间5 h.在此反应条件下,DEC的转化率为48%,催化剂重复使用5次,仍具有较高的催化活性.
[1]PARRISH J P,SALVATORE R N,JUNG K W.Perspectives on alkyl carbonates in organic synthesis[J].Tetrahedron,2000,56(42):8207-8237.
[2]PLICHTA E J,BEHL W K.A low-temperature electrolyte for lithium and lithium-ion batteries[J].J Power Sources,2000,88(2):192-196.
[3]HASEGAWA K,KOSHINA H,OKUNO H.Nonaqueous electrolyte secondary batteries:U.S.Patent 5,484,669[P].1996-1-16.
[4]LUO H P,XIAO W D.A reactive distillation process for a cascade and azeotropic reaction system:Carbonylation of ethanol with dimethyl carbonate[J].Chem Eng Sci,2001,56(2):403-410.
[5]TUNDO P,TROTTA F,MORAGLIO G,et al.Continuous-flow processes under gas-liquid phase-transfer catalysis(GL-PTC)conditions:the reaction of dialkyl carbonates with phenols,alcohols,and mercaptans[J].Ind Eng Chem Res,1988,27(9):1565-1571.
[6]SHEN Z L,JIANG X Z,ZHAO W J.A new catalytic transesterification for the synthesis of ethyl methyl carbonate[J].Catal Lett,2003,91(1/2):63-67.
[7]GAN H,PALAZZO M J,TAKEUCHI E S.Method for preparing nonaqueous electrolytes for alkali ionelectrochemical cells containing unsymmetric organic carbonates:U.S.Patent 6,057,062[P].2000-5-2.
[8]PALANI A,GOKULAKRISHNAN N,PALANI CHAMY M,et al.Transesterification of dimethyl carbonate with diethyl carbonate over Al-Zn-MCM-41and Al-MCM-41molecular sieves[J].App Catal A:Gen,2006,304:152-158.
[9]亓虎,薛冰,许杰,等.离子液体催化碳酸二甲酯和乙醇酯交换合成碳酸甲乙酯[J].工业催化,2013,21(2):58-62.
[10]YANG Z Z,HE L N,DOU X Y,et al.Dimethyl carbonate synthesis catalyzed by DABCO-derived basic ionic liquids via transesterification of ethylene carbonate with methanol[J].Tetrahedron Lett,2010,51(21):2931-2934.
[11]DHARMAN M M,JU H Y,SHIM H L,et al.Significant influence of microwave dielectric heating on ionic liquid catalyzed transesterification of ethylene carbonate with methanol[J].J Mol Catal A:Chem,2009,303(1):96-101.
[12]骆铭,韩生,何忠义,等.碱性离子液体催化合成碳酸二丙酯[J].石油化工,2012,40(12):1316-1320.

