运用手持技术探究84消毒液漂白性的原因及其影响因素
任斌+吴晓红+杨文远+肖敏+马金刚
摘要:84消毒液是一种高效含氯消毒剂,被广泛应用于衣物漂白和卫生消毒中。通过解读84消毒液的产品标签,提炼出了影响84消毒液漂白性的三个因素(温度、pH、光照),并运用手持技术,探究了84消毒液漂白性的原因以及这三个对其漂白性能的影响因素。研究结果表明:常温下,当84消毒液pH为8~13时,其氧化性随pH降低而增大,因而漂白性能较好,而光照时间过长和温度过高均会降低84消毒液的漂白性能。此研究运用简便易操作的手持技术,数据结果处理方便,准确率高。
关键词:84消毒液;漂白性;手持技术;实验探究;影响因素
文章编号:1005–6629(2015)10–0053–04 中图分类号:G633.8 文献标识码:B
84消毒液是生活中常用的含氯消毒液,其使用过程蕴含着丰富的化学知识。《普通高中化学课程标准(实验)》强调:从学生已有的经验和将要经历的社会生活实际出发,帮助学生认识化学与人类生活的密切联系,关注人类面临的与化学相关的社会问题,培养学生的社会责任感、参与意识和决策能力[1]。基于此,笔者将利用手持技术对84消毒液中所蕴含的的化学知识进行揭秘,从而引导学生感受化学知识在社会生活中的应用,理解某些宏观现象背后的微观本质。
1 初探84消毒液的漂白性
84消毒液是一种以次氯酸钠为主的高效消毒剂,因其具有杀菌漂白效果,被广泛应用于卫生消毒、衣物漂白等。为认识84消毒液漂白性,取少量含有酚酞的氢氧化钠溶液,在不断滴加84消毒液后,溶液红色褪去。那么84消毒液漂白含有酚酞的氢氧化钠溶液的实质是什么?
首先,酚酞的变色范围是pH=8.2~10.0,在酸性溶液中,酚酞以无色型体存在,当溶液呈碱性时,酚酞分子结构会转变为醌式结构,溶液呈现红色,而这种醌式结构极其不稳定,遇到强碱或强氧化剂时,醌式结构被破坏而转变为羧酸盐等型体而呈现无色,如图1所示。
另外,84消毒液的主要成分为次氯酸钠(NaClO),次氯酸钠溶液中存在ClO-、HClO、Cl2,且ClO-、HClO、Cl2都具有氧化性,当向含有酚酞
的氢氧化钠溶液中滴加84消毒液后,溶液红色褪去,褪色过程中可能发生了如下的反应:
可能1:酚酞的显色范围是8.2~10.0,84消毒液中的HClO、Cl2与NaOH发生反应,溶液的pH降低到8.2以下,致使酚酞显无色。
可能2:具有氧化性的ClO-、HClO、Cl2将酚酞氧化成其他物质,致使溶液中不存在酚酞,所以溶液红色褪去。
可能3:以上两种可能同时发生。
为验证上述假设,取30mL pH=13.0的氢氧化钠溶液并加入2滴酚酞溶液,向溶液中不断滴加84消毒液,直至溶液红色褪去,并测定漂白(褪色)后溶液的pH。向漂白后的溶液中滴加2滴酚酞溶液,观察溶液颜色变化。
由于84消毒液具有漂白性,使用广泛pH试纸会导致测出的pH不准确,而采用pH传感器测量,不仅测量数据准确,还能够对整个漂白过程的pH变化进行监测,所以我们通过pH传感器进行测量,并得出了pH变化曲线,如图2所示。观察实验现象和图像可知,逐滴加入84消毒液后,溶液的pH保持不变,由此验证假设1和假设3错误;向漂白后的溶液中滴加酚酞溶液,溶液再次变红,说明84消毒液漂白含有酚酞的氢氧化钠溶液的实质是具有强氧化性的ClO-、HClO、Cl2将酚酞氧化,即假设2正确。
2 再探影响84消毒液漂白性的因素
标签和说明书是产品的语言,阅读84消毒液产品说明(如图3所示)可知,84消毒液不能与洁厕灵等酸性清洁剂混用。经查阅相关文献后获知:工业上在使用84消毒液时,要加少量酸,而家庭使用84消毒液时不必加酸。加酸对84消毒液的漂白性有何影响?另外,产品标签指出:不能用热水稀释原液,且储存时84消毒液应放置在避光阴凉处。由此,我们可以提炼出温度、光照、pH三个因素对84消毒液漂白性可能有影响,并利用手持技术对这三个因素进行了更深入的探究。
2.1 探究酸碱性对84消毒液漂白性的影响
2.1.1 实验原理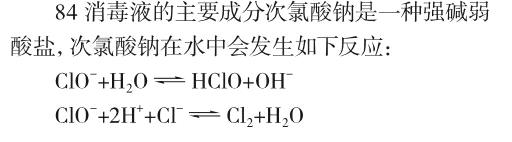
因此,84消毒液中的主要成分会随着氢离子浓度改变而改变。查阅文献可知,pH与次氯酸钠溶液的平衡关系如图4所示:当84消毒液的pH小于2时,溶液中的主要成分为Cl2;当pH为4~6时,溶液的主要成分为HClO;当溶液的pH大于8时,溶液中的主要成分为ClO-。因此,随着84消毒液溶液的pH不同,溶液的主要组成成分会发生变化[2]。
另外,由上述探究可知,84消毒液漂白性的实质是84消毒液具有强氧化性,而反应溶液氧化性最直观的参数就是氧化还原电位,因此我们利用氧化还原电位传感器测量不同pH条件下的ORP来研究其氧化性的变化。
2.1.2 实验装置图
实验装置如图5所示。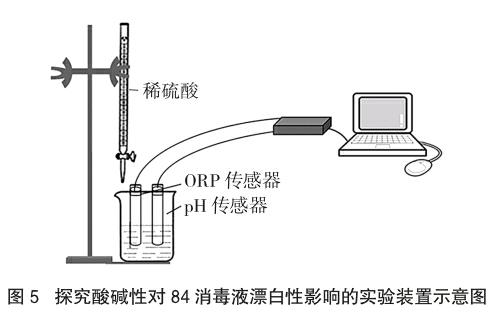
2.1.3 实验过程
取30mL 84消毒液倒入烧杯中,将pH传感器和ORP传感器浸入到装有84消毒液的烧杯中;打开装有0.5 mol/L稀硫酸溶液的酸式滴定管,向84消毒液中滴加稀硫酸;启动数据采集器,绘制加入稀硫酸过程中84消毒液的pH与ORP的变化曲线。
2.1.4 实验数据
从图6可以看出:随着84消毒液pH的降低,其ORP逐渐增大;当pH>10时,ORP的值变化幅度较大,之所以有这样的变化是因为pH>10时,加入的稀硫酸与溶液中的OH-反应,随着OH-不断被消耗,加入的H+和溶液中的ClO-结合形成了HClO,且HClO的氧化能力远远大于ClO-,从而引起了大幅度变化,这与图4的结论相吻合。另外,在实验过程中发现,当溶液的pH小于7时,大量氯气会逸出,因此,我们只考察了84消毒液pH>8时的ORP变化[3]。
2.1.5 实验结论
常温下,84消毒液的氧化性随pH降低而增大(当pH大于8时)。84消毒液的漂白性实质是利用其氧化性将有色物质氧化为无色物质。因此,为实现更好的漂白效果,工业使用84消毒液时,可加入少量酸调节84消毒液pH至8~10。而家庭使用84消毒液时用量较少,空气中的二氧化碳溶于水就可起弱酸作用,因此不必加酸。家庭使用84消毒液时,之所以不可将其与酸性洗涤剂混合使用,是为了防止产生有毒的氯气。
2.2 温度和光照对84消毒液漂白性的影响
次氯酸钠溶液不稳定、易分解,而在光照和受热条件下分解速率加快,分解原理如下: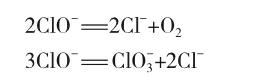
随着光照和温度升高,溶液中的有效氯质量分数降低,氧化能力也会改变。因此,我们利用氧化还原反应电位传感器测量不同温度和光照条件下溶液的ORP变化以研究温度和光照对84消毒液氧化能力的影响。
2.2.1 实验步骤
a.取烧杯倒入84消毒液30mL,将烧杯放置在距离10厘米的100W白炽灯下进行光照,利用氧化还原电位传感器测量ORP变化;
b.取四个烧杯,分别倒入84消毒液30mL。将四个烧杯分别放入20℃、30℃、40℃、50℃水浴中加热,测量ORP变化。
2.2.2 实验数据
2.2.3 实验结论
由实验图像可知,光照和温度都会影响84消毒液的氧化能力,且温度越高、光照时间越长,次氯酸钠分解速率越快。因此,84消毒液在储存时,应放置在避光的阴凉处,在使用时不能用热水稀释,防止84消毒液漂白性减弱。
3 启示
84消毒液来自于生活,关于84消毒液的漂白效果、储存问题以及不能与“洁厕灵”混用的原因这些问题也都源自于生活。从生活中发现问题,用化学思维解答问题,利用先进实验仪器揭示宏观现象背后的微观本质,这充分体现了“从生活中学化学,在生活中用化学”的思想。而在解决这些问题的过程中,借助手持技术的实验能够迅速捕捉到反应过程所需的信息,如酸碱性、电压、电导率等,并将信息进行转换,最终以曲线、表格等形式展现出来,不仅突破了时空局限,更“直播”了“变化”的过程[4]。这也启示我们:将科学知识应用到生活世界的同时,引导学生带着发现的“眼睛”观察生活中的类似化学问题,激发学生的探究兴趣,并能够继续运用手持技术解决类似化学问题,从而更深地理解宏观现象背后的微观本质。
(注:此实验设计荣获2014年全国化学数字化实验教学应用及创新设计大赛一等奖)
参考文献:
[1]中华人民共和国教育部制定.普通高中化学课程标准(实验)[S].北京:人民教育出版社,2003.
[2]陈永忠.次氯酸钠溶液漂白性实质探究[J].中小学实验与装备,2013,23(3):8~9.
[3]周相武,汪晓军,刘姣等.次氯酸钠溶液的氧化性研究[J].氯碱工业,2006,(8):28~30.
[4]邓育红.手持技术在生活化实验中的应用[J].教学仪器与实验,2013,29(12):23~26.

