高效液相色谱法测定脑脉康颗粒中黄芪甲苷含量
万萌萌,康新莉,谭睿,宋英,盛蓉
(1.西南交通大学生命科学与工程学院,四川成都610031;2.成都中医药大学附属医院,四川成都610075)
高效液相色谱法测定脑脉康颗粒中黄芪甲苷含量
万萌萌1,康新莉1,谭睿1,宋英2,盛蓉2
(1.西南交通大学生命科学与工程学院,四川成都610031;2.成都中医药大学附属医院,四川成都610075)
目的建立测定脑脉康颗粒君药黄芪中黄芪甲苷含量的高效液相色谱(HPLC)法。方法色谱柱为Agilent C18柱(250 mm×4.6 mm,5 μm),柱温为30℃,流动相为乙腈-水(36∶64),流速为1 mL/min。结果黄芪甲苷进样质量浓度线性范围是0.035 4~0.354 2 g/L,线性回归方程为logA=1.602 0 logCi+3.022 1,r2=0.999 9(n=8);平均回收率为102.60%,RSD=2.96%(n=6)。结论该方法简便、准确、专属性强,可用于测定脑脉康颗粒君药黄芪中黄芪甲苷的含量。
脑脉康颗粒;黄芪;黄芪甲苷;高效液相色谱法
脑脉康颗粒是由黄芪、丹参等药材组方的复方制剂,黄芪为方中君药,主要含有黄芪甲苷,故选择黄芪甲苷作为控制制剂质量的指标成分。关于黄芪中黄芪甲苷的测定方法,已有报道的有薄层扫描法、超临界萃取-气相色谱-质谱(GC-MS)分析法、气相色谱法、毛细管气相色谱法、高效液相色谱(HPLC)法以及反相高效液相色谱法等。现参考2010年版《中国药典(一部)》[1]及相关文献,建立了测定脑脉康颗粒中黄芪甲苷含量的HPLC法,为制剂质量标准的完善与提高提供依据,现报道如下。
1 仪器与试药
Waters 2695型高效液相色谱仪;Empower 2化学工作站,Waters 2424型蒸发光散射(ELSD)检测器;Sartoius BS110型十万分之一电子分析天平(北京赛多利斯仪器系统有限公司)。乙腈为色谱纯,其他试剂均为分析纯;脑脉康颗粒(批号分别为20120917,20120918,20120919),缺黄芪阴性样品(批号为20120923),均由成都中医药大学附属医院药剂科提供;黄芪甲苷对照品(中国药品生物制品检定所,供含量测定用,批号为110781-200613)。
2 方法与结果
2.1 色谱条件[2-10]
色谱柱:Agilent C18柱(250 mm×4.6 mm,5 μm);流动相:乙腈-水(36∶64);流速:1.0 mL/min;柱温:30℃;ELSD参数:漂移管60℃,气体压力30 Psi,喷雾器加热60%模式,增益20。
2.2 溶液制备
称取黄芪甲苷对照品13.00 mg,精密称定,置25 mL容量瓶中,加甲醇至刻度,摇匀,即得0.520 0 g/L的对照品溶液。精密量取样品(批号为20120917)溶液10 mL共4份,用水饱和的正丁醇振摇提取4次,每次40 mL,收集正丁醇液,用1%NaOH溶液洗涤2次,每次40 mL,弃去氨液,在用正丁醇饱和的水溶液充分洗涤2次,每次40 mL,收集正丁醇萃取液,蒸干,残渣加甲醇溶解,转移至5 mL容量瓶中,加甲醇至刻度,摇匀,用微孔滤膜(0.45 μm)滤过,取续滤液,作为供试品溶液。缺黄芪阴性样品(批号为20120923),研细,取约5.2 g,精密称定,置50 mL容量瓶中,加甲醇溶液,超声处理(功率为250 W,频率为40 KHz)30 min,放冷,用甲醇溶液定容至刻度,摇匀,滤过,取续滤液,即得阴性对照品溶液。
2.3 方法学考察
专属性考察:精密吸取2.2项下种溶液各5 μL,按拟订色谱条件进样测定。结果供试品溶液色谱中,黄芪甲苷色谱峰与相邻色谱峰达到基线分离,理论塔板数按黄芪甲苷峰计算不低于4 000,分离度大于1.5,阴性无干扰。色谱图见图1。
线性关系考察:精密称取黄芪甲苷对照品(17.71 mg),置25 mL容量瓶中,加甲醇定容至刻度,得质量浓度为0.708 4 g/L的黄芪甲苷对照品溶液。精密量取上述溶液0.5,0.6,0.7,0.8,0.9,1.0,2.0,5.0 mL,分别配制成质量浓度为0.035 4,0.042 5,0.049 6,0.056 7,0.063 8,0.070 8,0.141 7,0.354 2 g/L的黄芪甲苷对照品溶液,依次进样10 μL,测定峰面积。以峰面积对数(log A)对质量浓度的对数(log Ci)进行线性回归,得回归方程logA=1.602 0 logCi+3.022 1,r2=0.999 9(n=8)。结果表明,黄芪甲苷质量浓度线性范围为0.035 4~0.354 2 g/L。
精密度试验:精密吸取同一对照品溶液10 μL,按拟订色谱条件连续进样测定6次。结果黄芪甲苷平均峰面积为6 134 335,RSD=1.44%(n=6),表明仪器精密度良好。
稳定性试验:精密吸取同一供试品溶液10 μL,于0,4,8,12,24 h时依法进样,测定峰面积,计算含量。结果黄芪甲苷平均含量为0.153 2 mg/g,RSD=5.28%(n=5),表明供试品溶液在24 h内稳定。
重复性试验:精密量取样品(批号为20120917)溶液10 mL,共6份,依法制备供试品溶液并进样10 μL,测定峰面积,计算含量。结果黄芪甲苷平均含量为0.153 2 mg/g,RSD=5.28%(n=6),表明方法重复性较好。
加样回收率试验:精密量取已知含量的样品(批号为20120917)5 mL,共6份,分别精密加入对照品溶液(0.9 g/L)1 mL,按供试品溶液的制备方法制备溶液,进样10 μL,测定含量,计算回收率。结果见表1。

图1 高效液相色谱图
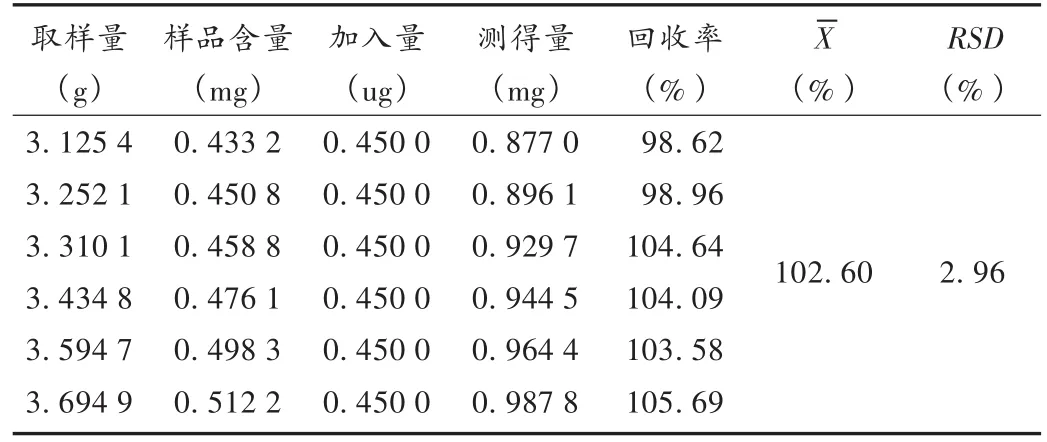
表1 黄芪甲苷加样回收试验结果(n=6)
2.4 样品含量测定
取3批中试样品,依法制备供试品溶液,按拟订色谱条件进样10 μL,测定峰面积,计算含量。结果见表2。
3 讨论
2010年版《中国药典(一部)》黄芪项下规定,黄芪饮片中黄芪甲苷含量不得少于400 μg/g,故3批样品中黄芪甲苷的含量均符合要求。在含量测定试验中,丹参中的丹参酮ⅡA虽然为该复方制剂的主要成分之一,但是由于在黄芪为该方中的君药,且黄芪甲苷的含量测定用到了ELSD,更具有指标意义。故选用黄芪甲苷为含量测定的指标成分。在测定不同的3批样品时,黄芪甲苷的含量变化不大,说明该测定方法具有良好的稳定性。
参考药典及相关文献,结合化合物的性质,试用了色谱柱Phenomenex C18柱(250 mm×4.6 mm,5 μm)、Agilent C18柱(250 mm×4.6 mm,5 μm),结果分离度均良好,理论塔板数均大于5 000。本试验中选用Agilent C18柱(250 mm×4.6 mm,5 μm)。同时,考虑到ELSD的特点,温度太低不利于检测,试用柱温30℃进行试验,结果分离度良好,样品稳定,故选用柱温为30℃。选择流动相时,试用乙腈-水(32∶68)、乙腈-水(36∶64)、乙腈-水(40∶60),结果以乙腈-水(36∶64)为流动相时黄芪甲苷峰峰形和保留时间较好。选择ELSD参数时,根据仪器型号并参考相关文献,选择漂移管温度60℃、气体压力30 Psi、喷雾器加热60%模式、增益20为检测条件,发现黄芪甲苷峰形、峰面积较佳,故采用此检测条件。

表2 样品中黄芪甲苷含量测定结果(mg/g)
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:化学工业出版社,2010:249.
[2]田南卉,杨国红,方颖,等.高效液相色谱法蒸发光散射检测器测定黄芪和制剂中黄芪甲苷的含量[J].药物分析杂志,2000,20(3):199.
[3]段亚丽,谢梅冬.黄芪化学成分及其有效成分黄芪甲苷含量测定的研究现状[J].中国兽药杂志,2005,39(3):35-38.
[4]冯祚臻,俸小平,官东秀.黄芪甲苷的提取及含量测定研究进展[J].中国药业,2006,15(11):80-82.
[5]胡芳弟,封士兰,赵健雄,等.HPLC法测定黄芪中黄酮类成分和黄芪甲苷的含量[J].分析测试技术与仪器,2003,9(3):173-177.
[6]蔡进章,王增寿,章晓东.反相高效液相色谱法测定黄芪中黄芪甲苷的含量[J].中国药业,2004,12(12):36-37.
[7]钱广生,刘三康.HPLC测定黄芪注射液中黄芪甲苷的含量[J].华西药学杂志,2002,17(1):41-42.
[8]郭洪祝.高效液相色谱法测定胰复康胶囊中黄芪甲苷含量[J].中国中药杂志,2000,25(10):609-611.
[9]陈岳蓉,马玲云,马双成.HPLC-ELSD测定芪鹿益肾片中黄芪甲苷的含量[J].中国保健,2004(8):629-631.
[10]马艳蓉,刘泓,柴国林,等.HPLC—ELSD测定黄芪中黄芪甲苷含量及相关试验条件选择的探讨[J].现代中药研究与实践,2004,17(6):17-19.
[11]李飞,周洪雷,杜吴忱,等.高效液相色谱-蒸发光散射检测法测定心脑补益口服液中黄芪甲苷含量[J].中国药业,2011,20(5):16-17.
Determination of AstragalosideⅣin Naomaikang Granules by HPLC
Wan Mengmeng1,Kang Xinli1,Tan Rui1,Song Ying2,Sheng Rong2
(1.Southwest Jiaotong University,Chengdu,Sichuan,China 610031;2.Teaching Hospital of Chengdu University of T.C.M,Chengdu,Sichuan,China610075)
ObjectiveTo establish a method for quality control of Naomaikang Granules.MethodsThe chromatography column was Agilent C18(250 mm×4.6 mm,5 μm).The mobile phase consisted of Acetonitrile-water(36∶64)at a flow rate of 1 mL/min,at 30℃. ResultsAstragaloside IV showed a good linear relationship within the range of 0.0354 mg/mL~0.354 2 mg/mL,equation of linear regression was logA=1.602 0 logCi+3.022 1,R2=0.999 9(n=8),the average recovery was 102.60%,RSD was 2.96%(n=6). ConclusionThe methods are simple,exact and reproducible,and can be used for the qualitative and quantitative control of Naomaikang Granules.
Naomaikang Granules;milkvetch root;astragalosideⅣ;HPLC
R284.1;R286.0
A
1006-4931(2015)20-0075-02
万萌萌,女,在读硕士研究生,研究方向为中药质量标准规范化和新制剂研发,(电子信箱)774235565@qq.com;谭睿,女,博士研究生,教授,研究方向为中药质量标准规范化和新制剂研发,本文通讯作者,(电话)028-87600993(电子信箱)tanrui@swjtu.edu.cn。
2015-03-25)

