反相高效液相色谱法测定川楝子中川楝素含量
李婵,雷久雨,南叶飞
(1.陕西省食品药品监督管理局药品认证中心,陕西西安710061;2.西安恒生堂制药有限公司,
陕西西安710061;3.西安石油大学,陕西西安710061)
反相高效液相色谱法测定川楝子中川楝素含量
李婵1,雷久雨2,南叶飞3
(1.陕西省食品药品监督管理局药品认证中心,陕西西安710061;2.西安恒生堂制药有限公司,
陕西西安710061;3.西安石油大学,陕西西安710061)
目的建立测定川楝子药材中川楝素含量的反相高效液相色谱(RP-HPLC)法,并与高效液相色谱-质谱(HPLC-MS)法进行比较。方法色谱柱为Agilent TC-C18柱(250mm×4.6mm,5μm),流动相为乙腈-水(25∶75),检测波长为210 nm,柱温为35℃,流速为1mL/min,进样量为10μL。结果川楝素质量浓度在0.036~0.280 g/L范围内与峰面积线性关系良好(r=0.999 8),平均回收率为102.38%,RSD=3.89%(n=6)。应用RP-HPLC和HPLC-MS法检测3批次药材川楝素含量分别为0.17%,0.17%,0.18%和0.18%,0.18%,0.19%。结论所建立方法使用仪器普及率高,操作简单,成本低,检测精密度和准确度满足应用要求。与HPLC-MS法比较,RP-HPLC法检测含量稍高,基层药品检验部门和一般制药企业可利用该方法对川楝素进行质量控制。
反相高效液相色谱法;川楝素;含量测定
川楝子是楝科植物川楝Melia toosendan Sieb.et Zucc.的干燥果实,味苦,性寒[1-2],有行气止痛、疏肝泄热等功效[3]。对川楝子化学成分的研究,主要集中于一些三萜类化合物[4],如川楝素[5-6]。川楝素具有驱虫、抗癌、抗菌、影响神经肌肉及细胞、影响呼吸中枢及消炎等多种生物活性[7-11],也是川楝子、苦楝皮等药材含量控制的指标成分。2010年版《中国药典(一部)》采用高效液相色谱-质谱(HPLC-MS)联用检测的方法对川楝子和苦楝皮中的川楝素进行含量测定,但仪器昂贵、运行成本大、对仪器操作人员的技术水平要求也高,故普及性较差。为此,探索对川楝子中川楝素进行定量分析的反相高效液相色谱(RP-HPLC)法,以利于基层药检部门及相关制药企业更广泛、便捷地使用。
1 仪器与试药
Agilent1100 series型高效液相色谱仪(美国安捷伦公司);手动进样系统;FW200A型高速万能粉碎机(北京科伟永兴仪器有限公司);PL203型电子天平(梅特勒-托利多公司);BT25s型十万分之一天平(赛多利斯公司);KQ-500DB型超声波清洗器(昆山市超声仪器有限公司);DK-98-Ⅱ型电热恒温水浴锅(天津市泰斯特仪器有限公司);UPDR-Ⅱ-10T型超纯水机(成都超纯科技有限公司)。川楝素对照品(中国药品生物制品检定所,批号为111842-201102);川楝子(西安中药饮片厂,批号为20140201,20140501,20140801);甲醇(天津市彪仕奇科技发展有限公司,批号为130603);乙腈(天津市彪仕奇科技发展有限公司,批号为11037501)为色谱纯,水为自制超纯水。
2 方法与结果
2.1色谱条件
色谱柱:Agilent TC-C18柱(250 mm×4.6 mm,5μm);流动相:乙腈-水(25∶75);检测波长:210 nm;柱温:35℃;流速:1mL/min;进样量:10μL。理论板数按川楝素峰计算不低于3 000。
2.2溶液制备
取川楝素对照品0.007 70 g,精密称定,置25mL容量瓶中加甲醇溶解并稀释至刻度,摇匀,制成每1mL含川楝素0.308 0mg的溶液,作为对照品溶液。取川楝子粉末(过3号筛)1.006 5 g,精密称定,置50mL具塞锥形瓶中,精密加入甲醇25mL,称定质量,超声提取30min,取出,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过;重复提取3次,合并滤液蒸干,甲醇溶解定容至10mL的容量瓶中,摇匀,滤过,取续滤液,即得供试品溶液。
2.3方法学考察
专属性试验:分别精密吸取2.2项下对照品溶液、供试品溶液和空白溶液(甲醇)各10μL,注入高效液相色谱仪。结果对照品中川楝素的保留时间为35.942,46.227min,供试品中川楝素的保留时间为35.873,46.073min,空白溶液在对照品的川楝素保留时间处无色谱峰出现。结果见图1,表明该方法专属性强。
线性关系考察:取川楝素对照品贮备液,稀释成质量浓度为0.287 0,0.143 5,0.107 6,0.071 7,0.035 8 g/L的对照品溶液,分别精密吸取10μL,注入高效液相色谱仪,以平均峰面积值和质量浓度进行线性回归,得回归方程Y=10 019 082.226 X+ 7 652.520,r=0.999 8(n=5)。结果川楝素质量浓度在0.036~0.280 g/L范围内与峰面积线性关系良好。
耐用性试验:试验所用色谱柱分别为安捷伦色谱柱、菲罗门色谱柱,流动相组成分别为25∶75,28∶72,30∶70的乙腈-水溶液,柱温分别为33,35,37℃时,精密吸取对照品溶液各10μL,注入高效液相色谱仪,记录色谱图,依据保留时间进行定位,其分离度和理论板数见表1。可见,分离度和理论板数均在标准范围之内,符合规定,确保流动相的组成比例、不同厂牌的同类型色谱柱、柱温的变化因素能通过系统适用性。

图1 高效液相色谱图
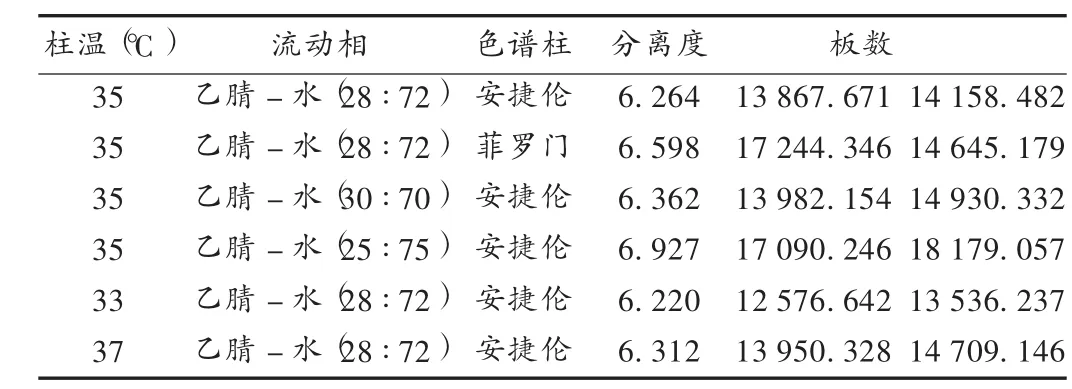
表1 耐用性试验结果(n=6)
精密度试验:精密称取川楝素对照品,平行制配对照品溶液6份,在拟订色谱条件下,1日内重复进样6次,在6日内重复进样6次。结果日内精密度的RSD=1.06%(n=6),日间精密度的RSD=1.15%(n=6),表明该方法精密度良好。
稳定性试验:精密吸取同一供试品溶液,分别于0,6,12,18,24 h时测定。结果川楝素峰面积分别为970 265.594,968 786.391,953 199.969,996 572.750,962 307.109,RSD为1.70%(n=5),表明供试品溶液在24 h内稳定。
重复性试验:精密吸取川楝素对照品溶液10μL连续进样6次,计算峰面积。结果的RSD为1.80%(n=6),表明该方法重复性良好。
加样回收试验:精密称取已知含量的川楝子样品6份,每份1.000 0 g,依次分别精密加入川楝素对照品0.63,0.59,0.84,0.80,1.13,0.99mg,按2.2项下方法制备供试品溶液,按2.1项下色谱条件进样测定,计算回收率。结果见表2。
2.4样品含量测定
采用RP-HPLC法对3批次川楝子进行川楝素含量测定,并与HPLC-MS法的测定结果进行比较,考察测定结果的系统误差。结果见表3。

表2 川楝素加样回收试验结果(n=6)

表3 样品含量测定结果比较(%)
3 讨论
采用HPLC法对川楝子药材中川楝素含量测定方法进行研究,结果表明,其系统适用性、精密度、重复性、专属性、线性范围及稳定性试验结果均符合规定,所建立川楝素分析方法的分离度和理论板数均符合标准要求,说明具有较强的适应性,可供制药企业或药检部门选择。同时,与HPLC-MS法所检测的同批川楝子含量结果进行对比,测量误差符合规定。本研究中建立的RP-HPLC法具有简便可行、灵敏度高、重复性好的特点,在基层药检部门及药品企业可作为2010年版《中国药典(一部)》中川楝子药材川楝素含量测定的替代方法。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:附录130-附录131.
[2]国家药典委员会.中华人民共和国药典·第一增补本[M].北京:中国医药科技出版社,2012:84-85.
[3]孙建,周洪雷.中药川楝子临床应用研究[J].辽宁中医药大学学报,2008,10(1):27-28.
[4]谢帆,张勉,张朝凤,等.川楝子的化学成分研究[J].中国药学杂志,2008,43(14):1 066-1 069.
[5]周英,王慧娟,郭东贵,等.川楝子化学成分的研究[J].中草药,2010,41(9):1 421-1 423.
[6]白靖文,赵李霞,冯时.植物源农药川楝素UAE方法研究[J].东北农业大学学报,2011,42(1):81-84.
[7]罗刚,全枉珠.川楝素药理研究进展[J].华西药学杂志,1988,3(3):154-156.
[8]程蕾,雷勇,梁媛媛,等.川楝子不同提取部位药效及毒性的比较研究[J].中药材,2007,30(10):1 276-1 279.
[9]王小娟,刘妍如,肖炳坤,等.川楝素抗肿瘤作用机制研究[J].科学技术与工程,2011,11(2):281-285.
[10]蔡梅超,周洪雷,孙建,等.川楝子炮制前后挥发油化学成分的气相色谱-质谱联用分析[J].中国药业,2010,19(17):11-12.
[11]沈雅琴,张明发,朱自平,等.苦楝皮的镇痛抗炎和抗血栓形成作用[J].中国药业,1998,7(10):30-31.
Determ ination of Toosendanin in Melia Toosendan by RP-HPLC
Li Chan1,Lei Jiuyu2,Nan Yefei3
(1.Drug Certification Center,Shaanxi Provincial Administration Bureau of Food and Drug,Xi′an,Shaanxi,China 710061;2.Xi′an Hengshentang
Pharmacutical Co.,Ltd.,Xi′an,Shaanxi,China 710061;3.Xi′an Petroleum University,Xi′an,Shaanxi,China 710061)
Objective To establish a RP-HPLC method for the determination of the toosendanin content in Melia toosendan and to compare it with the HPLC-MS.M ethods The chromatographic conditions were as follows:the Agilent TC-C18column(250 mm× 4.6 mm,5μm),the mobile phase of acetonitrile-water(25∶75)at a flow rate of 1 mL/min,the detection wavelength of 210 nm and the sample size of 10μL.Results The linear range of toosendanin in Melia toosendan was 0.036-0.280 g/L(r=0.999 8).The average recovery rate was 102.38%,RSD=3.89%(n=6).The toosendanin contents in 3 batches of medicinal material determined by RP-HPLC and HPLC-MS were 0.17%,0.17%,0.18%and 0.18%,0.18%,0.19%respectively.Conclusion The established method has high popularizing rate for using instrument,is easy to operate,has low cost,its detection precision and accuracy meet the application requirements.Compared with HPLC-MS,the detected content of RP-HPLC is slightly higher.The primary drug inspection department and general pharmaceutical enterprise can use this method to conduct the quality control on toosendanin.
RP-HPLC;toosendanin;content determination
R284.1;R282.71
A
1006-4931(2015)16-0087-03
2015-02-05;
2015-03-11)

