黄瓜疫霉菌拮抗菌的筛选及鉴定
周 珍,向 阳,解 娜,易图永,3
(1. 湖南农业大学植物保护学院,湖南 长沙 410128;2. 永顺县农业局,湖南 永顺 416700;3. 植物病虫害生物学与防控湖南省重点实验室,湖南 长沙410128)
黄瓜疫病是由黄瓜疫霉菌(Phytophthora melonis)引起的黄瓜主要病害之一,在黄瓜种植区的发生日趋严重。据统计,青海[1]、海南[2]、江苏[3]等地的黄瓜栽培区都曾大面积发生黄瓜疫病,造成黄瓜的产量减少和口感下降,严重打击了农民种植黄瓜的积极性[4]。目前,对该病的防治以化学农药为主[5],但某些药剂存在毒性大、残留时间长、容易诱导病原物产生耐药性等缺点[6-7],不宜长期大量使用。而生物防治具有低残留、高效等优点,已成为防治植物病害的发展趋势[8]。在诸多生物防治策略中,利用拮抗微生物或其次级代谢产物防治作物病害的报道较多[9-10]。其中,放线菌因来源广、代谢产物活性高等优势受到广泛关注[11]。据报道,由微生物产生的20 000 多种活性物质中近一半来源于放线菌[12]。但目前放线菌应用于黄瓜疫病防治的报道还比较少见。研究采用平板稀释法[13-14]、平板对峙法[15-16]等从土壤中筛选到5 株对黄瓜疫霉菌有较好拮抗作用的放线菌株,并对拮抗作用最强的菌株No.2 做了发酵液的初步拮抗试验及生理生化特性的研究,以期为黄瓜疫病的生物防治提供基础。
1 材料与方法
1.1 试验材料
试验于2011~2013年进行。黄瓜疫霉菌TX-8(Phytophthora melonis)由湖南农业大学植物保护学实验室提供。土壤样品分别从贵州黄果树国家重点风景名胜区、湖南新宁崀山风景区、张家界国家森林公园收集200~250 g,放置在4℃冰箱保存。
1.2 试验方法
1.2.1 土壤放线菌的分离 将土壤样品干燥、研磨后,采用平板稀释法分离。称量10 g 土样装入含90 m L 无菌水的300 m L 锥形烧瓶中,用小玻璃珠均匀振荡30 min,即为10-1稀释液。静置数秒后,以10-1稀释液为母液依次制备10-2~10-6稀释液。分别取0.1 m L 各浓度稀释液滴加到高氏一号培养基上28℃倒置培养,设3 次重复。
1.2.2 拮抗放线菌的筛选 采用平板对峙法。将直径为7 mm 的黄瓜疫霉菌块放置于PDA 平板中央,菌块四周对称接种平板稀释法分离得到的放线菌,28℃倒置培养。7 d 后观察抑菌带长度,保存拮抗作用明显的菌株。
1.2.3 发酵液对黄瓜疫霉菌的拮抗作用 将上一步保存的菌株接种到高氏一号培养基上,28 ℃、180 r/m in 在摇床上培养7 d。培养液用0.22 μm 细菌滤液器过滤。取5 m L 滤液与20 m L 马铃薯葡萄糖琼脂(PDA)培养基混匀后倒板,平板中央放置直径为7 mm 病原菌,放入28℃温箱倒置培养,以无菌水处理作为对照,每组3个重复。抑制率计算公式如下:
病原菌菌丝直径=交叉垂直直径的平均值
抑制率(%)=(对照菌落直径-处理菌落直径)/对照菌落直径×100
1.2.4 抑菌谱测定 以拮抗效果最好的放线菌为材料,将直径为7 mm 的黄瓜疫霉病菌块,放置在PDA平板中央,两边对称接种拮抗菌置于28℃温箱培养6~8 d。采用相同方法对水稻瘟稻病菌(Magnaporthe oryzae)、柑橘炭疽病菌(Colletotrichum gloeosprioides)、烟草黑胫病菌(Phytophthora parasitica var.nicotianae)、油菜菌核病菌(Sclerotinia sclerotiorum)、辣椒疫霉菌(Phytophthora capsici)进行抑菌测定。
1.2.5 拮抗菌的鉴定 (1)菌落形态和培养特征鉴定。将供试菌株划线接种在多种基础固体培养基上于28℃恒温箱培养,分别在5、7、10、14 d 时于光学显微镜下观察拮抗菌的形态、气生菌丝、基质菌丝和有无色素;观察孢子的形态、特征及是否有横向断裂横隔。(2)生理生化鉴定。参照《链霉菌鉴定手册》分别对拮抗菌进行碳源利用、淀粉水解、明胶液化、牛奶胨化和凝固、纤维素上生长、硫化氢的生成等各项试验。(3)分子生物学鉴定。采用改良的SDS 法提取放线菌的基因组DNA,采用16S rRNA 通用引物进行PCR 反应,正向引物27F:5’-AGAGTTTGATCCTGGCTCAG-3’,反向引物1 492R:5’-GGTTACCTTGTTAC GACTT-3’。PCR 反应体系(20 μL)为10×PCR Buffer 2 μL,1.25 mmol/L dNTPs 0.8 μL,引物各0.5 μL,DNA 模板1 μL,TaqDNA 酶0.5 μL,用去离子水补足至20 μL。PCR 扩增条件为94℃5 m in;94℃40 s,51℃40 s,72℃90 s,30 次循环;72℃5 m in。PCR 产物胶回收后连入pGM-T 载体,并转入TOP10 感受态细胞。挑选单菌落进行菌液PCR 鉴定后送上海生工生物工程股份有限公司测序。所得序列在NCBI 中进行BLAST分析比对,利用Mega5 软件构建系统进化树。
2 结果与分析
2.1 拮抗放线菌的筛选
收集土壤样品经过处理后,采用稀释法分离得到放线菌菌株106 株,细菌菌株126 株。采用平板对峙法,以黄瓜疫霉菌为指示菌进行拮抗活性测定,获得26 株对黄瓜疫霉菌有拮抗作用的菌株,占总菌株的11.2%,其中抑菌带达到5 mm 及以上的拮抗菌有5 株。
2.2 发酵液对黄瓜疫霉菌的拮抗作用
对上一步筛选到的5个菌株发酵培养后,5 倍稀释发酵滤液进行抑菌活性检测(表1)。结果发现2 号菌株对黄瓜疫霉菌的抑制率高达76%(图1)。
2.3 抑菌谱检测
为进一步研究2 号菌的生物防治价值,采用对峙法对其他病原菌进行拮抗效果测定。其中,对烟草黑胫病菌、辣椒疫霉病菌、油菜菌核病菌、柑橘炭疽病菌和稻瘟病菌等都表现出不同程度的拮抗效果,抑菌率为55%~75%。
2.4 拮抗菌的分离鉴定
2.4.1 形态特征 2 号菌在高氏一号培养基上最初呈白色,7 d 后菌落呈烟灰色(图2),单菌落圆形,表面干燥。通过光学和电子显微镜观察到孢子丝长而直,边缘有成丛的趋势,不产生螺旋孢子丝,孢子柱形或长圆形,表面光滑,不透明,常在气生菌丝上形成长孢子链(图3)。
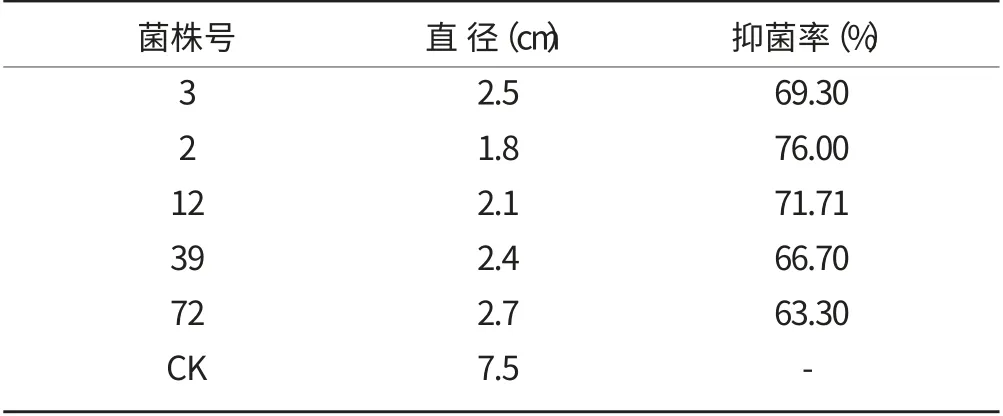
表1 有效菌株对黄瓜疫霉菌的抑制作用

图1 2 号菌株对黄瓜疫霉菌的抑制效果
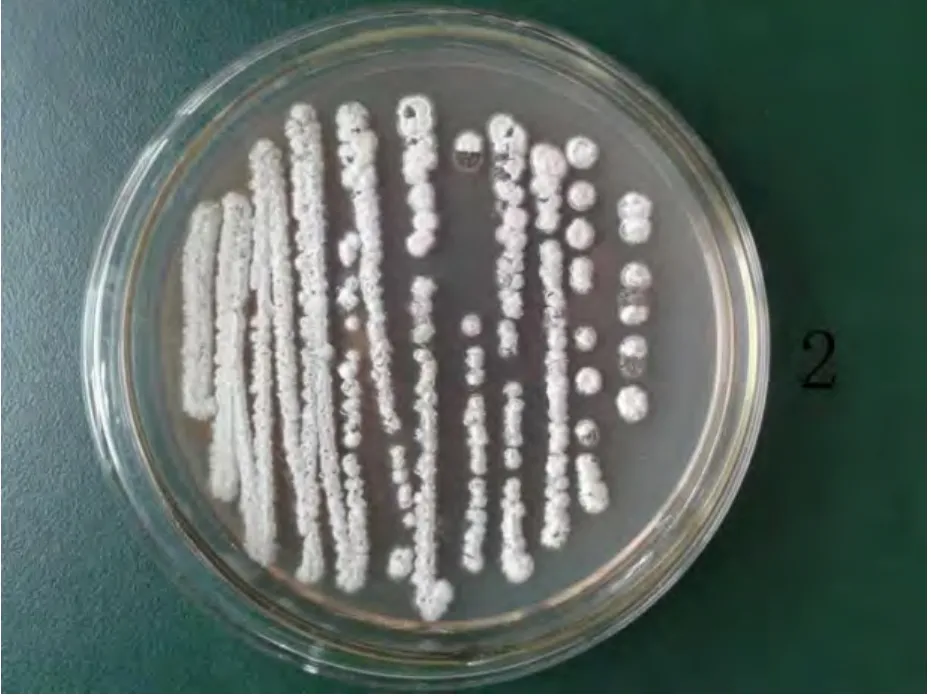
图2 拮抗菌株2 号菌的培养特征

图3 电镜下2 号菌的孢子形态
2.4.2 培养特征 不同培养基上2 号菌气生菌丝颜色不一致,在高氏一号培养基上长时间生长后菌丝变厚,呈烟灰白。在察氏、PDA 培养基上气生菌丝分别呈灰色、白色,有可溶性色素(表2)。

表2 各类培养基上拮抗菌株2 号菌的培养特征
2.4.3 生理生化特性 对2 号菌株的生理生化特性测定结果表明(表3),该菌株能利用D-半乳糖、乳糖、甘露糖、山梨糖、麦芽糖、D-木糖、蔗糖,但不能利用鼠李唐、山梨醇、甘露醇,对L-阿拉伯糖的利用还有待进一步确认;2 号菌株能使明胶液化,不能分解纤维素,但能在纤维素培养基上生长,淀粉水解能力较强,不能使牛奶胨化凝固,不产生硫化氢,能产生过氧化氢酶,吲哚试验中未出现红色环状物。
2.4.4 分子生物学鉴定 2 号菌株16S rDNA 扩增获得一条1 500 bp 左右的单一带,测序结果与NCBI 数据库进行对比,选取10 株模式链霉菌属菌株用Mega5 软件构建系统进化树(图4),结果显示,2 号菌株与绛红褐链霉菌(S. purpeofuscus)在同一分支,同源性高达99%。同时结合培养特征习性、生理生化特征分析及分子测定结果。

表3 2 号菌株的生理生化特征
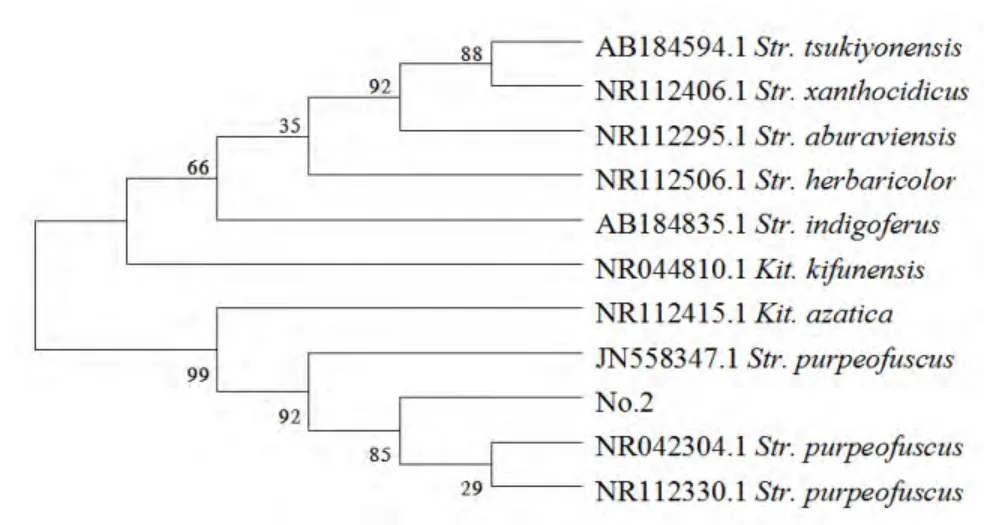
图4 16S rDNA 序列分析构建的系统发育树(邻近法)
3 结论与讨论
黄瓜疫病俗称死藤、瘟病等,在黄瓜整个生育周期均可发生。此病常造成黄瓜大面积死亡,轻者减产30%~40%,严重时甚至绝收。目前,对黄瓜疫病的防治主要以化学防治为主,但其对人畜的毒副作用和残留问题至今难以有效解决。为解决化学药剂带来的诸多问题,生防菌对植物病原菌的抑制研究已成为热点。目前,已发现许多对植物病害具有防治作用的生防细菌,其中以假单胞杆菌[17](Pseudomonas spp.)、芽孢杆菌[18-19](Bacillus spp.)和链霉菌[20-21](Streptomyces spp.)等居多。由于国内外对黄瓜疫病的生防菌研究较少,在众多已发现的生防菌中,目前仅发现华丽黄链霉菌[22](Streptomyces flaveus)、枯 草 芽 孢 杆 菌[23](Bacillus subtilis)等少数菌株对黄瓜疫霉菌有较好抑制作用。
研究通过平板对峙法及发酵液抑菌试验,从土壤中筛选到5 株对黄瓜疫霉菌有较好拮抗作用的放线菌株,其中拮抗菌No.2 对黄瓜疫霉菌表现出最强的拮抗活性,发酵液稀释5 倍后对病菌菌丝生长抑制率仍高达76%。通过形态特征、生理生化、16S rDNA 分子鉴定等方法,发现No.2 菌株具有典型的链霉菌属特征,初步确定为绛红褐链霉菌(Streptomyces purpeofuscus)。目前,还未发现有将绛红褐链霉菌用于黄瓜疫病防治方面的报道,表明No.2 是一株新发现的对黄瓜疫霉菌具有较好防效的放线菌株。作为应用到生产中最早的生防菌[24],放线菌及其代谢产物已经成为农药研发的新主体之一[25]。目前,拮抗菌No.2还只进行了发酵液的一些抑菌试验及生理生化特性的试验,要应用到生产及新农药的研发中还需进一步研究。
[1]何春玉.高原黄瓜疫病的发生及防治措施[J].北方园艺,2007,(11):196-196.
[2]林兴祖,冯健敏.海南冬种黄瓜疫病的发生及其防治[J].植物医生,2008,(6):13-14.
[3]沙锦文,王学平,杨玉洁,等.沿江地区春季黄瓜疫病的发生与防治[J].上海蔬菜,2005,(2):51-52.
[4]田东蓉,胡小朋.黄瓜疫病的发生与综合防治[J].北方园艺,2008,(8):204-204.
[5]杨泓威,易图永,雷 颖,等.丁子香酚对黄瓜疫霉菌的室内毒力测定[J].湖南农业科学,2012,(3):68-70.
[6]CabaasR,Castellá G,AbarcaM L,etal.Thiabendazole resistanceand mutations in theβ-tubulin gene of Penicillium expansum strains isolated from apples and pears with blue mold decay[J].FEMS Microbiology Letters,2009,297(2):189-195.
[7]Banno S,Fukumori F,Ichiishi A,et al.Genotyping of benzimidazoleresistant and dicarboximide-resistant mutations in Botrytis cinerea using real-time polymerase chain reaction assays[J].Phytopathology,2008,98(4):397-404.
[8]潘朝勃,李其利,莫贱友,等.杧果炭疽菌拮抗细菌的筛选鉴定及其防病效果[J].植物保护学报,2013,40(006):517-522.
[9]高小宁,陈金艳,黄丽丽,等.油菜菌核病内生拮抗细菌的筛选及防病作用研究[J].农药学学报,2010,(2):161-167.
[10]于 婷,尚玉珂,李艳芳,等.短小芽孢杆菌BSH-4抗菌物质的提取及其特性[J].植物保护学报,2009,(1):65-69.
[11]史 册,韩 梅,张一鸣,等.人参病原菌拮抗放线菌的分离筛选与鉴定[J].生物技术通报,2014,(9):102-108.
[12]Demain A L,SanchezS.Microbialdrugdiscovery:80 yearsofprogress[J].The JournalofAntibiotics,2009,62(1):5-16.
[13]周德庆.微生物学实验手册[M].上海:上海科学技术出版,1986:208-210.
[14]方中达.植病研究方法(第三版)[M].北京:中国农业出版社,1998:243-245.
[15]周棱波,黎定军,陈 武,等.烟草赤星病拮抗菌的筛选[J].湖南农业科学,2011,(7):100-101.
[16]易图永,高必达,何 昆,等.水稻纹枯病菌生防细菌的筛选[J].湖南农业大学学报,2000,26(2):116-118.
[17]Zhou T,Chen D,Li C,et al.Isolation and characterization of Pseudomonas brassicacearum J12 as an antagonist against Ralstonia solanacearum and identification of its antimicrobial components[J].MicrobiologicalResearch,2012,167(7):388-394.
[18]黎志坤,朱红惠.一株番茄青枯病生防菌的鉴定与防病定殖能力[J].微生物学报,2010,(3):342-349.
[19]Tan S,Jiang Y,Song S,et al.Two Bacillus amyloliquefaciens strains isolated using the competitive tomato root enrichmentmethod and their effects on suppressing Ralstonia solanacearum and promoting tomato plantgrowth[J].Crop Protection,2013,43:134-140.
[20]Tan H,Zhou S,Deng Z,et al.Ribosomal-sequence-directed selection for endophytic streptomycete strains antagonistic to Ralstonia solanacearum to control tomato bacterial wilt[J].Biological Control,2011,59(2):245-254.
[21]K berl M,Ramadan E M,Adam M,et al.Bacillus and Streptomyces were selected as broad-spectrum antagonists against soilborne pathogens from arid areas in Egypt[J].FEMSMicrobiology Letters,2013,342(2):168-178.
[22]张 涛.黄瓜疫霉菌生防菌的筛选与培养基优化[D].长沙:湖南农业大学,2012.
[23]伍善东,刘冬华,郭照辉,等.黄瓜疫病菌拮抗细菌的分离及鉴定[J].安徽农业科学,2014,42(20):6692-6693.
[24]熊仕俊,孙成龙,施 闯,等.番茄青枯病菌拮抗放线菌的筛选及鉴定[J].北方园艺,2014,(5):114-117.
[25]Thumar JT,Dhulia K,Singh SP.Isolation and partialpurification ofan antimicrobial agent from halotolerant alkaliphilic Streptomyces aburaviensis strain Kut-8[J].World Journal of Microbiology and Biotechnology,2010,26(11):2081-2087.

