脉冲激光沉积NiCo2S4薄膜及其电化学特征
刘家斌 张 辉 崔艳华*, 刘效疆*, 刘敬松
(1中国工程物理研究院电子工程研究所,绵阳 621000)
(2西南科技大学材料科学与工程学院,绵阳 621000)
近年来,锂离子电池由于在大规模储能和新能源汽车领域具有巨大应用前景而受到广泛的关注[1]。许多研究者都致力于探索新的电极材料以此来提高锂离子电池的能量密度和倍率性能。在探索新型锂离子电池电极材料的过程中,过渡金属硫化物如 NiS[2-4],CoS[5-7],MoS2[8]等由于其相对较高的理论容量和相对低廉的价格受到了广泛的关注,比如NiS具有590 mAh·g-1的容量,比目前商用的负极碳材料容量大很多。然而,大多数过渡金属硫化物由于具有较低的导电性以及在嵌锂和脱锂过程中会发生较大的体积变化,导致结构退化严重;使得材料的电化学性能快速下降,从而极大的限制了其在锂离子电池中的应用[9-10]。相对于二元过渡金属硫化物而言,三元或四元的金属硫化物,如CoSbS[11],Cu2ZnSnS4[12-15]和 CuInZnS[16],由于其本身较高的理论容量,且多种过渡金属的结合可能发展出更利于锂离子迁移的物质结构并提高硫化物的电导率,从而可能提供更高的电化学活性,因此可能比二元金属硫化物拥有更好的电化学性能。最近NiCo2S4[17-19]作为一种超级电容器电极材料得到广泛报道,由于其物质结构中具有两种不同的过渡金属元素,因此比二元金属硫化物具有更丰富的氧化还原反应和更好的导电性。然而目前尚无NiCo2S4作为锂离子电池电极材料的报道,结合其良好的导电性,我们很容易联想到其可能在锂离子电池中也有比二元硫化物更好的电化学性能,因此,研究NiCo2S4在锂离子电池中的电化学性能及其电化学反应机理是十分必要的。
激光脉冲沉积方法近年来多用于锂离子电池的材料制备,一方面可以制备用于全固态薄膜锂离子电池的电极材料,另一方面由于将电化学活性物质制备成纳米薄膜能够有效降低内阻,且无需添加导电剂和粘结剂等其他成分,更便于了解材料本身的电化学行为特征[20],因此常用于研究材料本身的电化学反应机理。本文采用了脉冲激光沉积法制备了纳米结构的NiCo2S4薄膜电极,测试了NiCo2S4薄膜作为锂离子电池电极材料的电化学性能,并利用非原位高分辨率透射电子显微镜和选区电子衍射对其结构进行了表征,探索了NiCo2S4薄膜电化学反应机理。
1 实验部分
1.1 样品制备
将 nNi∶nCo∶nS=1∶2∶4.2 的 Ni粉、Co 粉和 S 粉(Alfa Aesar,均为 99.99%,S过量是为了补充 S的损失)经过研磨均匀后称取混合物1.5 g,压成直径为13 mm的靶。另外采用不锈钢片作为基片(1 cm×1 cm),基片与靶距离为38 mm,激光与靶表面成45°入射角。沉积过程中基片温度为200℃。沉积后原位退火1 h。 355 nm 激 光 由 Nd:YAG(DCR-150,Spectra Physics)产生的1 064 nm基频经三倍频后获得,重复频率 10 Hz,脉宽 10 ns,能量密度约为 2 J·cm-2,沉积时间为 0.5 h。
1.2 薄膜表征
薄膜的质量用全自动电子天平(Sartorius,BP-211D)测量基片在沉积前后的质量差来确定。薄膜的晶体结构采用X射线衍射分析 (XRD,Bruker D8 ADVANCE)来表征;薄膜形貌采用扫描电子显微镜SEM(Cambridge S-360)进行表征。薄膜放电和充电后的成份采用JEOL 2010透射电子显微镜表征测量,其中TEM加速电压为200 kV。
1.3 电化学性能测试
电化学测量采用双电极系统(循环伏安测试采用三电极系统),其中制备的薄膜作为工作电极,锂片作为对电极和参比电极,电解液为1 mol·L-1LiClO4/EC(碳酸乙烯酯)+DMC(碳酸二甲酯))(体积比 1∶1,国泰华荣)。电池的装配在干燥的手套箱(MB-BL-1)中操作。恒电流充放电测试在LAND电池测试系统 (测试精度,99%)(武汉金诺电子有限公司)上进行,充放电条件:电压范围 0~3.0 V,电流密度 3 μA·cm-2。 循环伏安测试采用电化学工作站(上海辰华仪器有限公司),电压范围 0~3.0 V,扫描速率 0.1 mV·s-1。
2 结果与讨论
图1是利用脉冲激光沉积技术制备的NiCo2S4薄膜的 XRD 图,从图中可以看出,在 26.8°、31.5°、38.3°、50.4°和 55.3°都出现了明显的 NiCo2S4相的衍射峰,这表明通过脉冲激光法制备的薄膜组分主要为纯相的NiCo2S4,并没有其他明显的杂质衍射峰出现。
图2(a)和(b)分别是原始NiCo2S4薄膜表面和截面的非原位扫面电镜图。从(a)图中可以看出通过脉冲激光法制备的薄膜比较致密,表面比较平整,没有出现裂缝。在薄膜的表面出现了部分的颗粒可能是由脉冲激光沉积技术本身的缺陷所导致的。从(b)图中可以看出,薄膜的厚度大约为258 nm,且薄膜与基片之间的结合比较紧密。
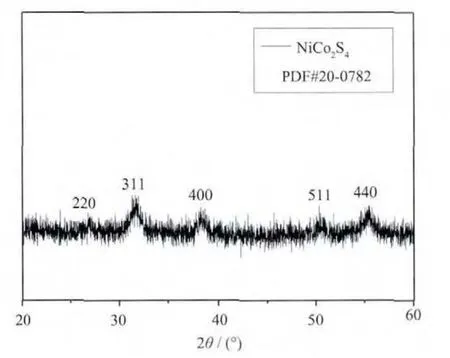
图1 NiCo2S4薄膜的XRD图Fig.1 XRD pattern of NiCo2S4 thin film
图 3为NiCo2S4薄膜在0~3.0 V范围间的循环伏安特性曲线,扫描速率为 0.1 mV·s-1,开路电压为2.90 V。从循环伏安图中可以看出NiCo2S4薄膜在放电过程中出现了 1.4、0.8、0.22 V 的 3 个还原峰,在充电过程中出现了 1.9,1.0 和 0.45 V 的 3 个与还原峰相对应的氧化峰,表明NiCo2S4薄膜的放电过程和充电过程都是分步骤进行的。首次放电过程中,经过1.4、0.8 和 0.22 V 处 的 3 个 还 原 过 程 ,Li逐 步 与NiCo2S4薄膜反应,最终可能生成Li2S、Ni和Co;而在首次充电过程中, 出现 1.9,1.0 和 0.45 V 的 3 个氧化反应过程,最终可能生成CoS和NiS,但是在充放电过程中具体的电化学反应比较复杂,需要进一步研究确定。在第二次到第三次循环中,NiCo2S4薄膜3个还原峰、氧化峰位置几乎一致,表明从第二次循环后,NiCo2S4薄膜具有良好的循环性能。在首次循环过程中,由于SEI膜的生成和Co的三价变成二价导致了一定的不可逆容量损失。

图2 原始NiCo2S4薄膜的表面(a)和截面(b)的非原位扫描电镜图Fig.2 Surface(a)and cross-sectional(b)ex situ SEM images of NiCo2S4 thin film

图3 NiCo2S4薄膜前3圈循环伏安曲线Fig.3 First three CVs of NiCo2S4 thin film
图4 是NiCo2S4薄膜作为锂电池电极在前5次的充放电曲线图,循环电压范围为0~3.0 V。首次放电曲线在1.40和0.8 V附近都出现了明显的放电平台,很好的对应了循环伏安曲线中的2个还原峰。同时首次的放电比容量达到698 mAh·g-1,非常接近NiCo2S4理论容量 (704 mAh·g-1),由此可以推断出NiCo2S4在首次放电过程中几乎完全分解,生成了Li2S、Ni和Co。第一次充电过程中在1.8 V有1个平台,对应于Li2S的分解和Ni、Co金属颗粒被氧化,除此之外并没有明显的充电平台,这可能是由于动力学原因导致的。第二次以后的放电曲线同样在1.4和0.8 V出现了2个明显的平台,但是与第一次放电平台相比,这2个平台变得更加倾斜,出现了一定的容量损失。此后的充放电曲线几乎一致,表现出了良好的循环性能,此外第2次开始到第5次放电容量趋于稳定,保持在 365 mAh·g-1。
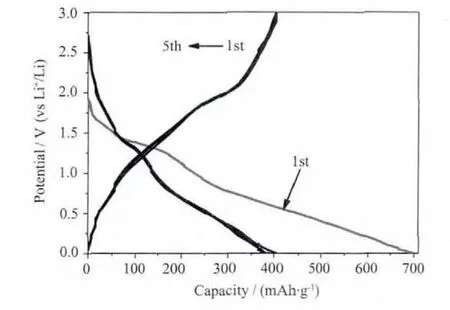
图4 NiCo2S4薄膜电极前5圈的恒流放电/充电曲线Fig.4 First five charge-discharge profiles of NiCo2S4 thin film

图5 NiCo2S4薄膜,NiS和CoS薄膜电池前200圈循环性能对比图Fig.5 Cycling performance of NiCo2S4,NiSand CoSthin films
为了对比NiCo2S4薄膜和NiS与CoS薄膜的循环性能,我们在与NiCo2S4薄膜相同条件下制备了NiS与CoS薄膜。图5是NiCo2S4、NiS和CoS薄膜前200次放电容量与循环次数的关系图。NiS和CoS薄膜是在与NiCo2S4薄膜相同条件下测试的。从图中可以看出NiCo2S4薄膜首次放电到第二次放电过程中容量衰减较大,这可能是首次放电过程中电解液分解生成不可逆的SEI层所导致的,并且原始薄膜中的三价Co只能回到二价,因此带来了不可逆容量损失。然后放电容量在2次循环之后趋于稳定,保持在365 mAh·g-1,显示出很好的可逆性。而且与二元硫化物CoS和NiS的薄膜相比,NiCo2S4薄膜有更好的循环性能和较大的可逆容量。根据之前文献报道[21-24],其原因可能是纳米复合材料中的LinX(n=1 or 2,X=F,O or S)和金属之间的晶界可以储存多余的锂,此外复合材料中的晶界要比单一体系多,使得锂离子的传输更容易。NiCo2S4薄膜的充放电曲线和循环性能图可以表明,NiCo2S4薄膜比单一体系硫化物具有更好的电化学性能,可以被用来作为锂离子电池的负极材料。
为了研究NiCo2S4薄膜的锂电化学反应机理,我们通过非原位TEM研究了NiCo2S4薄膜在第一次循环中薄膜成份的变化。图6(a)(b)是NiCo2S4薄膜首次放电至0 V后的非原位TEM高分辨像和选区电子衍射图。图中可以看到明显的晶格条纹,而电子衍射花样是由一些离散的点组成的衍射环,经过标定可得,放电后的薄膜主要由Ni(JCPDSNo.4-850)、Co(JCPDSNo.5-7727)和 Li2S(JCPDSNo.23-369)构成。这个结果说明放电到0 V后,NiCo2S4发生了分解,形成了Ni、Co金属颗粒和Li2S的混合物。

图6 NiCo2S4薄膜放电到0 V时的(a)非原位TEM高分辨和(b)和选区电子衍射图Fig.6 Ex situ high resolution TEM image(a)and SAED(b)of NiCo2S4 thin film discharging to 0 V

图7 NiCo2S4薄膜充电到3 V时的(a)非原位TEM高分辨和(b)和选区电子衍射图Fig.7 Ex-situ high resolution TEM image(a)and SAED(b)of NiCo2S4 thin film charging to 3.0 V
同理,图7(a)(b)是NiCo2S4薄膜首次充电至3.0 V时薄膜的高分辨像和选区电子衍射图。从高分辨像中可以看到,经过放电-充电后的NiCo2S4薄膜生成了CoS和NiS。选区电子衍射图经过标定可得,充电后的薄膜主要由NiS(JCPDS No.12-41)和CoS(JCPDSNo.65-407)组成,一系列的多晶衍射环可以归属于CoS和NiS不同的晶面。这说明了经过充电后薄膜变成了CoS和NiS的混合物。基于以上高分辨率透射电子显微镜和选区电子衍射的结果,我们可以得出在0~3.0 V之间充放电过程中NiCo2S4薄膜发生的如下电化学反应:

从循环伏安图和恒流充放电循环图中可以得出,首次循环后的充放电容量和平台基本保持不变,说明发生了相同的可逆氧化还原过程,对应于NiS和CoS复合薄膜的可逆分解与生成,且生成的NiS和CoS复合薄膜比单一的NiS或CoS薄膜具有更高的放电容量和更好的循环性能。
3 结 论
采用脉冲激光溅射Ni,Co和S粉末的混合靶成功制备了用于锂离子电池的NiCo2S4薄膜电极材料。该NiCo2S4薄膜的厚度约为258 nm,首次放电容量为 698 mAh·g-1,200次循环之后的容量为 365 mAh·g-1。充放电测试、循环伏安曲线和ex situ TEM表征结果证实了NiCo2S4薄膜首次放电过程中和Li发生电化学反应生成Li2S、Ni和Co,在后续的循环过程中则发生NiS和CoS复合薄膜可逆分解与生成,而且NiS和CoS复合薄膜表现出了比单一的NiS或CoS薄膜更高的放电容量和更好的循环性能。
[1]Tarascon JM,Armand M.Nature,2001,414:359-367
[2]Geng H,Kong S F,Wang Y.J.Mater.Chem.A,2014,2:15152-15158
[3]Ruan H C,Li Y F,Qiu H Y,et al.J.Alloys Compd.,2014,588:357-360
[4]Mi L W,Chen Y F,Wei W T,et al.RSC Adv.,2013,3:17431-17439
[5]Gu Y,Xu Y,Wang Y.ACSAppl.Mater.Inter.,2013,5:801-806
[6]Wang Q H,Jiao L F,Du H M,et al.J.Mater.Chem.,2011,2:327-329
[7]Wang Y,Wu JJ,Tang Y F,et al.ACSAppl.Mater.Interfaces,2012,4:4246-4250
[8]Sen U K,Mitra S.J.Solid State Electrochem.,2014,18:2701-2708
[9]Zhang Z,Zhou C K,Huang L,et al.Electrochim.Acta,2013,114:88-94
[10]Liu S Y,Lu X,Xie J,et al.ACS Appl.Mater.Interfaces,2013,5:1588-1595
[11]Lee J O,Seo J U,Song J H,et al.Electrochem.Commun.,2013,28:71-74
[12]Li J J,Shen J,Li Z Q,et al.Mater.Lett.,2013,92:330-333
[13]Yang X,Xu J,Xi L J,et al.J.Nanopart.Res.,2012,14:931
[14]Zhou W H,Zhou Y L,Feng J,et al.Chem.Phys.Lett.,2012,546:115-119
[15]Yin X S,Tang C H,Chen M H,et al.J.Mater.Chem.A,2013,1:7927-7932
[16]Tang X S,Yao X Y,Chen Y,et al.J.Power Sources,2014,257:90-95
[17]Wan H Z,Jiang J J,Yu J W,et al.CrystEngComm,2013,15:7649-7651
[18]Yang JQ,Guo W,Li D,et al.Electrochim.Acta,2014,144:16-21
[19]Chen H C,Jiang J J,Zhang L,et al.J.Power Sources,2014,254:249-257
[20]ZHANG Hua(张华),ZHOU Yong Ning(周永宁),WU Xiao Jing(吴晓京),et al.Acta Phys.-Chim.Sin.(物理化学学报),2008,24:1287-1291
[21]Jamnik J,Maier J.Phys.Chem.Chem.Phys.,2003,5:5215-5220
[22]Zhukovskii Y F,Kotomin E A,Balaya P,et al.Solid State Sci.,2008,10:491-495
[23]Yu X Q,Sun J P,Tang K,et al.Phys.Chem.Chem.Phys.,2009,11:9497-9503
[24]Dai H Q,Zhou Y N,Sun Q,et al.Electrochim.Acta,2012,76:145-515

