基于阻滞扩散模型估算柴油脱硫吸附剂的适宜孔径分布
许承志,郑美琴,熊莹,黄清明,陈晓晖
(1福州大学石油化工学院,化肥催化剂国家工程研究中心,福建 福州350002;2福州大学测试中心,福建 福州 350002)
引 言
车用燃油中含硫化合物不仅会损害发动机,其燃烧产生的SOx还是导致酸雨、雾霾等环境问题的主要原因[1]。从源头控制燃油中的硫含量已成为解决相关环境问题的最有效、最经济的手段。随着世界各国制定日益严格的环保法规,推进车用燃油的清洁化,如何经济高效地实现车用燃油的深度脱硫成为全社会关注的课题。
加氢脱硫(HDS)是目前工业上应用最广且较为成熟的燃油脱硫工艺,但HDS工艺对烷基苯并噻吩、二苯并噻吩、烷基二苯并噻吩以及其他多环有机硫化物的脱除效率低,要实现深度脱硫,需大幅度提高反应温度、氢气分压或者增大反应器体积、降低空速,使装置投资费用和操作费用大幅提高[2-3]。此外,随着原油储量的减少,高硫原油和重质原油的逐步开采,也必然导致脱硫成本的提高[4]。因此,开发非加氢脱硫技术已成为目前脱硫技术研发的 热点。
吸附法脱硫具有操作条件温和、氢耗小甚至不耗氢、脱硫效果好、烯烃不被饱和、容易放大实现工业化、可与现有的HDS工艺结合使用、投资和操作费用低等优点而被广泛关注,是最有希望实现零硫目标的脱硫方法[5-6]。目前已研究报道的吸附剂主要是将Cu、Ag、Ni、Ce等活性组分负载在分子筛[7-9]、活性炭[10-13]、SiO2和金属氧化物[2,14-15]以及MOF等[16-19]多孔载体上,活性组分主要分布在载体的多孔结构表面,载体的孔结构不仅直接影响着负载活性组分的分散,对吸附脱硫过程中的传质也有重要影响,但目前对燃油脱硫吸附剂及其载体适宜孔径分布的研究鲜有报道。
目前通过实验较难实现对吸附剂或催化剂适宜孔径分布的单因素分析,对分子在孔道内扩散以及适宜孔径分布的研究主要依靠数值模拟进行,已有较多的研究报道,但主要集中在气相反应或吸附过程,对柴油等复杂液相体系的研究仍然较少。本文通过色谱分析国II、国III、国IV标准0#柴油中的主要含硫组分,以苯并噻吩(BT)、二苯并噻吩(DBT)、4,6-二甲基二苯并噻吩(4,6-DMDBT)为模型化合物,基于简捷的阻滞扩散模型[20-21]和堆积孔模型[22]估算氧化铝基柴油脱硫吸附剂的适宜孔径分布范围,并与相应的实验数据对比分析,以期为柴油脱硫吸附剂孔径分布的调控提供指导,也为其他催化剂适宜孔径分布的估算提供借鉴。
1 实验材料和模型方法
1.1 材料与分析仪器
市售柴油(国Ⅱ、国Ⅲ、国Ⅳ)由中国石化加油站提供。柴油中的含硫组分采用Agilent GC6890色谱进行分析,色谱配备脉冲火焰光度检测器(PFPD)和火焰离子化检测器(FID)双检测器,色谱柱为HP-5 5% Penyl Methyl Siloxane(30 m×0.32 mm×0.25 μm)毛细管柱,分流比为10:1(国Ⅱ、国Ⅲ柴油)和1:1(国Ⅳ柴油),进样量为0.5 μl,色谱柱程序升温采用初始温度为50 ℃,保持1 min,以5.0℃·min-1的速率升温至260℃的程序进行。柴油中的总硫含量采用江苏江分电分析仪器有限公司提供的TS-3000型硫测定仪,通过紫外荧光法进行测定。
不同织构的氧化铝由拟薄水铝石(P-DF-03,由中国铝业股份有限公司山东分公司提供)通过水热改性、成型改性等不同的改性方法获得[23]。氧化铝的孔结构由美国FEI公司的TECNAI G2F20型场发射透射电子显微镜测定。氧化铝的孔结构参数采用美国Micromeritics公司ASAP 2020m型物理吸附仪测定,氧化铝的孔径分布采用N2脱附支数据,通过BJH模型计算得到。
1.2 阻滞扩散模型
采用何志敏等[20-21]提出的阻滞扩散模型,估算模型化合物在不同孔径的孔道内的扩散阻滞因子H

式中,Deff为溶质在孔道内的有效扩散系数,D∞为溶质在溶液主体中的扩散系数。同时考虑分子尺寸和形状,分子在微孔中的扩散阻滞因子H可按式(2)进行估算
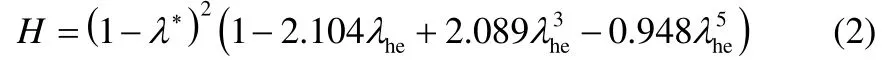
式中,λ∗= r∗/rp,λhe= rhe/rp,r∗为分子几何特性半径,rhe为分子的水力学当量半径,rp为孔道半径,采用式(3)~式(8)估算不同形状分子的r∗和rhe。
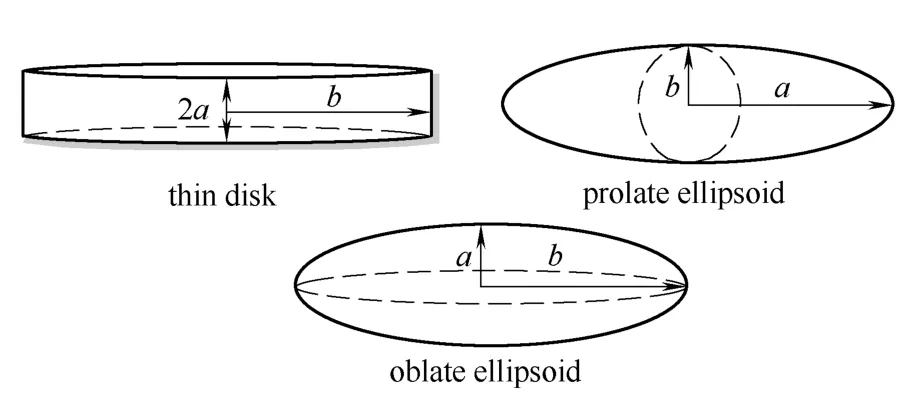
图1 不同形状分子的形状参数示意图 Fig.1 Shape parameters of molecules in different shapes
1.2.1 薄圆盘形分子

式中,a为薄圆盘的1/2厚度,b为薄圆盘的半径。
1.2.2 椭球形分子 椭球形分子按其轴比τ=a/b可分为长椭球形分子(τ>1)和扁椭球形分子(τ<1),其中a为椭球的半轴长,b为椭球的赤道半径,则长椭球形分子的几何特性半径和水力学当量半径的计算式如下

扁椭球形分子几何特性半径和水力学当量半径的计算式如下

圆球、细长棒形、柔性线团分子的几何特性半径和水力学当量半径的计算式可参考文献[21]。
1.3 堆积孔模型
氧化铝例样的TEM图如图2所示,由图可知本文所用的氧化铝的孔结构为类球形纳米粒子堆积而成的蠕虫状堆积孔结构,其比表面积S与平均孔径dp存在以下近似关系[22]

式中,ρ为氧化铝纳米颗粒的密度,本文所用的氧化铝的ρ约为1.4 g·cm-3。

图2 氧化铝的透射电镜图 Fig.2 TEM image of alumina
由图2可知该氧化铝样品的纳米粒子直径dn为10~25 nm,经式(10)计算得氧化铝的孔径dp为 2.34~5.85 nm,这与N2物理吸附测得氧化铝孔径主要分布在2.25~6.11 nm,平均孔径为4.56 nm的实验结果较吻合,采用平均孔径计算得到的比表面积220.0 m2·g-1也与实验测定值222.9 m2·g-1相近[23],因此堆积孔模型可用于估算氧化铝孔结构参数。
1.4 吸附脱硫性能测试
采用静态吸附表征不同孔结构氧化铝的吸附脱硫性能,剂油比为1 g吸附剂:30 ml国Ⅱ柴油,在60℃下水浴振荡吸附2 h,通过测定吸附前后柴油中的硫含量变化,计算吸附剂对柴油的脱硫率。
2 实验结果与讨论
2.1 不同标准0#柴油中的含硫化合物
本文所用市售国Ⅱ、国Ⅲ、国Ⅳ标准0#柴油的总硫含量分别为799.5、245.5、37.4 mg S·L-1,不同标准柴油中的含硫化合物组成如图3所示。由国Ⅱ柴油到国Ⅳ柴油,柴油中的总硫含量逐步降低,含硫化合物的组成也逐渐趋于单一,国Ⅳ柴油中主要含硫化合物为C2-DBT和C3-DBT,这是因为多烷基取代的含硫化合物上的烷基对硫原子的空间遮蔽作用,尤其是二苯并噻吩4、6位上的取代基,对硫原子与活性中心的相互作用具有很强的抑制作用,使其难以被加氢脱硫工艺脱除[24]。
2.2 含硫化合物在孔道内的扩散阻滞因子
根据不同标准柴油含硫化合物组成,选取苯并噻吩(BT)、二苯并噻吩(DBT)、4,6-二甲基二苯并噻吩(4,6-DMDBT)为模型化合物,DFT模型计算得到的分子外形尺寸如图4所示[25]。

表1 BT、DBT、4,6-DMDBT的外形参数、几何特性半径和水力学当量半径的取值 Table 1 Shape parameters, mean projected radius and hydrodynamically equivalents sphere radius of BT, DBT and 4,6-DMDBT
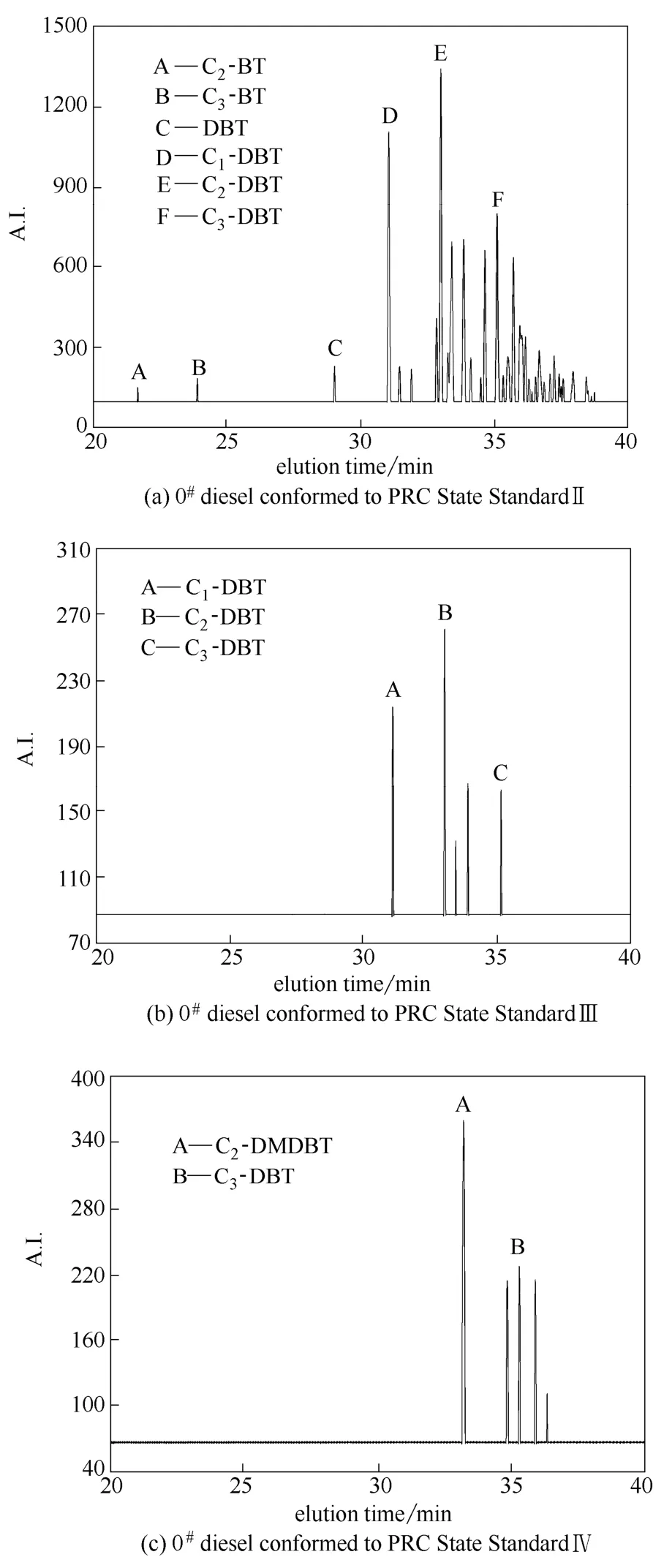
图3 不同标准0#柴油的GC-PFPD信号图 Fig.3 GC-PFPD signal diagrams of 0#diesel

图4 苯并噻吩、二苯并噻吩和4,6-二甲基二苯 并噻吩的分子外形尺寸 Fig.4 Molecular dimensions and shapes of BT, DBT, and 4,6-DMBT
由图4可知,含硫化合物分子呈扁平状,因此可将BT、DBT、4,6-DMDBT这3种模型分子的外形近似成薄圆盘或扁椭球,参数取值如表1所示。
分别按薄圆盘形分子和扁椭球形分子计算模型化合物在不同大小孔径d孔道内的扩散阻滞因子H如图5所示。
对比图5(a)、(b),可以看出将模型化合物分子视为薄圆盘形的阻滞因子略大于扁椭球形分子,例如将苯并噻吩(BT)视为薄圆盘形分子和扁椭球形分子,其在孔径为4 nm孔道内的扩散阻滞分别为0.251和0.294,这是因为将模型化合物分子视为薄圆盘形分子时,其分子体积偏大导致阻滞因子的估算值偏高,如将BT视为长方体、薄圆盘形、扁椭球形时其体积分别约为0.276、0.448、0.298 nm3。但不论是将模型化合物分子视为薄圆盘形分子还是扁椭球形分子,分子在孔道内的扩散阻滞因子均随孔道直径的增大而逐渐接近于1,即吸附剂平均孔径越大,含硫化合物在孔道内的扩散阻力越小。但结合堆积孔模型发现,吸附剂的比表面积与其平均孔径存在近似反比的关系,如图6所示,即平均孔径的增大亦会导致吸附剂比表面积的降低,进而 导致吸附活性位的减少。

图5 BT、DBT、4,6-DMDBT在不同孔径孔道内的 扩散阻滞因子 Fig.5 Hindered diffusion coefficients of BT, DBT and 4,6-DMDBT in different sizes pore

图6 氧化铝的比表面积与其平均孔径的变化关系曲线 Fig.6 Changing curve of specific surface area with average pore diameter of alumina support
在前期工作的基础上,参考馏分油加氢精制、重油加氢精制催化剂对适宜孔径分布的划分[26],将氧化铝的孔径分布划分为小于4 nm、4~10 nm(馏分油加氢精制催化剂)、10~20 nm(重油加氢精制催化剂)和大于20 nm 4个部分。结合阻滞扩散模型和堆积孔模型,对比分析发现在氧化铝的平均孔径为4~10 nm时,含硫化合物的扩散阻滞因子为0.24~0.65,而氧化铝的比表面积为100~250 m2·g-1,能较好地同时满足较低的扩散阻力和足够大的比表面积两个方面的要求,因此,推测4~10 nm为氧化铝基柴油脱硫吸附剂较适宜的孔径分布范围。
2.3 不同孔结构氧化铝的吸附脱硫性能
具有不同织构的氧化铝的4~10 nm范围内的孔面积占总孔面积的百分比与其吸附脱硫性能[23]的关系,如图7所示,二者总体呈正相关关系,初步推证氧化铝基脱硫吸附剂的适宜孔径分布范围为4~10 nm。相关度较差的主要原因是不同方法改性得到的氧化铝,其表面性质,如表面酸碱性、表面缺陷位等,也存在一定的差异,对氧化铝的吸附脱硫性能也有十分重要的影响,实验中难以实现氧化铝表面性质和孔结构单一因素的考察。

图7 氧化铝中4~10 nm范围内的孔面积占总孔面积的百分比与其对国Ⅱ柴油脱硫率的关系曲线 Fig.7 Desulfurization rate of 0#diesel comfored to PRC State Standard Ⅱ vs.percentage of pore area in range of 4—10 nm
结合上述模型计算结果以及不同孔结构氧化铝中4~10 nm范围内的孔面积占总孔面积的百分比与其吸附脱硫性能的正相关关系,可以初步推测氧化铝基柴油脱硫吸附剂较适宜的孔径分布范围为4~10 nm。
3 结 论
本文通过GC-PFPD色谱分析国Ⅱ、国Ⅲ、国Ⅳ标准0#柴油中的主要含硫组分,结合简捷的阻滞扩散模型和堆积孔模型,估算氧化铝基柴油脱硫吸附剂的适宜孔径分布,具体结论如下。
(1)GC-PFPD色谱分析结果表明,苯并噻吩(BT)、二苯并噻吩(DBT)及其烷基取代衍生物是0#柴油中的主要含硫化合物,C2-DBT、C3-DBT是国IV柴油中的主要含硫化合物。
(2)将BT、DBT、4,6-DMDBT 3种模型化合物近似为薄圆盘形或扁椭球形分子,结合阻滞扩散模型和氧化铝的堆积孔模型,发现当氧化铝的平均孔径为4~10 nm时,含硫化合物的扩散阻滞因子为0.24~0.65,而氧化铝的比表面积为100~250 m2·g-1,可同时满足较低的扩散阻力和足够大的比表面积,初步推测氧化铝基脱硫吸附剂的适宜孔径分布范围为4~10 nm。
(3)不同氧化铝的吸附脱硫性能表明,氧化铝中4~10 nm范围内的孔面积占总孔面积的百分比与其吸附脱硫性能呈正相关关系,相关度较差的原因是不同氧化铝载体的表面性质存在一定差异,初步推证氧化铝基脱硫吸附剂的适宜孔径分布范围为4~10 nm。
(4)鉴于本文所用的阻滞扩散模型和堆积孔模型均做了较多的简化,未考虑模型化合物与吸附剂之间的相互作用、溶液性质等对扩散的影响以及纳米粒子非球形度等对载体孔结构参数估算的影响,需结合上述参数对模型做进一步修正,但本文结论对氧化铝基脱硫吸附剂的孔结构调控有重要的指导意义,也为其他催化剂或吸附剂的孔结构调控提供借鉴。
符 号 说 明
a ——薄圆盘的1/2厚度或旋转椭球的半轴长
b ——薄圆盘的半径或旋转椭球的赤道半径
D——溶质的扩散系数,cm2·s-1
d ——直径,nm
H——扩散阻滞因子
r ——半径,nm
S ——比表面积,m2·g-1
λ ——溶质分子半径与孔半径比
ρ ——纳米颗粒密度,g·cm-3
τ ——旋转椭球的轴比
下角标
eff ——在孔道中的
he ——水力学当量
n ——纳米颗粒
p ——孔道
∞ ——在溶液主体中的
上角标
∗——几何特性
[1] Wang Z, Wu T, Shi G, Fu X, Tian Y, Feng Y, Wu X, Wu G, Bai Z, Zhang W.Potential source analysis for PM10 and PM2.5 in autumn in a northern city in China [J].Aerosol and Air Quality Research, 2012, 12: 39-48.
[2] Baeza P, Aguila G, Gracia F, Araya P.Desulfurization by adsorption with copper supported on zirconia [J].Catalysis Communications, 2008, 9 (5): 751-755.
[3] Song C.An overview of new approaches to deep desulfurization for ultra-clean gasoline, diesel fuel and jet fuel [J].Catalysis Today, 2003, 86 (1-4): 211-263.
[4] Shahadat Hussain A, Tatarchuk B J.Adsorptive desulfurization of jet and diesel fuels using Ag/TiOx-Al2O3and Ag/TiOx-SiO2adsorbents [J].Fuel, 2013, 107: 465-473.
[5] Chandra Srivastava V.An evaluation of desulfurization technologies for sulfur removal from liquid fuels [J].RSC Advances, 2012, 2 (3): 759-783.
[6] Song C, Ma X, Sprague M J, Subramani V.Deep desulfurization of hydrocarbon fuels [P]: US, 8158843.2012-04-17.
[7] Wang Wangyin (王旺银), Pan Mingxue (潘明雪), Qin Yucai (秦玉才), Wang Lingtao (王凌涛), Song Lijuan (宋丽娟).Effects of surface acidity on the adsorption desulfurization of Cu (Ⅰ)Y zeolites [J].Acta Physico-Chimica Sinica(物理化学学报), 2011, 27 (5): 1176-80.
[8] Xue M, Chitrakar R, Sakane K, Hirotsu T, Ooi K, Yoshimura Y, Feng Q, Sumida N.Selective adsorption of thiophene and 1-benzothiophene on metal-ion-exchanged zeolites in organic medium [J].Journal of Colloid and Interface Science, 2005, 285 (2): 487-492.
[9] Tang Huang (唐煌), Li Wangliang (李望良), Liu Qingfen (刘庆芬), Guan Lili (关莉莉), Song Jiaqing (宋家庆), Xing Jianmin (邢建民), Liu Huizhou (刘会洲).Mesoporous aluminosilicate adsorbent for adsorption desulfurization of diesel fuel [J].Science in China:Series B(中国科学: B辑), 2009, 39 (2): 176-182.
[10] Kim J H, Ma X, Zhou A, Song C.Ultra-deep desulfurization and denitrogenation of diesel fuel by selective adsorption over three different adsorbents: a study on adsorptive selectivity and mechanism [J].Catalysis Today, 2006, 111 (1/2): 74-83.
[11] Zhou A, Ma X, Song C.Liquid-phase adsorption of multi-ring thiophenic sulfur compounds on carbon materials with different surface properties [J].The Journal of Physical Chemistry B, 2006, 110 (10): 4699-4707.
[12] Wang Q, Liang X, Qiao W, Liu C, Liu X, Zhang R, Ling L.Modification of polystyrene-based activated carbon spheres to improve adsorption of dibenzothiophene [J].Applied Surface Science, 2009, 255 (6): 3499-3506.
[13] Yu Moxin (余谟鑫), Li Zhong (李忠), Xia Qibin (夏启斌), Wang Shuwen (王书文).Effect of thermal oxidation of activated carbon surface on its adsorption of dibenzothiophene [J].Journal of Chemical Industry and Engineering(China) (化工学报), 2007, 58 (4): 938-943.
[14] Watanabe S, Ma X, Song C.Selective sulfur removal from liquid hydrocarbons over regenerable CeO2-TiO2adsorbents for fuel cell applications [J].Prepr.Pap.-Am.Chem.Soc., Div.Fuel Chem., 2004, 49 (2): 511-513.
[15] Guo J, Janik M J, Song C.Density functional theory study on the role of ceria addition in TixCe1-xO2adsorbents for thiophene adsorption [J].The Journal of Physical Chemistry C, 2012, 116 (5): 3457-3466.
[16] Cychosz K A, Wong-Foy A G, Matzger A J.Liquid phase adsorption by microporous coordination polymers: removal of organosulfur compounds [J].Journal of the American Chemical Society, 2008, 130 (22): 6938-6939.
[17] Cychosz K A, Wong-Foy A G, Matzger A J.Enabling cleaner fuels: desulfurization by adsorption to microporous coordination polymers [J].Journal of the American Chemical Society, 2009, 131 (40): 14538-14543.
[18] Favre-RéGuillon A, SéVignon M, Rocault M, Schulz E, Lemaire M.Deep desulfurization of diesel feedstock by selective adsorption of refractory sulfur compounds [J].Industrial & Engineering Chemistry Research, 2008, 47 (23): 9617-9622.
[19] Zhao Shaoyun (赵少云), Chen Aiping (陈爱平), Liu Wei (刘伟), Chen Xiaoping (陈晓萍).Montmorillonite assembled with nano-SiO2-particles for gasoline desulfurization [J].Journal of Inorganic Materials(无机材料学报), 2006, 21 (4): 953-957.
[20] He Zhimin (何志敏), Yu Guocong (余国琮), Diego Barba.Effect of molecular dimension and shape on hindered diffusion of macromolecules in micropores [J].Journal of Chemical Industry and Engineering(China) (化工学报), 1993, 44 (2): 143-50.
[21] He Zhimin (何志敏).Theoretical effects of molecular dimension and configuration on effective diffusion coefficient of macromolecules in microporous membranes [J].Transactions of Tianjin University(天津大学学报), 1995, 1 (1): 42-47.
[22] Inoue M, Kominami H, Inui T.Synthesis of large pore-size and large pore-volume aluminas by glycothermal treatment of aluminium alkoxide and subsequent calcination [J].Journal of Materials Science, 1994, 29 (9): 2459-2466.
[23] Xiong Ying (熊莹).Study on the modification of mesostructured alumina for diesel desulfurization by adsorption [D].Fuzhou: Fuzhou University, 2014.
[24] Xiao J, Wang X, Chen Y, Fujii M, Song C.Ultra-deep adsorptive desulfurization of light-irradiated diesel fuel over supported TiO2-CeO2adsorbents [J].Industrial & Engineering Chemistry Research, 2013, 52 (45): 15746-15755.
[25] Moosavi E S, Dastgheib S A, Karimzadeh R.Adsorption of thiophenic compounds from model diesel fuel using copper and nickel impregnated activated carbons [J].Energies, 2012, 5 (10): 4233-4250.
[26] Li Guoyin (李国印), Zhi Jianping (支建平), Zhang Yulin (张玉林).Pore structure control of activated alumina [J].Chinese Journal of Inorganic Chemistry(无机化学学报), 2007, 23 (4): 563-568.

