血清癌胚抗原与晚期肺非小细胞鳞癌化疗疗效的关系
吴红波 张静 吴慧娟 陈丽娟 穆晓倩 赵艳秋
血清癌胚抗原与晚期肺非小细胞鳞癌化疗疗效的关系
吴红波 张静 吴慧娟 陈丽娟 穆晓倩 赵艳秋
目的 探讨血清癌胚抗原(CEA)变化与晚期肺非小细胞鳞癌化疗疗效的关系。方法 回顾性分析107例晚期肺非小细胞鳞癌(non-small cell lung carcinoma,NSCLC)患者的临床资料,符合入组标准的患者60例,按照RECIST评价标准,分为病情进展组(disease progression,PD组)、稳定组(disease stability,SD组)和病情好转(partial remission,PR及complete remission,CR)组。分别采用吉西他滨(gemcitabine,GP组)、紫杉醇(paclitaxel,PTX)、多西他赛进行治疗。统计分析3组患者血清癌胚抗原变化与NSCLC化疗疗效之间的关系。结果 (1)GP组、PTX组及多西他赛组临床缓解率分别为50.00%、65.00%及80.00%;(2)(PR及CR)组、SD组及PD组CEA变化水平升高例数分别为9、11及6例,降低例数分别为9、12及13例;(3)血清癌胚抗原的变化与NSCLC化疗疗效无显著相关性。结论 血清癌胚抗原的变化与NSCLC化疗疗效无显著相关,差异无统计学意义,不能作为晚期NSCLC化疗疗效的评判指标。
血清癌胚抗原;晚期非小细胞肺癌;化疗疗效
在我国,肺癌的临床发病率以及死亡率呈现逐年上升的发展趋势,其中肺非小细胞鳞癌(non-small cell lung carcinoma,NSCLC)占肺癌的85%,而且绝大多数患者在确诊的时候已经属于晚期。晚期肺非小细胞鳞癌的一个最为重要的治疗手段为全身化疗,其具有十分重要的地位[1]。临床上,选择一线化疗方案含铂化疗方案,肺癌患者生存期得到明显地延长,然而化疗带来的毒副作用及对患者生存质量的影响[2]。但目前对提前预测化疗疗效的指标较少。本研究主要探讨了血癌胚抗原的变化与晚期非小细胞肺癌化疗疗效的关系,现报道如下。
1 资料与方法
1.1 一般资料 回顾性分析了2010年10月~2014年4月入住郑州大学附属肿瘤医院的107例晚期NSCLC鳞癌患者的临床资料,选取符合入组条件的60例患者,其中吉西他滨(gemcitabine,GP)化疗组(n=20)、紫杉醇(paclitaxel,PTX)化疗组(n=20)及多西他赛化疗组(n=20)。60例患者中男39例,女21例;年龄范围52~78岁,平均年龄(66.09±4.39)岁;KPS(Karnofsky)评分范围为60~80分,平均分(71.32±6.55);病理类型:鳞癌40例,腺癌20例;X-Ray分型:中心型53例,周边型7例;临床分期:IIIA期24例,IIIB期21例,IV期15例。3组失访例数分别为1例、0例,死亡例数均为1例。3组患者在一般资料方面的差异均无统计学意义,具有可比性。
1.2 诊断标准[3]根据中华人民共和国卫生部制定的NSCLC的临床诊断标准。分期标准:根据国际抗癌联盟2009年制定的NSCLC分期系统。
1.3 入选标准 主要包括:(1)存在明确的病理诊断(非小细胞肺癌),年龄在50~80岁之间;(2)KPS>80分,预计生存期>3个月者;(3)心、肝、肾以及造血系统功能基本正常者;(4)在近期未接受过静脉中药注射治疗及化疗;(5)自愿签署知情同意书者。
1.4 排除标准 主要包括:(1)无确切病理诊断者;(2)预计生存期<3个月者;(3)并发心、肝、肾及造血系统等严重疾病者;(4)精神疾病患者及儿童、孕妇;(5)无法自愿签署知情同意书者。
1.5 化疗方案 吉西他滨组:吉西他滨(剂型为注射剂,武汉能仁医药化工有限公司,生产批号:H20133404)1.0g/m2,d1、d8;PTX组:(剂型为注射剂,哈药集团生物工程有限公司生产,批号:H20130219)静脉注射135~175mg/m2,d1;多西他赛组:(剂型为注射剂,北京协和药厂,批号:H20140223)静脉注射60~75mg/m2,d1;联合顺铂(DDP,cisplatin):(剂型为注射剂,浙江海强化工有限公司,批号:H20130328)静脉注射75mg/m2,d1。
1.6 临床疗效评价标准[4]主要包括:(1)完全缓解(complete remission,CR):全部目标病灶均完全消退;(2)部分缓解(partial remission,PR):基线条件下的最大直径之和减少在30%以上;(3)稳定(disease stability,SD):基线条件下的最大直径之和有所减少,但并未达到PR;(4)进展(disease progression,PD):基线条件下的最大直径之和至少增加20%或者有新病灶出现。临床疾病缓解率(%)=PR(%)+CR(%)。
1.7 血清癌胚抗原[5]均收集化疗第1周期前后的血清,本研究对于血清中的癌胚抗原水平含量,主要采取罗氏全自动电化学发光分析仪(罗氏诊断产品(上海)有限公司)进行测定,并加入诊断试剂和质控品,采取双盲法进行测定。洗液中的癌胚抗原以清蛋白浓度进行校正[3]。
1.8 观察指标 比较3组患者临床疗效及血癌胚抗原变化水平与NSCLC化疗疗效之间的相关关系、病灶数目及病灶直径。
1.9 统计学方法 应用SPSS17.0统计软件对统计所得的具体数据进行分析,正态计量资料采用“x±s”表示,组间比较采用t检验,计数资料比较用χ2检验;P<0.05为差异有统计学意义。
2 结果
2.1 患者各组化疗方案疗效 GP组、PTX组及多西他赛组临床缓解率分别为50.00%、65.00%及80.00%。前2组临床缓解率均显著低于多西他赛组,差异具有统计学意义(P<0.05)。见表1。
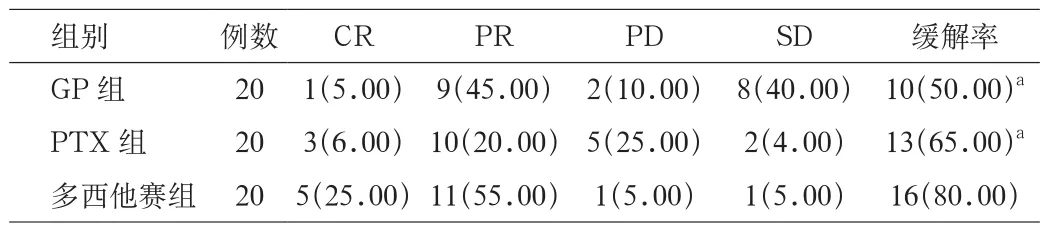
表1 3组临床缓解率比较[n(%)]
2.2 血清癌胚抗原变化与NSCLC化疗疗效的相关性 经分析,血清癌胚抗原变化与NSCLC化疗疗效无显著相关性(P>0.05)。见表2。

表2 CTCs与NSCLC化疗疗效的相关关系(n)
2.3 3组病灶数目及病灶直径对比 GP组灶数目及病灶直径分别为(2.53±0.28)个与(4.30±0.38)cm,PTX组分别为(2.66±0.42)个与(4.02±0.31)cm,多西他赛组分别为(2.18±0.11)个与(4.45±0.52)cm,3组病灶数目及病灶直径差异均无统计学意义。
3 讨论
肺非小细胞鳞癌是临床中比较常见的一种病症,而且严重的影响患者的身体健康。该病具有较高的发病率和死亡率;目前对于晚期鳞癌患者主要治疗手段为全身化疗,但有效率仅为
30%[6],所以早期预测晚期肺非小细胞鳞癌患者的化疗疗效的指标显得尤其重要。癌胚抗原为大肠癌组织中的一种糖蛋白,一般健康人的血清中的癌胚抗原含量比较低[7-8]。因此,检测患者血清中的癌胚抗原对该病的诊断具有重要的意义,但对于在判定疗效方面的研究结果尚无定论。本研究通过回顾性研究,分析化疗第
1周期癌胚抗原的变化,来预测全身化疗的疗效。主要探讨了3组患者临床疗效及血癌胚抗原与NSCLC化疗疗效之间的关系,发现癌胚抗原与NSCLC化疗疗效之间无显著的统计学差异,考虑与该研究的样本量较小,且在治疗过程中存在患者失访及死亡的情况。在今后的研究中,应尽可能扩大入组患者例数,尽可能避免中途治疗的终止,希望能得出更有意义的研究结果。
综上所述,癌胚抗原的水平变化与NSCLC化疗疗效无显著相关,不能作为晚期NSCLC化疗疗效的评判指标。
[1] 张宁宁,王阿曼.肺鳞癌的分子病理学研究进展[J].临床肿瘤学杂志,2013,18(10):947-951.
[2] 李峻岭,石远凯.肺鳞癌治疗进展[J].癌症进展,2012,10(2):120-123.
[3] 高莉华,王雷,郭秀梅等.长春瑞滨联合顺铂治疗晚期肺鳞癌疗效观察[J].中国实用医药,2014(15):172-173.
[4] 李淼,晋国权.吉西他滨联合顺铂对晚期肺鳞癌及肺腺癌治疗的临床疗效比较[J].临床肺科杂志,2013,18(2):211-212.
[5] 成德生.肺功能减低对肺癌手术效果的影响分析[J].当代医学,2014,20(33):17-18.
[6] 周学军.吉西他滨联合奈达铂对晚期肺鳞癌患者的疗效分析[J].泰山医学院学报,2013,34(10):780-781.
[7] 戴宝平,李春娟.肺鳞癌患者治疗前后CEA、CA125、SCC、NSE、CYFRA21-1检测的临床意义[J].医药前沿,2012(34):186.
[8] 李辉.肺结核合并肺癌64例临床分析[J].当代医学,2012,18(5):45-46.
Objective To investigate the relationship between changes in leukemia antigen and late lung squamous non-small cell to chemotherapy. Methods A retrospective analysis of 107 cases with advanced non-small cell lung squamous (non-small cell lung carcinoma, NSCLC) patients with clinical data, in line with the standard set of 60 patients, according to RECIST evaluation criteria are divided into groups of disease progression (disease progression, PD group), stable group (disease stability, SD group) and got better (partial remission, PR and complete remission, CR) group. Respectively gemcitabine, paclitaxel (paclitaxel, PTX), docetaxel treatment. Statistical analysis of the relationship between the three groups of patients with serum carcinoembryonic antigen changes in NSCLC chemotherapy. Results (1) GP group, PTX group and docetaxel group clinical remission rate was 50.00%, 65.00% and 80.00%, respectively; increased (2) (PR and CR) group, SD group and the PD group CEA levels in the number of cases 9, 11 and 6 cases, respectively, to reduce the number of cases 9, 12 and 13 cases, respectively; (3) changes in serum carcinoembryonic antigen with NSCLC chemotherapy was no significant correlation. Conclusion Serum carcinoembryonic antigen NSCLC chemotherapy and no significant correlation, the difference was not statistically significant, can not be used as indicators to judge the efficacy of chemotherapy in advanced NSCLC.
Carcinoembryonic antigen (CEA); Advanced non-small cell lung cancer; Chemotherapy
10.3969/j.issn.1009-4393.2015.7.042
河南 450008 郑州大学附属肿瘤医院内科 (吴红波 张静 吴慧娟 陈丽娟 穆晓倩 赵艳秋)

