铜负载Y 分子筛中Cu 物种的表征及分析
王玉春,郑华艳,李梦云,李忠
(1 太原理工大学煤化工研究所,煤科学与技术教育部和山西省重点实验室,山西 太原 030024;2 运城学院 应用化学系,山西 运城 044000)
Y 分子筛是一种由6 个方钠石笼和6 个六棱柱笼交互连接形成的具有十二元环超笼的八面沸石结构的分子筛[1],其中超笼直径约为1.3nm,形成了Y分子筛的主要孔道。Y 分子筛这种特殊的三维孔道结构不仅为物理、化学反应提供特殊的微环境,同时还表现出良好的分子择形选择性,即只允许直径小于孔径的分子进出。另一方面,Y 分子筛具有合适的Si/Al 比(为1.5~3)及可调节的表面酸性,是性能优良的固体酸催化剂。此外,Y 分子筛还具有比表面积大和热稳定性高的优点,因而作为催化剂载体也展现出独特的魅力[2]。特别是人工Y 型沸石分子筛的合成,为负载型Y 分子筛催化剂和掺杂(骨架内)型Y 分子筛催化剂的发展提供了良好的机遇。
CuY 是一种重要的过渡金属负载型分子筛,它是在充分利用Y 分子筛特殊结构和性能的基础上,通过离子交换、浸渍等方法在Y 分子筛中引入丰富多变的铜物种,进而实现特殊功能的一种CuY。由于其在选择性吸附和深度脱硫[3-5]、氮氧化合物选择性还原[6-7]及甲醇氧化羰基化[8-10]等领域显示出极大的应用潜力,自20 世纪60 年代以来得到了广泛的关注。
CuY 中Cu 物种具有丰富多样的存在形式,既可以以Cu2+和Cu+形式交换Y 分子筛中可交换的骨架外阳离子,也可以以CuO、Cu2O 和Cu0的形式分散在Y 分子筛表面。不同实验条件下,制备的CuY 中铜物种的形态及分布各异。在溶液离子交换法制备的CuY 中,Cu2+通过交换超笼中Π 位的Na+高度分散于Y 分子筛表面[11-12],但是溶液的酸度不同,交换程度也截然不同。在0.1mol/L 的Cu(NO3)2水溶液(pH = 4.3)中,铜物种的存在形式主要是交换度较低的[Cu(H2O)4]2+。用氨水将溶液的pH 值调节到9.5 时,Cu2+以[Cu(NH3)4(OH)]+形式存在,使得交换度大大提高[13]。固态离子交换制备的CuY分子筛,Cu+可以完全交换Y 分子筛Brönsted 酸位的质子[14-15],特别是在无水气氛下,由于Cu+的离子半径为0.96Å(1Å=0.1nm)[16],远远小于Y 分子筛各种笼的窗口,故Cu+能落位在铜离子可以交换的所有位置[17]。与离子交换不同,浸渍法通过铜盐在Y 分子筛表面的直接吸附(只有很少量的Cu2+交换到Y 分子筛骨架外阳离子),再经高温焙烧后,可以得到负载铜氧化物的Y 分子筛[18-19]。另外,焙烧温度对CuY 中Cu 物种的存在形式也有较大的 影响。
研究表明,CuY 的性能与Cu 物种的存在状态、价态及落位具有密切的关系。本文作者课题组[20-22]对比了不同方法制备的CuY 在催化甲醇氧化羰基化合成碳酸二甲酯反应中的催化活性,发现浸渍法制备的CuY 催化剂,由于Cu 物种主要以铜氧化物的形式分散在Y 分子筛表面,且自还原能力弱,因而催化剂活性较低,而溶液离子交换法制备的CuY中,由于铜物种以离子形式交换了分子筛骨架外平衡电荷的阳离子,其自还原能力较强,而且可以形成更多的活性中心,进而提高了CuY 的催化活 性[21-22]。Kieger 等[7]研究发现,Cu 负载超稳Y 分子筛催化剂催化NH3选择性还原NO,低于327℃时,由于铜氧化物的团聚导致引起温室效应、破坏臭氧层的N2O 的生成,通过控制离子交换时的pH 值在5.0 左右,可以避免铜氧化物的团聚,进而避免N2O的生成。在高于327℃时,落位在方钠石笼中Π 位的Cu2+和(CuOCu)2+是促进生成N2O 的物种,因此,通过在铜离子交换之前引入助剂离子,占据方钠石中的Π 位,使得活性组分尽可能落位在反应物分子易于接触的超笼中的Ш 位,同时避免方钠石笼中的Cu2+和(CuOCu)2+的形成,进而提高CuY 的催化活性及减少N2O 的生成。
值得提出的是,CuY 中Y 分子筛独特的结构以及负载于其上形式多变的铜物种在为CuY 带来极大应用价值的同时,也为其表征带来了较大的困难,而探讨Cu 物种在Y 分子筛上的存在状态、价态以及落位与CuY 性能的关系,对CuY 制备工艺的改进和性能的提高具有重要的意义。因此,随着CuY制备方法的发展,众多科研工作者也在CuY 中Cu物种的存在状态、价态和落位的表征进行了深入研究,取得了一系列有意义的进展,主要体现在通过XRD、TEM、XPS、H2-TPR 和CO-IR、NO-IR、EPR等手段获得CuY 中Cu 物种的存在状态、价态以及落位的信息。
1 Cu 物种的存在状态分析
CuY 中Cu 物种的存在状态有:骨架外离子(Cu2+和Cu+)、吸附在表面的氧化物(CuO 和Cu2O)以及Cu0。采用X 射线衍射分析(XRD)和透射电子显微镜(TEM)可以分析Cu 物种的种类、分散情况及粒径。
1.1 X 射线衍射分析
通过XRD 对CuY 进行表征分析,可以得到Y分子筛本身晶体结构的变化,同时可获得Cu 物种物相及分散状态的相关信息[23-26]。Özkar 等[25]采用XRD 分析了溶液离子交换制备的Cu2+负载Y 分子筛(Cu2+Y)以及液相还原Cu2+Y 制备的Cu0负载Y分子筛(Cu0Y),如图1 所示,发现Cu2+Y 和Cu0Y的Y 分子筛结晶度和晶格结构均未发生明显的变化,且无论是Cu2+还是Cu0物种均未出现特征衍射峰,表明Cu 物种分散很好且Y 分子筛负载Cu 物种后其晶体结构未遭到破坏。Richter 等[18]利用XRD研究了焙烧温度及Cu 负载量对浸渍法制备的CuY物相的影响。从XRD 图谱(图2)可见,不同的焙烧温度和Cu 负载量时,Y 分子筛的特征衍射峰均无明显变化,但是400℃焙烧2h 的样品(10~17CuYP)出现了CuO 的衍射峰,且随着负载量的增加,衍射峰越加明显;而650℃氩气中焙烧20h的样品(17CuYa)虽然也出现了CuO 物种的衍射峰,但其强度明显低于样品17CuYP上CuO 的衍射峰,且未出现Cu 和Cu2O 物种的衍射峰。表明浸渍法制备的CuY 中,Y 分子筛的晶体结构保持完整,而且引入的Cu 物种以CuO 的形式负载于Y 分子筛的表面。惰性气氛下650℃焙烧可以促进CuO 的分散,使其结晶度下降,但CuO 未发生自还原反应。

图1 Y 分子筛、Cu2+Y 和Cu0Y 的XRD 图谱
1.2 透射电子显微镜分析
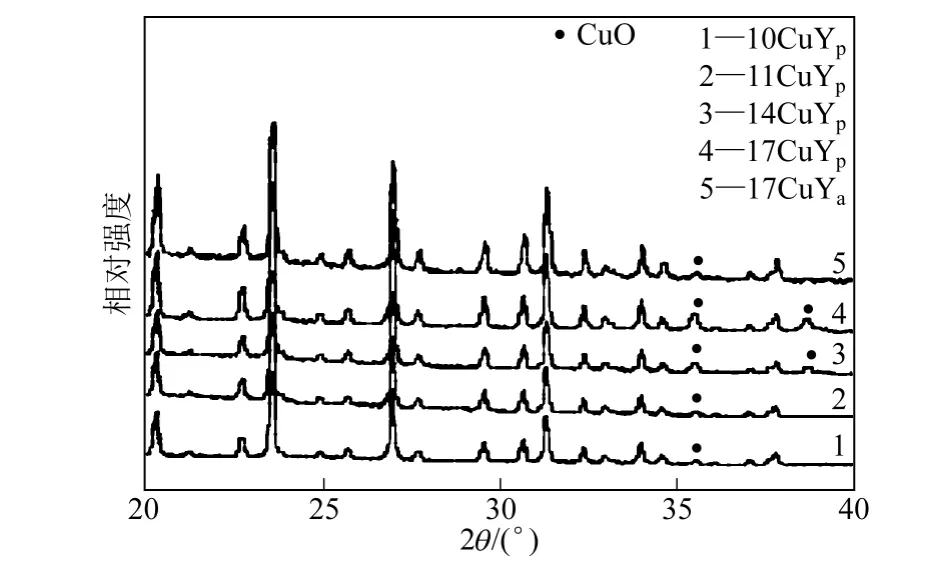
图2 不同Cu 负载量CuY 的XRD 图谱
透射电子显微镜(TEM)能有效地进行显微形貌观察,实现原子和分子尺度上的原位观察,是催化剂微观表征的重要手段之一。采用TEM 对CuY进行微观结构分析,可以同时观察Y 分子筛的结构 变化和Cu 物种的存在状态和晶粒大小。Zahmakiran等[24]采用溶液离子交换法和液相还原法制备了Cu0Y,然后在氧气气氛下处理,得到了Cu2O 负载Y 分子筛,采用高分辨率透射电镜进行了表征,如图3 所示,可见在负载Cu2O 过程中,Y 分子筛的微孔孔道未被破坏,且Cu2O 呈纳米级分散在Y 分子筛的表面,其粒径为(4.8±2.6)nm。
值得提出的是,由于CuY 催化剂表面的铜物种与载体间的作用力很弱,虽然弱的电子光束不足以引起分子筛孔道的塌陷,但是足以导致表面的铜物种发生团聚,而更强的电子光束既能引起分子筛孔道的塌陷,同时表面的铜物种也随之团聚。因此,在对CuY 进行TEM 表征时,尤其是观察Cu 物种是否进入Y 分子筛孔道时,必须聚焦马上拍照,方可得到精确的信息。Richter 等[18]的实验结果很好地证明了这一点。图4 所示的CuY 的TEM 图是以NH4Y 为载体、以Cu(NO)3为铜源,采用等体积浸渍法制备了Cu 的负载量为17%(质量分数)的CuY催化剂(17Cu-Y)。聚焦后马上拍照,Cu 物种纳米粒子尺寸为1.5~4nm[图4(a)],曝光3min 后拍照,催化剂表面的纳米粒子发生了团聚,长大到清晰可见的5nm 球状颗粒,见图4(b)。

图3 Cu2O 负载Y 分子筛的HTEM 图和Cu2O 的粒径柱 状图

图4 样品17Cu-Y 的TEM 图
2 Cu 物种的价态
X 射线光电子能谱(XPS)是一种以X 射线为激发光源的光电子能谱,利用其高能光子照射被测样品,样品的各轨道电子均可能从原子中激发而成为光电子,且各种原子、分子的轨道电子结合能是一定值,故采用XPS 可测定固体表面的电子结构和表面组分的化学组成。Cu2p3/2 的电子结合能位于930~936eV 范围内,如果在940~945eV 结合能范围内出现卫星伴峰,则表明样品表面含有二价铜物种,若未出现卫星伴峰,说明样品表面只含有一价铜物种、Cu0或二者的混合物,进而根据俄歇能谱的动能进行判断,动能在912~913eV,则表明一价铜物种的存在,动能在916~918eV 表明Cu0的存在[27]。许多学者采用XPS 分析了样品表面Cu 物种的价态及组成[19,28-30],本文作者课题组[11,20-21]采用XPS 系统分析了采用浸渍法和溶液离子交换法制备的CuY 表面Cu 物种的价态及含量组成,其中CuY中的Cu 物种是两种价态共存的,采用高斯分峰拟合法,根据面积百分比计算出各价态Cu 物种的含量,图5 和表1 是通过离子交换法(CuY-I)和浸渍法(CuY-H 和CuY-Na 分别以HY 和NaY 为载体)制备的CuY 的XPS 图谱及含量分析[21]。
CuY 中Cu 物种价态的表征还可以采用氢气程序升温还原、CO-IR、NO-IR 和电子顺旋共振。
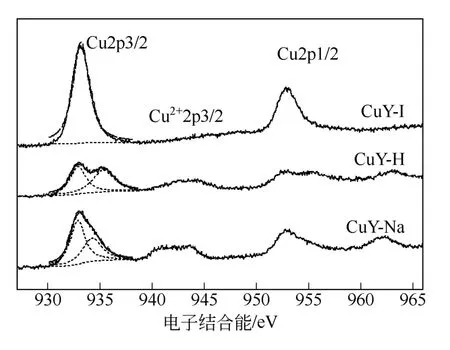
图5 催化剂Cu2p 的XPS 谱

表1 不同催化剂的Cu2p3/2 XPS 分峰谱图分析
3 Cu 物种的落位
Y 分子筛具有3 种笼结构,其中六棱柱笼和方钠石笼的六元环窗口为0.23nm,超笼的十二元环窗口为0.74nm[31],以其为载体制备负载型催化剂,活性组分的落位对于反应起到至关重要的作用,如CuY 催化剂催化甲醇氧化羰基化合成碳酸二甲酯,反应物CO 和O2的动力学直径分别为0.376nm 和0.346nm,因此落位在六棱柱笼和方钠石笼的Cu 物种就不能起催化作用[20]。因此,人们对Cu 活性组分在Y 分子筛中的落位进行了大量的研究[17,32]。
通常采用Maxwell I. E.和De Boer J. J.命名的Y分子筛中Cu 的落位[33],他们认为Cu 至少有12 个落位。图6 的Y 分子筛晶胞中标识出了铜离子可交换的7 个主要位置[34]:Ⅰ、Ⅰ'、Ⅱ、Ⅱ'、Ⅱ''、Ⅲ、Ⅲ',其中Ⅰ是六棱柱笼的中心,Ⅰ'在六棱柱的轴线上,偏离六棱柱笼与方钠石笼共用的六边形平面落位在方钠石笼中,Ⅱ在方钠石笼与超笼间的六边形平面的中心,偏离这个平面落位在方钠石笼的Ⅱ'和落位在超笼中的Ⅱ'',超笼与小笼间的四边形平面上的落位为Ⅲ以及偏离这个平面落位在超笼中的 Ⅲ'。
Cu 物种的落位情况可以采用H2-TPR、原位红外光谱和ESR 等表征手段进行分析。
3.1 氢气程序升温还原
氢气程序升温还原(H2-TPR)是一种表征催化剂中可还原物种的重要方法。对CuY 而言,可根据H2-TPR 的耗氢峰对应的还原温度判断Cu 物种在分子筛超笼、方钠石笼和六棱柱笼中的落位及价态。另外,对Cu 物种对应的耗氢峰进行高斯拟合还可以确定其含量。众多学者[3,12,35-36]采用H2-TPR 对Y 分子筛中的Cu 物种进行了定性和定量分析。他们认为铜物种发生的还原反应如式(1)~式(3)。

图6 Y 分子筛的晶胞
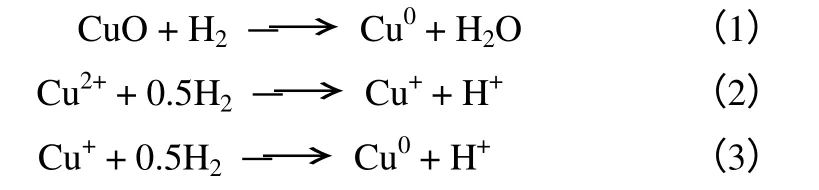
其中CuO 一步还原为Cu0,其还原温度在500K左右,且与分散状态和其与载体间的作用力有 关[32]。Cu2+的还原分两步进行,Cu2+首先还原为Cu+,还原的难易程度与落位有关,由易到难:超笼>方钠石笼>六棱柱笼,其还原发生在900K 以下的低温区(LT),而Cu+的还原发生在1000K 以上的高温区(HT)[7,37]。为了阐述这一结论,将不同交换度CuNaY 的H2-TPR 展示在图7,对于所有的CuNaY 催化剂,在LT 区存在两个不能完全分开的耗氢峰,温度分别约535K 和645K,在770K 还有一肩峰,这3 个峰分别归属于落位在超笼、方钠石笼和六棱柱笼中Cu2+还原为Cu+的耗氢峰。对其高斯拟合分峰,通过面积百分比可以定量Y 分子筛各笼中Cu2+的含量,利用高温耗氢量扣除低温耗氢量,然后根据化学反应平衡关系即可得到Cu 负载Y 分子中Cu+物种的含量[38]。
3.2 原位红外光谱

图7 CuY 催化剂的H2-TPR 图
红外光谱分析是一种非常有效的表征催化剂表面性能的光学表征手段之一,通常采用探针红外光谱研究催化剂的表面活性中心,该表征方法是基于化学吸附原理及特征,红外光谱变化反映活性中心 的配位状态和化学环境变化。探针分子包括CO、NO、CO2、NH3和吡啶等,这些探针分子与催化剂表面发生相互作用,通过测定吸附态探针分子的红外光谱简捷地获得催化剂中活性中心的信息[6]。过渡金属Cu+与CO 有较强的相互作用,以CO 为探针分子研究CuY,可以获得Cu+的落位信息,Fierro等[39]采用CO-IR 表征分析了离子交换法制备的CuY 催化剂,如图8 所示,发现在2164cm-1、2157cm-1、2144cm-1、2132cm-1和2112cm-1出现了振动峰,分别归属于Ⅰ、Ⅰ'、Ⅱ''、Ⅱ和分散在CuO上的Cu+吸附CO 的C—O 伸缩振动频率。随着CO吸附量的增加,依次生成Cu+(CO)、Cu+(CO)2和Cu+(CO)3,因此,振动峰的数目也随之增加,如图9[40]所示。
由于Cu2+与CO 间的作用力很弱,且CO 吸附会引起Cu+落位迁移,而NO 既能与Cu+络合又能与Cu2+络合,且NO 不会引起Cu 离子迁移[40],故采用NO 探针红外光谱对CuY 进行Cu 物种及其落位分析更佳,如图10 所示。1850~1650cm-1波数范围的振动峰归属于NO 与Cu+络合的伸缩振动峰,1792cm-1和1815cm-1分别是落位在超笼中Π*和Π位上的Cu+-NO 的伸缩振动峰,而1975~1850cm-1波数范围内的归属NO 与Cu2+络合的伸缩振动峰,1955cm-1和1923cm-1分别是落位在超笼中Π 和Π*位上的Cu2+-NO 的伸缩振动峰。

图8 CuY 样品的CO 傅里叶变换红外光谱
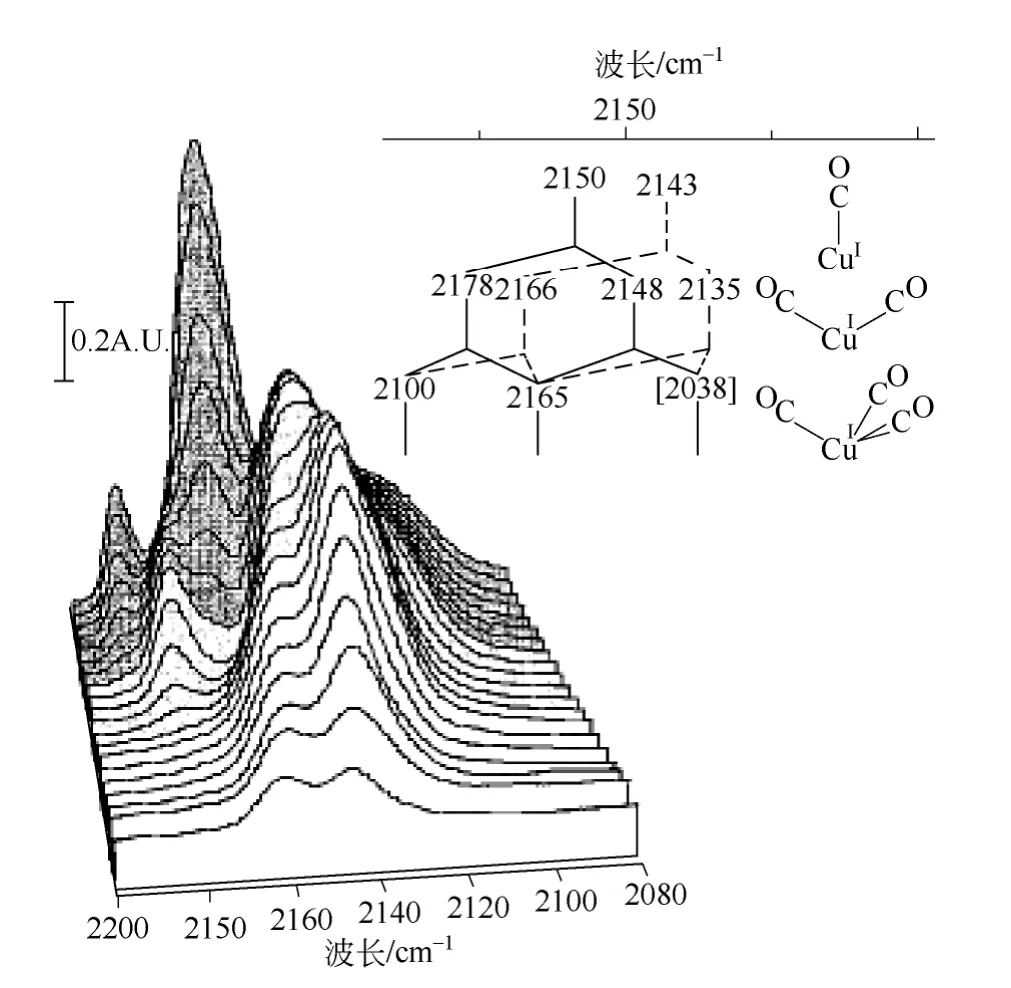
图9 CO 吸附在CuIY 在液氮温度时的红外光谱图
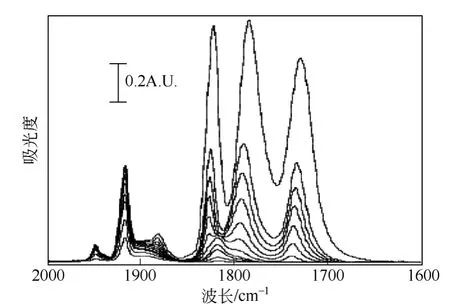
图10 NO 吸附在CuI,IIY 在液氮温度时的红外光谱图
3.3 电子顺磁共振
对于所有的物种而言,其各个轨道上的两个电子自旋态都是不同的,故电子自旋产生的磁矩就会相互抵消,而具有孤对电子的物质则具有永久磁矩,在外磁场中呈现顺磁性,未成对的单电子则发生能级分裂。在垂直于外磁场的方向加一个频率等于单电子的Larmor 旋进频率的射频场,此时就会产生共振吸收,即为电子顺磁共振(EPR)[41]。该表征方法利用波谱分裂因子g 值可知物质内局部磁场特征,进而了解物质结构的信息,另外,对吸收曲线进行一次微分和两次积分,可确定物质的含量[42]。对于过渡金属Cu+(3d10)和Cu2+(3d9),Cu2+的d 轨道存在单电子而Cu+没有,因此采用EPR 表征CuY 只能定性和定量Cu2+物种,且根据波谱分裂因子和超精细分裂常数可以分析 Cu2+的落位信 息[43-45]。Blasco 等[43]采用EPR 研究了溶液离子交换法制备的CuY 催化剂,如图11 所示。a 为CuY 催化剂在500℃抽真空后的EPR 图谱,b 为吸附丙烷(丙烷/Cu = 2)后再350℃下热处理30min 后的EPR图谱。大量文献[46-49]显示信号E 归属于落位在超笼中的Π 位的六元环上或方钠石笼中的Ⅰ'位的Cu2+,信号F 归属于Ⅰ'位或六棱柱笼中Ⅰ位上的Cu2+。CuY 吸附丙烷后350℃热处理后再作EPR 分析,发现E 信号降低,而F 信号基本未发生变化,这是由于丙烷的动力学直径为0.43nm,大于方钠石和六棱柱笼的窗口(0.23nm)而小于超笼的窗口(0.74nm),因此丙烷只能进入超笼吸附在Π 位上使得E 信号降低。另外在热处理过程中,落位在方钠石笼中Ⅰ'位的Cu2+迁移至超笼中,这进一步印证了上述的分析结果。
另外,通过XRD 结构精修也可以确定Cu 离子的落位,如Palomino 等[40]通过XRD 结构精修,发现固态离子交换制备的CuY 中有23.4(2)和11.5(3)个铜离子分别落位在方钠石笼连接六棱柱笼和超笼的六元环中心,6.1(3)个铜离子落位在超笼中连接方钠石笼的六元环中心。
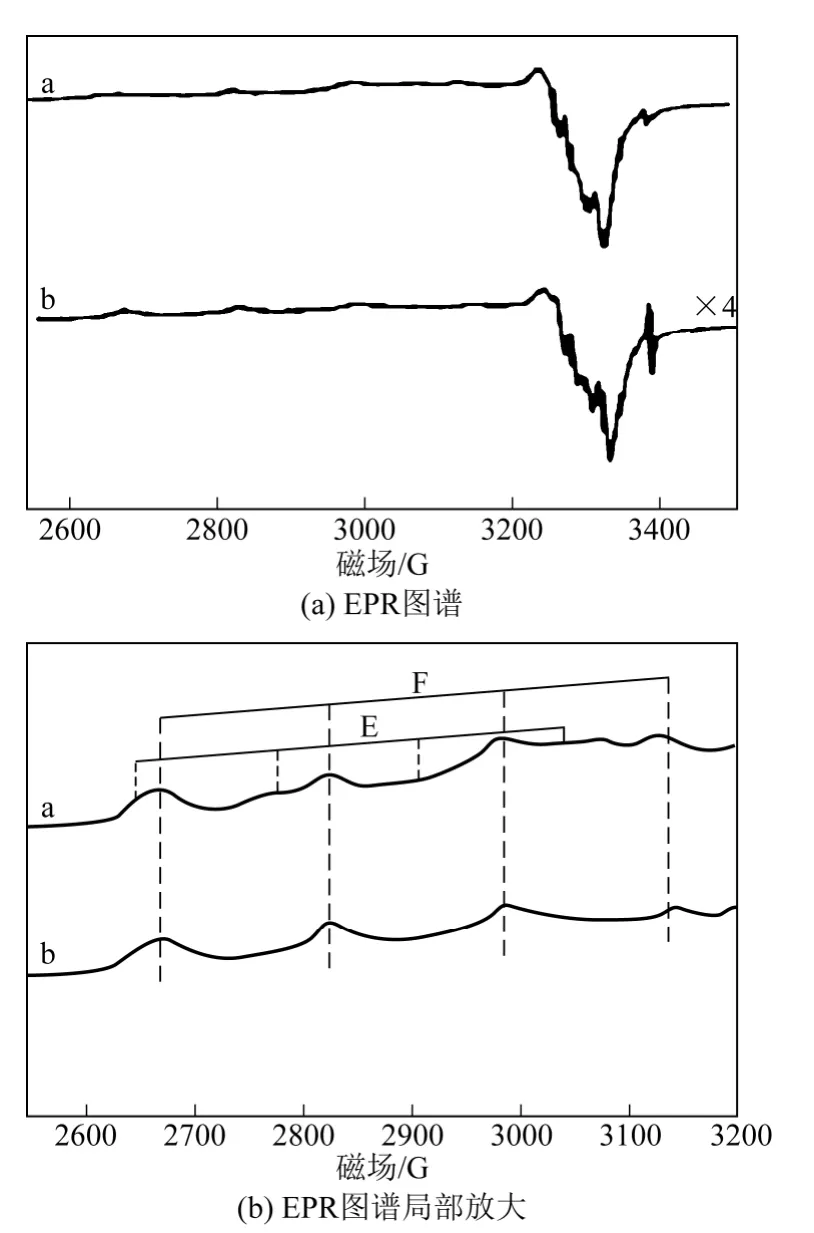
图11 CuY 分子筛在-168℃下的EPR 图谱
4 总结与展望
CuY 应用前景非常广泛,制备方法影响Cu 物种在CuY 上的存在状态(交换到骨架上的离子状态或吸附在Y 分子筛表面的氧化物状态)、价态(Cu2+、Cu+、Cu0或几种价态共存)和落位(Ⅰ、Ⅰ'、Ⅱ、Ⅱ'、Ⅱ''、Ⅲ、Ⅲ'和U)。可以采用多种表征手段对CuY 进行表征:采用XRD 可以分析Y 分子筛的晶相结构、Cu 物种的种类和分散状态;TEM 可以表征Cu 物种在Y 分子筛上的分散及颗粒大小;根据氢气程序升温还原过程中的耗氢量及还原温度,可以定量分析Cu2+、Cu+、CuO 的含量及铜离子的落位情况;探针红外也可以定性分析Cu 离子的落位情况,以CO 为探针只能得到Cu+的落位信息,且会引起Cu+的落位迁移,而以NO 为探针分子,既可以同时得到Cu2+和Cu+的落位信息,又不会引起Cu 离子的迁移,得到更准确的Cu 离子的落位信息,EPR 可以了解到Cu2+的落位信息,对其图谱微分-积分处理还可以定量Cu2+的含量。综合采用这些表征方法,对CuY 进行分析表征可以得到有关结构、物相、价态、落位及含量的更加全面、准确的信息,进而通过制备方法调控CuY 中Cu 物种存在状态、价态及落位,另外还可以通过提前引入助剂阳离子调控Cu 离子的落位等,制备出催化性能更佳的催化剂。
[1] Ibrahim K,Hall A. New occurrences of diagenetic faujasite in the Quaternary tuffs of northeast Jordan[J]. European Journal of Mineralogy,1995,7:1129-1135.
[2] 徐如人,庞文琴,于吉红,等. 分子筛与多孔材料化学[M]. 北京:科学出版社,2004:246-247.
[3] Song H,Wan X,Dai M,et al. Deep desulfurization of model gasoline by selective adsorption over Cu-Ce bimetal ion-exchanged Y zeolite[J]. Fuel Processing Technology,2013,116:52-62.
[4] Takahashi A,Yang R T,Munson C L,et al. Cu(Ⅰ)-Y-zeolite as a superior adsorbent for diene/olefin separation[J]. Langmuir,2001,17(26):8405-8413.
[5] Hernández-Maldonado A J,Yang F H,Qi G. et al. Desulfurization of transportation fuels by π-complexation sorbents:Cu(Ⅰ)-,Ni(Ⅱ)-,and Zn(Ⅱ)-zeolites[J]. Applied Catalysis B:Environmental,2005,56(1-2):111-126.
[6] Ochońska J,McClymont D,Jodłowski P J,et al. Copper exchanged ultrastable zeolite Y:A catalyst for NH3-SCR of NOxfrom stationary biogas engines[J]. Catalysis Today,2012,191(1):6-11.
[7] Kieger S,Delahay G,Coq B. Influence of co-cations in the selective catalytic reduction of NO by NH3over copper exchanged faujasite zeolites[J]. Applied Catalysis B:Environmental,2000,25(1):1-9.
[8] King S T. Reaction mechanism of oxidative carbonylation of methanol to dimethyl carbonate in Cu-Y zeolite[J]. Journal of Catalysis,1996,161(2):530-538.
[9] 王坤,李忠 李安民. 氧化羰基化合成碳酸二甲酯催化剂的研究进展[J]. 化工进展,2013(11):2631-2637.
[10] 仇鹏 王保伟. 羰基合成碳酸二甲酯的研究进展[J]. 化工进展,2010,29(6):56-62.
[11] 王佳臻,郑华艳 孟凡会,等. 制备方法对CuY 催化剂活性组分Cu 落位及催化性能影响[C]//中国化学会第28 届学术年会. 成都,2012.
[12] 王瑞玉 李忠. CuNaY 分子筛的制备及其催化甲醇氧化羰基化[J]. 燃料化学学报,2013,32(11):1361-1366.
[13] Gentry S J,Hurst N W,Jones A. Temperature programmed reduction of copper ions in zeolites[J]. Journal of the Chemical Society,Faraday Transactions 1:Physical Chemistry in Condensed Phases,1979,75:1688-1699.
[14] Huang S Y,Chen P Z,Yan B,et al. Modification of Y zeolite with alkaline treatment:Textural properties and catalytic activity for diethyl carbonate synthesis[J]. Industrial & Engineering Chemistry Research,2013,52(19):6349-6356.
[15] Huang S,Wang Y,Wang Z,et al. Cu-doped zeolites for catalytic oxidative carbonylation:The role of Brønsted acids[J]. Applied Catalysis A:General,2012,417-418:236-242.
[16] Richter M,Fait M J G,Eckelt R,et al. Gas-phase carbonylation of methanol to dimethyl carbonate on chloride-free Cu-precipitated zeolite Y at normal pressure[J]. Journal of Catalysis,2007,245(1):11-24.
[17] Drake I J,Zhang Y,Briggs D,et al. The local environment of Cu+in Cu-Y zeolite and its relationship to the synthesis of dimethyl carbonate[J]. The Journal of Physical Chemistry B,2006,110(24):11654-11664.
[18] Richter M,Fait M J G,Eckelt R,et al. Oxidative gas phase carbonylation of methanol to dimethyl carbonate over chloride-free Cu-impregnated zeolite Y catalysts at elevated pressure[J]. Applied Catalysis B:Environmental,2007,73(3-4):269-281.
[19] Nam J K,Choi M J,Cho D H,et al. The influence of support in the synthesis of dimethyl carbonate by Cu-based catalysts[J]. Journal of Molecular Catalysis A:Chemical,2013,370:7-13.
[20] 付廷俊,郑华艳,牛燕燕,等. Ce,La 和Cs 离子对CuY 催化甲醇氧化羰基化活性中心的影响[J]. 化学学报,2011(15):1765-1772.
[21] 李忠,付廷俊 郑华艳. CuY 制备方法对其催化甲醇氧化羰基化活性中心的影响[J]. 无机化学学报,2011(8):1483-1490.
[22] 王佳臻,郑华艳 李忠. CuY 催化剂中Cu 活性中心落位调控及其催化性能的影响[C]//第十七届全国分子筛学术大会,银川,2013.
[23] Yi D,Huang H,Meng X,et al. Adsorption-desorption behavior and mechanism of dimethyl disulfide in liquid hydrocarbon streams on modified Y zeolites[J]. Applied Catalysis B:Environmental,2014,148-149:377-386.
[24] Zahmakiran M,Özkar S. Preparation and characterization of zeoliteframework stabilized cuprous oxide nanoparticles[J]. Materials Letters,2009,63(12):1033-1036.
[25] Zahmakıran M,Durap F,Özkar S. Zeolite confined copper(0) nanoclusters as cost-effective and reusable catalyst in hydrogen generation from the hydrolysis of ammonia-borane[J]. International Journal of Hydrogen Energy,2010,35(1):187-197.
[26] Li X,Zhang X,Lei L. Preparation of CuNaY zeolites with microwave irradiation and their application for removing thiophene from model fuel[J]. Separation and Purification Technology,2009,64(3):326-331.
[27] Ren J,Liu S,Li Z,et al. Structural feature and catalytic performance of Cu-SiO2-TiO2cogelled xerogel catalysts for oxidative carbonylation of methanol to dimethyl carbonate[J]. Catalysis Communications,2011,12(5):357-361.
[28] Alonso F,Melkonian T,Moglie Y,et al. Homocoupling of terminal alkynes catalysed by ultrafine copper nanoparticles on titania[J]. European Journal of Organic Chemistry,2011(13):2524-2530.
[29] Yuan Y , Cao W , Weng W. CuCl2immobilized on amino-functionalized MCM-41 and MCM-48 and their catalytic performance toward the vapor-phase oxy-carbonylation of methanol to dimethylcarbonate[J]. Journal of Catalysis,2004,228(2):311-320.
[30] Lázaro Martínez J M,Rodríguez-Castellón E,Sánchez R M T,et al. XPS studies on the Cu(Ⅰ,Ⅱ)-polyampholyte heterogeneous catalyst:An insight into its structure and mechanism[J]. Journal of Molecular Catalysis A:Chemical,2011,339(1-2):43-51.
[31] 徐舒涛,张维萍,韩秀文,等. 不同金属离子交换的FAU 型分子筛的超极化129Xe NMR 研究[J]. 催化学报,2009(9):945-950.
[32] Delahay D B G. Recent advances in CuI/IIY:Experiments and modeling[J]. Catalysis Reviews,2006,48:269-313.
[33] Maxwell I E,De Boer J J. Crystal structures and dehydrated divalent-copper-exchanged faujasite[J]. The Journal of Physical Chemistry,1975,79(17):1874-1879.
[34] Berthomieu D,Jardillier N,Delahay G,et al. Experimental and theoretical approaches to the study of TMI-zeolite (TMI=Fe,Co,Cu)[J]. Catalysis Today,2005,110(3-4):294-302.
[35] Torre-Abreu C,Henriques C,Ribeiro F R,et al. Selective catalytic reduction of NO on copper-exchanged zeolites:The role of the structure of the zeolite in the nature of copper-active sites[J]. Catalysis Today,1999,54(4):407-418.
[36] Antunes A P,Ribeiro M F,Silva J M,et al. Catalytic oxidation of toluene over CuNaHY zeolites:Coke formation and removal[J]. Applied Catalysis B:Environmental,2001,33(2):149-164.
[37] Kieger S,Delahay G,Coq B. et al. Selective catalytic reduction of nitric oxide by ammonia over Cu-FAU catalysts in oxygen-rich atmosphere[J]. Journal of Catalysis,1999,183(2):267-280.
[38] 李忠,付廷俊,王瑞玉,等. 高活性甲醇氧化羰基化CuY 催化剂的结构及催化活性中心[J]. 高等学校化学学报,2011(6):1366-1372.
[39] Campos-Martín J M,Guerrero-Ruiz A,Fierro J L G. Changes of copper location in CuY zeolites induced by preparation methods[J]. Catalysis Letters,1996,41(1-2):55-61.
[40] Palomino G T,Bordiga S,Zecchina A,et al. XRD,XAS,and IR characterization of copper-exchanged Y zeolite[J]. The Journal of Physical Chemistry B,2000,104(36):8641-8651.
[41] 赵地顺. 催化剂评价与表征[M]. 北京:化学工业出版社,2011:264-274.
[42] Singh R K,Kothiyal G P,Srinivasan A. Electron spin resonance and magnetic studies on CaO-SiO2-P2O5-Na2O-Fe2O3glasses[J]. Journal of Non-crystalline Solids,2008,354(27):3166-3170.
[43] Moreno-González M,Blasco T,Góra-Marek K,et al. Study of propane oxidation on Cu-zeolite catalysts by in-situ EPR and IR spectroscopies[J]. Catalysis Today,2014,227:123-129.
[44] Seelan S,Sinha A K,Srinivas D,et al. Spectroscopic investigation and catalytic activity of copper(Ⅱ) phthalocyanine encapsulated in zeolite Y[J]. Journal of Molecular Catalysis A:Chemical,2000,157(1-2):163-171.
[45] Yahiro H,Ohmori Y,Shiotani M. Magnetic interaction between copper (Ⅱ) ion and paramagnetic NO and O2molecules in Y-type zeolite at low temperature:An EPR study[J]. Microporous and Mesoporous Materials,2005,83(1-3):165-171.
[46] Yu J S,Kevan L. Temperature dependence of copper(Ⅱ) migration and formation of new copper(Ⅱ) species during catalytic propylene oxidation on copper(Ⅱ)-exchanged Y zeolite and comparison with X zeolite[J]. The Journal of Physical Chemistry,1990,94(19):7612-7620.
[47] Ichikawa T,Kevan L. Location of cupric ions in Y zeolites by electron spin echo spectrometry:Contrast between sodium- and potassium-Y zeolites and comparison with X zeolites[J]. The Journal of Physical Chemistry,1983,87(22):4433-4437.
[48] Schoonheydt R A. Transition metal ions in zeolites:Siting and energetics of Cu2+[J]. Catalysis Reviews,1993,35(1):129-168.
[49] Conesa J C,Soria J. Electron spin resonance of copper-exchanged Y zeolites. Part 1.Behaviour of the cation during dehydration[J]. Journal of the Chemical Society,Faraday Transactions 1:Physical Chemistry in Condensed Phases,1979,75:406-422.

