拓扑替康每周方案二线化疗对敏感型复发小细胞肺癌的疗效及安全性分析
邢镨元,李峻岭
肺癌是目前全球发病率和病死率最高的恶性肿瘤,严重危害人类的公共健康安全,其中小细胞肺癌(small cell lung cancer,SCLC)占肺癌总发病人数的15%~20%,预后极差。以化疗为主的综合治疗仍是目前SCLC的主要治疗方式。虽然近10年肺癌的临床治疗领域取得了突飞猛进的发展,但是SCLC的治疗水平仍然停滞不前。尤其是一线化疗后复发/耐药的患者疾病进展迅速,并且治疗的敏感性下降,缺乏有效的治疗手段,生存时间极大缩短,是临床治疗的难题和重点研究方向。拓扑替康 (topotecan)是一种水溶性半合成喜树碱衍生物,拓扑异构酶Ⅰ抑制剂,是目前唯一被批准单药用于敏感型复发SCLC二线化疗药物,能够通过血-脑脊液屏障。既往国外大型Ⅲ期临床研究证实:治疗敏感型复发SCLC,单药拓扑替康三周方案与传统CAV方案 (环磷酰胺+阿霉素+长春新碱)比较,两者具有相似的客观缓解率 (ORR)及生存时间,单药拓扑替康三周方案耐受性更好,单药拓扑替康治疗组较CAV治疗组明显改善因肺癌引起的相关症状,提高患者生活质量 (QOL)[1]。在安全性方面,单药拓扑替康三周方案主要的毒副作用是血液学毒性,78%的患者会发生Ⅳ度粒细胞计数减少,27%的患者会发生Ⅳ度血小板计数减少,37%的患者会发生Ⅲ~Ⅳ度贫血[1-2],严重制约了其临床应用及患者用药依从性,在身体基础条件虚弱或连续多周期给药后患者的耐受性更低。基础研究显示,拓扑替康作用于非小细胞肺癌细胞时,肿瘤细胞暴露于拓扑替康的最初8~24 h抑瘤作用最强,其后逐渐减弱,这种抑瘤作用与细胞内拓扑异构酶Ⅰ水平呈负相关;进一步研究发现,在拓扑替康作用于肿瘤细胞7 d后从培养基中去除拓扑替康,肿瘤细胞内拓扑异构酶Ⅰ水平迅速回升至基线水平[3],以上结果为拓扑替康每周给药方案提供了理论依据。本研究回顾性分析接受单药拓扑替康每周方案二线化疗的敏感型复发SCLC患者的临床资料,为后续临床治疗提供参考。
1 资料与方法
1.1 临床资料 选取2012年7月—2013年7月中国医学科学院肿瘤医院收治的接受单药拓扑替康每周方案二线化疗的敏感型复发SCLC患者13例为研究对象,其中男10例,女3例;年龄25~71岁,中位年龄60岁;体力状况评分 (ECOG评分)为0~2分,0分2例、1分5例、2分6例;初诊时局限期7例,广泛期6例;一线化疗或同步放化疗采用EP方案11例,CE方案2例;复发时合并脑转移8例,合并骨转移6例,合并其他内脏转移8例。伴有副瘤综合征3例,其中2例表现为低钠血症,1例表现为肌无力。患者治疗前均有吸烟史、家族史、病理诊断、肿瘤分期、实验室检查、影像学资料等临床资料的详细记录。
1.2 方法
1.2.1 治疗方案 采用注射用盐酸拓扑替康 (和美新,葛兰素史克生产,生产批号1002A、1003、1003#001、2003)4 mg/m2,第1、8、15天给药,28 d为1个周期,每8周进行肿瘤疗效评估。患者服药期间定期随访复查血液学及影像学检查。
1.2.2 近期疗效及毒副作用评价 按照实体瘤的评价标准 (RECIST 1.1)对疗效进行评定[4],观察指标包括完全缓解 (CR)、部分缓解 (PR)、稳定 (SD)和进展 (PD),ORR〔ORR=(CR+PR)/总例数〕和疾病控制率 (DCR) 〔DCR=(CR+PR+SD)/总例数〕。无疾病进展生存时间 (PFS)定义为从首次给药至有客观证据证实的疾病进展时间。毒副作用评价按NCICTC 3.0 版本标准进行评价[5]。
1.3 统计学方法 出院后开始随访,随访时间截至2014-12-31。采用SPSS 16.0统计学软件进行数据处理,利用Kaplan-Meier法进行生存分析。
2 结果
2.1 近期疗效 13例患者接受化疗1~6个周期,中位治疗周期数为3个周期,患者均可进行肿瘤疗效评估。PR 1 例 (7.7%), SD 5 例 (38.5%), PD 7 例(53.8%),ORR 为 7.7% (1/13),DCR 为 46.2%(6/13)。中位随访时间为40周 (13~72周),中位PFS为12.0周 〔95%CI(8.7,15.3)周〕(见图1)。
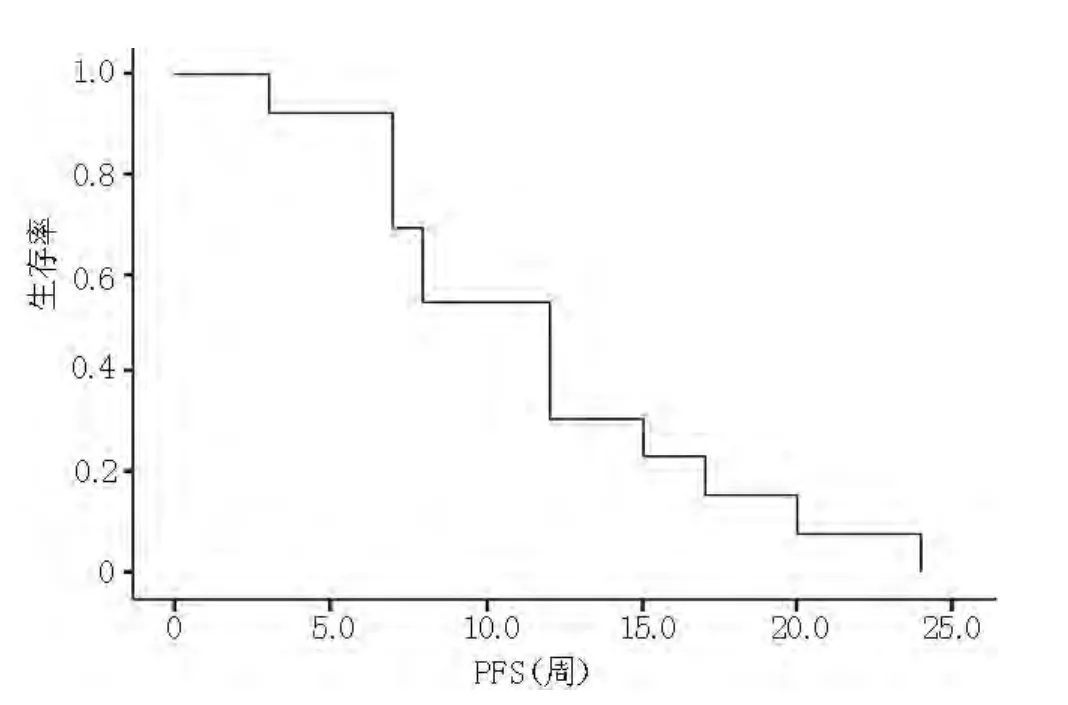
图1 SCLC患者PFS生存曲线Figure 1 The survival curve of PFS in SCLC patients
2.2 毒副作用 本组患者单药使用注射用盐酸拓扑替康化疗的主要毒副作用表现为中性粒细胞计数减少、贫血、血小板计数减少、恶心、呕吐、脱发、疲乏、肝功能损伤等,其中出现Ⅲ/Ⅳ级毒副作用的均为血液学毒性,包括中性粒细胞计数减少2例、白细胞计数减少2例、血小板计数减少2例、贫血1例。
3 讨论
SCLC是一种恶性程度高、生物学行为差异明显、分子表型无法明确分类的肿瘤,治疗方面多年来一直没有突破性进展。SCLC对化疗的敏感性高,初治患者有效率高,80%左右的患者能从治疗中获益,一旦出现肿瘤复发,治疗就变得非常棘手。即便是在抗肿瘤新药层出不穷的今天,拓扑替康仍是唯一被美国食品药品监督管理局 (FDA)批准用于敏感型复发SCLC二线化疗的标准方案。所谓敏感型复发SCLC,是指复发时间距离末次一线化疗超过3个月。FDA推荐的用法为1.2 mg· (m2)-1·d-1,连续5 d,3周为1个周期,即传统三周方案[6]。由于这种给药方式带来的Ⅲ/Ⅳ级血液学毒性发生率较高,极大限制了其临床应用。因此,催生了学者对于每周给药化疗方式的探索。
拓扑替康每周方案二线化疗在安全性方面存在优势,起初的验证结果来源于多项卵巢癌临床研究,在SCLC治疗中也有报道。几乎所有已经发表的比较拓扑替康两种给药方式的文献均支持每周方案[7-10]。尤其是Ⅲ/Ⅳ级血液学毒性,每周方案更具优势,甚至ECOG评分较差或>65岁老年SCLC患者仍表现良好的安全性[11-12]。本研究属于回顾性研究,入组患者的年龄偏大,中位年龄60岁;ECOG评分2分者6/13;脑转移发生率较高 (8/13),整体基线状况较差。治疗中主要毒副作用表现为血液学毒性和恶心、呕吐、脱发、疲乏、肝功能损伤等。其中出现Ⅲ/Ⅳ级毒副作用均为血液学毒性,包括中性粒细胞计数减少2例、白细胞计数减少2例、血小板计数减少2例、贫血1例,全组耐受良好,未出现治疗相关性死亡或因严重毒副作用终止治疗的情况。国外还有一些学者采用口服剂型拓扑替康每周方案也获得了较好的安全指标及有效率[13]。我国目前已经批准上市的拓扑替康为静脉使用的针剂,口服剂型尚未获批准,因此本研究中患者所使用的均为针剂。由于每周方案患者耐受性极大提高,因此在此基础上与新药的联合使用也成为治疗敏感型复发SCLC探索的方向。近期报道的一项临床研究中采用针剂拓扑替康每周方案与新药ziv-aflibercept(针对血管内皮生长因子的一种重组融合蛋白)联合治疗含铂方案耐药的SCLC,结果显示,3个月无进展生存率及疾病控制率明显提高,总生存时间的延长未达到统计学差异,联合组毒性有所增加[14]。为了进一步提高治疗的有效率,学者将每周给药剂量由4 mg/m2增至6 mg/m2,结果提示,治疗有效率并未相应提高,反而骨髓抑制毒性明显升高,因此提高给药剂量这一途径并不可行[15]。虽然上述结果并不是非常令人满意,但是也为复发SCLC的治疗模式提供了参考。
在有效性方面,公开发表的一项Ⅱ期临床研究结果显示,22例敏感型复发SCLC患者采用拓扑替康每周方案无一例评估有效[7],但亦有未公开发表的文献及国内小样本量荟萃分析显示,其与传统三周方案疗效相当[11-12,16]。本研究中患者近期疗效评估,PR 1例、SD 5例、PD 7例,ORR为7.7%,DCR为46.2%,中位PFS为12.0周。2012年 Altinbas等[17]针对拓扑替康每周方案二线化疗复发SCLC进行了一项回顾性分析,共入组62例患者,其中包括初始治疗为局限期和广泛期患者,结果提示,年轻的、一线化疗后无进展生存时间较长的患者从拓扑替康每周方案二线化疗中获益最多。以上结果与本研究结论提示,并非全部敏感型复发SCLC患者适合采用拓扑替康每周方案二线化疗。拓扑替康每周方案因其良好的治疗耐受性,为敏感型复发SCLC二线化疗提供了很好的个体化治疗选择,但是否会引起疗效的降低仍存有争议,需要进一步行大样本、前瞻性、随机临床研究加以验证。
[1] von Pawel J,Schiller JH,Shepherd FA,et al.Topotecan versus cyclophosphamide,doxorubicin,and vincristine for the treatment of recurrent small-cell lung cancer [J].J Clin Oncol,1999,17(2):658-667.
[2] Armstrong DK,Spriggs D,Levin J,et al.Hematologic safety and tolerability of topotecan in recurrent ovarian cancer and small cell lung cancer:an integrated analysis [J].Oncologist,2005,10(9):686-694.
[3] Eckardt JR.Emerging role of weekly topotecan in recurrent small cell lung cancer[J].Oncologist,2004,9(Suppl 6):25-32.
[4] Eisenhauer EA, Therasse P, Bogaerts J, et al.New response evaluation criteria in solid tumours:revised RECIST guideline(version 1.1)[J].Eur J Cancer,2009,45(2):228-247.
[5] Common Terminology Criteria for Adverse Events-Instructions and Guidelines[DB/OL].[2015 - 03 - 04].https://webapps.ctep.nci.nih.gov/webobjs/ctc/webhelp/welcome_ to_ctcae.htm.
[6] Huber RM,Reck M,Gosse H,et al.Efficacy of a toxicity-adjusted topotecan therapy in recurrent small cell lung cancer[J].Eur Respir J,2006,27(6):1183-1189.
[7] Shah C,Ready N,Perry M,et al.A multi-center phaseⅡ study of weekly topotecan as second-line therapy for small cell lung cancer[J].Lung Cancer,2007,57(1):84-88.
[8] Armstrong DK,Spriggs D,Levin J,et al.Hematologic safety and tolerability of topotecan in recurrent ovarian cancer and small cell lung cancer:an integrated analysis [J].Oncologist,2005,10(9):686-694.
[9] Herzog TJ,Sill MW,Walker JL,et al.A phase Ⅱ study of two topotecan regimens evaluated in recurrent platinum-sensitive ovarian,fallopian tube or primary peritoneal cancer:a Gynecologic Oncology Group Study(GOG 146Q)[J].Gynecol Oncol,2011,120(3):454-458.
[10] Sehouli J,Stengel D,Harter P,et al.Topotecan weekly versus conventional 5-day schedule in patients with platinum-resistant ovarian cancer:a randomized multicenter phaseⅡtrial of the north-eastern german society of gynecological oncology ovarian cancer study group [J].J Clin Oncol,2011,29(2):242-248.
[11] Murphy PB,Hainsworth JD,Spigel DR,et al.Topotecan-Single agent activity in a weekly intravenous(Ⅳ)schedule for first-line therapy in poor prognosis extensive stage small cell lung cancer(SCLC):A Minnie Pearl Cancer Research Network phaseⅡtrial[J].J Clin Oncol,2006,24(18S):17000.
[12] Patton JF, Hainsworth JD, SpigelDR, et al.Weeklybolus topotecan as first-line therapy for extensive stage small cell lung cancer in patients who are elderly,poor performance status,or have severe coexistent illness:A Minnie Pearl Cancer Research Network phase Ⅱ trial[J].J Clin Oncol,2004,22(14S):7275.
[13] Agelaki S,Kontopodis E,Kotsakis A,et al.A phase Ⅰ clinical trial of weekly oral topotecan for relapsed small cell lung cancer [J].Cancer Chemother Pharmacol,2013,72(1):45-51.
[14] Allen JW,Moon J,Redman M,et al.Southwest Oncology Group S0802:a randomized,phaseⅡ trial of weekly topotecan with and without ziv-aflibercept in patients with platinum-treated smallcell lung cancer [J].J Clin Oncol,2014,32(23):2463-2470.
[15] Spigel DR,Greco FA,Burris HA 3rd,et al.A phase Ⅱ study of higher dose weekly topotecan in relapsed small-cell lung cancer[J].Clin Lung Cancer,2011,12(3):187-191.
[16] Cai HP,Wang Z.Meta-analysis of effect and safety of standard regimens and weekly regimens of topotecan treating NSCLC [J].Journal of Pharmaceutical Practice,2014,32(1):23-26,30.(in Chinese)
蔡和平,王卓.拓扑替康标准方案与周疗方案治疗小细胞肺癌的荟萃分析 [J].药学实践杂志,2014,32(1):23-26,30.
[17] Altinbas M,Kalender ME,Oven B,et al.Weekly topotecan for recurrent small cell lung cancer-a retrospective Anatolian Medical Oncology Group study [J].Asian Pac J Cancer Prev,2012,13(6):2909-2912.

