尼可地尔原料药含量测定方法的比较研究
肖 瑶成都市食品药品检验研究院,四川成都 610000
尼可地尔原料药含量测定方法的比较研究
肖 瑶
成都市食品药品检验研究院,四川成都 610000
[摘要]目的 比较尼可地尔原料药含量测定的不同方法,并确立更加简单、快速的含量测定方法。 方法 采用高效液相色谱法测定尼可地尔原料药的含量,并与日本药局方第16改正版中收载的非水滴定法进行比较。 结果 采用高效液相色谱法尼可地尔的线性范围为14.32~238.60μg/mL(r=1.0000),平均回收率为100.2%(RSD=0.5%)。两种方法的测定结果无显著性差异。 结论 高效液相色谱法简单、快速、准确,可作为尼可地尔原料药的含量测定方法。
[关键词]尼可地尔;含量测定;高效液相色谱法;非水滴定法
尼可地尔是钾通道开放剂,属于冠脉扩张药,可有效治疗心绞痛,近年在临床上得到了广泛的应用。[1-4]尼可地尔的含量测定方法文献上有报道电化学法[5-6]、分光光度法[7]和高效液相色谱法[8],而日本药局方(JP16)收载了尼可地尔原料药,其含量测定方法为非水滴定法[9]。本研究建立了高效液相色谱法测定尼可地尔的含量,并与日本药局方(JP16)中的非水滴定法进行比较,两种测定方法的结果无显著性差异,而采用本研究建立的高效液相色谱法又能与日本药局方中尼可地尔有关物质的分析方法实现统一。
1 仪器与试药
1.1仪器
Agilent1260型高效液相色谱仪,Agilent 1260VWD紫外吸收检测器;HP8453紫外分光光度仪;赛多利斯BP211D电子天平。
1.2试药
尼可地尔工作对照品(印度Vital Laboratories Pvt.Ltd.,批号:WS/13:060214,含量:99.8%);尼可地尔原料药(印度Vital Laboratories Pvt.Ltd.,批号:N03,N04,N05);四氢呋喃、三乙胺、三氟乙酸均为色谱纯;水为二次蒸馏水;其他试剂均为分析纯。
2 方法与结果
2.1高效液相色谱法
2.1.1色谱条件 采用Thermo Hypersil GOLD (250mm×4.6mm,5μm)色谱柱;流动相为水-四氢呋喃-三乙胺-三氟乙酸(982︰10︰5︰3);检测波长为254nm;柱温25℃;流速为1mL/min;进样体积10μL。
2.1.2溶液的制备 供试品溶液的制备 取尼可地尔供试品适量,精密称定,用流动相溶解并稀释制成每1mL约含80μg的溶液,作为供试品溶液。
对照品溶液的制备:取尼可地尔工作对照品适量,精密称定,用流动相溶解并稀释制成每1mL约含80μg的溶液,作为对照品溶液。
2.1.3专属性试验 取尼可地尔工作对照品适量,分别在高温、高湿、光照、酸、碱及氧化条件下[10]进行破坏,并进样分析,见图1。结果表明尼可地尔峰与其他杂质峰分离良好,说明方法专属性良好。
2.1.4检测限与定量限 根据S/N=3为检测限、S/N=10为定量限,精密称取尼可地尔工作对照品适量,用流动相溶解并稀释制成相应溶液,按“2.1.1”项下进行测定,结果尼可地尔检测限为0.29ng,定量限为0.86ng。
2.1.5线性与范围考察 精密称取尼可地尔工作对照品适量,用流动相溶解并稀释成浓度为14.32、28.63、57.26、95.44、143.2、238.60μg/mL的系列对照品溶液,按“2.1.1”项下进行测定,记录色谱图,见表1。以峰面积(y)为纵坐标,尼可地尔浓度(x)为横坐标,进行线性回归,回归方程为y=23.162x+2.4318(r=1.0000),结果表明尼可地尔在14.32~238.60μg/mL范围内线性关系良好。

图1 强制降解试验Ⅰ:高湿,Ⅱ:高温,Ⅲ:光照,Ⅳ:酸破坏,Ⅴ:碱破坏,Ⅵ:氧化
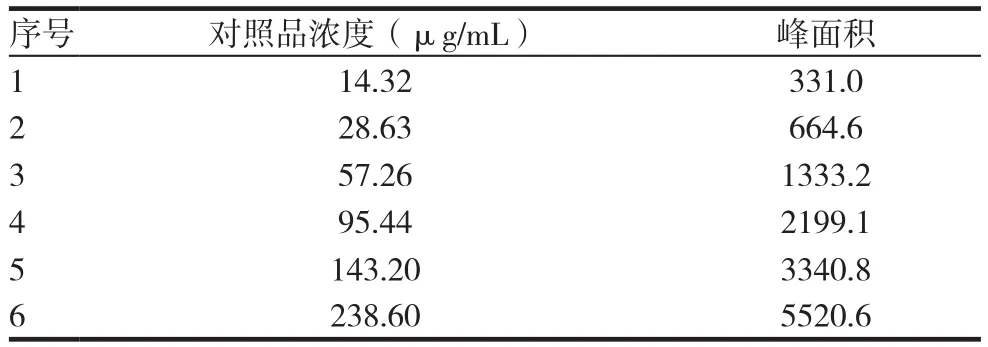
表1 线性测定结果
2.1.6回收率试验 取已知含量的尼可地尔原料药(含量:99.9%)约10mg,精密称定,共9份,分别置250mL量瓶中,精密加入尼可地尔工作对照品适量,按“2.1.2”项下操作,分别制成浓度约为64、80 和96μg/mL的溶液,各三份,按“2.1.1”项下进行测定,记录峰面积,计算回收率。结果见表2。低浓度回收率为100.4%,中浓度回收率为99.5%,高浓度回收率为100.7%;RSD分别为0.09%、0.15%、0.04%。平均回收率(n=9)为100.2%,RSD为0.5%。
2.1.7重复性试验 取同一批尼可地尔原料药(批号:N03)6份,按“2.1.2”项下制备供试品溶液,进行测定,平均含量为99.9%,RSD为0.7%,表明方法重复性良好。
2.1.8供试品溶液稳定性试验 取供试品溶液,在室温下放置,分别在0、2、4、6、8、24h按“2.1.1”项下进行测定,见表3。

表2 HPLC法回收率测定结果

表3 供试品溶液稳定性试验结果
尼可地尔峰面积RSD为0.4%,结果表明供试品溶液在24h内稳定。
2.1.9耐用性 取同一批尼可地尔原料药(批号:N03),按“2.1.2”项下制备供试品溶液,分别使用Thermo Hypersil GOLD(250mm×4.6mm,5μm)色谱柱、资生堂(150mm×4.6mm,5μm)色谱柱、菲罗门(150mm×4.6mm,5μm)色谱柱进行测定,结果含量分别为99.9%、99.7%、99.9%,表明方法耐用性良好。
2.1.10样品测定 取3批尼可地尔原料药,按“2.1.2”项下制备供试品溶液和对照品溶液,按“2.1.1”项下进行测定,记录峰面积,按外标法计算尼可地尔含量,见表6。
2.2非水滴定法
2.2.1测定方法 取本品约0.3g,精密称定,加醋酸酐-冰醋酸(7︰3)混合溶液30mL使溶解,照电位滴定法(中国药典2010年版二部附录ⅦA),用高氯酸滴定液(0.1mol/L)滴定,并将滴定的结果用空白试验校正。每1mL高氯酸滴定液(0.1mol/L)相当于21.12mg的C8H9N3O4。
2.2.2重复性试验 取同一批尼可地尔原料药(批号:N03)6份,按“2.2.1”项下测定,平均含量为100.4%,RSD为0.5%。
2.2.3回收率试验 精密称取尼可地尔工作对照品适量,按“2.2.1”项下测定见表4。
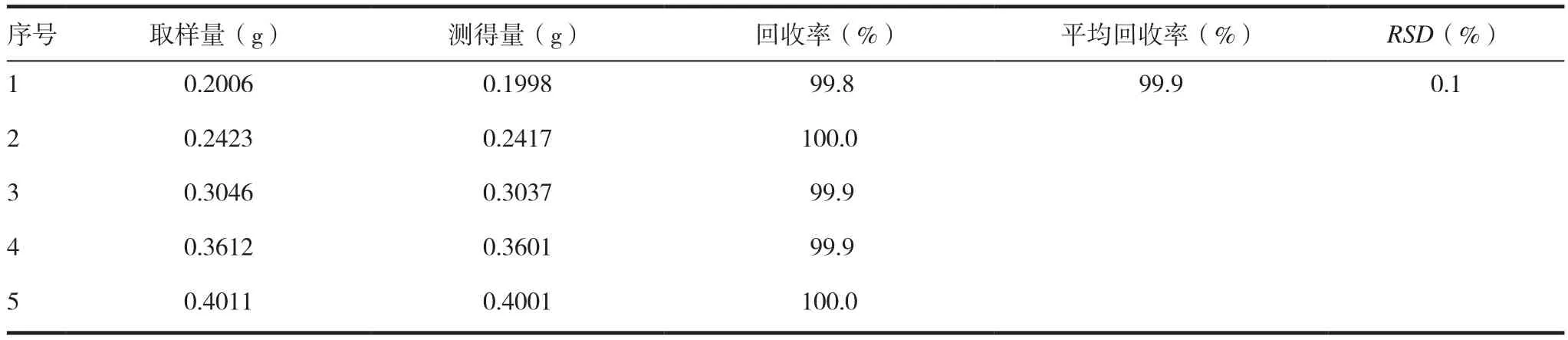
表4 非水滴定法回收率测定结果
2.3两种测定方法结果的比较
取尼可地尔原料药(批号:N03)用高效液相色谱法和非水滴定法进行测定,并将结果进行t检验[11-13]分析,t测=2.109(<t表2.228),P=0.18(>0.05),结果表明两种方法的测定结果无显著性差异(α=0.05),见表5。

表5 两种含量测定方法结果比较(n=6)
分别采用高效液相色谱法和非水滴定法测定尼可地尔原料药的含量,见表6。
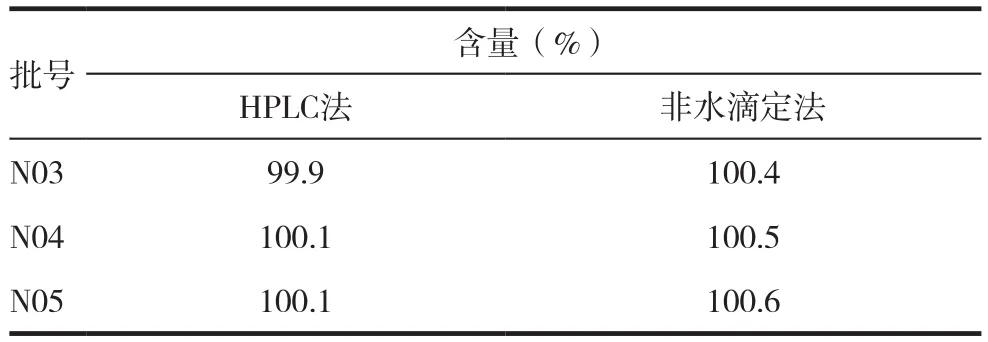
表6 样品含量测定结果(n=3)
3 讨论
尼可地尔在日本药局方中有收载,其中有关物质检查项采用高效液相色谱法,因此本文借鉴有关物质的液相色谱条件建立了含量测定方法。对尼可地尔进行强制降解试验发现尼可地尔对湿度和光照相对稳定,不易被破坏;而在高温、酸碱及氧化条件下很不稳定,易被破坏。在尼可地尔供试品溶液室温放置过程中,部分杂质会不断增加,但对尼可地尔主峰面积影响不大,所以在含量测定中尼可地尔室温放置24h稳定。
在考察该含量测定方法与日本药局方中的非水滴定法的测定结果有无显著性差异时,我们取N03批样品各6份,分别测定,将两个样本均值进行比较。首先进行F检验,结果F测<F0.05,5,5,说明两组数据的精密度不存在显著性差异,即两种方法的精密度相当;然后进行t检验,结果t测<t0.05,10,说明在95%的置信水平上两种方法的测定结果无显著性差异。表明该高效液相色谱法能有效控制尼可地尔的质量。
虽然非水滴定法作为容量分析法测定结果准确度高、成本低,但是当对样品进行批量分析检验时,其时间成本偏高,而本文建立的高效液相色谱法利用仪器的高效、准确可以为药物分析工作者带来便利。另外由于该含量测定方法与有关物质项的色谱条件一致,所以能一定程度上缩短药品检验时间、提高检验工作效率。
作为抗心绞痛的有效治疗药物,目前尼可地尔的剂型有片剂、注射剂等[14-16],本研究建立的含量测定方法可以为后续的制剂研究提供参考。
[参考文献]
[1] 罗碧辉.尼可地尔临床疗效的系统评价[D].广州:南方医科大学,2013:66.
[2] 赵勇,刘先霞.尼可地尔在三支血管病变冠心病患者中的应用价值[J].海南医学,2015,26(11):1572-1574.
[3] Hitoshi Matsuo,Sachiro Watanabe,Tomonori Segawa,et al.Evidence of pharmacologic preconditioning during PTCA by intravenous pretreatment with ATP-sensitive K+channel opener nicorandil[J].European Heart Journal,2003(24):1296-1303.
[4] Yun-Fei Xia,Zheng-Ping Wang,Ya-Chun Zhou,et al. Cerebral protective effect of nicorandil premedication on patients undergoing liver transplantation[J].Hepatobiliary & Pancreatic Diseases International,2012,11(2):132-136.
[5] 苏贻娟,贺利民.尼可地尔的极谱催化波法测定[J].分析测试学报,2003,22(2):66-68.
[6] 程忠洲,苏贻娟,宋俊峰,等.表面活性剂增敏单扫描示波极谱法测定尼可地尔[J].分析实验室,2000,19(2):9-12.
[7] 沈向忠,严济祥.比色法测定尼可地尔及其片剂含量[J].中国医药工业杂志,1990,21(7):315-316.
[8] 罗平,冯敏,林宁.高效液相色谱法测定尼可地尔缓释片的含量[J].湖北中医药大学学报,2015,17(1):42-44.
[9] 日本厚生劳动省.日本药局方第16改正版[S].2011:811-812.
[10] 徐丽佳,陈晓辉,刘中博,等.HPLC法和非水电位滴定法测定盐酸艾咪朵尔含量[J].药物分析杂志,2009,29 (11):1790-1792.
[11] 沈卫阳,郭静沫,施睿,等.非布司他原料2种含量测定方法的比较研究[J].西北药学杂志,2015,30(2):134-137.
[12] 肖庆,袁进.基于Excel进行科研设计资料均数t检验[J].中国老年学杂志,2010,3(11):14.
[13] 李发美.分析化学[M].第6版.北京:人民卫生出版社,1986:17-22.
[14] 高波,贺莉,肖杰,等.口服尼可地尔预防桡动脉途径介入诊疗中桡动脉痉挛作用的临床研究[J].临床心血管病杂志,2014,30(6):495-497.
[15] 罗助荣,黄明方,陈浩.冠脉内注射尼可地尔改善PCI术中无复流现象的临床报告[J].中西医结合心血管杂志,2015,3(5):192-194.
[16] 李步良,黄东,王昉.高效液相色谱法测定尼可地尔中的有关物质[J].中国医药科学,2014,4(2):52-54.
[中图分类号]R927.2
[文献标识码]B
[文章编号]2095-0616(2015)23-75-04
收稿日期:(2015-07-29)
Comparative study on determination method of nicorandil
XIAO Yao
Chengdu Institutes for Food and Drug Control, Chengdu 610000,China
[Abstract]Objective To compare different methods for the determination of nicorandil and establish a more simple and faster determination method. Methods The HPLC method was used to determine the content of nicorandil and compared with nonaqueous titration method stated in the Japanese pharmacopoeia sixteenth edition. Results The linear range of nicorandil was 14.32 - 238.60μg/mL(r=1.0000),and the average recovery rate was 100.2% (RSD=0.5%)by HPLC. There was no significant difference between the results of HPLC and nonaqueous titration method. Conclusion The HPLC method was simple, fast and accurate, which could be used to determine the content of nicorandil.
[Key words]Nicorandil; Determination; HPLC; Nonaqueous titration

