药物洗脱支架治疗无保护左主干远端分叉病变的长期预后
吴雪锋 钱菊英 秦晴
在接受冠状动脉造影(coronary angiography, CAG)的患者中,左主干病变的发病率约占5% ~7%[1-2]。2011 年美国心脏病学会基金会(ACCF)/美国心脏协会(AHA)/心血管造影和介入联合会(SCAI)经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)指南[3]推荐冠状动脉旁路移植术(coronary artery bypass graft,CABG)作为无保护左主干(unprotected left main coronary artery,ULMCA)病变的首选治疗方案。然而,随着介入相关器械的不断改进,术者经验的不断积累,PCI 在复杂病变的治疗中扮演着越来越重要的角色。置入药物洗脱支架(drug-eluting stents,DES)的PCI 在一些中心已经成为ULMCA 的一种可供选择的治疗策略,多项研究结果也显示出良好的应用前景[4-7]。但是有研究显示,当粥样斑块病变累及左主干远端分叉部位时,使用DES 治疗ULMCA 远端分叉病变的预后欠佳[8]。本研究拟评估使用DES 治疗ULMCA远端分叉病变的长期预后。
1 对象与方法
1.1 研究对象
2005 年1 月至2009 年12 月,在复旦大学附属中山医院接受PCI 并置入DES 的ULMCA 远端分叉病变患者共119 例,排除失访的8 例患者,共纳入111 例作为研究对象。
患者行PCI 术的原因有以下三种:(1)介入医师评估患者的病变解剖特点适合行PCI;(2)患者拒绝行CABG;(3)患者有CABG 的禁忌证。ULMCA远端分叉病变的定义:左主干远端直径狭窄≥50%,或者左前降支(left anterior descending artery,LAD)或左回旋支(left circumflex artery,LCX)开口直径狭窄≥70%,并且无通畅的桥血管至LAD 或LCX。
1.2 手术过程
冠状动脉的PCI 术遵循手术时的最新指南。分叉病变的分型按照Medina 分型标准[9]。ULMCA 远端分叉病变的DES 置入策略包括必要时T 支架术、T 支架术、对吻支架术以及Crush 支架术。由介入医师依据个体情况选择支架策略以及是否使用血管内超声(intravascular ultrasound,IVUS)检查。
1.3 随访
通过返院复查或者电话拜访等手段收集随访资料。任何与不良事件有关的信息均通过医疗病历进行确认。研究的主要终点为随访过程的主要不良心脑 血 管 事 件 (major adverse cardiac and cerebrovascular event,MACCE),包括死亡、非致死性心肌梗死、脑血管意外以及靶病变血运重建(target lesion revascularization,TLR)。死亡是指心原性死亡或者非心原性死亡,若死因不明确,则记录为心原性死亡。非致死性心肌梗死是指存在心肌缺血的症状、心电图改变以及心肌酶≥3 倍正常上限。脑血管意外是指缺血性卒中、出血性卒中以及短暂性脑缺血发作。TLR 是指支架置入前后5 mm 范围内,病变行再次PCI 或者CABG。随访时间自手术日期开始计算,至终点事件发生日期或者随访截止日期(2011 年1 月14 日)为止。
1.4 统计学分析
使用SPSS 15.0 进行统计分析。连续性变量以均数±标准差表示,分类变量以数值和百分比表示,生存曲线采用Kaplan-Meier 法,采用Cox 回归模型对可能影响随访终点事件的因素进行筛选以确定独立预测因素。以P <0.05 为差异有统计学意义。
2 结果
2.1 基线资料
111 例患者的平均年龄为(65.6 ±10)岁,其中男96 例(86.5%),女15 例(13.5%)。合并高血压病64 例(57.7%),糖尿病24 例(21.6%),高脂血症44 例(39.6%)。既往吸烟54 例(48.6%),陈旧性心肌梗死病史18 例(16.2%),PCI 史36 例(32.4%)。临床表现为稳定型心绞痛39 例(35.1%),不稳定型心绞痛72 例(64.9%)。估算的肾小球滤过率(eGFR)为(73.6 ±23.1)ml/(min·1.73 m2),左心室射血分数(left ventricular ejection fraction,LVEF)为(64.1 ±9.9)%,平均SYNTAX 评分为(22.1 ±8.5)分。
2.2 分叉病变的解剖特点及介入治疗相关资料
左主干参考血管直径为(3.81 ±0.61)mm。病变血管为左主干7 例(6.3%),左主干合并单支病变48 例(43.2%),左主干合并双支病变42 例(37.8%),左主干合并三支病变14 例(12.6%)。分叉病变的Medina 分型:1,1,1 型35 例(31.5%),1,1,0 型25 例(22.5%),1,0,1 型7 例(6.3%),1,0,0 型27 例(24.3%),0,1,1 型1 例(0.9%),0,1,0 型14 例(12.6%),0,0,1 型2 例(1.8%)。患者接受必要时T 支架术88 例(79.3%),Crush 支架术18 例(16.2%),对吻支架术2 例(1.8%),T 支架术3 例(2.7%)。边支血管置入支架45 例(40.5%)。左主干平均置入支架(1.04 ±0.19)枚。采用IVUS 辅助治疗的患者46 例(41.4%),最终球囊对吻扩张69 例(62.2%)。
在35 例病变同时累及左主干远端、左前降支开口及左回旋支开口的患者中(Medina 分型1,1,1型),17 例(48.6%)采用必要时T 支架术,15 例(42.9%)采用Crush 支架术,2 例(5.7%)采用对吻支架术,1 例(2.9%)采用T 支架术。
2.3 随访结果
111 例患者的中位随访时间为2.3 年。随访过程中,34 例(30.6%)复查了CAG。总的无MACCE生存率为87.4%(图1),共记录到14 例患者发生MACCE 事件(表1)。无TLR 生存率为94.6%(图2),共有6 例患者发生TLR,左前降支及左回旋支开口各有一处狭窄2 例,再狭窄位于左回旋支开口2 例,再狭窄位于左主干支架内1 例,再狭窄位于左主干支架近端1 例;其中4 例接受了再次PCI,2 例接受CABG。无非致死性心肌梗死的生存率为97.3%,无脑血管意外的生存率为98.2%。随访过程中死亡5 例,其中2 例为心原性死亡,3 例为非心原性死亡。4 例(3.6%)发生支架内血栓,其中明确的极晚期支架内血栓1 例,很可能的亚急性支架内血栓3 例。Cox 回归模型分析显示,糖尿病是TLR的独立预测因素(OR 2.62,95% CI 1.12 ~1.62,P=0.004)。
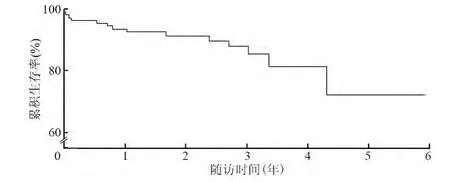
图1 无主要不良心脑血管事件生存率
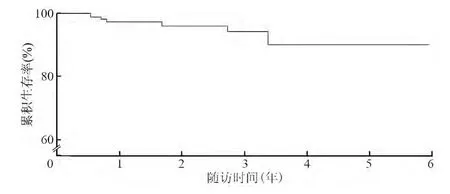
图2 无靶病变血运重建事件生存率
3 讨论
本研究最主要的结论是:(1)经过个体分析及评估后,使用DES 治疗ULMCA 远端分叉病变是安全并且有效的;(2)必要时T 支架术作为本研究中患者的主要支架置入策略,TLR 的发生率较低。
CABG 是ULMCA 的首选治疗方案[3]。自从DES 诞生以及抗血小板治疗改进以来,在ULMCA病变处置入DES已成为一种备选方案。有研究显示,使用DES 治疗ULMCA 与CABG 相比,死亡、心肌梗死等终点事件发生率的差异无统计学意义[4-5]。Meta 分析显示,PCI 与CABG 在包括脑血管意外的复合终点事件上的差异无统计学意义[6]。然而,病变累及ULMCA 远端分叉仍是预后不良的独立危险因素[8]。在ULMCA 远端分叉病变处行PCI 术,累积的主要不良心脏事件(major adverse cardiac event,MACE)发生率可达28.5%;而在左主干近中段置入支架,累积的MACE 发生率为19.1%;两者的区别主要是因为左主干分叉病变有更高的TLR发生率[10]。
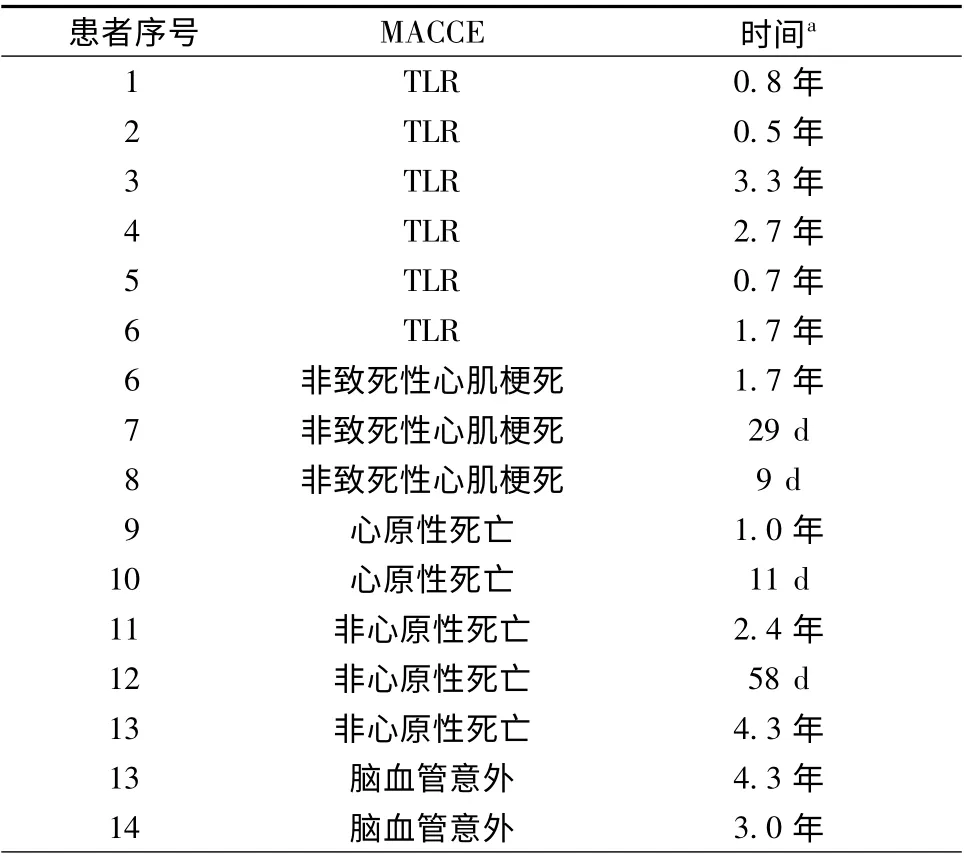
表1 MACCE 的发生情况
本研究中长期随访的MACCE 发生率为12.6%,这可能与本研究患者较低的平均SYNTAX积分以及较高的LVEF 有关。此外,本研究中TLR的发生率仅为5.4%,可能与以下因素有关:(1)仅有30.6%的患者因为出现临床症状或者由于个人意愿复查了CAG。常规复查CAG 有助于检测出更多的无症状再狭窄患者[11]。研究发现,ULMCA 置入西罗莫司洗脱支架后常规复查CAG,有38%的患者接受了靶血管血运重建(target vessel revascularization,TVR),仅有14%的TVR 合并有临床症状[12]。(2)本研究中仅有31.5%的患者为“真性”分叉病变,79.3%的患者接受必要时T 支架术的置入策略,提示本研究患者的病变解剖特点相对简单。Palmerini 等[13]研究发现,当ULMCA 远端分叉病变适合使用单支架技术时,可以取得和左主干开口及中段病变类似的预后。(3)本研究中左主干的平均参考血管直径为3.81 mm,较大的参考血管直径也有助于减少TLR 的发生率[14-15]。
本研究中的再狭窄病变均为局灶性病变,与先前的研究报道一致[16]。4 例患者接受了再次PCI,2例患者接受了CABG。在随访过程中,这6 例患者未再次发生不良事件。事实上,对于ULMCA 置入DES 后发生再狭窄的最佳治疗策略仍未明确。一项韩国的小样本研究显示,经过仔细的临床评估后,再次PCI 可取得与CABG 相似的预后[17]。一项注册研究评估了再次介入治疗的疗效,结果提示再次置入DES 治疗左主干分叉病变支架内再狭窄是安全有效的[18]。研究显示,当需要再次置入支架处理再狭窄病变时,选择另一种类型的DES 可以取得更好的预后[19]。
必要时T 支架术作为本研究人群主要的支架策略,是由介入医师根据个体情况决定的。ULMCA远端分叉病变的最佳支架策略尚存在争论。Valgimigli 等[20]报道支架策略对于不良心脏事件没有影响;而有研究显示与双支架策略相比,单支架策略与更好的预后相关[21-22]。大多数研究都是非随机的,并且在病变的复杂程度上不一致,而临床病变的复杂性是影响支架策略选择最重要的因素。上述研究中所显示出来的差异可能是由于病变不同的复杂性所导致的。值得注意的是,尽管本研究大多数患者采用必要时T 支架术,但仍有40.5%的患者在边支置入了支架,并且在真性分叉病变中,超过一半的患者接受了双支架置入技术。由于左主干部位意义重大,保护边支、完整覆盖病变是非常重要的。
综上所述,使用DES 对ULMCA 远端分叉病变进行PCI 治疗是安全且有效的,长期随访的MACCE发生率为12.6%,TLR 发生率为5.4%。
[1]Stone PH,Goldschlager N. Left main coronary artery disease:review and appraisal. Cardiovasc Med,1979,4:165-177.
[2]DeMots H,Rosch J,McAnulty JH. Left main coronary artery disease. Cardiovasc Clin,1977,8:201-211.
[3]Levine GN,Bates ER,Blankenship JC,et al. 2011 ACCF/AHA/SCAI Guideline for percutaneous coronary intervention. A report of the American College of Cardiology Foundation/American Heart Association Task Force on practice guidelines and the Society for Cardiovascular Angiography and Interventions.J Am Coll Cardiol,2011,58:44-122.
[4]Park DW,Kim YH,Yun SC,et al. Long-term outcomes after stenting versus coronary artery bypass grafting for unprotected left main coronary artery disease:10-year results of bare-metal stents and 5-year results of drug-eluting stents from the ASAN-MAIN(ASAN Medical Center-Left MAIN Revascularization)Registry.J Am Coll Cardiol,2010,56:1366-1375.
[5]Alam M,Huang HD,Shahzad SA,et al. Percutaneous coronary intervention vs. coronary artery bypass graft surgery for unprotected left main coronary artery disease in the drug-eluting stents era--an aggregate data meta-analysis of 11,148 patients.Circ J,2013,77:372-382.
[6]Athappan G,Patvardhan E,Tuzcu ME,et al. Left main coronary artery stenosis:a meta-analysis of drug-eluting stents versus coronary artery bypass grafting. JACC Cardiovasc Interv,2013,6:1219-1230.
[7]刘志忠,单守杰,张俊杰,等. 第二代药物洗脱支架治疗无保护左主干病变的疗效及安全性分析. 中国介入心脏病学杂志,2014,22:702-706.
[8]Valgimigli M,Malagutti P,Rodriguez-Granillo GA,et al. Distal left main coronary disease is a major predictor of outcome in patients undergoing percutaneous intervention in the drug-eluting stent era:an integrated clinical and angiographic analysis based on the Rapamycin-Eluting Stent Evaluated At Rotterdam Cardiology Hospital (RESEARCH)and Taxus-Stent Evaluated At Rotterdam Cardiology Hospital (T-SEARCH)registries. J Am Coll Cardiol,2006,8:1530-1537.
[9]Louvard Y,Medina A. Definitions and classifications of bifurcation lesions and treatment. EuroIntervention,2015,19:V23-V26.
[10]Naganuma T,Chieffo A,Meliga E,et al. Long-term clinical outcomes after percutaneous coronary intervention for ostial/midshaft lesions versus distal bifurcation lesions in unprotected left main coronary artery:the DELTA Registry (drug-eluting stent for left main coronary artery disease): a multicenter registry evaluating percutaneous coronary intervention versus coronary artery bypass grafting for left main treatment. JACC Cardiovasc Interv,2013,6:1242-1249.
[11]Chieffo A,Morici N,Maisano F,et al. Percutaneous treatment with drug-eluting stent implantation versus bypass surgery for unprotected left main stenosis: a single-center experience.Circulation,2006,21:2542-2547.
[12]Price MJ,Cristea E,Sawhney N,et al. Serial angiographic follow-up of sirolimus-eluting stents for unprotected left main coronary artery revascularization. J Am Coll Cardiol,2006,4:871-877.
[13]Palmerini T,Sangiorgi D,Marzocchi A,et al. Ostial and midshaft lesions vs. bifurcation lesions in 1111 patients with unprotected left main coronary artery stenosis treated with drugeluting stents:results of the survey from the Italian Society of Invasive Cardiology. Eur Heart J,2009,17:2087-2094.
[14]Rathore S,Terashima M, Katoh O, et al. Predictors of angiographic restenosis after drug eluting stents in the coronary arteries: contemporary practice in real world patients.EuroIntervention,2009,5:349-354.
[15]Stolker JM,Kennedy KF, Lindsey JB, et al. Predicting restenosis of drug-eluting stents placed in real-world clinical practice:derivation and validation of a risk model from the EVENT registry. Circ Cardiovasc Interv,2010,3:327-334.
[16]Pei HJ,Sui YG,Wu YJ,et al. Long-term clinical outcomes of patients with unprotected left main bifurcation lesions treated with 2-stent techniques. Chin Med J(Engl),2013,126:2409-2413.
[17]Lee JY,Park DW,Kim YH,et al. Incidence,predictors,treatment,and long-term prognosis of patients with restenosis after drug-eluting stent implantation for unprotected left main coronary artery disease. J Am Coll Cardiol,2011,57:1349-1358.
[18]Takagi K,Ielasi A,Shannon J,et al. Clinical and procedural predictors of suboptimal outcome after the treatment of drugeluting stent restenosis in the unprotected distal left main stem:the Milan and New-Tokyo (MITO)registry. Circ Cardiovasc Interv,2012,5:491-498.
[19]Alfonso F,Pérez-Vizcayno MJ,Dutary J,et al. Implantation of a drug-eluting stent with a different drug (switch strategy)in patients with drug-eluting stent restenosis. Results from a prospective multicenter study (RIBS III[Restenosis Intra-Stent:Balloon Angioplasty Versus Drug-Eluting Stent]). JACC Cardiovasc Interv,2012,5:728-737.
[20]Valgimigli M,Malagutti P,Rodriguez Granillo GA,et al. Singlevessel versus bifurcation stenting for the treatment of distal left main coronary artery disease in the drug-eluting stenting era.Clinical and angiographic insights into the Rapamycin-Eluting Stent Evaluated at Rotterdam Cardiology Hospital (RESEARCH)and Taxus-Stent Evaluated at Rotterdam Cardiology Hospital (TSEARCH)registries. Am Heart J,2006,152:896-902.
[21]Palmerini T,Marzocchi A,Tamburino C,et al. impact of bifurcation technique on 2-year clinical outcomes in 773 patients with distal unprotected left main coronary artery stenosis treated with drug-eluting stents. Circ Cardiovasc Interv,2008,1:185-192.
[22]Karrowni W,Makki N,Dhaliwal AS,et al. Single versus double stenting for unprotected left main coronary artery bifurcation lesions:a systematic review and meta-analysis. J Invasive Cardiol,2014,26:229-233.

