缅甸产钝叶樟挥发油的化学成分研究
刘 娜,尹艳清,周树娅,马小丽,王丁丁,李 良,杨丽娟
(1.云南民族大学 教育部民族药资源化学国家民委-重点实验室,云南 昆明 650500;2.云南大学 教育部自然资源药物化学重点实验室,云南 昆明 650091)
缅甸产钝叶樟挥发油的化学成分研究
刘 娜1,尹艳清1,周树娅1,马小丽2,王丁丁2,李 良2,杨丽娟1
(1.云南民族大学 教育部民族药资源化学国家民委-重点实验室,云南 昆明 650500;2.云南大学 教育部自然资源药物化学重点实验室,云南 昆明 650091)
运用超声提取、回流提取、水蒸汽蒸馏、浸泡提取4种方法对缅甸产钝叶樟植物的挥发油进行了提取,通过气质联用(GC-MS)技术结合计算机检索首次分析了缅甸产钝叶樟挥发油的化学成分. 分别鉴定出42、40、22、36个成分, 其中黄樟素(safrole)相对含量最高, 达到19.76%~28.47%.比较4种提取方法, 得油率分别为3.49%、2.50%、0.85%、1.92%, 表明超声提取法效果最优.
钝叶樟;挥发油;化学成分;黄樟素;气相色谱-质谱
钝叶樟(Cinnamomumobtusifolium)系樟科(Lauraceae)樟属(Cinnamomum)常绿乔木[1].主要分布在缅甸、印度、孟加拉、老挝、越南等地区,在中国云南、广东、湖南等地也有分布[2].生长于山坡、沟谷的疏林或密林中,海拔600~1 780 m.其树皮、枝、果用于腰膝痹痛,虚寒胃痛,风寒感冒,闭经腹痛.鲜品捣烂敷用于接骨和瘀血.茎皮治胃寒痛,风湿骨痛,腰肌劳损,温中散寒,理气止痛,止血,接骨,用于胃寒痛,阳痿,闭经; 外用于外伤出血,骨折,蛇咬伤等功效[3].目前,已有文献对湖南[4-5],浙江[6-7],云南[8-9],广西[10-11],福建[12],四川[13],安徽[14]等地樟树叶的化学成分进行了研究,发现其主要成分为芳樟醇,黄樟素,松油醇,芳姜黄酮,氧化石竹烯,α-蒎烯等化合物.但缅甸产钝叶樟(Cinnamomumobtusifolium)的化学成分研究尚未见报道.
本研究运用超声提取、回流提取、水蒸汽蒸馏、浸泡提取4种方法对缅甸产钝叶樟植物的挥发油进行了提取,并通过气质联用(GC-MS)技术结合计算机检索首次分析了缅甸产钝叶樟挥发油的化学成分.
1 实验部分
1.1 仪器与材料
Trace1310型气相色谱与ISQ单四级杆质谱联用仪;旋转蒸发仪;超声仪;水蒸汽蒸馏提取装置;回流装置.乙醚,无水硫酸钠(均为分析纯).
植物样品钝叶樟于2012年8月采自缅甸,经中科院西双版纳热带植物研究所唐勇博士鉴定为Cinnamomumobtusifolium.
1.2 4种方法对钝叶樟挥发油提取
1.2.1 超声提取法
原料粉碎过0.356 mm筛,称取50.0 g 装入 1 000 mL 锥形瓶中,加乙醚400 mL,置于超声中,超声温度为25 ℃,时间为20 min,功率为100 W.待提取完毕后,抽虑,重复3次,合并滤液,真空浓缩至无液滴流出,测得挥发油得率为3.49%.
1.2.2 回流提取法
原料粉碎过0.356 mm筛,称取50.0 g装入 1 000 mL 锥形瓶中,加乙醚400 mL,置于恒温水浴锅中,温度为40 ℃,时间为4 h.待提取完毕后,抽虑,真空浓缩至无液滴流出,测得挥发油得率为2.50%.
1.2.3 水蒸汽蒸馏法
将粉碎好的钝叶樟粉末称取50 g装入 1 000 mL的圆底烧瓶中,加500 mL水及一个大的搅拌子连接回流冷凝管,至于恒温油浴锅中,调节电磁搅拌器温度135 ℃搅拌速度300 r/min,蒸馏10 h收集流出液,用乙醚萃取,经无水硫酸钠干燥,过滤,至于旋转蒸发仪上蒸干,测得挥发油得率为0.85%.
1.2.4 浸泡提取法
将粉碎好的钝叶樟粉末称取50 g装入 1 000 mL的瓶子中,加入300 mL乙醚浸泡3天(3次),过滤收集乙醚至于旋转蒸发仪上蒸干,测得挥发油得率为1.92%.
1.3 挥发油GC-MS分析条件
Trace1310型气相色谱与ISQ单四级杆质谱联用仪.气相色谱条件: 石英毛细管柱TG-5MS,30 m×0.25 mm,膜厚0.25 μm.载气为氦气,分流比60∶1,柱前压40 kPa,柱流量0.8 mL/min,进样口温度250 ℃,接口温度250 ℃,进样量1 μL.升温程序: 从40 ℃开始以3 ℃/min升到10 ℃,保持1 min,然后4 ℃/min升到180 ℃,保持1 min,再以5 ℃/min升到250 ℃,保持4 min; 质谱条件: 离子源温度250 ℃,电离方式EI,电子能量70 eV,扫描质量范围(m/z):30~500 .
2 结果与分析
2.1 4种方法提取钝叶樟挥发油的GC-MS总离子流图
4种方法提取纯叶样样发油的GC-MS总离子流图见图1~4.
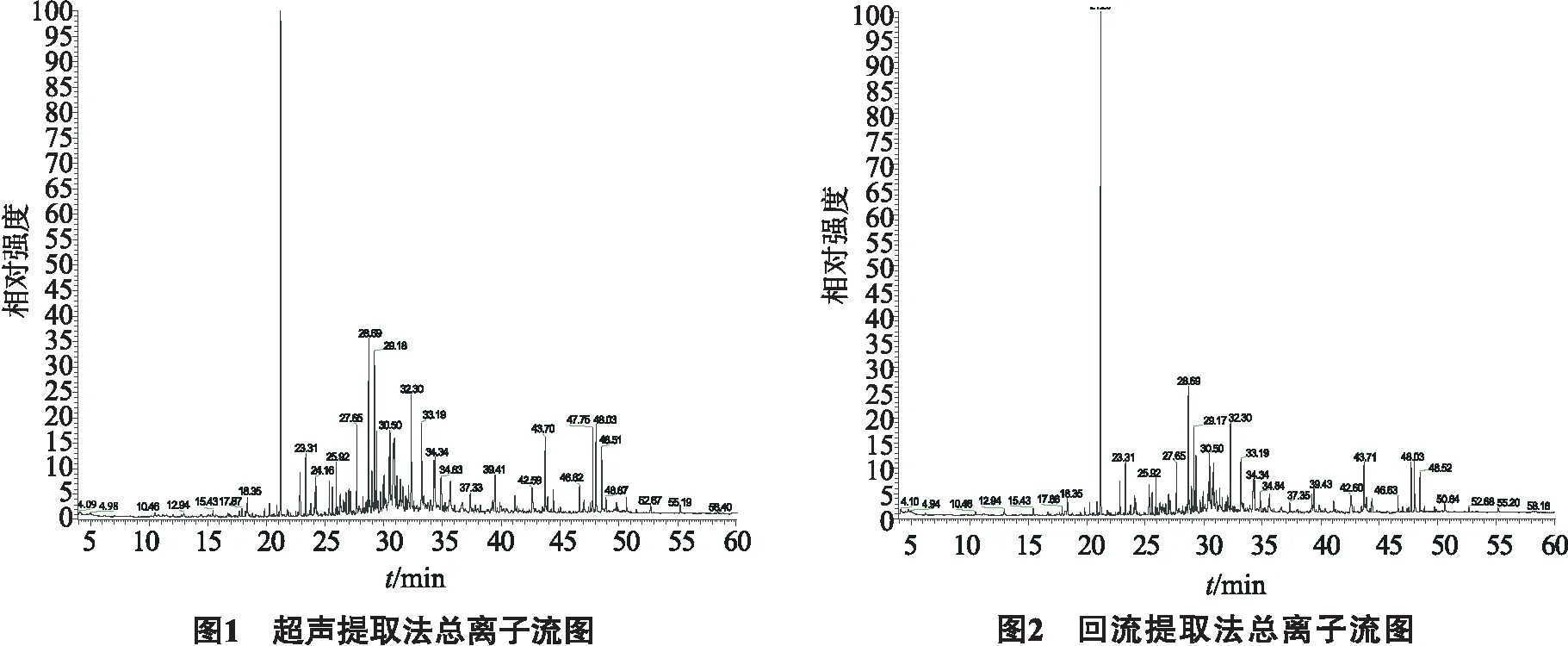
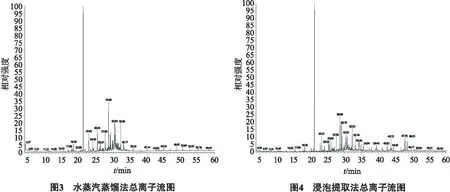
2.2 钝叶樟挥发油成分的GC-MS分析
钝叶樟挥发油成分的GC-MS分析结果见表1.

表1 纯叶样样发油成分的GC-MS分析结果
续表

序号保留时间/min化合物名称分子式相对百分含量/%超声回流水蒸气浸泡3242.59E,E,Z-1,3,12-十九烷三烯-5,14-二醇C19H34O21.941.92—2.143343.705-乙基-4-十三烷酮C15H30O3.522.35—2.333444.4117-十八碳炔酸C18H32O20.860.78—0.863544.833,7,11-三甲基-1,6,10-十二烷三烯-3-甲酸乙酯C16H26O20.20———3644.997-甲基-Z-十四碳烯-1-醇乙酸酯C17H32O20.19—0.53—3746.631'-(丁炔-3-酮-1-基)-,(1R,2S,5R)-薄荷醇C14H22O20.940.88—0.743847.022-甲基-1-十六烷醇C17H36O0.44—0.39—3947.754α-乙酰氧基-5,5,8-三甲基八氢苯并[b]吡喃C14H24O32.732.28—2.194048.034,7-十八碳二炔酸甲酯C19H30O23.152.65—2.384148.51乙酸,1-[2-(2,2,6-三甲基-二环[4.1.0]庚烷-1-基)-乙基]-乙酸乙烯酯C16H26O22.061.85—1.824248.872,6,10-三甲基十四烷C17H360.49—0.71—4349.75(Z,Z)-2-(9,12-十八癸二烯基氧基)-乙醇C20H38O20.25———4450.641,3-乙基-5-(2-乙基丁基)-十八烷C26H540.510.380.68—4551.452,3-二甲基-5-三氟甲基1,4-苯二醇C9H9F3O20.17———4652.671,3-乙基-5-(2-乙基丁基)-十八烷C22H42O0.380.290.68—4755.19异戊酸香叶酯C15H26O20.380.42——
2.3 提取挥发油的4种方法比较
4种方法提取挥发油的温度、时间以及得油率如表2所示.

表2 4种挥发油提取方法比较
挥发油的4种提取方法中,超声提取法无需高温度、无需加热,或者加热温度低,萃取时间短大大降低能耗,挥发油的得油率为3.49%,其提取挥发油的效率最高,所以,超声提取法为最优的挥发油提取法.
3 结语
运用超声提取、回流提取、水蒸汽蒸馏、浸泡提取4种方法对缅甸产钝叶樟植物的挥发油进行了提取,得油率分别为3.49%、2.50%、0.85%、1.92%,结果表明超声提取法效果最优; 并通过气质联用(GC-MS)对其挥发油的化学成分进行了分析,主要为萜类,倍半萜类,芳香醇类,酯类等,其中黄樟素(safrole)相对含量最高,达到19.76%~28.47%,占总精油含量的近1/5~1/4,它是合成香料的重要原料[15-16].其余含量较高的成分为: 氧化石竹烯(1.56%~8.76%),正十五碳醛(3.11%~7.98%),2-亚丙烯基环丁烯(6.06%),环氧化蛇麻烯 Ⅱ(6.02%),14-8S,14-雪松烯二醇(5.67%),芳姜黄酮(0.86%~3.48%)等,芳姜黄酮有抗生育活性[17].因此,缅甸产钝叶樟可以作为生物医药,名贵香料,化工等的原料,本研究为缅甸产钝叶樟的资源功能评价及综合利用提供了科学依据.

[1] 中国森林编辑委员会.中国森林(3卷):阔叶林 [M].北京:中国森林出版社,2000.
[2] 王中生.樟科观赏树种资源及园林应用 [J].中国野生动植物源,2001,20(1):31-33.
[3] Department of traditional medicine,Ministry of Health.Medicinal plants of Myanmar[M].Myanmar,2009,41-42.
[4] 廖矛川,杨芳云,沙光普.樟树叶化学成分研究 [J].中南民族大学学报:自然科学版,2012,31(3):52-55.
[5] 王芃,张党权,章怀云.樟树叶化学成分的GC/MS分析 [J].中南林业科技大学学报,2010,30(10):117-120.
[6] 李祖光,朱国华,曹慧.微波辅助水蒸气蒸馏樟树叶挥发油的研究 [J].浙江工业大学学报,2008,36(6):597-601.
[7] 孙崇鲁,胡晓渝.香樟叶不同溶剂提取物清除DPPH自由基的研究 [J].中南药学,2014,12(3):223-225.
[8] 李锡文.云南樟及其相近种的精油化学与植物分类 [J].植物分类学报,1975,13(4):36-50.
[9] 刘亚,李茂昌,张成聪.香樟树叶挥发油的化学成分研究 [J].分析试验室,2008,27(1):88-92.
[10] 李桂珍,梁忠云,覃子海.广西樟树叶油一种新的生化类型 [J].广西林业科学,2011,40(2):143-144.
[11] 莫建光,黄艳,周翔.广西樟树叶精油的化学成分研究 [J].广东农业科学,2013,18:89-90,114.
[12] 张国防,陈存及,陈志平.福建省樟树叶精油的主成分分析及其化学型 [J].植物资源与环境学报,2008,17(1):24-27.
[13] 曹玫,贾睿琳,江南.油樟叶挥发油的镇痛活性研究 [J].广西植物,2013,33(4):552-555.
[14] 秦国正,丁家鹏,窦德宇.超临界萃取香樟叶精油的工艺研究 [J].皖南医学院学报,2011,30(5):362-364.
[15] 李长宇,李祖光.顶空固相微萃取-气相色谱-串联质谱法测定香精香料中黄樟素 [J].理化检验-化学分册,2013,49:216-218,221.
[16] 韩熠,张承明.食品及化妆品中香豆素和黄樟素类化合物分析方法研究进展[J].香料香精化妆品,2013,1:45-49.
[17] 耿娓琴,陈钟璞.芳姜黄酮和姜烯衍生物的合成及抗生育活性初探 [J].华东化工学院学报,1990,16(1):61-66.
(责任编辑 王 琳)
Chemical constituents of volatile oil ofCinnamomumobtusifoliumfrom Myanmar
LIU Na1,YIN Yan-qing1,ZHOU Shu-ya1,MA Xiao-li2,WANG Ding-ding2,LI Liang2,YANG Li-juan1
(1.Key Laboratory of Chemistry in Ethnic Medicinal Resources, State Ethnic Affairs Commission and Ministry of Education of China,Yunnan Minzu University, Kunming 650500,China;2.Key Laboratory of Medicinal Chemistry for Natural Resources,Ministry of Education of China, Yunnan University, Kunming 650091 China)
The chemical constituents of volatile oil ofCinnamomumobtusifoliumfrom Myanmar were studied. Using four methods(ultrasonic,reflux,steam distillation and immersion extraction),the volatile oils of this plant were extracted, and the extracted rates of volatile oil were 3.49%,2.50%,0.85% and 1.92%,respectively.The results showed that the best extraction method was the ultrasonic extraction. The chemical constituents of volatile oil were analyzed by GC-MS. In the above-mentioned four methods,42,40,22 and 36 compounds were identified respectively.The highest constituent of the essential oils was safrole(relative contents at 19.76%—28.47%).
cinnamomumobtusifolium;volatile oils;chemical constituents;safrole;GC-MS
2014-02-14.
国家自然科学基金(21162042);云南民族大学创新团队项目;云南民族大学大学生创新性实验项目(2013HXSRTZ08);云南民族大学研究生创新项目(11HXYJS08).
刘娜(1987-),女,硕士研究生.主要研究方向:天然药物化学.
杨丽娟(1971-),女,博士,教授,硕士生导师.主要研究方向:超分子化学与药物化学.
R284.2
A
1672-8513(2015)01-0029-05

