不同穿刺点行子宫内电转对小鼠胚胎皮层发育的影响
张鹏 吴翠莹 陶庆霞 牛力军 陈文锦 刘宁 徐如祥
·基础研究·
不同穿刺点行子宫内电转对小鼠胚胎皮层发育的影响
张鹏 吴翠莹 陶庆霞 牛力军 陈文锦 刘宁 徐如祥
目的探讨子宫内电转技术操作过程中三种不同的穿刺点对胚胎死亡率、皮层厚度和皮层面积,以及细胞分化、增殖、迁移和细胞凋亡的影响。方法通过应用免疫荧光染色对Tbr1,Tbr2,Pax6,Ctip2,Caspase-3和Ki67等标记物的检测分析,评价三种不同穿刺点对细胞分化、增殖、迁移和细胞凋亡的影响。应用SPSS13.0软件使用单因素方差分析的方法对分化、增殖和凋亡实验中的细胞数量进行统计分析。结果三种不同的穿刺点无论对胚胎死亡率、皮层厚度和皮层面积,还是细胞分化、增殖、迁移和细胞凋亡的影响均无统计学意义(P>0.05)。结论三种不同的穿刺点对宫内电转胚胎无显著性影响。
基因转移技术;穿刺点;分化;增殖;
随着生物信息学的迅猛发展,越来越多的生物学片段被鉴定出来,然而识别这些生物学片段与判定该片段的功能是两个不同的概念,后者通常需要使用多种手段来决定。目前存在多种基因功能鉴定的方法,例如,转基因和基因打靶技术可以改变某一基因并使其稳定传递至下一代[1,2];重组病毒和启动子基因枪可以传导基因到体内组织[3,4]等。然而上述方法存在局限性,转基因的生产过程、获得基因打靶小鼠或重组病毒的过程耗时、耗力,实现靶基因在精准时间与位置成功表达非常困难。相比而言,子宫内电转技术,操作时间短、见效快,并可使基因的过表达或失活限定在特定时间段特定组织内。
子宫内电转技术是将质粒DNA注射进入胎鼠脑室内,然而施加电压于子宫壁外合适位置,在电场的作用下,质粒DNA向正极电极板方向移动,最终到达目标特定脑区。借助该方法,可向脑组织内转染表达不同颜色荧光蛋白的基因以观察细胞的迁移与分化情况,从而分析该基因的功能[5,6,7]。与其它方法相比,子宫内电转技术具有多种优点:高效性,时空精确性,并可同时将多种基因转染进同一细胞[7]。甚至该技术可标记细胞有丝分裂的大概时间,根据这一特点,不同时间段电转可使基因表达于不同类型的细胞[2]。利用子宫内电转技术通过功能获得与缺失同样被用来研究某些基因功能[6,27]。通过对大脑生理发育过程中或病理过程中神经元或其他细胞的错位表达分析,子宫内电转技术也用于阐明基因功能的分子机制[8-10]。
虽然透过子宫壁可以看到胎鼠头部,然而要精确的将DNA质粒注入靶位置难度很大,尤其是胎脑的腹侧区。在子宫内电转技术的操作过程中,穿刺部位的选择是关键。本篇文章将重点研究从不同穿刺位置穿刺对皮层发育的影响。
材料与方法
一、实验动物
CD1(ICR)品系小鼠为本研究的实验对象,购自北京维通利华实验动物技术有限公司(北京,中国)。该实验所涉动物操作均符合当地动物管理协会的相关规定。
二、质粒
质粒含GFP/DsRed报告基因,该报告基因位于CAG启动子的下游(addgene 11150,addgene 11151)。该质粒使用无内毒素质粒提取试剂盒纯化提取(德国Qiagen公司,12362)。
三、子宫内电转技术
本研究子宫内电转技术所用电转仪为BTX, ECM830,参数为脉冲5个,电压45 V,间隔时间1 s,每个脉冲持续时间为50 ms。整个操作在生物安全柜内完成。CD1胎鼠使用异氟烷呼吸麻醉机(Matrx VIP3000)进行气体麻醉,氧流量为0.2~0.3 L/ min。将手术区域的毛发剃光,并准备好手术操作所需无菌器械。手术区域使用碘酊和75%乙醇消毒3遍。当准备工作结束,将腹部切开3 cm切口以充分暴露手术视野。然后将胚胎取出,在选定好的位置进行精确电击。实时监测体温,并使用加热毯使其维持在37℃。转染GFP/DsRed质粒用于观察电转的效果。通过口控的注射管系统(美国Drummond Company,Inc),使用拉制的玻璃微电极。将大概1 μl的DNA质粒溶液(3 μg/μl)混合fast green溶液(0.1%,美国sigma,F7258),注射入脑室。通过镊形电极(BTX,45-0489)透过子宫外壁钳住胚胎并给予适当电击。实验共分成4组:单纯电击(对照组);从后囟旁开1 mm位置穿刺(A组);从头侧沿前后轴刺入脑室(B组);从前囟和后囟连线中点旁开1 mm位置穿刺(C组)。位于子宫口位置的胚胎并未注射质粒。当所有胚胎电击完毕后,使腹腔内充满温的无菌生理盐水,缝合腹部肌肉与皮肤。将动物移入干净的鼠笼以促进其恢复[11]。
四、DNA注射所需微量注射管的准备.
使用P-97拉针仪拉制玻璃微电极,然后按“pull”按钮以拉断电极,通过磨针仪(WPI,48000)可将玻璃电极的尖端打磨至直径60 μm。用标记笔为玻璃电极每3 mm划一刻度线予以标记,3 mm可代表1 μl的质粒溶液。将玻璃电极进行121°C下30 min高压灭菌。
五、免疫荧光染色
在胚胎13.5 d进行电转,在胚胎18 d使用苯巴比妥溶液对小鼠进行麻醉,消毒后剖腹取胚胎。将电转过的胎脑使用4%福尔马林溶液(美国Sigma, 158127)4°C固定2 h至过夜不等。使用30%蔗糖溶液(美国Amresco,57-50-1)对组织脱水,脱水完毕,对组织进行冰冻切片,厚度20µm。风干1 h后置于﹣80°C冰箱保存。将切片用10%BSA配制的一抗作用过夜,次日,将切片用室温0.01M PBS冲洗3次,每次5 min,后加入二抗,37°C作用1 h。使用含DAPI的封片剂进行封片。
六、细胞计数与测量
使用共聚焦显微镜(德国Leica SP5Ⅱ)对所有冠状切片进行皮层板(CP)厚度与细胞数量的体视学分析,以计数SVZ区与CP区特定标记的细胞数量以及测量该区的厚度与面积。通过计数每层阳性标记细胞的的数量可以大概估算出SVZ区与CP区阳性标记细胞的总数(大概有20~30张切片)[17]。每组包含小鼠的数量为3只。通过DAPI标记细胞核并用Image-Pro Plus软件描记整个皮层轮廓以获得皮层面积及测量皮层厚度。
七、统计学分析
统计学分析由SPSS13.0软件完成。使用单因素方差分析的方法对分化、增殖和凋亡实验中的细胞数量进行分析。P<0.05被认为有统计学意义。使用Prism软件生成统计图。
结果
为了获得理想的实验结果,并降低胚胎死亡率,须注意多个细节。首先,微量注射管的准备很重要。毛细管尖端的直径、角度和平滑程度均为决定实验成败的关键因素。例如,若尖端太粗,易导致脑脊液的溢出(图1 A-a’);若尖端过细,则易堵塞;尖端无角度(图1 A-b’)或无尖(图1 A-c’)等粗糙的注射针尖更易给胚胎带来不必要的损伤。对微量注射针的尖端进行正确处理后更易于控制注射角度与位置。总之,理想的微量注射器的尖端应满足以下几个方面的要求:直径在40~60µm之间,角度大约15~30°(图1 A-d’),表面光滑锐利。正如表1所示,尖端不合适的微量注射器会导致高死亡率,然而对GFP的阳性率(存活胚胎中GFP阳性胚胎所占的比例)影响较小。本实验均采用理想针尖的微量注射器完成实验。为便于观察并分析电转效果,实验所用质粒均携带GFP/DsRed报告基因。将质粒注射进头部一侧脑室,然后利用镊形电极透过子宫壁向胚胎头部施加方波电脉冲,DNA质粒即被导入毗邻的神经细胞,并向阳极方向移动(图1 B)。
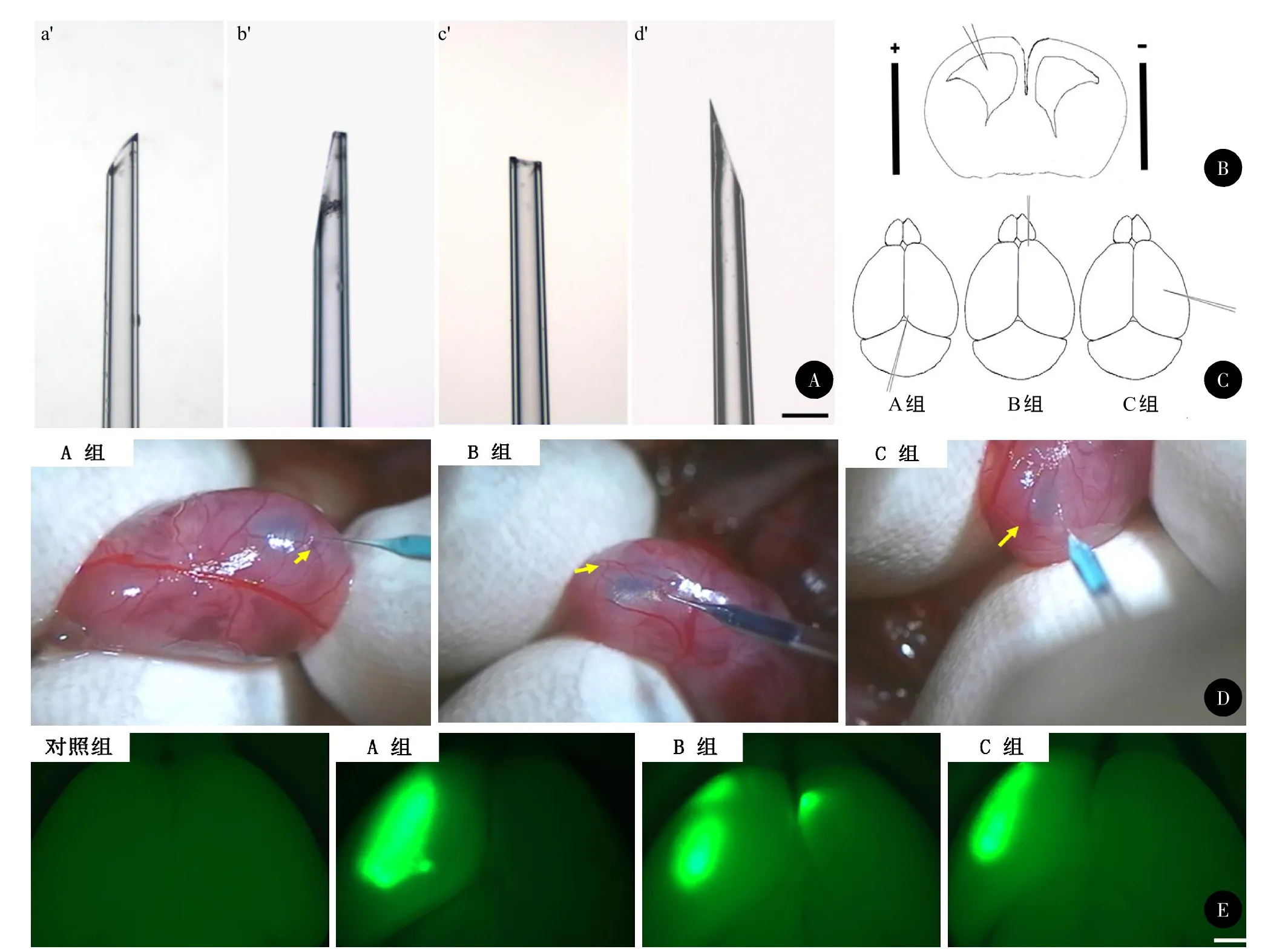
图1 玻璃微量注射针的准备与子宫内电转不同方法穿刺后效果展示
基于不同的穿刺部位,分为四组:对照组,A组,B组和C组(图1C)。当沿着3种途径将DNA质粒注射入侧脑室后,结果显示无论哪种注射途径均可成功表达GFP荧光蛋白(图1D、1E)。如表2示,细胞死亡率和GFP阳性率在各组之间并无统计学差异。
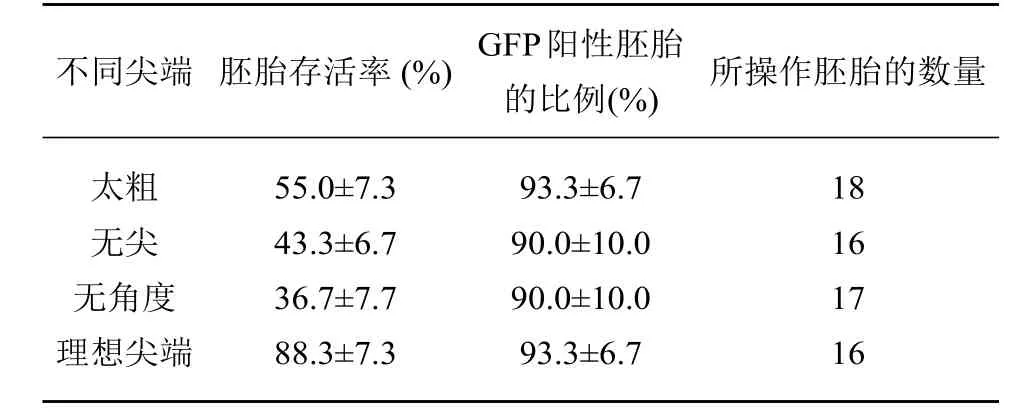
表1 不同尖端对胚胎存活率及GFP阳性率的影响
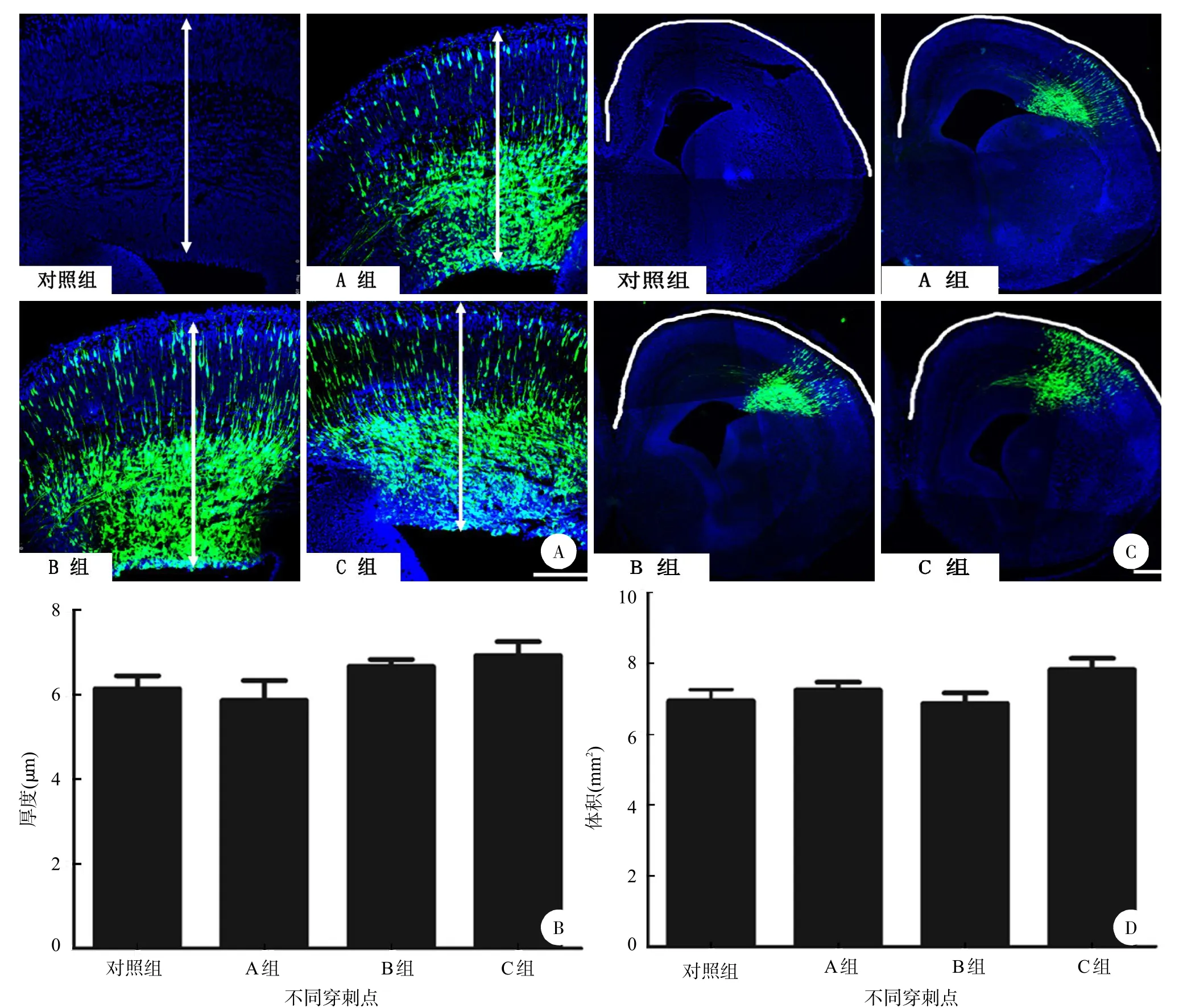
图2 不同穿刺点对皮层厚度与皮层体积的影响
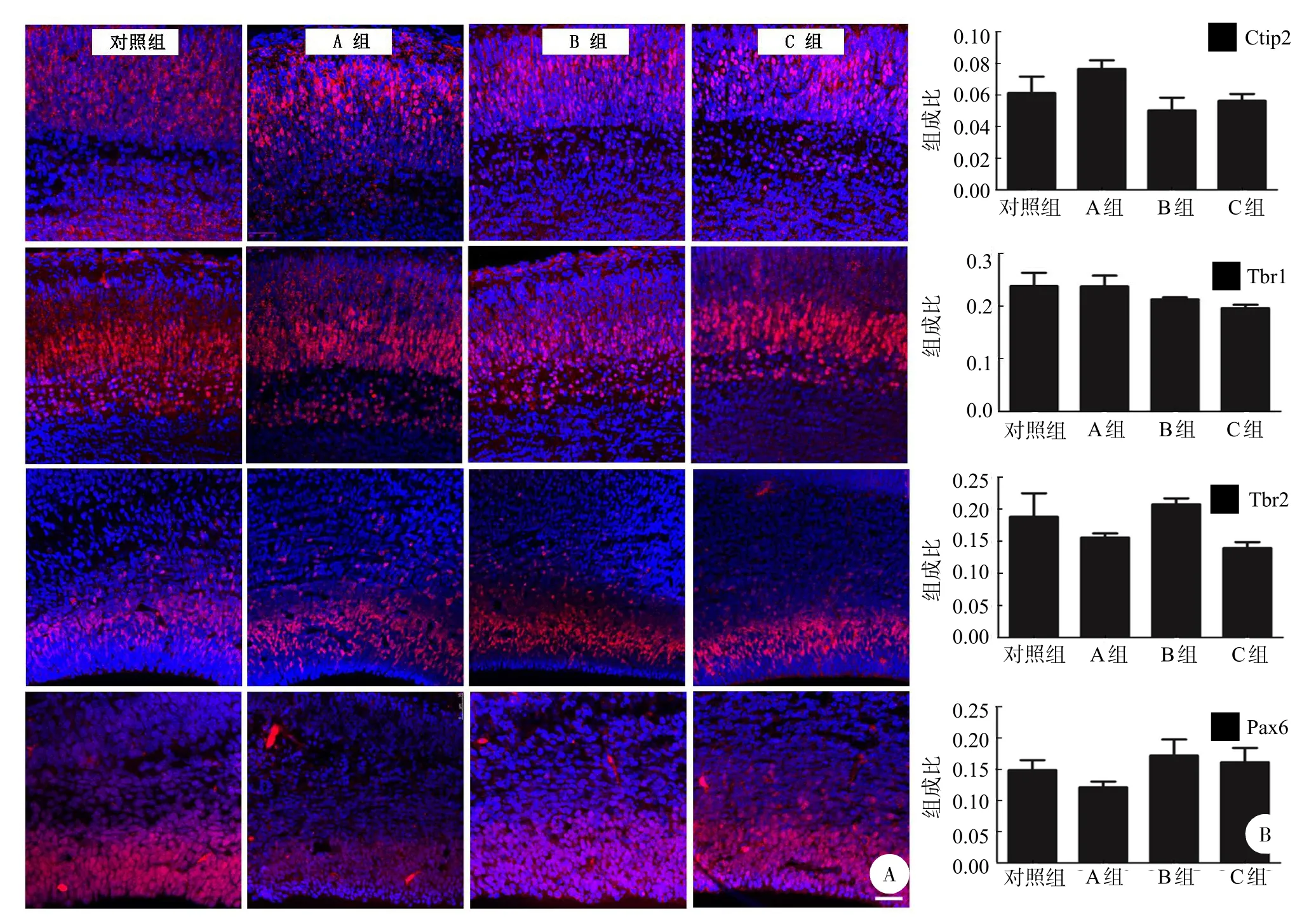
图3 不同穿刺点对细胞分化的影响
本研究同样观察了不同穿刺点对细胞增值和迁移的影响(图4)。Ki67蛋白是细胞增值的标记物。各组之间细胞增值并无明显差异(图4 A、4B)。通过分析不同脑区GFP阳性细胞的比例,发现三种不同穿刺点对VZ/SVZ区细胞的迁移的影响并无统计学意义(图4 A、4C)。Caspase-3进行标记结果表明各组之间并未统计学差异(图4 D、4E)。
综上所述,三种不同的穿刺途径对胚胎的死亡率、皮层厚度、细胞分化、细胞增值、细胞迁移及细胞凋亡并无统计学差异。
讨论
神经发生是早期大脑皮层发育过程中的重要事件,神经干细胞增殖并经历均衡与不均衡性分裂不断迁移分化,并不断发生可塑性变化并与其他神经元建立突触联系从而产生完整的神经功能,发育成为正常的大脑皮层[12,13]。子宫内电转技术需穿过皮层组织进入脑室,穿刺本身对脑组织会造成或轻或重的损伤,尤其是神经前体细胞池的侧脑室(SVZ)部位,分布有大量神经干细胞[13]。
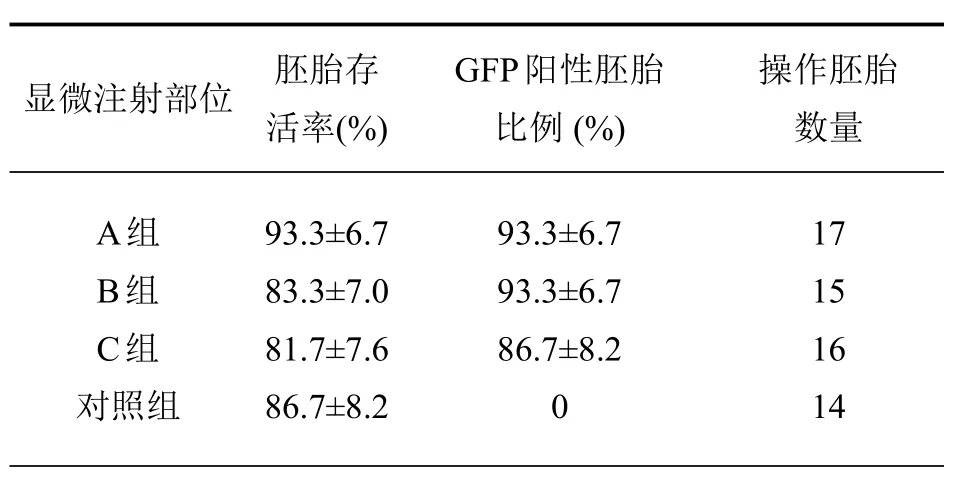
表2 不同穿刺点胚胎存活率及GFP阳性胚胎的比例
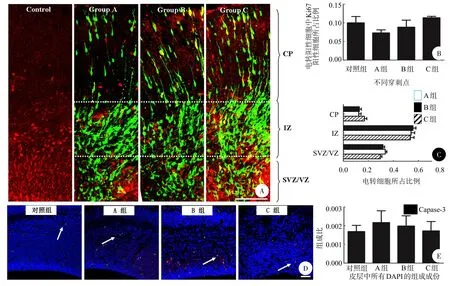
图4 不同穿刺点对细胞增殖、迁移和凋亡的影响
为了研究是否不同的穿刺部位对皮层发育有不同的影响,本实验检测并比较了三种穿刺途径对皮层面积及厚度的影响。结果表明,各组间并无统计学差异(图2)。
在神经发生阶段,背侧端脑脑室区(VZ)前体细胞的子细胞向侧脑室(SVZ)迁移,在到达皮层板(cortical plate,CP)之前,子细胞会再次分裂成为中间神经前体细胞(INP)[14,15]。VZ区分裂后皮层神经元通过不对称分裂依次产生VZ区前体细胞,并再次产生INP,不同区的细胞标记物不同,分别为Pax6(VZ区),Tbr2(SVZ区),Tbr1(layer VI区皮层神经元、layer V和VI区皮层神经元)[16]。为了检测是否不同穿刺部位影响神经干细胞的分化,分别检测了Ctip2,Tbr1,Tbr2和Pax6的表达情况(图3 A、B)。结果表明,各组表达Ctip2,Tbr1,Tbr2和Pax6的情况并无统计学差异。
作为一种在体研究基因功能的方法,子宫内电转技术在神经科学领域的应用越来越广泛。通过该技术,可以精确的对侧脑室的神经前体细胞进行基因过表达或敲低,以观察转染阳性细胞在神经发育过程中对细胞增殖、迁移情况以及形态变化情况的影响[18,19,20]。本研究拟比较到达侧脑室三种不同穿刺途径对皮层发育的影响,从而获得最佳的穿刺点。在同一发育阶段,电转后荧光蛋白表达阳性的细胞在皮层的分布符合神经元inside-out的迁移分布模式[26,27]。以往的研究已经表明Tbr2和Tbr1是同属于T区的转录因子。在胚胎皮层发育过程中,Tbr2的mRNA首先表达于预定皮层板(preplate, PP),接下来会表达在增殖比较旺盛的区域,比如皮层的室管膜下区(SVZ区)以及基底室管膜区(VZ区)[21,16]。然而,Tbr1主要表达于即将分化的皮层前体细胞,即PP区与皮层6区(layer 6)的新生神经元内[22,23]。此外,Pax6主要表达于VZ区,Ctip2高表达于皮层5区(layer 5)[24,25]。上述蛋白作为标记物可用于指示神经前体细胞分化的不同状态。本研究对上述指标进行了检测,发现不同穿刺点之间并无统计学差异。结果表明无论从后囟旁开1 mm穿刺,从头侧沿头-尾轴穿刺,还是从前后囟连线中点旁开1 mm穿刺,虽然均有轻微损伤,然而,其对细胞迁移和分化的影响均无明显差异。结果同样表明,不同穿刺点对皮层厚度与面积亦无明显影响。总之,我们可以采用以上任意一种穿刺点进行实验,不用担心干扰最终的实验结果。
在神经发育过程中,多种因素会对其造成严重影响,因此,在研究中采用一些有利的必要手段是必需的。在科学实验中,人工干预是一个重要且难以避免的因素,有时对研究本身会造成致命的影响。除外本文以上已经介绍的一些影响因素,对子宫内电转技术有影响的因素尚有很多,例如,子宫口附近的胚胎应避免操作,以免流产;如果每只胚胎均从头侧沿头-尾轴进行穿刺,最好固定一种穿刺点,否则需要频繁调整胚胎位置,易对胚胎造成不必要的损伤。除此之外,质粒准备过程需特别谨慎,注意祛除内毒素,否则易增加胚胎死亡率。整个手术操作时间不宜过长,尽量在20~30 min内完成,因为如果过长时间暴露在空气中,易导致胚胎脱水,增加死亡率。此外,镊形电极的钳夹位置,质粒溶液的浓度以及其它因素均会对实验造成很大影响。科学实验应力争以最小的实验损伤刺激获得最佳的实验结果。
[1]Venken KJ,Bellen HJ.Transgenesis upgrades for Drosophila melanogaster[J].Development,2007,134(20)∶3571-3584.
[2]Langevin L M,Mattar P,Scardigli R,et al.Validating in utero electroporation for the rapid analysis of gene regulatory elements in the murine telencephalon[J].Dev Dyn,2007,236(5)∶1273-1286.
[3]Yang N S,Sun W H.Gene gun and other non-viral approaches for cancer gene therapy[J].Nat Med,1995,1(5)∶481-483.
[4]Shukla V K,Doyon Y,Miller J C,et al.Precise genome modification in the crop species Zea mays using zinc-finger nucleases [J].Nature,2009,459(7245)∶437-441.
[5]Tabata H,Nakajima K.Efficient in utero gene transfer system to the developing mouse brain using electroporation∶visualization of neuronal migration in the developing cortex[J].Neuroscience,2001,103(4)∶865-872.
[6]Fukuchi-Shimogori T,Grove E A.Neocortex patterning by the secreted signaling molecule FGF8[J].Science,2001,294(5544)∶1071-1074.
[7]Saito T,Nakatsuji N.Efficient gene transfer into the embryonic mouse brain using in vivo electroporation[J].Dev Biol,2001, 240(1)∶237-246.
[8]Kawasaki H,Toda T,Tanno K.In vivo genetic manipulation of cortical progenitors in gyrencephalic carnivores using in utero electroporation[J].Biol Open,2013,2(1)∶95-100.
[9]Kita Y,Kawakami K,Takahashi Y,et al.Development of cerebellar neurons and glias revealed by in utero electroporation∶Golgi-like labeling of cerebellar neurons and glias[J].PLoS One,2013,8(7)∶e70091.
[10]Taniguchi Y,Young-Pearse T,Sawa A,et al.In utero electroporation as a tool for genetic manipulation in vivo to study psychiatric disorders∶from genes to circuits and behaviors[J].Neuroscientist,2012,18(2)∶169-179.
[11]Gal J S,Morozov Y M,Ayoub A E,et al.Molecular and morphological heterogeneity of neural precursors in the mouse neocortical proliferative zones[J].J Neurosci,2006,26(3)∶1045-1056.
[12]Rash B G,Lim H D,Breunig J J,et al.FGF signaling expands embryonic cortical surface area by regulating Notch-dependent neurogenesis[J].J Neurosci,2011,31(43)∶15604-15617
[13]Takahashi T,Nowakowski R S,Caviness V J.The leaving or Q fraction of the murine cerebral proliferative epithelium∶a general model of neocortical neuronogenesis[J].J Neurosci,1996,16 (19)∶6183-6196.
[14]Noctor S C,Martinez-Cerdeno V,Ivic L,et al.Cortical neurons arise in symmetric and asymmetric division zones and migrate through specific phases[J].Nat Neurosci,2004,7(2)∶136-144. [15]Haubensak W,Attardo A,Denk W,et al.Neurons arise in the basal neuroepithelium of the early mammalian telencephalon∶a major site of neurogenesis[J].Proc Natl Acad Sci U S A, 2004,101(9)∶3196-3201.
[16]Englund C,Fink A,Lau C,et al.Pax6,Tbr2,and Tbr1 are expressed sequentially by radial glia,intermediate progenitor cells,and postmitotic neurons in developing neocortex[J].J Neurosci,2005,25(1)∶247-251.
[17]Kee N,Teixeira C M,Wang A H,et al.Preferential incorporation of adult-generated granule cells into spatial memory networks in the dentate gyrus[J].Nat Neurosci,2007,10(3)∶355-362.
[18]Yeh M L,Gonda Y,Mommersteeg M T,et al.Robo1 modulates proliferation and neurogenesis in the developing neocortex[J].J Neurosci,2014,34(16)∶5717-5731.
[19]Furukawa T,Yamada J,Akita T,et al.Roles of taurine-mediated tonic GABAAreceptor activation in the radial migration of neu-rons in the fetal mouse cerebral cortex[J].Front Cell Neurosci, 2014,8∶88.
[20]Chi Z,Zhang J,Tokunaga A,et al.Botch promotes neurogenesis by antagonizing Notch[J].Dev Cell,2012,22(4)∶707-720.
[21]Bulfone A,Martinez S,Marigo V,et al.Expression pattern of the Tbr2(Eomesodermin)gene during mouse and chick brain development[J].Mech Dev,1999,84(1-2)∶133-138.
[22]Bulfone A,Smiga S M,Shimamura K,et al.T-brain-1∶a homolog of Brachyury whose expression defines molecularly distinct domains within the cerebral cortex[J].Neuron,1995,15 (1)∶63-78.
[23]Hevner R F,Shi L,Justice N,et al.Tbr1 regulates differentiation of the preplate and layer 6[J].Neuron,2001,29 (2)∶353-366.
[24]Chen B,Schaevitz L R,Mcconnell S K.Fezl regulates the differentiation and axon targeting of layer 5 subcortical projection neurons in cerebral cortex[J].Proc Natl Acad Sci U S A,2005,102(47)∶17184-17189.
[25]Lian G,Lu J,Hu J,et al.Filamin a regulates neural progenitor proliferation and cortical size through Wee1-dependent Cdk1 phosphorylation[J].J Neurosci,2012,32(22)∶7672-7684.
[26]Angevine J J,Sidman R L.Autoradiographic study of cell migration during histogenesis of cerebral cortex in the mouse [J].Nature,1961,192∶766-768.
[27]Berry M,Rogers A W.The migration of neuroblasts in the developing cerebral cortex[J].JAnat,1965,99(Pt 4)∶691-709.
Influence of three puncture sites of in utero electroporation on embryonic cortex development
Z hang Peng,Wu Cuiying,Tao Qingxia,Niu Lijun,Chen Wenjin,L iu Ning,Xu Ruxiang.
A ffiliated Bayi Brain Hospital,The Military General Hospital of Beijing P LA,Beijin g 100700,China
Xu Ruxiang,Email:zjxuruxiang@163.com
ObjectiveTo compare the influence of three different puncture sites of in utero electroporation on the death rate of mice embryos,the thickness and the area of cortex,cell differentiation,cell proliferation,cell migration and cell apoptosis.MethodsIt groups on the bases of common puncture sites as follows∶1.electric shock only(control);2.injection near the posterior fontanel,at about one millimeter(here,group A);3.injection along the antero-posterior axis into the cephalic ventricle(group B);and 4.injection near the midpoint between the anterior fontanel and posterior fontanel,at about three millimeters(group C).We compared the four groups using littermate mice,and repeated the experiment with 5 pregnant mice.To detect whether different injection positions affect cell differentiation,cell proliferation,cell migration and cell apoptosis,we stained cells with anti-Tbr1,anti-Tbr2,anti-Pax6 anti-Ctip2,anti-Caspase-3 and anti-Ki67.In differentiation, proliferation,and apoptosis assays,the cell number was analyzed with SPSS 13.0 software,using one way ANOVA.ResultsWe found no statistical significant differences between the three puncture methods in the death rate of embryos,the thickness and the area of cortex,cell differentiation,cell proliferation,cell migration and cell apoptosis(P>0.05).ConclusionThree puncture sites used for in utero electroporation show no significantly different negative impacts during gene transfer into the embryonic mouse brain.
Gene transfer techniques;Puncture;Cell differentiation;Cell proliferation;
2015-06-09)
(本文编辑:杨艺)
DOI∶10.3877/cma.j.issn.2095-9141.2015.04.008
国家自然科学基金青年项目(项目编号:81401031)
北京军区总医院附属八一脑科医院
徐如祥,Email∶zjxuruxiang@163.com
张鹏,吴翠莹,陶庆霞,等.不同穿刺点行子宫内电转对胚胎皮层发育影响的实验研究[J/CD].中华神经创伤外科电子杂志,2015,1(4)∶219-226.
——一道江苏高考题的奥秘解读和拓展

