地佐辛注射液与常用输液的配伍稳定性研究
刘光斌 任洁 何苗苗 高颖
(酒钢医院药学部,甘肃 嘉峪关735100)
地佐辛注射液与常用输液的配伍稳定性研究
刘光斌 任洁 何苗苗 高颖
(酒钢医院药学部,甘肃 嘉峪关735100)
目的:在常温条件下考察8 h内地佐辛注射液与5种常用输液的配伍稳定性。方法:采用高效液相色谱法测定地佐辛注射液在5种输液中的含量变化,同时测定pH值、5-羟甲基糠醛变化。结果:与5种常用输液配伍后,在8 h内pH值和5-羟甲基糠醛基本没有变化,有效成分地佐辛的含量在8 h内基本无变化。结论:地佐辛注射液在5种常用输液中8 h内稳定。
地佐辛注射液;配伍;稳定性;高效液相色谱;含量
地佐辛是阿片受体混合激动-拮抗剂,对κ受体完全激动,对μ受体有部分激动、部分拮抗作用,不产生典型的μ受体依赖,可使胃肠平滑肌松弛,减少恶心呕吐的发生率,对δ受体几乎无活性,很少产生烦躁、焦虑不适感。其镇痛强度、起效时间和作用持续时间与吗啡相当,成瘾性小[1],对血压、心功能影响小[2]。已广泛用于围手术期镇痛、癌性疼痛、无痛麻醉技术等[3]。地佐辛注射液说明书中要求肌内或静脉注射,注射本品可完全快速吸收,建议首选肌注。然而临床实际使用地佐辛注射液与输液配伍静脉输注者仍然比较多[4],而关于地佐辛与常用输液的配伍稳定性未见公开报道。本研究从临床实际需要出发,采用高效液相色谱法(HPLC)对地佐辛注射液与5%葡萄糖注射液,10%葡萄糖注射液,生理氯化钠溶液,5%葡萄糖氯化钠注射液和乳酸林格氏注射液等5种常用输液配伍后的稳定性进行考察,为临床用药提供参考依据。
1 仪器与材料
1.1 仪器
LC-2010AHT型高效液相色谱仪(日本岛津),岛津LC solution工作站;AUY220电子分析天平(日本岛津);756紫外可见分光光度计(上海奥谱勒仪器有限公司);PHS-3C型实验室酸度计(上海伟业仪器厂)。
1.2 药品与试剂
地佐辛对照品(扬子江药业集团有限公司,含量99.9%);地佐辛注射液(扬子江药业集团有限公司,批号:12030121,13102541,14033041,规格:1 mL∶5 mg);5-羟甲基糠醛对照品(含量 >99%,批号:1415620,Aldrich公司);5%葡萄糖注射液(石家庄四药有限公司,规格:250 mL,批号:1403220509);10%葡萄糖注射液(西安京西双鹤药业有限公司,规格:500 mL,批号:1311169B);生理氯化钠溶液(西安京西双鹤药业有限公司,规格:250 mL,批号:131101 6G);5%葡萄糖氯化钠注射液(山东齐都药业有限公司,规格:500 mL,批号:3B13081904);乳酸林格氏注射液(石家庄四药有限公司,规格:500 mL,批号:131218518);乙腈为色谱纯;水为超纯水;其他试剂均为分析纯。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液的制备 精密称取地佐辛对照品20 mg,置100 mL量瓶中,加流动相稀释制成200 μg/mL地佐辛对照品储备溶液。
2.1.2 供试品溶液的制备 取地佐辛注射液1支(5 mg),置100 mL容量瓶中,加流动相稀释至刻度,制成每1 mL约含地佐辛50 μg的溶液。
2.1.3 配伍溶液的制备 取上述5种输液各200 mL,按照临床常用量分别加入地佐辛注射液4支(20 mg),摇匀;即得每1 mL约含地佐辛100 μg的配伍溶液。
2.1.4 阴性样品溶液的制备 参考其处方除不加地佐辛外,其他辅料正常加入,制备阴性制剂。按“2.1.2”项下方法制备阴性对照液。
2.2 检测波长的确定
取地佐辛对照品,用水制成50 μg/mL溶液,置于紫外-可见分光光度计中,以水为空白对照,在200~ 400 nm波长范围内进行扫描,记录紫外吸收光谱图,见图1。由图1可见,地佐辛溶液在282 nm波长有特征吸收峰,故确定本实验中地佐辛的测定波长为282 nm。
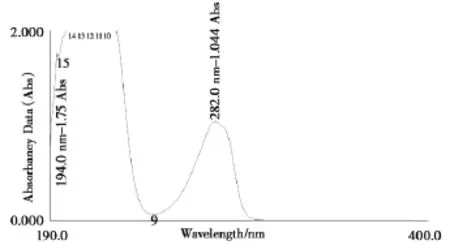
图1 地佐辛紫外吸收光谱图
2.3 色谱条件
色谱柱:Kromasil C18柱(250 mm×4.6 mm,5 μm);流动相:乙腈-三乙胺溶液(取水1 000 mL加三乙胺2.5 mL,用稀磷酸溶液(1→5)调pH值为3.0)(9∶91);流速:1.0 mL/min;柱温:25℃;检测波长:282 nm;进样量:10 μL。地佐辛对照品、阴性对照液、5种配伍剂溶液和5种配伍液的色谱图见图2。由图2可见,阴性对照液中的辅料和6种配伍剂溶液对配伍液中地佐辛的测定不产生干扰。
2.4 线性关系考察
分别精密量取200 μg/mL地佐辛对照品储备溶液,加流动相配制成浓度分别为25.0,50.0,100.0,150.0,200.0 μg/mL的溶液。按“2.3”项下色谱条件测定峰面积。以峰面积(A)对质量浓度(C)进行线性回归,得回归方程:
A=12 169.26 C+2 627.078,
r=0.999 999,n=5。结果表明地佐辛在25.0~ 200.0 μg/mL浓度范围内峰面积与质量浓度呈良好的线性关系。见图3。
2.5 精密度试验
取“2.4”项下浓度100.0 μg/mL的溶液,按照“2.3”项色谱条件重复进样 6次,记录峰面积,测得RSD=0.36%。结果表明,该方法精密度良好。

图2 高效液相色谱图注:A阴性对照液;B地佐辛对照品溶液;C生理氯化钠溶液;D生理氯化钠溶液配伍液;E乳酸林格氏注射液;F乳酸林格氏注射液配伍液;G 5%葡萄糖氯化钠注射液;H 5%葡萄糖氯化钠注射液配伍液;I 5%葡萄糖注射液;J 5%葡萄糖注射液配伍液;K 10%葡萄糖注射液;L 10%葡萄糖注射液配伍液;M 5-羟甲基糠醛对照品溶液;1地佐辛;2 5-羟甲基糠醛
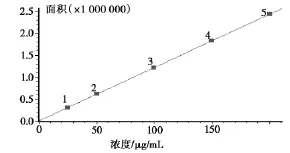
图3 地佐辛标准曲线
2.6 重复性试验
取批号为 14033041的地佐辛注射液 5支(5 mg),按“2.1.2”项制备样品溶液5份。按“2.3”项色谱条件分析测定,结果供试品中地佐辛平均含量为99.60%,RSD为0.78%,低于1.5%的要求。
2.7 回收率试验
取已知含量的同批样品 3份(14033041),分别取 2支(10 mg),再分别精密加入地佐辛对照品8 mg(80%),10 mg(100%),12 mg(120%),按“2.1.2”项制备溶液。按“2.3”项色谱条件测定,记录色谱图,用回归方程计算,然后计算加样回收率。结果表明,该含量测定方法回收率良好。见表1。
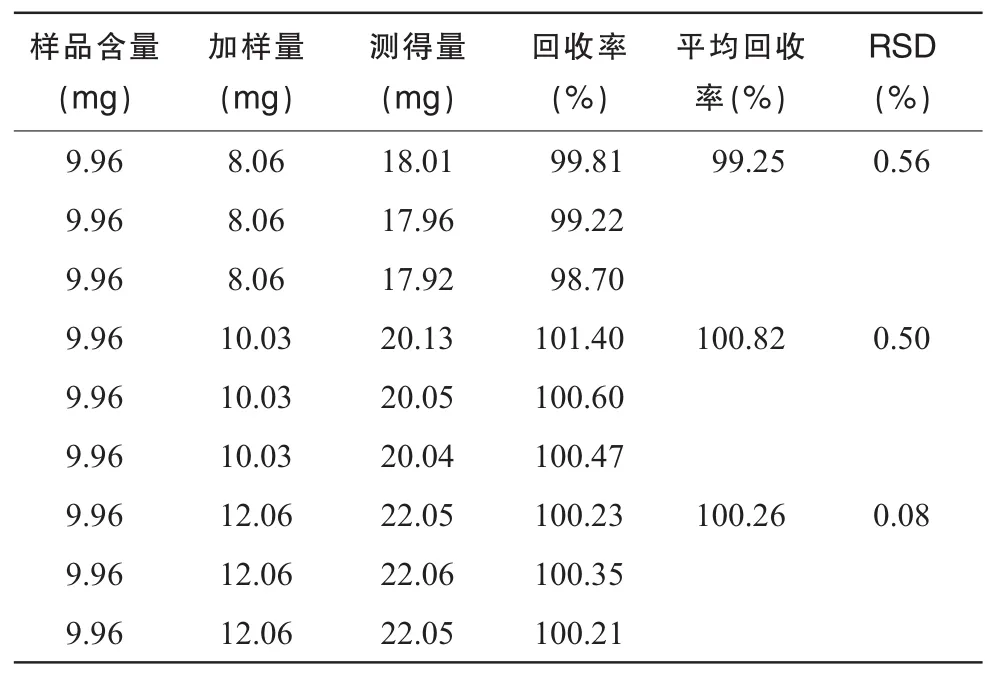
表1 回收率试验结果(n=9)
2.8 含量测定
分别取批号为12030121,13102541,14033041的地佐辛注射液各5支(5 mg),按“2.1.2”项制备样品溶液。按“2.3”项色谱条件测定,记录色谱图,按外标法以峰面积计算。结果见表2。
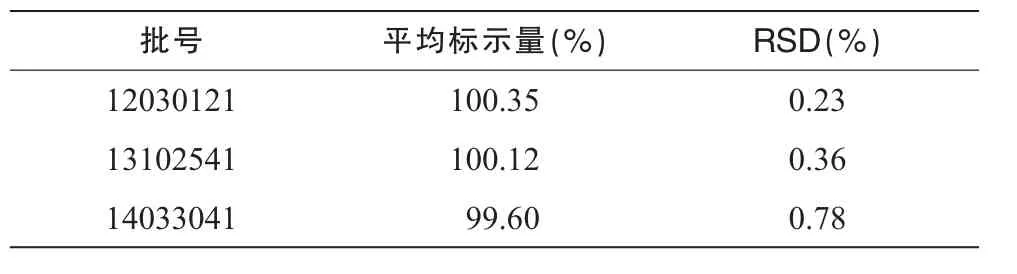
表2 样品含量测定结果(n=5)
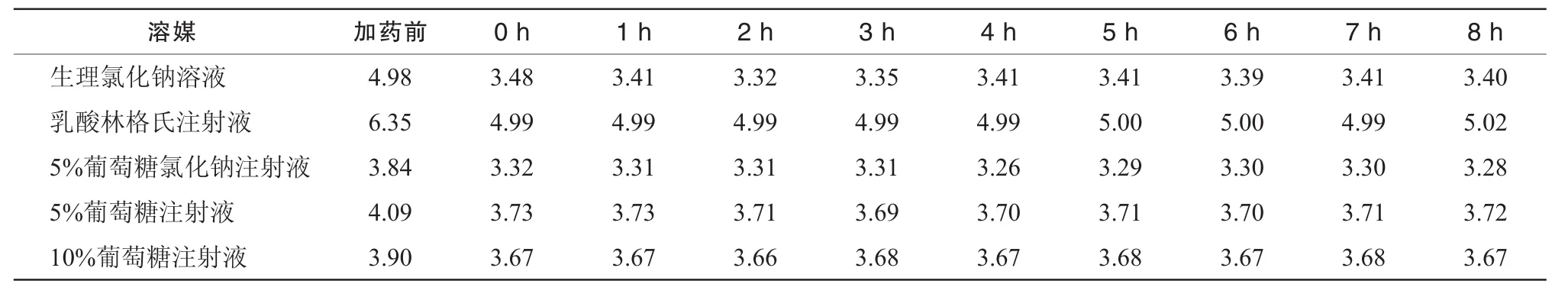
表3 5种配伍液在不同时间点的pH值测定结果

表4 5种配伍液中地佐辛的相对含量变化结果 (%)
2.9 配伍稳定性考察[5]
2.9.1 pH值变化情况 在室温下测定5种输液的pH值后,模拟临床用药,将地佐辛注射液 20 mg与生理氯化钠溶液,乳酸林格氏注射液,5%葡萄糖氯化钠注射液和5%,10%葡萄糖注射液各200 mL配伍后,在0,1,2,3,4,5,6,7,8 h时分别测定配伍液的pH值。因地佐辛注射液本身呈弱酸性,所以添加地佐辛注射液后的5种配伍液的pH值均有所下降,试验结果见表3。结果表明5种含药输液的pH值在加药后8 h内均未发生显著变化。
2.9.2 地佐辛含量变化情况 在室温(25±1)℃下,模拟临床用药,将地佐辛注射液20 mg与5种输液各200 mL配伍后,在0,1,2,3,4,5,6,7,8 h时分别按照“2.1.3”项制备配伍溶液,测定配伍溶液放置不同时间地佐辛的含量。试验结果见表4,结果表明5种含药输液的地佐辛含量均无显著变化。2.9.3 5-羟甲基糠醛(5-hydroxymethyl furfural,5-HMF)含量的变化 按照文献方法[6],取 5-HMF对照品适量,精密称定,加水制成每1 mL中约含10 μg的溶液,取20 μL注入液相色谱仪,色谱条件同地佐辛含量测定。在此色谱条件下,5-HMF与地佐辛能够很好地分离。经过考察,其精密度、稳定性、回收率试验均符合要求。
在测定配伍液中地佐辛浓度的同时检测5-HMF的含量。试验结果见表5。
根据《中国药典》2010年版规定:葡萄糖注射液中5-HMF“在284 nm的波长处测定,吸光度不得大于0.32”。有研究认为[7],《中国药典》所规定的“吸光度不得大于 0.32”时相对应的 5-HMF浓度约为2 μg/mL,所有葡萄糖类注射液中5-HMF的限度应定为 2 μg/mL。本试验结果表明3种含葡萄糖配伍液的5-HMF的吸光度均小于2 μg/mL,在限度控制范围内,且在8 h内无显著变化。
2.9.4 有关物质测定 取配伍溶液作为供试品溶液;另精密量取供试品溶液2.5 mL置100 mL量瓶中,加流动相稀释至刻度作为对照溶液;按“2.3”项色谱条件测定,对照溶液以 20 μL进样,调节检测灵敏度,使地佐辛的峰高约为满量程的20%;再取供试品溶液以20 μL进样,记录色谱图至地佐辛峰保留时间的3.5倍,结果见表6。结果表明,供试品溶液色谱图中杂质峰面积(5-HMF峰和溶剂峰除外)的和均小于对照溶液主峰面积(2.5%),未见有新物质峰出现。
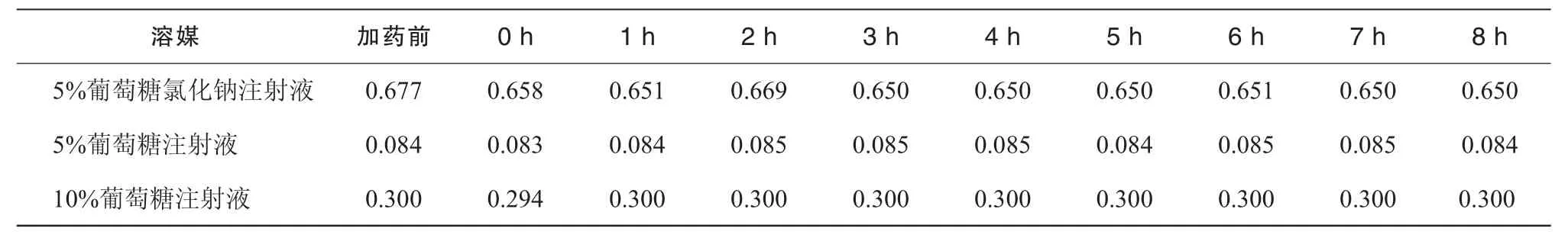
表5 3种含糖配伍液的5-HMF含量变化结果 (μg/mL)

表6 5种配伍液中有关物质变化结果 (%)
2.9.5 溶液颜色变化和可见异物观察 在0,1,2,3,4,5,6,7,8 h时分别用灯检法检查5种配伍液的颜色,并观察有无可见异物。结果配伍液在8 h内颜色均无变化,亦无明显可见异物,检查结果符合规定。
3 讨论
国家食品药品监督管理总局批准的地佐辛注射液的试行标准(YBH09182006)中,地佐辛的含量采用分光光度在281 nm波长处测定。含糖输液中5-HMF的最大吸收波长为284 nm,因此在研究地佐辛与含糖输液的配伍时无法用分光光度法直接测定地佐辛的含量。本研究建立了地佐辛注射液含量的HPLC测定方法,方法简便、准确、灵敏度高,可用于该药品的含量测定。
5-HMF是葡萄糖等单糖化合物在高温或弱酸等条件下脱水产生的一个醛类化合物,该化合物对人体横纹肌和内脏有损害[7],而地佐辛注射液与含有葡萄糖的输液所配溶液均呈弱酸性,在放置过程中可能会分解产生5-HMF。因此有必要检测和控制5-HMF的含量。
试验结果表明:地佐辛与5种输液配伍液的pH值、主药含量在前8 h变化不显著,地佐辛与3种含葡萄糖输液配伍液的5-HMF的含量在8 h内均在限度控制范围内;经有关物质测定,不同时刻的HPLC色谱图也未见有新物质色谱峰出现;地佐辛的5种配伍液在不同时间颜色无显著变化,也无明显可见异物,说明地佐辛与临床5种常用输液配伍在8 h内是相对稳定的。需要特别指出的是:药品应遵照说明书使用,本试验结果仅可为临床特殊情况下使用地佐辛注射液提供参考。
[1] Loeniskar A,Greenblatt DJ,Zinny MA.Pharmacokinetics of dezocine,a new analgesic:effect of dose and route of administration[J].Eur J Clin Pharmacol,1986,30(1):121-123.
[2] O’Brien JJ,Benfield P.Dezocine a preliminary review of its pharmacodynamic and pharmacokinetic properties and therapeutic efficacy[J].Drugs,1989,38(2):226-248.
[3] 耿立成,李丽,冯洁.地佐辛药理及临床应用新进展[J].医学综述,2012,18(23):4029-4031.
[4] 柯秀容,王小芳.静脉输注地佐辛致260例不良反应分析[J].海峡药学,2012,24(10):271.
[5] 刘光斌,赵丽萍,姜芳宁,等.注射用间苯三酚与6种常用输液的配伍稳定性考察[J].中国药房,2013,24(10):918-920.
[6] 曾令高.高效液相色谱法测定替硝唑葡萄糖注射液中5-羟甲基糠醛含量[J].中国药业,2010,19(19):18-19.
[7] 何伍,凌霄.含葡萄糖注射液中5-羟甲基糠醛限度的检测方法[J].中国医药工业杂志,2008,39(1):47-49.
Study on the Compatible Stability of Dezocine Injection in Commonly Used Infusions
Liu Guangbin,Renjie,He Miaomiao,Gao Ying(Department of Pharmacy of Jiugang Hospital,Gansu Jiayuguan 735100,China)
Objective:To study the compatible stability of dezocine injection dissolved in five commonly used infusions within 8 hours at a normal temperature.Methods:The content of compatible dezocine in the five transfusions were determined by HPLC and the pH values and 5-HMF of the solutions were also measured. Results:The pH values and 5-HMF and the effective components of dezocine dissolved in five infusions had basically no change within 8 hours.Conclusion:Dezocine injection was stable when compatible with 5 commonly used infusions within 8 hours.
Dezocine Injection;Compatibility;Stability;HPLC;Content
10.3969/j.issn.1672-5433.2015.11.003
2015-07-04)
刘光斌,男,主任药师。研究方向:临床药学、医院药学。E-mail:jgyylgb@sina.com

