前列地尔注射液在造影剂肾病中的预防作用
郑剑武 徐正明 黄世恩 骆荣华 沈 斌
前列地尔注射液在造影剂肾病中的预防作用
郑剑武 徐正明 黄世恩 骆荣华 沈 斌
造影剂肾病;冠状动脉造影;前列地尔注射液
近年来随着心内科介入诊治术的广泛开展,临床造影剂应用日益增多,造影剂相关并发症也相应增多,造影剂肾病(contrast-induced nephro-pathy,CIN)的发生率明显增加。CIN成为继低灌注性和药物性急性肾损伤后院内获得性肾损害(ARF)的第三位病因[1],也是影响介入手术远期疗效的重要因素。因此,加强PCI术后CIN的预防,对改善患者的预后具有极为重要的意义。目前关于CIN尚无满意的治疗方案,但积极有效的预防措施可降低CIN发病率,降低CIN死亡率[2]。笔者发现,冠状动脉造影术患者术前应用前列地尔注射液可有效预防CIN的发生,现报道如下。
1 临床资料
1.1 一般资料 2012年1月—2013年12月本院收治并行冠脉造影(CAG)或经皮冠状动脉介入治疗(PCI)术患者共328例,其中合并高血压患者278例,既往吸烟169例。均满足以下纳入标准:怀疑有冠心病可能,具有冠脉造影的指征,术前24h及术后24h、48h接受血清Cr浓度检测。排除:①围手术期间使用肾毒性药物者。②严重肝肾功能不全或肾移植史。③肿瘤患者。④重度心力衰竭。⑤甲状腺或肾上腺功能紊乱。⑥急慢性感染性疾病、高热。研究终止标准[3]:治疗期间出现无法耐受的严重不良反应、严重并发症或发现其他重大疾病。本研究采用随机单盲方法,将328例患者分为治疗组164例,男103例,女61例,年龄38~82岁,平均(68.84±10.01)岁;高血压病138例,吸烟88例;安慰剂组164例,男99例,女65例,年龄41~83岁,平均(65.84±9.83)岁;高血压病140例,吸烟81例;两组患者年龄分布、性别构成和合并症情况等一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 CIN诊断标准 使用造影剂后24~48h,血清肌酐(Scr)水平较术前升高0.5mg/dL(44.2μmol/L)或较基础值上升25%,并排除心衰、严重心律失常、心肌梗死等其它影响因素,定义为发生CIN[4]。Morcos SK等[5]证实出现CIN的患者,即Scr较术前升高25%或升高绝对值超过0.5mg/dl(44.2μmol/L),患者死亡风险增加10.09倍。
2 治疗方法
所有患者均使用低渗非离子造影剂碘普罗胺(商品名:优维显),手术采用Seldinger技术经股动脉或桡动脉径路完成冠脉造影剂PCI,所有患者均用0.9%氯化钠溶液进行常规水化。其中治疗组164例行冠脉造影术前30min给予前列地尔(商品名:凯时)10μg经10mL生理盐水稀释后静脉推注。安慰剂组164例行冠脉造影术前给予10mL生理盐水静脉推注,比较术前当天、术后24h、术后48h测定空腹血清肌酐(Scr)。观察两组CIN的发生率。
观察指标:测定患者术前当天及术后24h、48h血清肌酐(Scr)。均由本院化验室采用相同的仪器与试剂进行检测。
统计学方法:应用SPSS19.0软件对数据进行处理与分析。血清肌酐以均值和标准差(±s) 表示,组间比较采用t检验;CIN发病率采用卡方检验。P<0.05为差异有统计学意义。
3 治疗结果
3.1 两组血清肌酐(Scr)浓度比较 328例患者均成功完成冠脉造影检查或PCI治疗,观察期间均未出现无法耐受的严重不良反应、严重并发症或其他重大疾病。治疗组和安慰剂组患者术前血清肌酐(Scr)浓度比较差异无统计学意义(P>0.05),治疗组术后24h、48h血清肌酐(Scr)浓度与术前当天比较差异无统计学意义(P>0.05)。安慰剂组术后24h血清肌酐(Scr)浓度高于术前当天,差异有统计学意义(P<0.05)。术后24h血清肌酐(Scr)浓度安慰剂组高于治疗组,差异有统计学意义(P<0.05),见表1。
3.2 两组CIN发病率比较 治疗组术后出现CIN 9例,发病率5.49%;安慰剂组术后出现CIN 17例,发病率10.37%。治疗组CIN发病率明显低于安慰剂组,差异有统计学意义(P<0.05)。
表1 两组冠脉造影术前后血肌酐(Scr)水平比较(μmol/L,±s)
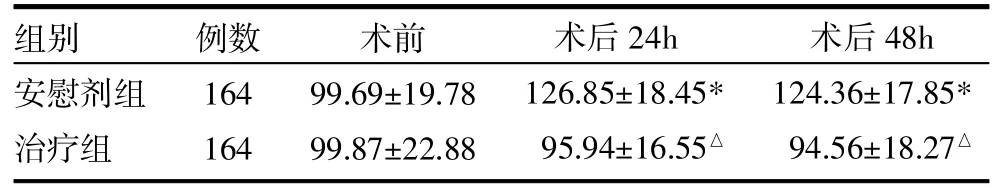
表1 两组冠脉造影术前后血肌酐(Scr)水平比较(μmol/L,±s)
注:与术前比较,*P<0.05;与安慰剂组比较,△P<0.05
组别安慰剂组治疗组例数164 164术前99.69±19.78 99.87±22.88术后24h 126.85±18.45* 95.94±16.55△术后48h 124.36±17.85* 94.56±18.27△
4 讨论
造影剂肾病(CIN)是指放射学造影术后无其他原因所致的急性肾功能减退,通常于造影后48h内出现,临床表现为外周血肌酐(Cr)水平上升,或绝对浓度值上升,呈非少尿型急性肾衰竭。目前认为,CIN的发生与肾功能受损、高龄、糖尿病、心力衰竭、贫血等多种因素有关[6-8]。临床CIN发生率约为9%~14%,如合并肾功能衰竭、糖尿病等高危因素时造影剂肾病的发生率会显著升高,高危患者造影剂肾病的发病率可高达20%,而在多个高危因素同时并存时,其发病率可高达40%~90%[9-10]。由造影剂所致急性肾功能衰竭患者中仅57.2%的患者肾脏功能可完全恢复,24.0%的患者最终发展至终末肾脏功能衰竭[11]。
研究表明CIN的病理机制与以下因素相关:①肾血流动力学改变,造影剂引起肾血管收缩和肾小管管型堵塞,使肾血流减慢,髓质缺血、缺氧引起损伤。②造影剂的肾毒性,通过氧自由基对肾小管有直接毒性作用,引起近端肾小管上皮细胞空泡形成,间质水肿和小管变性[12-13]。临床对于CIN预防措施有限。针对以上发病机制,有一定作用的预防手段主要有水化治疗、N-乙酰半胱胺酸(NAC)及选择对比剂的渗透性及剂量等方式。水化治疗可增加血容量,改善造影剂引起的肾组织缺血状态,增加体内体液和水的排出,减少药物在肾小管重吸收,防止肾小管内结晶等,被认为是预防CIN的经典手段。本研究也以常规水化治疗为基础,但从研究结果看,安慰剂组CIN的发生率与既往结果类似。而前列地尔组却明显减少CIN的发生,研究[14]发现,前列地尔注射液通过多个环节改善肾功能、扩张肾血管、增加肾血流量、抑制血小板聚集、防止血栓形成、降低血液黏度和红细胞聚集性、介导和恢复基底膜蛋白合成、抑制炎性介质产生和炎性细胞浸润、改善心功能、稳定循环、维持肾脏灌注等。
本组结果显示,与安慰剂组相比,术前使用前列地尔能够有效降低使用造影剂后血清肌酐的增加速度,减少肾功能损伤。但得出进一步可靠结论仍需扩大研究样本量和进行基础实验研究。
[1]Nash K,Hafeez A,Hou S.Hospital-acquired renal insufficiency[J].Am JKidney Dis,2002,39(5):930-936.
[2]James MT,Samuel SM,Manning MA,et al.Contrast-in duced acute kidney injury and risk of adverse clinical outcomes after coronary angiography:a systematic review and metaanalysis[J].Circ Cardiovasc Interv,2013,6(1):37-43.
[3]左伟,高君武,王海涛.强化护理联合前列腺素E1水化治疗在预防造影剂肾病中的作用[J].检验医学与临床,2014,(3):409-411.
[4]Stacul F,van der Molen AJ,Reimer P,et al.Contrast in duced nephropathy:updated ESUR ContrastMedia Safety Committee guidelines[J].Eur Radiol,2011,21(12):2527-2541.
[5]Morcos SK.Prevention of contrast media nephrotoxicity-the story so far[J].Clin Radiol,2004,59(5):381-389.
[6]Senoo T,Motohiro M,Kamihata H,et al.Contrast-induced nephropathy in patients undergoing emergency percutaneous coronary intervention for acute coronary syndrome[J]. Am JCardiol,2010,105(5):624-648.
[7]La Manna G,Pancaldi LG,Capecchi A,et al.Risk for contrast nephropathy in patients undergoing coronarography[J]. Artif Organs,2010,34(6):E193-199.
[8]Cronin RE.Contrast-induced nephropathy:pathogenesis and prevention[J].Pediatric nephrology(Berlin,Germany),2010,25(2):191-204.
[9]Ultramari FT,Bueno RR,da CCL,et al.Contrast media-induced nephropathy following diagnostic and therapeutic cardiac catheterization[J].Arquivos brasileiros de cardiologia,2006,87(3):378-390.
[10]Toprak O.Risk markers for contrast-induced nephropathy[J].Am JMed Sci,2007,334(4):283-290.
[11]Laville M,Juillard L.Contrast-induced acute kidney in jury:how should at-risk patients be identified and managed[J]. JNephrol,2010,23(4):387-398.
[12] Mathur VS.Pathophysiology of radiocontrast nephropathy and use of fenoldopam for its prevention[J].Rev Cardiovasc Med,2001,2 Suppl 1:S4-8.
[13]Heyman SN,Reichman J,Brezis M.Pathophysiology of radiocontrast nephropathy:a role for medullary hypoxia[J]. Invest Radiol,1999,34(11):685-691.
[14]Sketch MH Jr,Whelton A,Schollmayer E,et al.Prevention of contrastmedia-induced renal dysfunction with prostaglandin E1:a randomized,double-blind,placebo-controlled study[J].Am JTher,2001,8(3):155-162.
(收稿:2014-11-04 修回:2015-01-19)
杭州市医药卫生及重点专科专病科研专项(No.20140733Q27)
浙江省中西医结合医院心内科(杭州 310003)
郑剑武,Tel:18957119186;E-mail:108646675@qq.com

