壳聚糖包埋魔芋组合物对Pb(Ⅱ)和胆固醇的吸附研究
朱唯唯,罗立新,王 玉
(武汉大学化学与分子科学学院,湖北武汉 430072)
壳聚糖包埋魔芋组合物对Pb(Ⅱ)和胆固醇的吸附研究
朱唯唯,罗立新*,王 玉
(武汉大学化学与分子科学学院,湖北武汉 430072)
将魔芋葡甘聚糖颗粒在常温下溶于壳聚糖稀酸溶液制成的包埋液,制备能够保持魔芋助消化及降低血中胆固醇浓度等优良特性的新品种魔芋,并用红外光谱仪进行表征。通过静态吸附的方法系统探讨了吸附质初始浓度、吸附剂用量、吸附时间对Pb2+和胆固醇吸附效果的影响,并采用吸附动力学模型和等温吸附方程进行拟合。结果表明:产品同时具有魔芋葡甘聚糖和壳聚糖的功能基团;在37 ℃下,Pb2+和胆固醇的最大去除率分别为95.2%和48.7%;吸附过程符合准二级动力学方程和Freundlich吸附等温模型。说明壳聚糖包埋魔芋组合物可有效地吸附Pb2+和胆固醇,且属于不均匀表面的吸附。
魔芋葡甘聚糖,吸附,铅离子,胆固醇,包埋
魔芋是一种广泛种植于我国西部山区的经济作物,魔芋葡甘聚糖是其主要成分,也是国际卫生组织推荐的理想膳食纤维,具有不产生热量、强吸水、可凝胶化特性[1],在食品、保健、医药等多方面有重要用途[2],能够助控体重[3]、排除重金属离子[4]、控制血脂[5]、缓解便秘[6]及控制血糖[7]等。目前,针对魔芋膳食纤维特性的研究主要集中于直接使用的魔芋或交联后的魔芋颗粒[8],但魔芋葡甘聚糖在热水中会快速溶解,使得魔芋粉剂冲制的饮料会快速凝胶化,饮用方式也不太符合人们的常规要求,而交联又牺牲了魔芋的特性。所以,在保持魔芋原有的优良特性的基础上,开发出一种便于使用的魔芋产品显得尤为重要。壳聚糖是甲壳素经浓碱脱乙酰基后得到的衍生物,溶于稀酸,因此本文设计了一种壳聚糖包埋魔芋组合物[9],其在水中不溶或慢速溶解,可以保留魔芋葡甘聚糖的大多数优良特性,用于制备魔芋固体饮料原料或用作化妆品的添加剂等。对于这种产品的特性研究,本文选用高血脂代表性物质胆固醇和以Pb2+为代表的重金属离子为对象,考察了吸附效果,分析了吸附质浓度、吸附剂质量及吸附时间对吸附效果的影响,并用动力学模型和等温方程对其吸附行为进行了研究,以通过模拟实验的方式为其应用提供一定的理论基础。
1 材料与方法
1.1 材料与仪器
魔芋粉(葡甘聚糖含量82.29%,125~180 μm) 武汉纤浓生物科技有限公司;壳聚糖(脱乙酰化度90%) 潍坊海之源生物制品有限公司;壳聚糖包埋魔芋组合物 自制;其他试剂均为国产分析纯。
UV752紫外可见分光光度计 上海佑科仪器仪表有限公司;SHA-c数显水浴恒温振荡器常州博远实验分析仪器厂;JZ-2数显离心机 金坛市洪科仪器厂;傅里叶红外光谱仪iS10 美国Thermo公司。
1.2 实验方法
1.2.1 吸附材料的制备 根据文献[9]将1.5 g壳聚糖溶于含有2.25 mL冰醋酸的150 mL 30%乙醇溶液(体积百分数),配制成包埋液。于室温下在包埋液中加入20 g魔芋粉,搅拌30 min后再加入4. 5 g碳酸钠进入体系中,60 ℃固化2 h。经离心分离固形物,清洗干燥后即得壳聚糖包埋魔芋组合物原料(KGM@CTS),包埋组合示意图如图1,魔芋葡甘聚糖颗粒表面被壳聚糖包裹。包埋前后官能团的变化采用FT-IR进行分析。

图1 包埋组合示意图Fig.1 Scheme of embedding
1.2.2 浓度的测定 Pb2+和胆固醇浓度的测定分别参照GB7470-87水质铅的测定 双硫腙分光光度法[10]和GB/T5009.128-2003食品中胆固醇的测定[11]。
1.2.3 不同初始浓度对吸附的影响 配制50 mL一系列质量浓度的吸附质溶液,其中,Pb2+和胆固醇分别处于pH为5.5的缓冲溶液和冰乙酸溶液中,均加入1.0 g/L KGM@CTS,在37 ℃恒温振荡120 min,离心分离,取上层清液测定剩余吸附质的浓度,每组实验均重复3次,取平均值,用吸附量[12]表示吸附效果。
1.2.4 不同吸附剂质量对吸附的影响 分别配制50 mL 240 mg/L Pb2+溶液和3.0 g/L胆固醇溶液,均加入一系列质量浓度的 KGM@CTS,在37 ℃恒温振荡120 min,离心分离后测定,用去除率[12]表示吸附效果。
1.2.5 不同吸附时间对吸附的影响 配制50 mL 240 mg/L Pb2+溶液和3.0 g/L胆固醇溶液,分别向其中加入2 g/L和1 g/L KGM@CTS,均在37 ℃恒温振荡一系列不同的时间,离心分离后测定,用吸附量表示吸附效果。
1.2.6 不同pH对吸附的影响 研究发现[13],大多数膳食纤维在pH为6时对金属离子的束缚能力最强,pH为0.65时解析释放,所以,本文考察了pH对于Pb2+吸附的影响,设计了一组实验:配制50 mL 240 mg/L Pb2+溶液,改变溶液的pH分别为2.5、3.5、4.5、5.5、6.5,加入2.0 g/L KGM@CTS,在37 ℃恒温振荡80 min,离心分离后测定,用去除率表示吸附效果。
1.2.7 正交设计实验 对于Pb2+,在确定的初始浓度、吸附剂质量、吸附时间和pH单因素实验结果的基础上,选用L9(34)正交表1进行实验;在胆固醇正交实验中,对初始浓度、吸附剂质量和吸附时间三个因素选用L9(33)正交表2进行,以去除率为考察指标,找出最佳吸附条件。
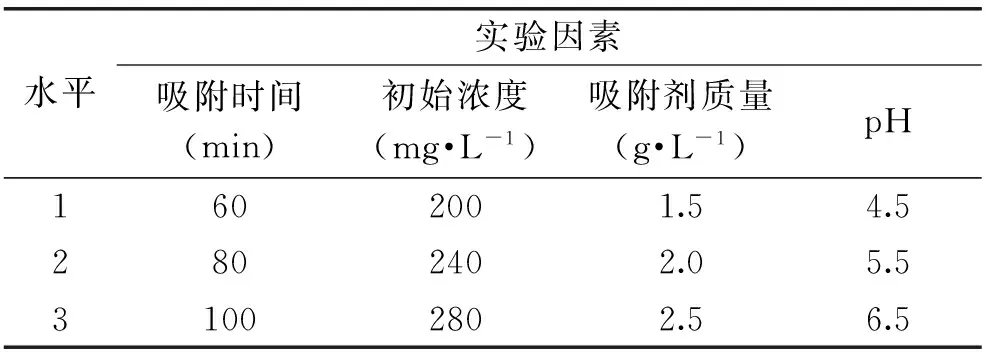
表1 Pb2+正交设计表

表2 胆固醇正交设计表
2 结果与讨论
2.1 壳聚糖包埋魔芋组合物的表征
在图2中,a和b的显著差别在于1600 cm-1处壳聚糖有-NH2面内弯曲振动吸收峰,而c中可以看到1574 cm-1的壳聚糖特征峰,说明壳聚糖包埋效果的存在。从d中可以看出,KGM@CTS用稀酸溶洗再用醇析出后的固体成分的谱图中壳聚糖特征峰几近消失,可以认为这主要是壳聚糖被溶解后的魔芋成分。

图2 红外光谱图Fig.2 FT-IR spectra
2.2 不同条件对壳聚糖包埋魔芋组合物吸附性能的影响

图3 初始浓度对吸附效果的影响Fig.3 Effect of initial concentration on sorption efficiency
2.2.1 初始浓度对吸附效果的影响 实验结果如图3所示,对于铅离子,吸附量随着Pb2+浓度升高而明显增大,然后趋于平衡达到饱和状态。当初始浓度由60 mg/L提高到240 mg/L时,吸附量由68.77 mg/g增至134.26 mg/g,由于魔芋颗粒易溶于水无法形成吸附对比,而罗立新等[8]研究的不溶于水的交联魔芋葡甘聚糖微球离子交换容量为约44 mg/g,这说明KGM@CTS对Pb2+的吸附能力要优于交联魔芋葡甘聚糖,同时也表明,在未达到饱和状态之前,Pb2+浓度越大,该材料的利用率也越高。
对于胆固醇,KGM@CTS的吸附作用随其浓度增加而增大,在胆固醇浓度为0.1~1.0 g/L时,吸附量明显增加,浓度为1.0~3.0 g/L时,吸附量增幅较小。在3.0 g/L左右时,吸附量达到最大值146.80 mg/g,与陈亚非等[14]研究的水不溶性膳食纤维对胆固醇的作用所得到的最高吸附量40.75 mg/g,本文结果更好。
2.2.2 吸附剂的质量对吸附效果的影响 实验结果如图4所示,可以看出,吸附剂的用量会明显影响其吸附效率,Pb2+的去除率在吸附剂加入量为2 g/L时达到最大值92.5%,胆固醇的去除率在吸附剂加入量为1 g/L时达到最大值36.0%。研究表明,在同样的吸附条件下,KGM@CTS对二者的吸附作用有较大不同,这可能跟两者与KGM@CTS结合方式的不同及溶液的性质有较大关系。

图4 吸附剂质量对吸附效果的影响Fig.4 Effect of adsorbent dosage on sorption efficiency
2.2.3 吸附时间对吸附效果的影响 实验结果如图5所示,可以看出,在吸附初始阶段,吸附剂对Pb2+的吸附呈线性递增趋势,在进行80 min左右的时候接近最大值并进入平衡状态,而对于胆固醇,在120 min时,达到了吸附平衡,吸附量为129.76 mg/g,平衡后随着时间的增大,吸附量基本不变。

图5 吸附时间对吸附效果的影响Fig.5 Effect of contact time on sorption efficiency
2.2.4 pH对吸附效果的影响 溶液的pH是影响吸附剂对金属离子吸附的重要因素之一,pH的大小不仅影响吸附点解离,而且影响重金属离子的溶液化学。pH>6.5时,溶液中的Pb2+会发生水解,形成Pb(OH)+、Pb(OH)2、Pb(OH)3-,此时吸附剂表面为负电荷,与Pb(OH)3-互相排斥,不利于吸附。如图6中实验结果所示,在pH从2.5增加到5.5的阶段,吸附剂对Pb2+的去除率几乎呈线性增加,pH为2.5时,去除率为25%,pH为5.5时,去除率增加到93%,当pH比较低时,溶液中主要以Pb2+和Pb(OH)+的形式共存,与存在的大量H+会形成竞争吸附的关系,pH升高,溶液中H+的数量减少,竞争关系减弱,有利于Pb2+的吸附,其去除率随之增大[15]。

图6 pH对吸附效果的影响Fig.6 Effect of pH on sorption efficiency
2.2.5 正交实验 Pb2+吸附的正交实验结果如表3所示,由极差R分析可知,各因素对其吸附效果的影响大小顺序为:pH>吸附剂质量>初始浓度>吸附时间,最优组合为A2B2C3D2,即吸附80 min,初始浓度240 mg/L,吸附剂质量2.5 g/L,溶液pH为5.5。此条件下,去除率达到95.2%。

表5 KGM@CTS吸附剂对Pb2+和胆固醇吸附动力学拟合参数
胆固醇吸附的正交实验结果如表4所示,各因素对其吸附效果的影响大小顺序为:初始浓度>吸附剂质量>吸附时间,最优组合为A2B2C3,即吸附120 min,初始浓度为3.0 g/L,吸附剂质量为1.5 g/L。此条件下,去除率达到48.7%。
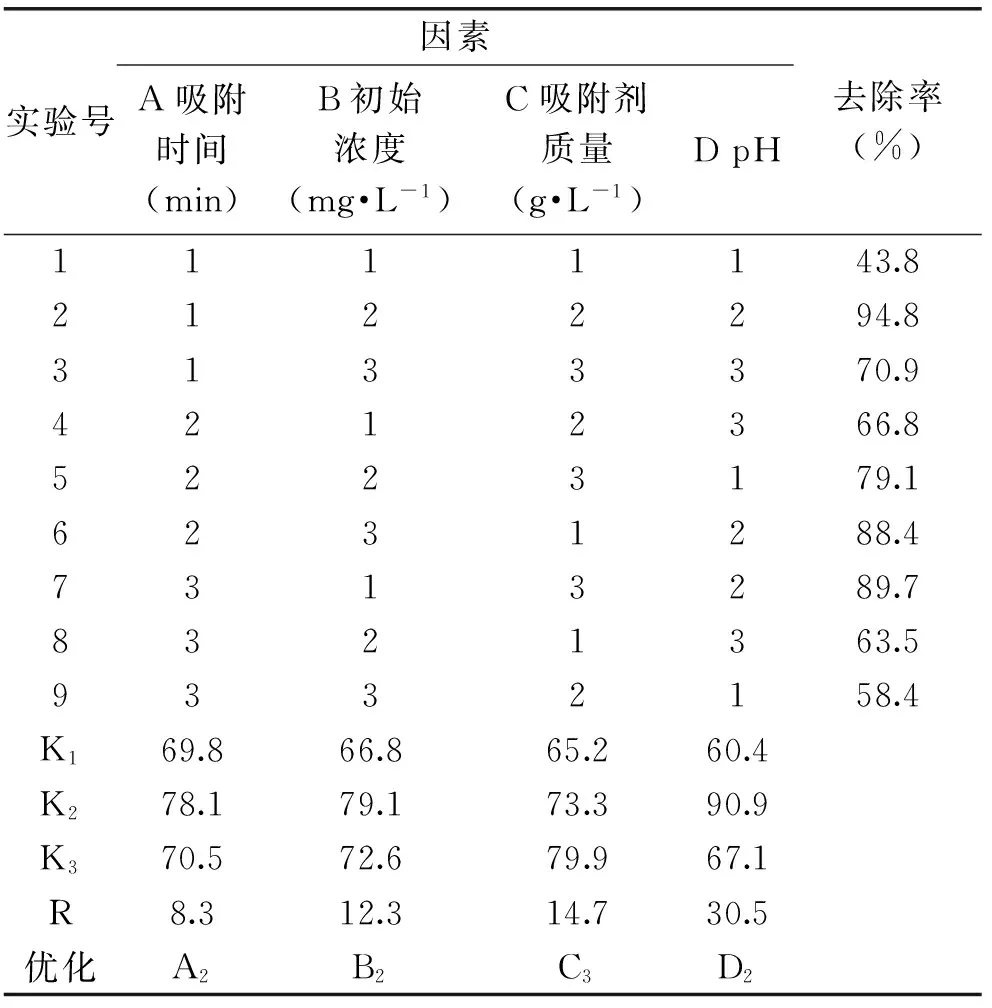
表3 Pb2+正交实验结果
2.2.6 吸附动力学研究 对实验所得数据分别采用准一级和准二级动力学模型[16]进行拟合,所得曲线如图7,参数列于表5。从图7可以看出,KGM@CTS对Pb2+和胆固醇吸附的准二级动力学模型拟合的很好(准一级模型图略)。在准一级动力学模型中,在吸附初始阶段拟合较好,但随着时间的延长,拟合度不高,产生这一现象主要是因为在准一级动力学中反应速率只与浓度因素有关,在吸附的初始,由于吸附剂表面有大量的活性位点,而活性位点随着时间的延长而减小,当减少到一定程度的时候,其吸附过程不只受到溶液浓度的控制,因此随着时间的延长会出现非线性的关系。在准二级动力学模型中吸附反应不仅受浓度一种因素的影响,还受活性位点的影响,从表5中可以看出,准二级动力学拟合曲线计算出的吸附量和实验值更加相近,也更加证实了此吸附更适合用准二级动力学模型来描述。

表4 胆固醇正交实验结果

图7 准二级动力学模型Fig.7 Pseudo-second-order simulation plot
2.2.7 吸附等温线方程 常用来描述液-固体系吸附过程的是Langmuir和Freundlich吸附方程式。Langmuir[17]模型成立的条件是吸附剂表面均匀,每个吸附位点只吸附一个分子且被吸附的分子之间没有相互作用力,即单分子层吸附;Freundlich模型则不限定单分子吸附,可以适用于表面不均匀的现象,是一个简单的经验公式,更适用于低浓度的溶液或气压较低的吸附状态,既能很好地描述不均匀表面的吸附机理,又能够在更广的浓度范围内很好地解释实验结果。将实验所得数据用 Langmuir和Freundlich等温模型[18]进行拟合,拟合曲线如图8,参数列于表6。从图8和表6可以看出,KGM@CTS对Pb2+和胆固醇的吸附过程和Freundlich吸附模型拟合的更好,由表6可以得出,KF和n值均大于1,则表示KGM@CTS吸附剂对Pb2+和胆固醇的吸附能力比较强。
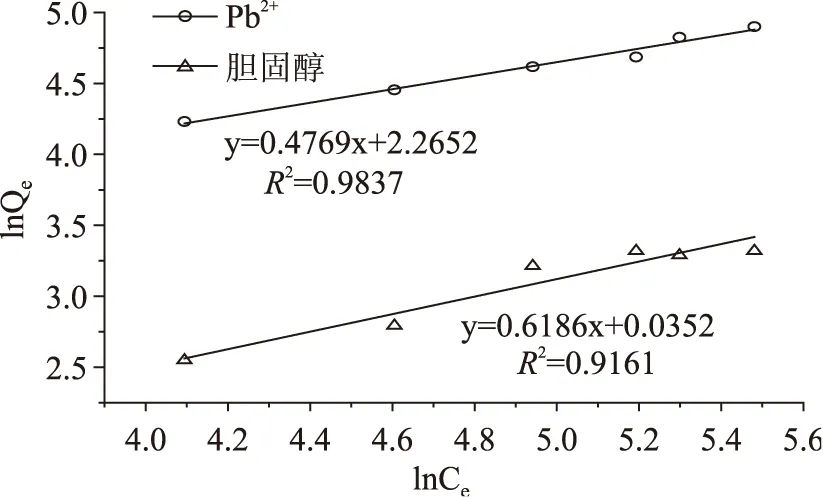
图8 Freundlich吸附曲线图Fig.8 The Freundlich adsorption表6 KGM@CTS吸附剂对Pb2+和胆固醇的吸附模型参数

样品LangmuirFreundlichQ0(mg·g-1)KLR2nKFR2Pb2+238.0950.00560.82262.09699.63300.9837胆固醇232.5580.00070.84811.61661.03580.9161
3 结论
KGM包埋前后的红外谱图显示KGM@CTS中可检测出壳聚糖特有的氨基存在,则其可同时具有魔芋和壳聚糖的功能基团,吸附能力优于交联魔芋葡甘聚糖颗粒。
KGM@CTS对Pb2+和胆固醇的静态吸附动力学研究表明:在37 ℃时,对Pb2+的吸附平衡时间为80 min,最佳pH为5.5,初始浓度为240 mg/L,吸附剂质量为2.5 g/L,最大去除率为95.2%;对胆固醇的吸附平衡时间为120 min,初始浓度为3.0 g/L,吸附剂质量为1.5 g/L,最大去除率为48.7%。吸附过程符合准二级动力学方程和Freundlich吸附等温模型,说明此吸附属于不均匀表面的吸附。因此,KGM@CTS在模拟实验中,表现出了排除重金属离子及控制血脂等膳食纤维特性,则为产品的价值和进一步的开发使用提供了一定的理论依据。
[1]冲增哲,黑田俊朗,岸田典子.魔芋科学[M].古明选,译.成都:四川大学出版社,1990:157-171.
[2]Abbott PJ. EFSA Panel on Dietetic Products,Nutrition and Allergies. Glucomannan related health claims[J]. EFSA Journal,2010,8(10):1798.
[3]Cairello M,Marchini G. Evaluation of the action of glucomannan on metabolic parameters and on the sensation of satiation in overweight and obese patients[J]. La Clinica Terapeutica,1995,146:269-274.
[4]Hou YH,Zhang LS,Zhou HM. Influences of refined konjac meal on the levels of tissue lipids and the absorption of four minerals in rats[J]. Biomed Environ Sci,1990,3(3):306-314.
[5]Judelson DA,Gomez AL,Kraemer WJ. Effects of a carbohydrate-restricted diet with and without supplemental soluble fiber on plasma low-density lipoprotein cholesterol and other clinical markers of cardiovascular risk[J]. Metabolism,2007,56:58-67.
[6]Staiano A,Simeone D. Effect of the dietary fiber glucomannan on chronic constipation in neurologically impaired children[J]. Journal of Pediatrics,2000,136:41-45.
[7]Vuksan V,Sievenpiper JL. Konjac-mannan and American ginsing:emerging alternative therapies for type 2 diabetes mellitus[J]. Journal of the American College of Nutrition,2001,20:370-380.
[8]罗立新,冯长根.交联魔芋葡甘聚糖微球的制备与表征[J].林产化学与工业,2004,24(2):77-79.
[9]罗天瑞,罗立新,肖湘,等.一种壳聚糖包囊魔芋的组合物及其制备工艺和用途:中国,ZL200910272658.7[P]. 2009-11-04.
[10]中国科学院环境化学研究所.GB/T7470-1987水质铅的测定:双硫腙分光光度法[S].北京:中国标准出版社,1987.
[11]中国预防医学科学院营养与食品卫生研究所. GB/T5009.128-2003食品中胆固醇的测定[S].北京:中国标准出版社,2003.
[12]王翼伟,王栋,徐岩,等.黄酒中氨基甲酸乙酯吸附去除的动力学和热力学研究[J].食品工业科技,2015,36(1):130-133.
[13]Thompson S,Weber C. Influence of pH on the binding of coper,zinc,and iron in six fiber sources[J]. Journal of Food Science,1979,44(3):752-754.
[14]陈亚非,赵谋明.水溶性与水不溶性膳食纤维对油脂、胆固醇和胆酸钠吸附作用研究[J].现代食品科技,2005,21(3):58-60.
[15]余亮.Fe3O4/4A沸石复合材料的制备及吸附铅离子性能的研究[D].长沙:中南大学,2012.
[16]刘莉.魔芋葡甘聚糖交联羧甲基改性及其对金属离子的吸附和解吸性能研究[D].武汉:华中农业大学,2008.
[17]王光信,孟阿兰,任志华.物理化学[M].第3版.北京:化学工业出版社,2007:237.
[18]王金玲,沈敏,瞿阳,等.交联羧甲基魔芋葡甘聚糖吸附Cu2+的机理[J].湖北农业科学,2009,48(1):161-163.
Adsorption property of Pb(Ⅱ)and cholesterol by chitosan coated konjac glucomannan
ZHU Wei-wei,LUO Li-xin*,WANG Yu
(College of Chemistry and Molecular Sciences,Wuhan University,Wuhan 430072,China)
A new konjac product with a chitosan coating was prepared by konjac glucomannan particles and a solution of chitosan in aqueous acetic acid at room temperature. This product can keep excellent characteristics of konjac such as helping digestion and reducing the concentration of cholesterol in the blood. The properties were characterized by FT-IR. Adsorption performance for Pb2+and cholesterol was evaluated in solutions systematically. Batch experiments were conducted as a function of initial concentration,adsorbent dosage and contact time. The kinetic data were analyzed by the pseudo-first-order,pseudo-second-order kinetics. Also the equilibrium data were examined with the Langmuir and Freundlich isotherm models. The results showed that the new product was characterized with functional groups of konjac glucomannan and chitosan. Adsorption at 37 ℃ resulted in the maximum removal rate of 95.2% and 48.7% for Pb2+and cholesterol,respectively. Kinetics fitted with the pseudo-second-order model. Besides,Freundlich model conformed to the equilibrium data. The results suggested the product can be an effective adsorbent for Pb2+and cholesterol,and the adsorption reaction occurred on an uneven surface.
konjac glucomannan;adsorption;lead ion;cholesterol;coating
2015-03-25
朱唯唯(1991-), 女,硕士,研究方向:天然产物提取和改性,E-mail:13545387147@163.com。
*通讯作者:罗立新(1966-),男,博士,副教授,研究方向:天然高分子改性与功能化,E-mail:lxluo@whu.edu.cn。
2013年湖北省中小企业技术创新计划项目(2013~2015,无编号)。
TS201.1
A
1002-0306(2015)23-0125-05
10.13386/j.issn1002-0306.2015.23.017

