清热解肌颗粒中挥发油的初步质量研究
刘 雪,崔 颖,黄顺旺,王 浩,陈师农,孙 备,吕 凌
(1.安徽中医药大学,安徽合肥 230012;
2.安徽省食品药品检验研究院,安徽省中药研究与开发重点实验室,安徽合肥 230051)
清热解肌颗粒为中药复方新药,其处方出自明代《伤寒六书》,由柴胡、羌活、白芷、生姜等药材组成,具有解肌清热之功效,主治感冒[1-2]。处方中的柴胡、羌活、白芷、生姜4味药材均含有挥发油,其中,《中国药典》规定羌活药材含挥发油不得少于1.4%(mL·g-1),文献报道[3-6],挥发油为上述 4味药材的主要有效成分,其药效与本制剂的解热、镇痛、抗炎、抗菌等药效基本相符,因此,本制剂工艺采用水蒸气蒸馏法提取挥发油,考虑到挥发油易逸散和氧化变质,采用倍他环糊精包合工艺,以提高挥发油在制剂中的稳定性[7-9]。鉴于中药复方制剂中挥发油含量测定和薄层鉴别研究的文献报道较少,同时,为了更好地控制本制剂的质量和保证临床疗效,本文在通过气—质联用色谱仪 (GCMS)对挥发油提取物成分进行归属鉴定的基础上,运用GC法采用单指标和总成分相结合的手段对制剂中的挥发油进行了含量测定,并进行薄层鉴别,从而达到有效控制其质量的目的。
1 仪器与试药
1.1 仪器 梅特勒电子天平(上海梅特勒-托利多有限公司),气相色谱质谱联用仪(美国布鲁克-道尔顿公司,MS.Workstation色谱工作站),气相色谱仪(Aglient7890A,FID检测器,Aglient中文工作站),硅胶G板(100 mm×100 mm,薄层层析用,青岛海洋化工厂分厂),挥发油测定器(天长市金桥分析仪器厂),GZX-9140MBE数显鼓风干燥箱(上海博讯实业有限公司医疗设备厂)。
1.2 试药 柴胡、羌活、白芷、生姜等药材购自安徽省金芙蓉中药饮片有限公司,并经安徽省食品药品检验研究院陈师农研究员鉴定;α-蒎烯对照品,批号110897-200502、β-蒎烯对照品,批号110827-201202、桉油精对照品,批号110788-201105(均由中国食品药品检定研究院提供);清热解肌颗粒自制(批号:20140706、20140707、20140708);水为去离子水,乙酸乙酯,石油醚(30~60℃)、甲苯、环己烷等试剂均为分析纯。
2 方法与结果
2.1 挥发油的薄层色谱鉴别[3]取清热解肌颗粒50 g,照挥发油测定法(中国药典2010年版一部附录X D)提取挥发油,取油层,加乙酸乙酯0.5 mL将挥发油溶解后,作为供试品溶液。按处方配比取柴胡、羌活、白芷和生姜对照药材,同法制成对照药材溶液。另取β-蒎烯对照品和桉油精对照品,分别加乙酸乙酯制成每1 mL含40 mg的溶液,作为对照品溶液。再按处方配比及制备工艺制成不含柴胡、羌活、白芷和生姜的阴性样品,同法制成阴性对照溶液。照薄层色谱法(中国药典2010年版一部附录ⅥB)试验,吸取上述5种溶液各2μL,分别点于同一硅胶G薄层板上,以石油醚30~60℃—乙酸乙酯(9∶1)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,热风加热至斑点显色清晰。供试品色谱中,在与药材挥发油、对照品色谱相应的位置上,显相同颜色的斑点,阴性无干扰,结果见图1。
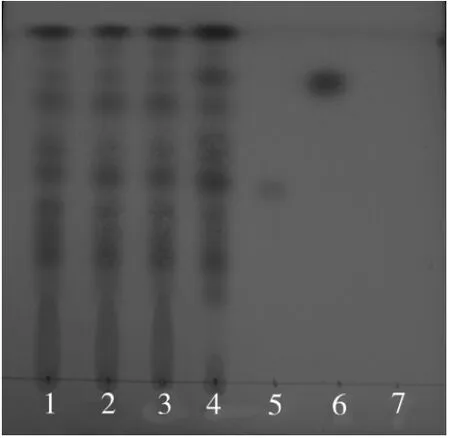
图1 制剂中挥发油的薄层色谱鉴别图
2.2 GC-MS 对挥发油提取物成分的鉴定[10]
2.2.1 色谱条件 色谱柱:DB-5 ms毛细管色谱柱 (30 m ×0.25 mm ×0.25μm,美国 HP公司);载气:氮气;流速:1.0 mL·min-1;柱温:40℃(1 min)至 50℃ (速率 5℃ ·min-1),50℃ (1 min)至74℃(速率4 ℃·min-1),74 ℃至220℃(速率5℃·min-1,至 220℃保持 1 min);进样口温度:250℃;质谱接口温度:280℃;离子源温度:280℃;电子轰击电压70 eV;全离子扫描,范围33~350 m·z-1;进样量:1.0μL;分流比:10∶1;运行时间:约 40 min。
2.2.2 供试品溶液的制备 取挥发油提取物约10 mg,置10 mL容量瓶中,加入乙酸乙酯适量使溶解,并稀释至刻度,摇匀,即得。
2.2.3 挥发油提取物鉴定 精密吸取供试品溶液1.0μL注入气相色谱仪中,记录色谱图。结果共测定出13个主要色谱峰,鉴定出12个化合物。结果见表1和图2。
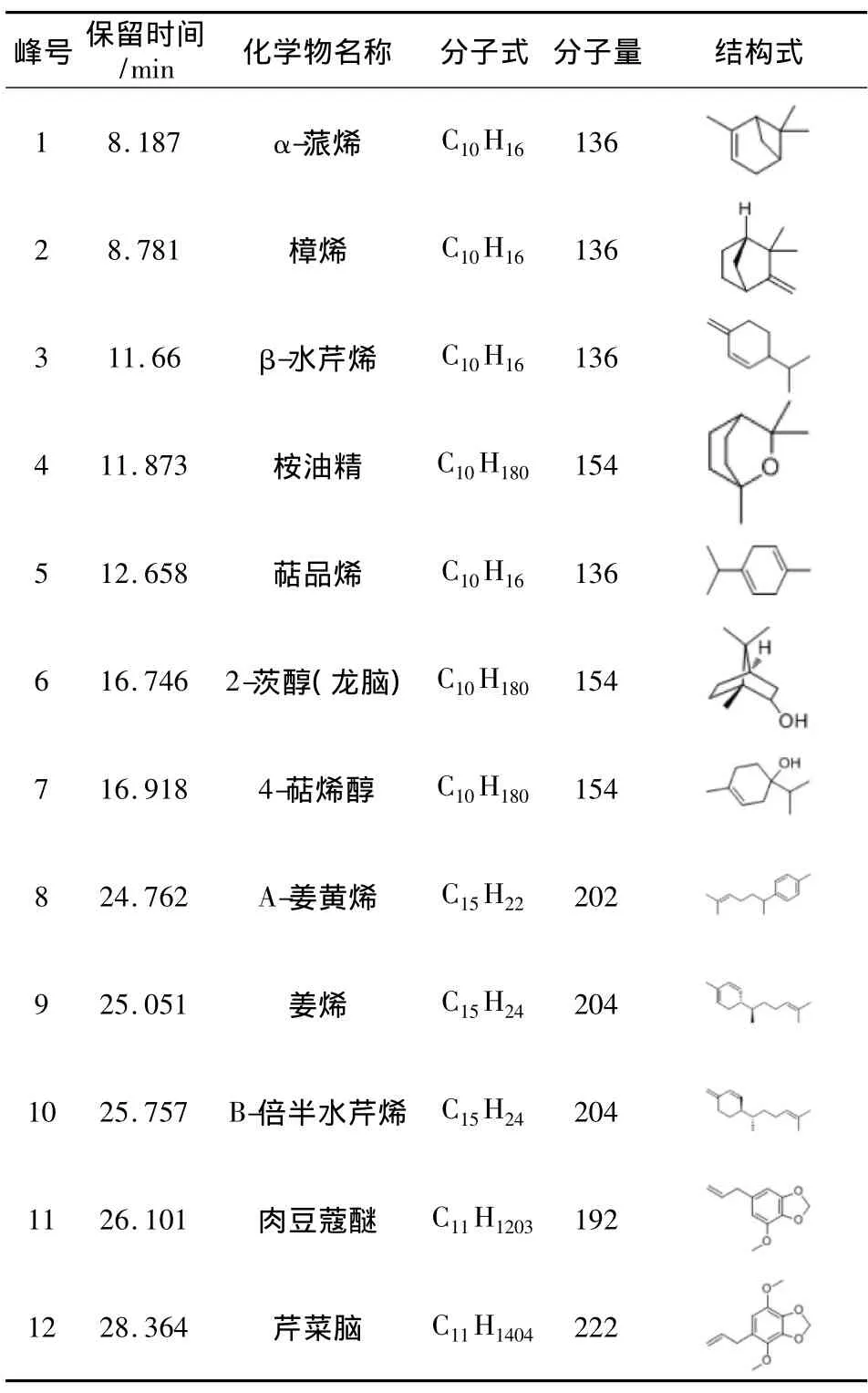
表1 挥发油化学成分分析
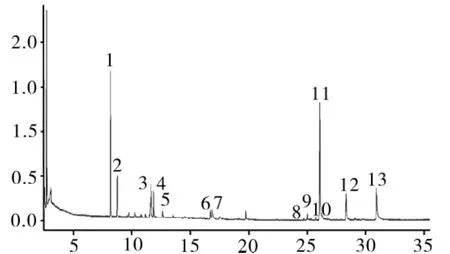
图2 挥发油的GC-MS色谱图
2.3 挥发油含量测定[11]
2.3.1 色谱条件 色谱柱:Agilent HP-5毛细管色谱柱 (30 m ×0.25 mm ×0.25μm);载气:氮气;流速1.0 mL·min-1;柱温:40 ℃(1 min)至 220 ℃(速率5℃·min-1,至220℃保持1 min);检测器:FID,温度250℃;进样口温度:240℃;进样量:1.0 μL;分流比:10 ∶1;运行时间:约38 min。
2.3.2 对照品溶液的制备 分别精密称取 α-蒎烯、β-蒎烯和桉油精对照品 60.5、49.8、46.5 mg,置10 mL容量瓶中,加乙酸乙酯使溶解并稀释至刻度,作为对照品贮备液。精密量取各对照品贮备液适量至同一量瓶中,得到混合对照品溶液,使其浓度分别为 15、2.5、5 mg·L-1的溶液。
2.3.3 供试品溶液的制备 取本品10 g,精密称定,置100 mL具塞锥形瓶中,加水10 mL振摇使颗粒分散溶化,再精密加入乙酸乙酯10 mL,密塞,称定重量,超声30 min后放置室温,再称定重量,用乙酸乙酯补足减失的重量,取上清液(乙酸乙酯层),即得。
2.3.4 阴性对照溶液的制备 按处方配比称取除柴胡、羌活、白芷、生姜药材以外的其他药材,按制备工艺和供试品溶液的制备方法制成阴性对照溶液。
2.3.5 专属性试验 取对照品溶液、供试品溶液和阴性对照溶液进样,结果阴性对照溶液在对照品相应位置上无色谱峰,说明其他成分对测定无干扰。结果见图3。
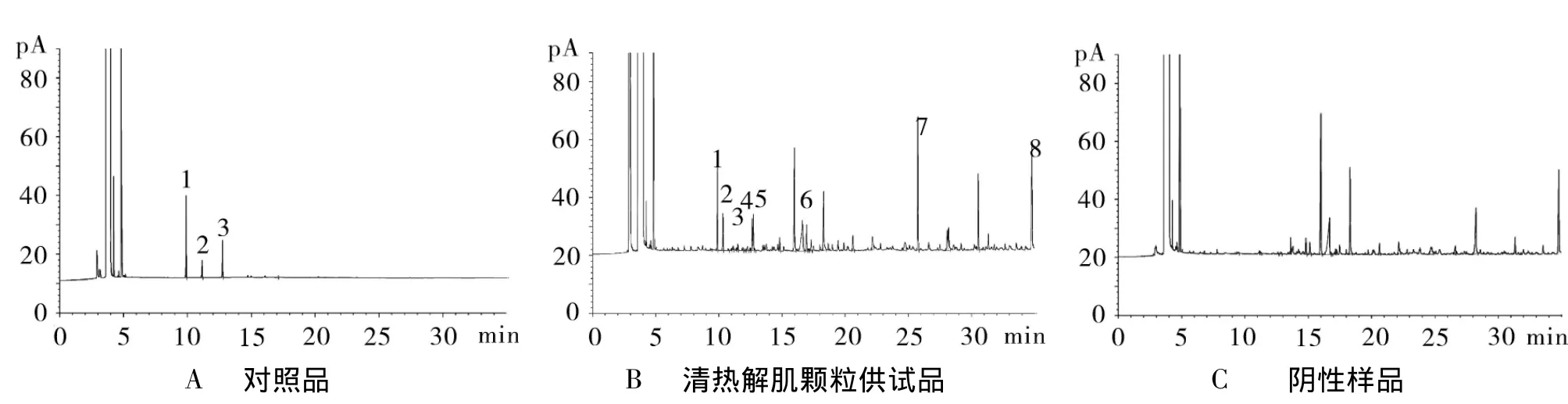
图3 清热解肌颗粒挥发油专属性GC色谱图
2.3.6 线性关系考察 将“2.3.2”项下对照品贮备液,用乙酸乙酯逐级稀释成系列浓度的混合对照品溶液,分别进样1.0μL,以峰面积A为纵坐标,以对照品浓度C(mg·L-1)为横坐标,绘制标准曲线,结果α-蒎烯、β-蒎烯和桉油精的回归方程分别为Y=2.626 2X+0.720 3(r=1.000)、Y=2.526 0X+0.082 0(r=1.000)、Y=2.169 5X+0.045 4(r=1.000),其线性范围分别为 1.89 ~605.00,1.25 ~99.60,2.32 ~185.81 mg·L-1。
2.3.7 稳定性试验 取供试品溶液分别于0、1.5、3、6、9、12、15、18 h(室温,未避光)进样,记录供试品中 α-蒎烯、β-蒎烯、桉油精的峰面积,结果 α-蒎烯、β-蒎烯和桉油精的 RSD 分别为 1.01%、4.60%、1.92%,表明供试品溶液至少在18 h内稳定。
2.3.8 精密度试验 按“2.3.3”项下供试品溶液处理方法平行处理6份样品,测定三种成分的峰面积,计算含量。结果 α-蒎烯、β-蒎烯和桉油精的RSD 分别为 1.32%、3.47%、1.41%(n=6),表明该方法的精密度良好。
2.3.9 重复性试验 取“2.3.2”项下配制的混合对照品溶液,按照“2.3.1”方法连续进样5次,进行测定。结果α-蒎烯、β-蒎烯和桉油精的RSD分别为0.87%、1.27%、0.50%(n=5),表明该方法的重复性良好。
2.3.10 加样回收率试验 取已知含量样品9份,每份10 g,精密称定,分别加入 α-蒎烯、β-蒎烯、桉油精对照品贮备液适量(按含量的80%,100%,120%加入),按“2.3.3”项下供试品溶液制备方法制备,进样1.0μL,计算各对照品的平均加样回收率和RSD值,结果见表2。
2.3.11 定量限试验 取“2.3.2”项下对照品溶液,逐级稀释。按照“2.3.1”方法测定,使当信噪比S/N≥10时即可。结果 α-蒎烯、β-蒎烯、桉油精的定量限分别为 1.89、1.25、2.32 ng。
2.3.12 样品含量测定 取3批同一工艺生产的产品,按“2.3.3”项下供试品溶液制备方法制备,按照“2.3.1”方法测定样品中 α-蒎烯,β-蒎烯,桉油精的含量,其余鉴定成分均以α-蒎烯作为对照计算含量。结果见表3。

表2 加样回收率试验结果(n=9)
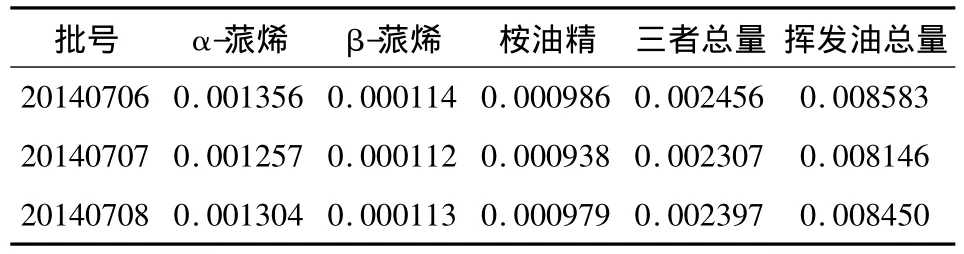
表3 三批样品含量测定结果/%
3 讨论
本处方中柴胡、羌活、白芷为多基原药材[3],本研究结合药材使用情况固定了药材基原及产地,北柴胡(Bupleurum chinense DC.),产地为陕西;羌活(Notopterygium incisum Ting ex H.T.Chang),产地为四川;白芷(Angelica dahurica(Fisch.ex Hoffm)Benth.Et Hook.f.),产地为安徽。基原及产地的固定,使得药材的挥发油含量和所含化学成分相对稳定,有利于产品质量的控制。
薄层鉴别试验中,采用三种展开剂[石油醚30~60℃—乙酸乙酯(9∶1);石油醚—甲苯—乙酸乙酯(7∶6∶1.5);环己烷—乙酸乙酯 (9.5∶0.5)][3,12-13],结果 α-蒎烯对照品均有干扰斑点,因此暂选用β-蒎烯,桉油精作为制剂中挥发油薄层色谱鉴别的对照品,α-蒎烯的薄层鉴别有待于进一步研究。
GC-MS对挥发油提取物的鉴定中,由于β-蒎烯含量较少,在化学成分分析表中未给出分析,但在挥发油含量测定试验中,通过对照品确定其保留时间;由于只获得α-蒎烯、β-蒎烯和桉油精三种对照品,其他成分均未获得标准物质,最终采用外标法计算样品中上述三种成分的含量,测得结果这三种成分含量较低,因此以α-蒎烯作为对照计算挥发油总量(即 α-蒎烯,β-蒎烯,桉油精,樟烯,β-水芹烯,萜品烯,肉豆蔻醚,芹菜脑8种成分含量之和)。
样品处理时通过考察单一因素变化对提取效果的影响,筛选出最佳提取方法。分别考察不加水、加水5 mL、加水10 mL以及样品研磨处理四种方法,结果表明不加水处理造成颗粒不易溶解,但加水不足易产生乳化导致乙酸乙酯层不易分离,而颗粒经研磨处理会造成挥发油含量降低,因此,选择了本实验中样品的处理方法。
[1] 王 姝.柴葛解肌汤药理作用的研究进展[J].卫生职业教育,2014,32(24):151 -152.
[2] 徐以亮.柴葛解肌汤配方颗粒质量标准研究[J].中国药业,2012,21(18):49 -51.
[3] 国家药典委员会.中国药典(一部)[S].北京:中国医药科技出版社,2010:170,236,97,97,382,389,34Ⅵ B,63 附录 X D.
[4] 霍梦逸,刘 新,林 於,等.柴胡挥发油中有效解热成分的研究[J].药物分析杂志,2013,33(7):1202 -1209.
[5] 高小坤.白芷挥发油镇痛、镇静作用实验研究[J].现代中西医结合杂志,2013,22(35):3880 -3882.
[6] 李 翔,王 敏.干姜挥发油的均匀设计提取和化学成分鉴定[J].华北国防医药,2010,22(3):216 -218.
[7] 李 希,谢守德,张 嵩,等.羌活挥发油-β-环糊精制备工艺的研究[J].中国中药杂志,2002,27(2):108 -110.
[8] 李树珍,官仕杰.八种中药挥发油环β-环糊精包接物的稳定性考察[J].中国中药杂志,1990,15(4):26 -28.
[9] 赵永亮,管景帅,温金娥,等.β-环糊精研究及应用进展[J].河南工业大学学报(自然科学版),2014,35(6):97-101.
[10]马雯芳,谭建宁,徐东来,等.GC-MS测定姜油中-蒎烯、桉油精和龙脑的含量[J].安徽农业科学,2012,40(21):11030-11031.
[11]赵祥升,黄立标,杨新全,等.肉豆蔻挥发油中α-蒎烯,β-蒎烯含量测定及动态分析[J].海峡药学,2012,24(8):57 -59.
[12]汪国华,张文惠.艾叶中桉油精的薄层色谱鉴别[J].江西中医学院学报,2000,12(1):29.
[13]张林林,薛 健,刘东静,等.油松节药材质量研究[J].医药导报,2010,29(2):240 -242.

