超声辅助肋间神经阻滞在胸科手术中的应用
白文庆 胡 杰麻醉科
(郑州大学附属洛阳中心医院超声科,洛阳 471000)
临床研究·
超声辅助肋间神经阻滞在胸科手术中的应用
白文庆 胡 杰**①麻醉科
(郑州大学附属洛阳中心医院超声科,洛阳 471000)
目的 探讨超声辅助肋间神经阻滞在胸科手术中应用的价值。 方法 选择单纯左胸第6~7肋骨切口的食管下段癌根治术70例,ASAⅠ~Ⅱ级,随机分为U组和C组,每组35例。U组全麻诱导前根据手术区域先行患侧超声引导下肋间神经阻滞,C组直接全麻插管。术中根据血压、心率调节全麻药的用量,手术结束时记录丙泊酚和舒芬太尼用量及全麻后患者的苏醒时间。术后镇痛U组采用超声引导下肋间神经阻滞,C组应用静脉泵术后镇痛,观察术后2(T1)、4(T2)、12(T3)、24 h(T4)的镇痛效果及术后恶心、呕吐的发生情况。 结果 U组术中丙泊酚、舒芬太尼用量明显少于C组[(656.5±32.3)mg vs.(845.8±47.0)mg,t=-19.638,P=0.000;(48.3±11.3)μg vs.(69.7±13.5)μg,t=-7.191,P=0.000]。U组清醒时间(18.5±3.8)min,明显短于C组(28.7±4.3)min(t=-10.516,P=0.000)。U组在T1、T2、T3时点VAS明显低于C组[T1:(2.3±0.8)分vs. (3.0±1.2)分,t=-2.871,P=0.005;T2:(1.8±0.7)分vs. (2.8±1.2)分,t=-4.258,P=0.000;T3:(1.5±0.5)分 vs. (2.6±0.9)分,t=-6.321,P=0.000],T4无统计学差异[(1.1±0.3)分 vs.(1.1±0.4)分,t=0.000,P=1.000]。术后恶心发生率C组高于U组[28.6%(10/35)vs. 5.7%(2/35),χ2=6.437,P=0.011]。C组呕吐1例,U组无发生,无统计学差异(Fisher’s检验,P=1.000)。 结论 超声辅助肋间神经阻滞应用在胸科手术能够减少术中麻醉用药,术后镇痛效果良好,减少术后恶心的发生率。
超声; 肋间神经; 阻滞
随着超声技术的发展,如高分辨率便携式超声仪器的问世和超声探头的改进,超声技术应用在临床各个领域如检查,诊断及定位等[1]。胸科手术由于对呼吸影响大,创伤大,单纯静脉麻醉用量大,患者术后苏醒、恢复缓慢。以往常采用全麻联合硬膜外麻醉来减少全麻药用量,并在术后镇痛中应用,但由于高位硬膜外穿刺难度大,并发症多,已在临床较少使用。超声辅助定位使以前麻醉效果不能确定的肋间神经阻滞得到广泛应用,本研究通过术中、术后超声辅助肋间神经阻滞与常规全麻及术后静脉镇痛相比,旨在探讨超声辅助肋间神经阻滞能否减轻术中麻醉用药及术后并发症。
1 临床资料与方法
1.1 一般资料
本研究通过我院伦理委员会批准(批文号:20140203),所有患者均自愿参加本研究,并签署知情同意书。病例选择标准:①无肝、肾等重要器官功能不全,无感染性疾病或过敏病史;②左室射血分数(EF)≥40%,且无左房心栓,近4周内未发生心肌梗死,心电图未见传导阻滞;③美国纽约心脏协会(New York Heart Association,NYHA)心功能Ⅱ~Ⅳ级;④均无心脏手术史,无电解质或酸碱平衡紊乱。病例排除标准:合并明显呼吸功能不全、肝肾衰竭;Ⅱ级以上房室传导阻滞、冠状动脉严重狭窄以及心动过缓;有精神病史、麻醉药物过敏史;术前未经控制的严重高血压史(未规律服药或者血压控制不佳)。选择我院2014年1月~2015年1月食管癌根治术70例,年龄40~68岁,体重45~78 kg,美国麻醉医师协会(American Society of Anesthesiology,ASA)麻醉分级Ⅱ~Ⅲ级。按入院时间顺序编号,然后按随机数字表分为U组和C组,每组35例:U组全麻诱导前根据手术区域先行患侧超声引导下的肋间神经阻滞,C组直接全麻插管;术后镇痛U组采用超声引导下肋间神经阻滞,C组应用静脉镇痛泵。2组患者均为食管下段癌,一般资料无显著性差异(P>0.05),有可比性,见表1。
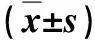
表1 2组一般资料比较
1.2 麻醉方法
①术前用药:所有患者入室前肌肉注射苯巴比妥那0.1,东莨菪碱0.3 mg。②麻醉诱导和维持:入室建立静脉通路,连接心电图(ECG),脉搏血氧饱和度(SpO2),无创血压(BP),脑电双频指数(BIS)监测,在局部麻醉下完成右颈内静脉穿刺置管监测中心静脉压(central venous pressure, CVP)。U组采用全麻联合超声辅助肋间神经阻滞镇痛,C组采用全凭静脉麻醉(total intravenous anesthesia,TIVA)联合术后静脉泵镇痛。U组应用便携式超声仪和高频直线探头,在腋后线第5~7肋间隙的位置,应用超声引导短轴平面技术,将探头与肋骨垂直放置,即可显示肋间神经的横截面超声图。肋骨呈城垛样表现,表面高回声,深部低回声,肋骨之间由高回声胸膜相连。肋骨下缘和胸膜的成角处即为肋间神经的位置。探头下外侧旁开0.5 cm处进针,看到针尖到达肋骨下缘和胸膜成角处,即胸膜外、肋骨下的阴影区域时,回抽注射器无回血,每束肋间神经可注入0.25%罗哌卡因4 ml,可见局麻药液的明显扩散以及相应位置的胸膜下陷[2]。C组采用异丙酚(target controlled infusion, TCI)联合舒芬太尼TIVA。术中丙泊酚靶浓度不超过0.2 μg/ml,舒芬太尼0.5~0.8 ng/ml,间断注射维库溴铵,维持BIS 40~60。术中常规监测ECG、血压、SpO2、血气、鼻咽温、中心静脉压及BIS值。静脉镇痛泵使用舒芬太尼加氟哌啶。2组患者均由同一组手术、麻醉人员完成。
1.3 观察指标
记录手术结束时丙泊酚和舒芬太尼的用量及全麻后患者的苏醒时间。观察患者术后2(T1)、4(T2)、12(T3)、24 h(T4)疼痛模拟评分(visual analogue scale,VAS)及术后恶心、呕吐的发生情况。
1.4 统计学处理
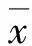
2 结果
U组患者丙泊酚、舒芬太尼的用量显著少于C组(P<0.05),且患者拔管时间、术后清醒时间短,见表2。U组T1,T2,T3时点术后VAS明显小于C组(P<0.05),T4无统计学差异(P>0.05),见表3。C组术后恶心发生率显著高于U组(P<0.05)。C组呕吐1例,U组无发生,无统计学差异(Fisher’s检验,P=1.000)。
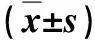
表2 2组患者术中情况比较
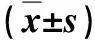
表3 2组患者术后VAS比较 分
3 讨论
近年来,随着麻醉领域可视化的普及,超声技术在麻醉领域得到长足发展。超声可以作为麻醉的辅助技术,从食道超声的术中监测到区域神经阻滞的超声引导,超声与麻醉越来越密不可分,尤其在神经阻滞方面,比传统的解剖定位、神经刺激仪更加可靠、安全、完美[2,3]。传统的盲探肋间神经阻滞能够为胸部手术提供良好的镇痛[4,5],但由于是盲探操作,容易阻滞不全,误穿胸膜、肋间动脉,很少在临床外科麻醉中使用。随着超声在麻醉中的广泛应用,超声能够准确定位肋间神经,清晰分辨神经周围的胸膜、血管等组织,不仅使神经阻滞效果确切,还降低并发症的发生率。
传统的血流动力学指标作为麻醉深度调节的依据,会出现以意识的深度抑制为代价而达到自主神经反射的过度抑制,容易导致麻醉药物过量,显然背离平衡麻醉的要求,同时还可能导致患者术后苏醒延迟的可能[6]。食管癌患者多为老年人,身体综合机能差,单纯全身麻醉可能导致苏醒延迟或不全,从而产生诸多的术后并发症。静脉麻醉复合神经阻滞在减少静脉麻醉药用量的同时减少因麻醉药而产生的副作用。本研究结果显示U组术中丙泊酚量明显少于C组(P<0.05),舒芬太尼用量也明显少于C组(P<0.05),说明肋间神经阻滞起到了镇痛效果,减少手术疼痛刺激,同时减少舒芬太尼的用量需求,可能与超声引导下肋间神经阻滞更加精准,通过阻滞感觉神经和交感神经,阻断躯体痛和内脏血管性疼痛的神经传导通路有关。U组患者术后清醒时间和拔管时间均明显短于C组,也说明U组减少舒芬太尼的用量,加快了患者的苏醒,减少术后苏醒延迟等并发症。U组术后2、4、12 h VAS明显小于C组(P<0.05),24 h无统计学差异(P>0.05),说明肋间神经阻滞的镇痛效果能够持续8~24 h,与马明志等[7,8]的研究结果相符。术后12 h内VAS U组明显低于C组可能是因为C组静脉镇痛的药物(阿片类)还未到达最佳的镇痛剂量,阿片类药物需要通过一定的血药浓度缓慢渗透过血脑屏障才能起到镇痛作用,即静脉镇痛需要一定的时间和剂量才能达到临床镇痛的效果。当静脉镇痛药达到一定血药浓度后,患者又可能出现恶心、呕吐,与阿片药物的作用有关,是不易避免的。因此,应用超声辅助肋间神经阻滞,在胸科手术中不仅能减少术中麻醉药物用量,而且还能术后镇痛,减少恶心呕吐等并发症,值得临床推广应用。
1 林育南,刘敬臣.超声技术在麻醉领域的应用.临床超声医学杂志,2014,11(16):760-762.
2 陈永权,孟 伟,金孝岠.超声引导下肋间神经阻滞联合全麻对乳腺癌手术的麻醉效果及术后镇痛的影响.中华临床医师杂志,2014,6(8):2027-2030.
3 Chan VW, Perlas A, McCartney CJ, et al. Ultrasound guidance improves success rate of axillary brachial plexus block. Can J Anesth,2007,54(3):176-182.
4 Vermeylen K, Engelen S, Sermeus L, et al. Supraclavicular brachial plexus blocks: review and current practice. Acta Anaesthesiol Belg,2012,63(1):15-21.
5 Bruce BG, Green A, Blaine TA, et al. Brachial plexus blocks for upper extremity orthopaedic surgery. J Am Acad Orthop Surg,2012,20(1):38-47.
6 李志刚,于金辉,李明颖,等. 麻醉深度指数在腹腔镜胆囊切除术中麻醉监测中的作用.中国微创外科杂志,2015,15(4):298-304.
7 马明志. 肋间神经阻滞联合静脉自控镇痛对胸腔镜术后患者镇痛效果观察. 临床麻醉学杂志,2009,47(30):89-90.
8 Marhofer P, Chan VW. Ultrasound-guided regional anesthesia: current concepts and future trends. Anesth Analg,2007,104(5):1265-1269.
(修回日期:2015-06-19)
(责任编辑:李贺琼)
Application of Ultrasound Assisted Intercostal Nerve Block in Patients Undergoing Thoracic Operation
BaiWenqing*,HuJie.
*DepartmentofUltrasound,LuoyangCentralHospitalAffiliatedtoZhengzhouUniversity,Luoyang471000,China
Correspondingauthor:HuJie,E-mail: 13721624858@163.com
Objective To investigate the application value of ultrasound assisted intercostal nerve block in thoracic operations. Methods A total of 70 cases of esophageal carcinoma treated by radical resection via a left thoracic 6-7 rib incision in our hospital were selected. The patients were classified as ASA Ⅰ-Ⅱ. They were randomly divided into U group and C group, with 35 cases in each group. The U Group was given intercostal nerve block under ultrasound guidance according to the operation area before the induction of anesthesia. The C group was given direct anesthesia intubation. According to intraoperative blood pressure and heart rate, the amount of anesthetics was adjusted. At the end of the operation, the amount of propofol and sufentanil anesthesia, and patients’ recovery time were recorded. Postoperative analgesia included ultrasound-guided intercostal nerve block in the U Group and intravenous postoperative analgesia pump in the C Group. The analgesic effects at 2 h (T1), 4 h (T2), 12 h (T3), and 24 h (T4), as well as complications of postoperative nausea and vomiting, were observed. Results The dosage of propofol and sufentanil in the U Group was less than that in the C Group [(656.5±32.3) mg vs. (845.8±47.0) mg,t=-19.638,P=0.000; (48.3±11.3) μg vs. (69.7±13.5) μg,t=-7.191,P=0.000]. The awake time was significantly shorter in the U Group (18.5±3.8) min than that in the C Group [(28.7±4.3) min,t=-10.516,P=0.000]. In the U Group, the VAS scores at T1, T2, and T3were significantly lower than those of the C Group [T1: (2.3±0.8) points vs. (3.0±1.2) points,t=-2.871,P=0.005; T2: (1.8±0.7) points vs. (2.8±1.2) points,t=-4.258,P=0.000; T3: (1.5±0.5) points vs. (2.6±0.9) points,t=-6.321,P=0.000]. However, the VAS scores at T4were not statistically different between the two groups [(1.1±0.3) points vs. (1.1±0.4) points,t=0.000,P=1.000]. The incidence of postoperative nausea was higher in the C Group than that in the U Group [28.6% (10/35) vs. 5.7% (2/35),χ2=6.437,P=0.011].Vomiting happened in 1 case in the C Group, while none in the U Group, without statistical difference (Fisher’s test,P=1.000). Conclusion Ultrasound assisted intercostal nerve block in thoracic surgery can reduce intraoperative anesthetic use, obtain good postoperative analgesic effects, and reduce the incidence of postoperative nausea.
Ultrasound; Intercostal nerve; Block
河南省洛阳市科技局基金项目(项目编号:1401085A-4)
,E-mail:13721624858@163.com
R614.2
A
1009-6604(2015)09-0812-03
10.3969/j.issn.1009-6604.2015.09.012
2015-04-20)

