克伦特罗在猪体内立体选择性降解行为研究
于遵波,张艳,吴银良*
(1.中国兽医药品监察所,北京 100081;2.宁波市农业科学研究院,浙江宁波 315040)
克伦特罗在猪体内立体选择性降解行为研究
于遵波1,张艳2,吴银良2*
(1.中国兽医药品监察所,北京 100081;2.宁波市农业科学研究院,浙江宁波 315040)
为了解克伦特罗在猪体内是否存在立体选择性降解行为,手性分离制备了克伦特罗单一对映体,然后对生猪进行饲喂含有克伦特罗外消旋体(2.0 mg/kg)和单一对映体(1.0 mg/kg)的饲料,7 d后进行屠宰,定期采集猪的肌肉、肝脏、肾脏、心脏、肺脏和尿液,测定克伦特罗对映体含量。结果表明,克伦特罗在猪体内存在立体选择性降解行为,肝脏、肾脏和肺脏中对映体(右旋体/左旋体)比例较高,心脏和肌肉中的对映体比例相对较低;休药3 d时,肝脏、肾脏、猪尿中的对映体比例均处于最高点。同时克伦特罗对映体在猪体内不存在相互转化现象。该研究为科学评估动物性食品残存的克伦特罗对人体健康造成的危害提供了科学依据。
克伦特罗;手性对映体;立体选择性降解;液相色谱串联质谱法
克伦特罗(Clenbuterol)俗称“瘦肉精”,属于选择性β2-肾上腺素受体激动剂,生产中常用其外消旋体非法应用于畜牧业,用来提高酮体瘦肉率。然而,由于克伦特罗易在动物组织中形成残留,曾多次发生严重的人畜中毒事故[1-2]。因此,克伦特罗在我国已禁止使用,但因其促生长效果好,违法使用的情况还时有发生。然而目前在评估克伦特罗对人体健康造成的危害时,对其是手性药物这一特征未加以充分考虑,仅对该药物作为纯的单一化合物来看待[3-5]。而手性药物不同异构体之间在毒性、致畸、致癌、致突变上往往存在差异,必然导致对其危害估计不是过高就是过低[6-8]。因此为更加科学评估该药物对人体健康造成的危害,应对其进行立体选择性降解行为进行研究。
随着动物性食品安全得到全社会的重视,国际上对于兽用的手性药物在动物体内的立体选择性降解行为研究有所升温,如Smith DJ分别对克伦特罗在鸡和猪中的立体选择性降解行为进行了研究,但猪体内猪肉样品仅提供了0天的数据[9],同时也未进行单一对映体饲喂试验;Cristofol C等研究了牛静脉注射阿苯哒唑后代谢产物阿苯哒唑亚砜在体液和组织中对映异构体比例随时间变化情况[10];但这些研究对单一对映体在畜禽体内是否存在转化现象缺乏进一步的研究。而在国内,对于手性药物在动物体内的立体选择性降解行为和机理研究较少,仅有周志强课题组对手性农药在兔子和大鼠中的立体选择性降解行为和机理进行了研究和探索,而对兽用手性药物在使用对象(畜禽)体内的立体选择性代谢规律的研究尚为空白。为进一步探明克伦特罗在猪肉中的立体选择性降解行为和了解单一对映体在畜禽体内是否存在转化现象,本研究在建立猪组织克伦特罗对映体残留量分析方法的基础上进行了克伦特罗在猪体内立体选择性降解试验。通过研究,首次明确克伦特罗单一对映体在猪体内不存在对映体转化现象。
1 材料和方法
1.1 仪器、试剂和材料 Waters 2695 Quattro MicroTM API高效液相色谱串联质谱仪(美国Waters公司);固相萃取仪(美国SUPELCO公司);Sigma离心机(北京博励行仪器有限公司);匀质器(德国IKA公司),-Milli-Q超纯水仪(美国Millipore公司)。盐酸克伦特罗(99%)购于中国药品生物制品检定所;盐酸克伦特罗-D9(100 μg/L)购于德国Dr.Ehrenstorfer公司;甲醇(色谱纯)购于美国默克公司;甲酸(色谱纯)购于美国天地有限公司;SCX (500 mg/3 mL)购于Supelco公司;其他试剂均为分析纯试剂。空白猪肉样品购于宁波市江东区欧尚超市,实验用肉猪为健康肉猪,体重70 kg左右,用药前测定是否含克伦特罗。
1.2 标准溶液的配制
1.2.1 外消旋体标准储备液(500 μg/mL) 准确称取含100.0 mg克伦特罗的盐酸克伦特罗标准品于100 mL容量瓶中,用甲醇定容至刻度,得克伦特罗标准储备液,单一克伦特罗对映体浓度为500 μg/mL。
1.2.2 标准工作液 将外消旋体标准储备液用流动相逐级稀释成2、10、20、50、100、200 μg/L的标准溶液(每个标准溶液含内标浓度为25 μg/L),现配现用。
1.3 方法
1.3.1 单一对映异构体的制备 对映异构体制备色谱分离条件:流动相:V(甲醇):V(乙酸):V(三乙胺)=99.98:0.01:0.01,进样量50 μL,柱温30 ℃。在此条件下,先出峰的为(-)-对映体,后出峰的为(+)-对映体,收集单一对映异构体。合并流出液,旋转浓缩至干,加入甲醇溶解并定容至50 mL,根据上述色谱条件,在240 nm处测定两对映异构体浓度。
1.3.2 动物试验方法
1.3.2.1 饲料配制 将上述外消旋体储备液和1.3.1项中两对映异构体溶液分别和500 g经粉碎的猪配合饲料混合,振荡混合2 h后,在60 ℃烘箱中烘干。再在动物试验前,与养殖场提供的猪饲料混合,饲料中外消旋体的浓度为2.0 mg/kg,单一对映异构体的浓度为1.0 mg/kg。
1.3.2.2 喂药和取样时间 外消旋体实验和单一对映体实验的动物数均为6头,用含有药物的饲料连续饲喂7 d后进行屠宰,分别于0,3,7,14,21和28 d采集每头猪的肌肉、肝脏、肾脏、心脏、肺脏和尿液。
1.3.3 测定方法 降解试验样品中克伦特罗对映体浓度的测定方法参考文献[11],所有组织样品测定方法均一致,猪尿样品取样量为5.0 mL。整个方法中仅对流动相的流速作了调整,由1.0 mL/min改为0.5 mL/min。
2 结果与分析
2.1 单一对映异构体的制备 经测定,制备的单一对映异构体甲醇溶液中(-)-对映体和(+)-对映体的浓度分别为1499 μg/mL和1529 μg/mL,经计算质量分别为74.95 mg和76.45 mg。
2.2 外消旋体实验结果 外消旋体的样品测定实验结果和对映异构体比例均详见表1,从表1中可见,0 d时(-)-对映体和(+)-对映体的浓度均是猪尿中最高,然后(-)-对映体依次是肺脏、肝脏、肾脏、心脏和肌肉,(+)-对映体依次是肝脏、肺脏、肾脏、心脏和肌肉。28 d降解后,除肺脏中的(+)-对映体浓度高于1.0 μg/kg外,其余组织和尿液中的(-)-对映体和(+)-对映体浓度均低于1.0 μg/kg。同时从表中可见,肝脏、肾脏和肺脏中对映异构体比例较高,心脏和肌肉中的对映异构体比例相对较低;休药3 d时,肝脏、肾脏、猪尿中的对映异构体比例均处于最高点。外消旋体实际样品测定图谱详见图1,从图中可见(-)-对映体和(+)-对映体峰形和分离均较好。

表1 克伦特罗外消旋体样品测定结果和对映体比例

图1 盐酸克伦特罗外消旋体0 d肺脏和0 d肝脏MRM色谱图(1.(-)-克伦特罗-D9对映体;2.(+)-克伦特罗-D9对映体;3.(-)-克伦特罗对映体;4.(+)-克伦特罗对映体)
2.3 单一对映体实验结果 单一对映体的样品测定实验结果详见表2,从表2中可见,(-)-对映体和(+)-对映体单一实验时,均不存在在猪体内转化现象;同时从表2可知,(-)-对映体实验时0 d测定结果肺脏中含量最高,其次是猪尿、肝脏、肾脏、心脏和肌肉,(+)-对映体实验时0 d测定结果肝脏中含量最高,其次是肺脏、猪尿、肾脏、心脏和肌肉。28 d降解后,(-)-对映体实验时,除肝脏样品中的浓度为1.06 μg/kg外,其余样品均低于1.0 μg/kg;(+)-对映体实验时,除肾脏和肺脏样品中的浓度分别为1.03 μg/kg和1.34 μg/kg外,其余样品均低于1.0 μg/kg。
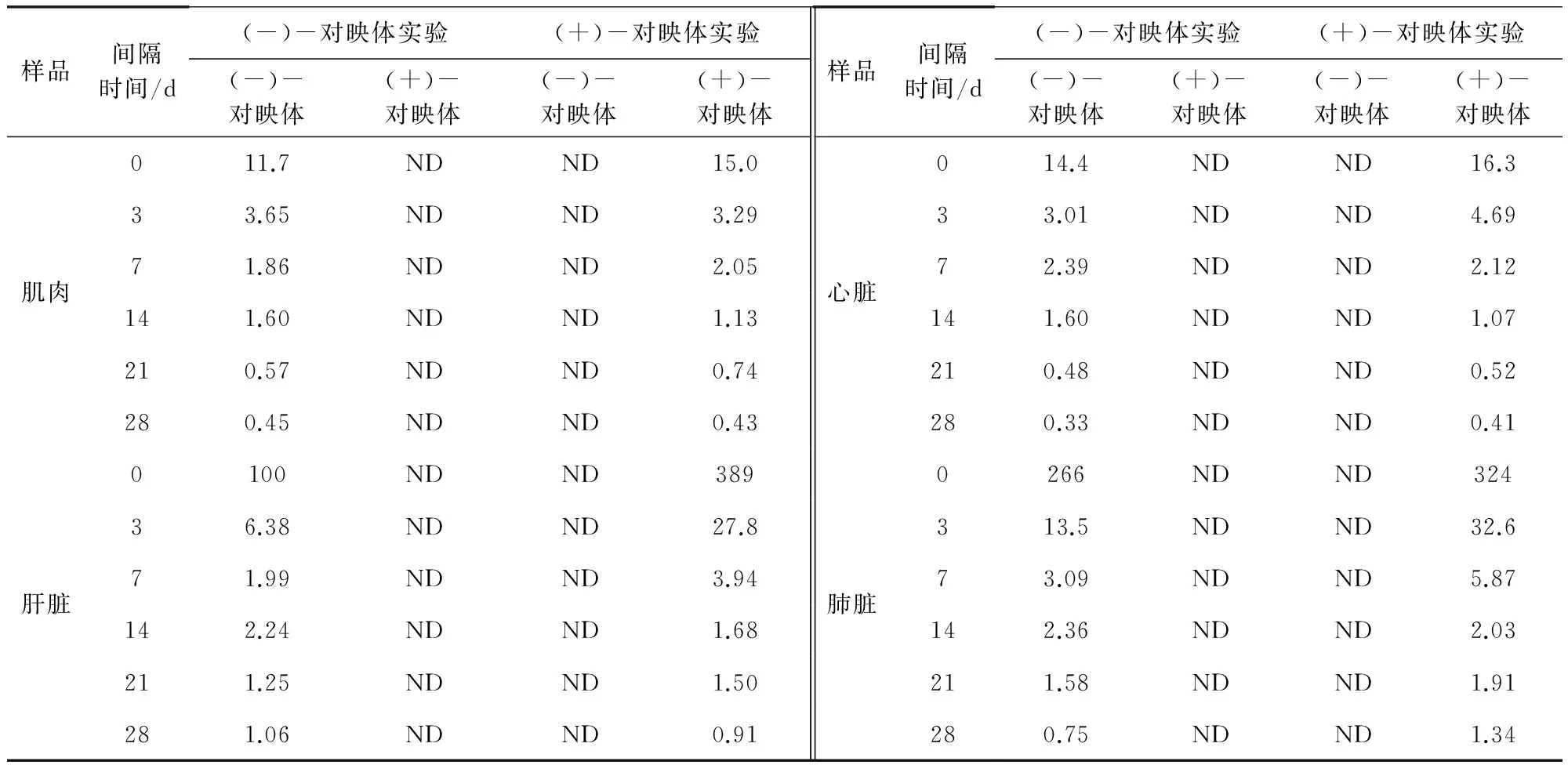
表2 克伦特罗单一对映体实验样品测定结果

续表
3 讨论和小结
3.1 单一对映体的制备 目前市场上尚无法购买到单一克伦特罗对映体原料药或标准品,为达到进行单一对映体实验的需要,必须通过手性分离制备出克伦特罗单一对映体。考虑到本实验对单一对映体需要量不是特别大,本实验采用对标准储备液进行进样,手性色谱柱(Astec CHIROBIOTICTMV)分离,分别收集两个组分来制备单一对映体。
3.2 外消旋体实验 对于β2-肾上腺素受体激动剂来说,引起副作用或急性毒性的主要成分是其左旋异构体,而通过外消旋体实验可知,克伦特罗左旋异构体代谢较快,特别是在肝脏、肾脏和肺脏组织中所占比例较小,因此在科学评估肝脏、肾脏和肺脏组织中残存的该药物对人体健康造成的危害时,有必要对其进行对映异构体分析。从本实验的肌肉中克伦特罗对映体实验数据看,评估肌肉中残存的该药物对人体健康造成的危害时,对映异构体分析的必要性较小。从实验数据看,外消旋体实验的结果与Smith DJ等的实验结果一致[9];同时本实验首次证明了肌肉样品随着消除时间的延长,肌肉中对映体比例波动较小。
3.3 单一对映体实验 本研究首次通过单一对映体实验明确了克伦特罗对映体在猪体内不存在对映体转化现象。同时从0 d测定结果可知,猪内脏器官中肺脏和肝脏中克伦特罗含量最高,且不同个体之间两者存在较大差异,有的肺脏中克伦特罗含量比肝脏中高,而有的个体肝脏中克伦特罗含量比肺脏中高。
本研究通过分离和制备了克伦特罗单一对映异构体,获得的(-)-对映体和(+)-对映体质量分别为74.95、76.45 mg。通过饲喂含有盐酸克伦特罗外消旋体、单一对映体的饲料,进行了外消旋体和单一对映体在猪体内的立体选择性降解试验,分析不同时间采集的样品可知克伦特罗在猪体内代谢存在立体选择性,其中左旋异构体代谢较快,特别是在肝脏、肾脏和肺脏组织中所占比例较小,因此在科学评估肝脏、肾脏和肺脏组织中残存的该药物对人体健康造成的危害时,有必要对其进行对映异构体分析;同时单一对映体在猪体内不存在转化现象。
[1] Elliott C T,Crooks S R.Monitoring for clenbuterol abuse in N.Ireland 1989-1994 [J].Vet Q,1996,18(2):41-44.
[2] Martine Z,Navaari J E.Food poisoning related to consumption of illicit β-agonist in liver [J].Lancet,1990,336(8726):1311-1315.
[3] 黄显会,蔡勤仁,刘 戎,等.克伦特罗在猪组织和尿液中残留消除规律研究[J].动物毒物学,2003,18(1): 32-37.
[4] Smith D J,Paukson G D.Distribution,elimination,and residues of [14C]clenbuterol HCL in Holstein calves[J].J Anim Sci,1997,75:454-461.
[5] Malucdlli A,Ellebdorff F,Meyer H H D.Tissue distribution and residues of clenbuterol,salbutamol,and terbutaline in tissues of treated broiler chicks[J].J Anim Sci,1994,72:1555-1560.
[6] Rentsch K M.The importance of stereoselective determination of drugs in the clinical laboratory[J].J Biochem Bioph Meth,2002,54(1):l-9.
[7] Lu X M,Liu P,Chen H S,etal.Enantioselective pharmacokinetics of mabuterol in rats studied using sequential achiral and chiral HPLC[J].Biomed Chromatogr,2005,19(9):703-708.
[8] Awadallah B,Schmidt P C,Wahl M A.Quantitation of the enantiomers of ofloxacin by capillary electrophoresis in the parts per billion concentration range for in vitro drug absorption studies[J].J Chromatogr B,2003,988(1):135-143.
[9] Smith D J.Stereochemical composition of clenbuterol residues in edible tissues of swine[J].J Agri Food Chem,2000,48(12):6036-6043.
[10]Cristofol C,Virkel G,Alvarez L,etal.Albendazole sulfoxide enantiomeric ratios in plasma and target tissues after intravenous administration of ricobendazole to cattle[J].J Vet Pharmacol Ther,2001,24:117-124.
[11]陈国,刘勇军,吕燕,等.液相色谱串联质谱法测定猪肉中克伦特罗手性对映体残留量[J].肉类研究,2015,29(5): 22-26.
(编辑:侯向辉)
Study on the Stereochemical Degradation of Clenbuterol in Swine Edible Tissues
YU Zun-bo,ZHANG Yan2,WU Yin-Liang2*
(1.ChinaInstituteofVeterinaryDrugControl,Beijing100081,China;2.TheNingboAcademyofAgriculturalSciences,Zhejiang,Ningbo315040,China)
Two single enantiomers had been acquired by chiral separation to investigate whether there is a stereochemical degradation behavior in swine tissues for clenbuterol.Then,experiments were carried out in swine by feeding diets with 2.0 mg/kg of clenbuterol and 1.0 mg/kg of its single clenbuterol enantiomer for consecutive 7 days,respectively.After 7 d,the swine tissues (muscle,heart,lung,liver and kidney) and urine samples were collected regularly,and the content of clenbuterol enantimers had been determined by LC-MS/MS.After residual data analysis,there is stereochemical degradation behavior in swine tissues for clenbuterol.The ratio of (+) stereoisomer/(-) stereoisomer is higher than 1.5 for most of liver,lung and kidney samples when the swine had been fed with clenbuterol diets; and the ratio of (+) stereoisomer/(-) stereoisomer is between 0.8 and 1.25 for muscle and heart samples.For liver,kidney and urine samples,the ratio of (+) stereoisomer/(-) stereoisomer is highest at 3 d interval.Moverover,there is not mutual transformation for clenbuterol enantiomer in swine tissues.Finally,the experiment provide scientific basis for scientific assessment of damage of residual clenbuterol in animal derived food.
clenbuterol; enantiomers; stereochemical degradation;liquid chromatography with tandem mass spectrometry
宁波市重大科技攻关项目(2013C11003)
于遵波,兽医师,博士,从事兽药安全性评估研究。
吴银良。E-mail:wupaddyfield@sina.com
2015-10-12
A
1002-1280 (2015) 12-0027-05
S859.84

