氯吡格雷与奥扎格雷对进展性脑血栓形成患者血小板活化功能的影响
李钰 周波 付菱
(武汉市中山医院 1.内分泌科,2.药学部,3.心内科, 湖北 武汉 430030)
氯吡格雷与奥扎格雷对进展性脑血栓形成患者血小板活化功能的影响
李钰1周波2付菱3
(武汉市中山医院 1.内分泌科,2.药学部,3.心内科, 湖北 武汉 430030)
目的 探讨氯吡格雷与奥扎格雷对进展性脑血栓形成患者血小板活化功能变化的影响。方法 将2012年2月~2013年11月入住的76例颈内动脉系统进展性脑血栓形成患者按照数字表法随机分为氯吡格雷治疗组和奥扎格雷治疗组各38例。应用单克隆抗体技术和流式细胞仪动态检测患者体内CD63及CD62p的表达水平,对比两组患者的临床疗效和治疗前、治疗7和14天时的血小板活化指标。结果 治疗前两组患者CD63和CD62p的表达水平差异无统计学意义(P>0.05),治疗后各时段氯吡格雷组患者CD63和CD62p水平均显著低于奥扎格雷组(均P<0.05)。治疗前,两组患者生活能力指数和神经功能缺损评分差异无统计学意义(均P>0.05),治疗后各时段氯吡格雷组患者生活能力指数和神经功能缺损评分均显著优于奥扎格雷组(均P<0.01或P<0.05)。结论 氯吡格雷与奥扎格雷均能显著抑制进展性脑血栓形成患者血小板的活化功能,控制血小板表达 CD62p和CD63,但奥扎格雷的疗效更好,具有更好的临床应用价值。
氯吡格雷; 奥扎格雷; 脑血栓; 血小板
进展性脑血栓形成是指患者发病后48小时内神经功能障碍症状依然继续恶化[1]。近几年来,进展性脑血栓形成的发病率呈逐年上升趋势,而且越来越年轻化,对人类的健康和生命安全构成了严重威胁。对于进展性脑血栓的治疗包括介入治疗和药物治疗等多种治疗手段,其中药物治疗是最为保守也是适应证最广的治疗方法[2]。药物治疗主要是通过改善患者凝血水平和降低血脂等方法改善患者临床症状。氯吡格雷和奥扎格雷是两种临床上常用的抗凝血药物[3,4],然而对两者抗凝血效果的研究较少。因此,对氯吡格雷和奥扎格雷的血小板活化功能影响的研究有助于对进展性脑血栓的临床治疗。
1 资料与方法
1.1 一般资料 选取2012年2月~2013年11月收治的76例颈内动脉系统进展性脑血栓形成患者为研究对象,其中男49例,女27例,年龄42~70岁,平均(59.7±8.8)岁。按照数字表法随机分成氯吡格雷组和奥扎格雷组各38例。氯吡格雷组中男24例,女l4例,平均年龄(59.4±8.0)岁;奥扎格雷组中男25例,女l3例,平均年龄(60.0±7.7)岁。两组患者的性别、年龄差异无显著性(P>0.05),具有可比性。
1.2 入选标准 ①符合第四次国家脑血管病学术会议诊断标准,神经功能障碍在发病48小时之后依然继续恶化,脑缺血症状呈阶梯式加重[5]。②病人存在感觉、语言、肢体运动等方面的障碍。③经MRI或CT检查确诊为颈内动脉系统进展性脑血栓形成患者。④没有出血症状或出血可能。⑤近期未行抗血小板药物治疗。⑥年龄不超过75岁,没有严重的肝、肾和心脏疾病。
1.3 治疗方法 氯吡格雷组患者口服氯吡格雷(由赛诺菲安万特公司生产,规格为75mg/片,批号为20120105)75mg,每天1次;奥扎格雷组患者应用奥扎格雷(由石家庄四药有限公司生产,规格为100ml/支,成分为奥扎格雷钠80mg+NaCl 0.9mg,批号为20120112)100ml/天,每天1次。两组患者同时静脉滴注0.9%生理盐水250 ml+胞二磷胆碱0.5 g,每天1次,2周为1个疗程。于治疗前、治疗7天和14天的早上抽取两组患者1.5 ml静脉血,马上注入到7支含有10 g/L EDTA·Na20.5 ml试管中,立即倒置,并于45分钟内检测。
1.4 测定CD62p、CD63表达水平 使用上海生工公司提供的ELISA试剂盒测定两组患者的CD62p、CD63表达水平,严格按照说明书操作。
1.5 神经功能缺损评价[6]于治疗前、治疗7天和14天后,分别对两组患者进行日常生活活动能力 (Barthel Index,BI) 和神经功能缺损(NIHSS)评分。

2 结果
2.1 两组患者治疗前后CD62p、CD63水平比较 治疗前两组患者CD63和CD62p的表达水平无统计学差异(P>0.05)。治疗后7d和14d时两组患者CD63和CD62p水平均显著降低(均P<0.01),且氯吡格雷组患者CD63和CD62p水平均显著低于奥扎格雷组(P<0.05),见表1。
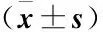
表1 两组患者治疗前后CD62p、CD63水平比较
注:与治疗前比较,①P<0.01;与奥扎格雷组比较,②P<0.05
2.2 两组患者治疗前后BI指数及NIHSS评分比较 治疗前,两组患者BI指数和NIHSS评分无统计学差异(P>0.05);治疗后各时段两组患者BI指数及NIHSS评分均显著改善(均P<0.01),且氯吡格雷组患者生活能力指数和神经功能缺损评分均显著优于奥扎格雷组(均P<0.01或P<0.05),见表2。
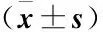
表2 氯吡格雷组和奥扎格雷组治疗前后NIHSS、BI指数比较
注:与治疗前比较,①P<0.01;与奥扎格雷组比较,②P<0.01,③P<0.0
2.3 不良反应 奥扎格雷组患者出现1例腹泻,氯吡格雷组患者出现腹泻、消化不良和皮疹各1例,两组患者均未出现严重不良反应事件。
3 讨论
若血小板处于静止状态,则其不会黏附于内皮细胞,进而发生聚集反应。在高切应力的作用下及发生血管损伤的情况时,血小板与血管壁发生碰撞反应,从而损伤血管壁上的凝血酶及纤维蛋白原等,造成血小板的形态改变、钙离子大量流失出去、伪足的形成和磷酸化反应的发生,导致血小板在血管内表皮细胞上发生黏附、聚集反应,并且分泌具有生理活性的物质,其作用于平滑肌细胞促进其收缩和增殖,最终诱导血管发生痉挛[7]。这就是血小板的活化反应。CD62p又被称为P-选择素(P-selectin),若激活血小板,其由血小板的α颗粒膜内被快速地移动到膜的表面,从而可以促进血小板、白细胞发生聚集反应[8];CD63是一种溶酶体糖蛋白,含有亲水基因,在信号传递中发挥重要作用[9]。
血栓烷A(TXA )可以诱导血小板发生黏附和聚集反应,奥扎格雷则可以抑制血栓烷A合酶的生理活性,通过作用于前列环素H(PGH)抑制血栓烷A的合成,导致前列环素H被迫转运到内表皮细胞,在此处前列环素H被转化为前列环素I,前列环素I具有阻碍血小板黏附、扩张血管的生理作用,因而可以抑制形成血栓[10]。所以,奥扎格雷能够有效地扩张血管、抗血小板聚集,使血流量增强,有效地治疗进展性脑血栓形成患者[11]。
血小板可被二磷酸腺苷(ADP)激活而聚集。当ADP与受体结合时,可激活血小板表面的糖蛋白Ⅱb/Ⅲa,激活的糖蛋白Ⅱb/Ⅲa结合于纤维蛋白原,导致血小板聚集效应的发生[12]。氯吡格雷是一种二磷酸腺苷受体抑制剂,能够有效地抑制多种因素引起的血小板聚集效应,进而有效地抑制血栓的形成[13]。
研究证实,两组患者治疗后血小板活化功能均显著降低,提示两种治疗方案均可以有效降低进展性脑血栓的发生和发展。而通过组间比较可知,氯吡格雷组降低血小板活性的效果优于奥扎格雷组。提示氯吡格雷抑制血栓形成的效果更优。其原因可能是氯吡格雷的使用剂量更大。由于已有研究证实,大剂量氯吡格雷安全有效,因此本研究中使用剂量较高[14]。而由于尚未见奥扎格雷大剂量运用报道,因此伦理委员会未予批准应用大剂量奥扎格雷。而两组患者的BI和NISHH评分在治疗后均显著改善,其原因是两组治疗方案均可以改善患者的凝血功能而减少血栓的形成。通过改善患者的大脑供血而改善患者的神经功能和生活能力。由于氯吡格雷的抑制血栓功能更佳,因此患者的BI指数更高,且NIHSS评分更低。
4 结论
氯吡格雷治疗进展性脑血栓安全有效,可以在降低患者血小板活化功能的同时,改善患者的神经功能和生活能力,具有临床应用价值。
[1]周言勇, 谈儒钢. 低分子肝素联合血塞通治疗进展性脑梗死的临床研究[J]. 医药前沿, 2012, 2(5):823-825.
[2]Simard J M, Sahuquillo J, Sheth K N,etal. Managing malignant cerebral infarction[J]. Current treatment options in neurology, 2011, 13(2): 217-229.
[3]Mehta S R, Bassand J P, Chrolavicius S,etal. Dose comparisons of clopidogrel and aspirin in acute coronary syndromes[J]. N Engl J Med, 2010, 363(10): 930-942.
[4]Zhang J, Yang J, Chang X,etal. Ozagrel for acute ischemic stroke: a meta-analysis of data from randomized controlled trials[J]. Neurological research, 2012, 34(4): 346-353.
[5]陈清棠.各类脑血管疾疾诊断要点[J].中华神经科杂志,1996,29(6):397.
[6]陈清棠.脑卒中患者临床神经功能缺损程度评分标准及临床疗效评定标准[J].中华神经科杂志,1996,29:381.
[7]蒋荣峰, 李丽娟. 血栓通注射液治疗脑血栓形成 40 例疗效观察[J]. 西部医学, 2012, 24(6): 1095-1096.
[8]周强, 易兴阳, 池丽芬. 血小板白细胞聚集体及其临床意义[J]. 温州医学院学报, 2010, 40(1): 96-99.
[9]张冰, 胡正刚, 王亚仙, 等. 急性脑梗死患者血小板 CD62P, CD63 表达的影响因素分析[J]. 中外医疗, 2011, 30(24): 46-47.
[10] Koumura A, Hamanaka J, Kawasaki K,etal. Fasudil and ozagrel in combination show neuroprotective effects on cerebral infarction after murine middle cerebral artery occlusion[J]. Journal of Pharmacology and Experimental Therapeutics, 2011, 338(1): 337-344.
[11] LI H, CHEN C. Clinical effects of sodium ozagrel combined with low molecular weight heparin on patients with progressive cerebral infarction[J]. Journal of Shandong University (Health Sciences), 2011, 5: 026.
[12] 章靓, 陈旺, 庞文生, 等. 血栓形成机制及血小板膜糖蛋白 Ⅱb/Ⅲa 受体拮抗剂的研究进展[J]. 国际药学研究杂志, 2009, 36(4): 268-271.
[13] Bouman H J, Schömig E, van Werkum J W,etal. Paraoxonase-1 is a major determinant of clopidogrel efficacy[J]. Nature medicine, 2011, 17(1): 110-116.
[14] Mehta S R, Tanguay J F, Eikelboom J W,etal. Double-dose versus standard-dose clopidogrel and high-dose versus low-dose aspirin in individuals undergoing percutaneous coronary intervention for acute coronary syndromes (CURRENT-OASIS 7): a randomised factorial trial[J]. The Lancet, 2010, 376(9748): 1233-1243.
Influence of clopidogrel and ozagrel on platelet activation in the patients with progressive cerebral thrombosis
LI Yu1, ZHOU Bo2, FU Ling3
(1.DepartmentofEndocrine,WuhanZhongshanHospital,Wuhan430030,China;2.DepartmentofPharmacy,WuhanZhongshanHospital,Wuhan430030,China;3.DepartmentofCardiovascular,WuhanZhongshanHospital,Wuhan430030,China)
Objective To investigate influence of clopidogrel and ozagrel on platelet activation in the patients with progressive cerebral thrombosis. Methods 76 patients with progressive cerebral thrombosis were randomly divided into clopidogrel treatment group and ozagrel treatment group. The expression level of CD63 and CD62p were measured with monoclonal antibody technology and dynamic flow cytometry. The activation effect and treatment effect were compared between two groups. Results The expression level of CD63 and CD62p had no statistically significant difference between the in two groups before treatment (P>0.05). The expression of CD63 and CD62p of clopidogrel group after treatment was lower than that of Ozagrel group after treatment (P<0.05). The indexes of neural function defect and life ability of patients before treatment had no significant difference (P>0.05). The indexes of neural function defect and life ability of patients after treatment of clopidogrel group were significantly better than that of Ozagrel group (P<0.01 orP<0.05). Conclusion Clopidogrel and Aozhageleijun can significantly inhibit the progress of platelet function, CD62p and CD63 expression of cerebral thrombosis patients.
Clopidogrel; Ozagrel; Cerebral thrombosis; Platelet
R 743.32
A
10.3969/j.issn.1672-3511.2015.06.027
2014-10-08; 编辑: 母存培)

