抗病毒治疗慢性乙型肝炎合并非酒精性脂肪肝疗效观察
刘素芬,武博荣,刘振中,吴秀颀,魏 娟,林 琳,董金红,张彦芳,董正洪,李兵顺
(河北省石家庄市第五医院,河北 石家庄 050021)
抗病毒治疗慢性乙型肝炎合并非酒精性脂肪肝疗效观察
刘素芬,武博荣,刘振中,吴秀颀,魏 娟,林 琳,董金红,张彦芳,董正洪,李兵顺
(河北省石家庄市第五医院,河北 石家庄 050021)
目的探讨抗病毒治疗慢性乙型肝炎(CHB)合并非酒精性脂肪肝(NAFLD)的效果。方法按照NAFLD评分将64例CHB合并NAFLD患者分为5分组、6分组、7分组、8分组,每组内再随机分为抗病毒组及对照组2个亚组。抗病毒组在治疗脂肪肝的同时进行抗病毒干预,对照组则只进行脂肪肝治疗。观察各评分组中2个亚组治疗前后的血清学指标、病毒学指标及肝脏病理学指标变化情况。结果相同NAFLD评分组内的抗病毒组治疗后ALT、AST、TC、TG、HBsAg及HBV DNA水平显著低于对照组(P均<0.05),炎症程度和脂肪肝分级改善程度均明显优于对照组(P均<0.05)。不同NAFLD评分组间, 7分组、8分组血清生化指标改善程度更为明显,5分组、6分组抗病毒疗效更佳。结论CHB合并NAFLD治疗过程中,积极的抗病毒干预相对于单纯的脂肪肝治疗具有更好的治疗效果。
非酒精性脂肪肝;慢性乙型肝炎;NAFLD评分;抗病毒
随着我国居民生活水平的提高及生活方式的改变,非酒精性脂肪肝(NAFLD)的发病率呈现逐年上升的趋势。而慢性乙型肝炎(CHB)一直以来都是严重影响人们健康的主要疾病之一,伴随CHB合并NAFLD患病人数的增多,CHB合并NAFLD引起了广泛重视[1-3]。笔者对本院2014年1—12月收治的32例CHB合并NAFLD患者进行了抗病毒治疗,研究了治疗后患者的血清学、病毒学及病理学等指标的变化规律,以期找到CHB合并NAFLD的有效临床治疗方法。现将结果报道如下。
1 临床资料
1.1一般资料 选取上述时期本院收治的连续6个月以上肝功能指标ALT>3ULN的CHB合并NAFLD患者64例,均符合文献[4-5]相关诊断标准,血常规检查正常。排除合并其他类型肝炎病毒感染者,伴有自身免疫性疾病、精神病、糖尿病者,妊娠及哺乳期者,伴影响抗病毒治疗疗效的疾病者。其中男36例,女28例;年龄31~62岁,平均45.5岁。将上述患者按照NAFLD评分分为5分组、6分组、7分组、8分组,每组内再随机分为抗病毒组及对照组2个亚组,每组8例,抗病毒组及对照组患者性别、年龄、肝功能、血脂水平及患病程度等比较差异均无统计学意义(P均>0.05),具有可比性。
1.2治疗方法 各组患者均给予保肝治疗:甘草酸二胺(正大天晴药业集团股份有限公司,国药准字H20040628) 150mg/次及复合磷酸酯酶肠溶片(青岛黄海制药有限责任公司,国药准字H37023438)100~200mg/次饭后服用,均3次/d。抗病毒组在此基础上给予恩替卡韦(正大天晴药业集团股份有限公司,国药准字H20100019)0.5mg/次口服,1次/d,疗程48周。
1.3观察指标 ①治疗前后清晨空腹抽取患者外周静脉血,通过日立7060全自动生化分析仪检测谷丙转氨酶(ALT)、谷草转氨酶(AST)、三酰甘油(TG)和总胆固醇(TC)。②治疗前后通过肝脏穿刺肝细胞活检进行肝脏组织学检查,考察肝细胞的脂肪变程度、炎症程度及气球样变程度的变化。<5%的肝细胞有脂肪变为S0,5%~33%的肝细胞有脂肪变为S1,34%~66%的肝细胞有脂肪变为S2,66%以上的肝细胞有脂肪变为S3。肝小叶内炎症程度和肝细胞气球样变程度由富有经验的病理科医生分别依据20倍镜下坏死灶计数和气球样变数目按照L0~L3和B0~B2作出评分[5]。③检查抗病毒组治疗前后HBsAg及HBV DNA定量变化情况。HBsAg采用ELISA方法检测,HBV DNA采用荧光定量PCR方法检测。
1.4统计学方法数据采用SPSS 17.0统计学软件进行统计分析。计数资料采用率表示,进行2检验;计量资料采用表示,进行t检验。P<0.05为差异有统计学意义。
2 结 果
2.1不同NAFLD评分组中抗病毒组与对照组治疗前后血清生化指标变化情况比较 不同NAFLD评分组中抗病毒组和对照组治疗后各项血清生化指标水平均显著低于治疗前(P均<0.05),而相同NAFLD评分组内对照组治疗后的各项指标水平则显著高于抗病毒组(P均<0.05)。虽然不同NAFLD评分组中抗病毒组治疗后的各项指标相近,但7分组、8分组治疗前的各项指标水平较高,因此,7分组、8分组的血清生化指标水平改善更为显著。见表1。
2.2不同NAFLD评分组中抗病毒组治疗前后病毒学指标变

表1 不同NAFLD评分组中抗病毒组与对照组治疗前后血清生化指标水平比较
注:①与治疗前比较,P<0.05;②与对照组比较,P<0.05。
化情况比较 不同NAFLD评分中抗病毒组治疗后HBsAg和HBVDNA水平均显著低于治疗前(P均<0.05)。此外, 5分组、6分组治疗后HBsAg和HBVDNA水平均显著低于7分组、8分组(P均<0.05)。见表2。

表2 不同NAFLD评分组中抗病毒组治疗前后病毒学指标比较
注:①与治疗前比较,P<0.05;②与5分组抗病毒组比较,P<0.05;③与6分组抗病毒组比较,P<0.05。
2.3不同NAFLD评分组中抗病毒组与对照组治疗前后肝组织学指标变化情况比较 不同NAFLD评分组中抗病毒组和对照组治疗后脂肪变程度、炎症评分及气球样变评分均有好转(P均<0.05)。而相同NAFLD评分组内,抗病毒组肝脂肪变程度明显轻于对照组(P均<0.05),炎症、气球样变低评分患者数目显著多于对照组(P均<0.05)。见表3。
2.4不同NAFLD评分组中抗病毒组与对照组疗效比较 不同NAFLD评分组中抗病毒组的肝功复常率和HBVDNA转阴率均显著高于对照组(P均<0.05)。5分组、6分组治疗后肝功复常率均显著低于7分组和8分组(P均<0.05),而HBVDNA转阴率均显著高于7分组和8分组(P均<0.05)。见表4。
3 讨 论
CHB是人体感染乙型肝炎病毒(HBV)后以肝细胞损害为主要病理改变的肝脏疾病,HBV通过引发机体免疫调节紊乱导致肝细胞损害、肝纤维化以及肝功能异常[6]。NAFLD是由胰岛素抵抗和遗传易感性等因素导致肝细胞内脂肪过度蓄积从而引发肝损伤的肝脏疾病[7-8]。CHB和NAFLD虽是两个独立疾病,但临床上往往合并出现,相互影响,造成肝脏纤维化的发生率增高,向肝硬化转化的进程加快,给临床治疗带来了困难[9-10]。
本研究结果表明相对于只进行脂肪肝治疗的患者,同时接受抗病毒治疗和脂肪肝治疗患者的ALT、AST、TC、TG以及HBsAg和HBVDNA改善程度更明显。虽然单纯进行脂肪肝治疗组患者的肝纤维化程度、炎症程度及气球样变程度有所缓解,但同时进行抗病毒治疗组效果更加明显;且治疗48周后肝功复常率和HBVDNA转阴率最大可以达到88%和100%。但不同NAFLD评分组抗病毒干预表现出了不同的效果,7分组和8分组生化学指标改善更为明显,而5分组、6分组抗病毒疗效更佳。提示对于脂肪肝程度重的患者抗病毒治疗疗效不佳,证明NAFLD是影响CHB抗病毒疗效的因素之一,对此类患者应加强脂肪肝综合治疗(包括药物、运动等综合干预措施)。但对于重度脂肪肝患者抗病毒治疗可辅助肝功能的改善,建议对单纯保肝治疗疗效不佳的患者同时联合应用抗病毒药物,以促进肝细胞功能的修复。对于NAFLD评分5分、6分的患者,肝功能ALT>3NLN时,建议加用抗病毒治疗,以减少肝脏所遭受的多重打击因素,本研究证实此类患者抗病毒效果满意。

表3 不同NAFLD评分组中抗病毒组与对照组治疗前后肝组织学指标比较 例
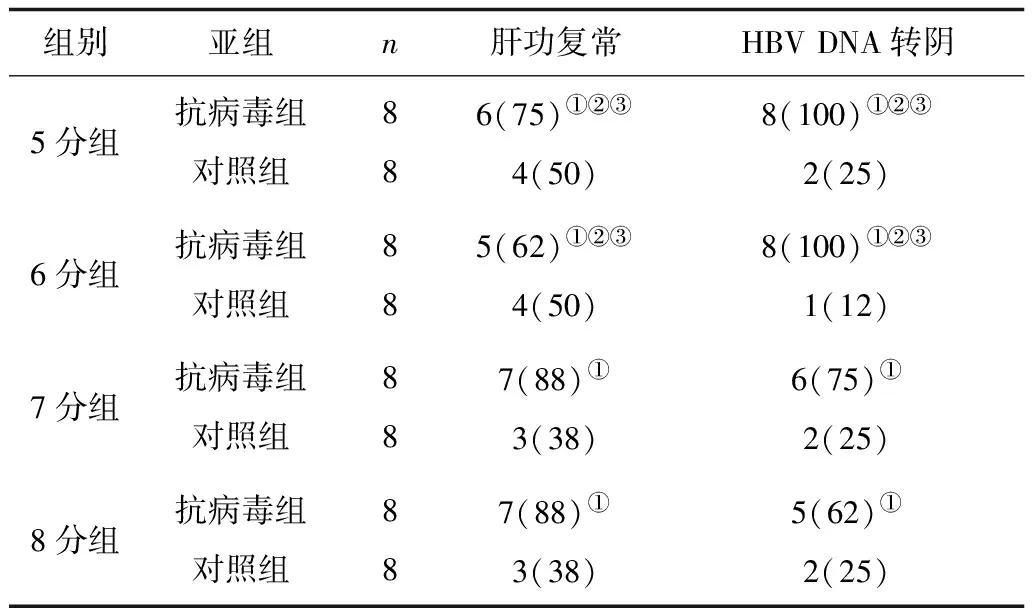
表4 不同NAFLD评分组中抗病毒组与对照组疗效比较 例(%)
注:①与对照组比较,P<0.05;②与7分组比较,P<0.05;③与8分组比较,P<0.05。
综上所述,对于CHB合并NAFLD患者在治疗脂肪肝病变的同时进行抗病毒干预可以在使HBsAg和HBVDNA转阴的同时,可明显提高肝功复常,改善NAFLD分级,抗病毒和脂肪肝治疗协同作用下可以更好地降低肝脏损伤程度,恢复肝脏功能。
[1] 吴柳,叶军,张洁.慢性乙型肝炎合并非酒精性脂肪性肝病患者临床及病理特征[J].肝脏,2013,18(11):735-737
[2] 杨学谨.慢性乙型肝炎合并非酒精性脂肪性肝病的临床分析[J].临床合理用药杂志,2014,7(7A):112-113
[3] 赵莹,邵清,陈国凤.慢性乙型肝炎合并非酒精性脂肪肝的研究动态[J].传染病信息,2013,26(5):315-318
[4] 中华医学会肝病学分会,中华医学会感染病学分会.慢性乙型肝炎防治指南[J].中国临床医生,2012,40(4):66-78
[5] 范建高.中国非酒精性脂肪性肝病诊疗指南(2010年修订版)[J/CD].中国医学前沿杂志:电子版,2012,4(7):4-10
[6] 朱艳萍.不同抗病毒治疗方案治疗慢性乙型肝炎的临床效果[J].世界华人消化杂志,2015,23(6):974-978
[7] 郭万越.非酒精性脂肪肝相关因素Logistic回归分析[J].实用肝脏病杂志,2011,14(5):376-378
[8] 夏菁,孙涛.非酒精性脂肪肝发病机制及治疗研究进展[J].海军总医院学报,2010,23(2):100-103
[9] 刘晓,朱月永.慢性乙型肝炎合并非酒精性脂肪肝的研究进展[J].实用肝脏病杂志,2009,12(4):318-320
[10] 饶紫兰,江家骥.慢性乙型肝炎与非酒精性脂肪肝相关性研究进展[J].中国卫生产业,2012(15):164-166
10.3969/j.issn.1008-8849.2015.18.016
R575.5
B
1008-8849(2015)18-1980-03
2014-11-20

