HPLC测定利胆消石颗粒中槲皮素和山奈素含量
刘译
(怀化市食品药品检验所,湖南怀化418000)
HPLC测定利胆消石颗粒中槲皮素和山奈素含量
刘译
(怀化市食品药品检验所,湖南怀化418000)
目的:建立利胆消石颗粒中槲皮素和山奈素含量测定方法。方法:色谱柱:DIKMA-C18柱(4.6mm×250mm;5μm),流动相为甲醇-0.4%磷酸(45∶55),流速为1.0m L/m in,检测波长为360 nm,柱温为30℃。结果:利胆消石颗粒中槲皮素和山奈素的线性范围分别为0.988~98.8μg/m L(r=0.999 8),0.979~97.9μg/m L(r=0.999 7),平均回收率为98.21%,98.18%,RSD值为0.71%,0.56%。结论:该方法简便,结果准确,可作为利胆消石颗粒的质量控制方法。
利胆消石颗粒;槲皮素;山奈素;含量测定;高效液相色谱法
利胆消石颗粒由金钱草、木通、芒硝、松子、乌药、莪术、海金沙、枳壳、丹参9味中药组成,具有消热利湿,利胆排石的功效。用于泌尿系结石,胆道结石,胆囊炎,胆道感染等。金钱草为本方中君药,金钱草中的有效成分为槲皮素和山奈素,现行质量标准没有对其进行含量测定,为了有效控制本品的质量,本研究参照《中国药典》[1]及相关文献[2-9]对金钱草中槲皮素和山萘素同时进行含量测定,结果满意,现报道如下。
1 仪器与试液
1.1 仪器
日本岛津LC-20ATVP高效液相色谱仪(LC-20AT四元泵,SPD-M 20A型二极管阵列检测器,SIL-20A自动进样器,LCsolution色谱工作站),METTLER TOLEDO十万分之一电子分析天平(瑞士)。
1.2 试药
利胆消石颗粒(怀化市第一人民医院,规格:20 g/包,批号:20131006,20131109,20131218),槲皮素对照品(原中国药品生物制品检定所,批号:100081-200406,纯度:100%),山萘素对照品(原中国药品生物制品检定所,批号:110861-200304,纯度100%),甲醇(色谱纯,TEDIA),磷酸(色谱纯,TEDA),甲醇(分析纯),水为去离子重蒸馏水(科室自制)。
2 含量测定
2.1 色谱条件
色谱柱为DIKMA-C18柱(4.6 mm×250 mm;5μm),流动相为甲醇-0.4%磷酸(45∶55),水流速为1.0 m L/m in,检测波长为360 nm,柱温为30℃。
2.2 溶液的制备
2.2.1 对照品溶液 精密称取经五氧化二磷干燥24 h至恒重的槲皮素对照品(9.88 mg)和山奈素对照品(9.79 mg)置100 m L棕色量瓶中,用80%甲醇溶液40 m L使溶解,并定容至刻度,摇匀,配制成混合对照品储备液。
2.2.2 供试品溶液 取装量差异项的内容物,精密称取样品5.0 g,置100 m L锥形瓶中,精密加入80%甲醇50 m L,称定重量,加热回流60 m in,放冷,再称定重量,用80%甲醇补足减失的重量,摇匀,滤过。精密量取续滤液25 m L,加入盐酸5 m L,置水浴中加热水解1小时,取出,迅速冷却,转移至50 m L量瓶中,用80%甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
2.2.3 阴性对照液 取除金钱草以外的其他8味药材按处方制备成不含金钱草样品,再按供试品溶液方法制备。
2.3 标准曲线制备
取混合对照品储备液0.1,0.5,1.0,2.0,4.0, 6.0,8.0,10.0 m L置10 m L棕色量瓶中,以流动相定容至刻度。按照2.1项下进样10μL,记录色谱图,见图1A。由峰面积(Y)(n=3)对响应的浓度(X)直线回归,槲皮素回归方程为:
Y=37 826 284.241 3X+18 988.318 6,
r=0.999 8,表明槲皮素在0.988~98.8μg/m L的浓度范围内线性相关;山奈素回归方程为:
Y=37 925 392.597 5X-26 716.769 4,
r=0.999 7,表明山奈素在0.979~97.9μg/m L的浓度范围内线性相关。
2.4 系统适用性试验
分别取对照品溶液、样品溶液、阴性对照液注入色谱仪,记录色谱图,从图1中可以看出,槲皮素峰和山奈素峰与其相邻峰完全分离,阴性对照色谱图在对应的槲皮素峰和山奈素峰位置处无干扰峰,即表明其他组分对测定无干扰。槲皮素峰和山奈素峰与其他组分峰的分离度都大于1.5。
2.5 精密度考察
取同一样品溶液连续进样6次,进样量10μL,测定峰面积,计算RSD值为0.68%,0.72%。结果表明仪器与色谱条件具有良好的精密度。
2.6 重复性试验
取同一批号(批号:20121006)的样品6份,按2.2.2方法制备供试品溶液,分别精密吸取各供试品溶液10μL注入高效液相色谱仪。测定峰面积,根据线性回归方程计算含量,相对标准偏差RSD分别为0.82%,0.77%。
2.7 稳定性试验
取同一样品溶液,在0,2,4,6,8,10,12 h分别进样10μL,依法测定,结果6次测定的槲皮素和山奈素峰面积RSD分别为1.01%,1.08%,表明样品溶液在12 h内相对稳定。

图1 槲皮素和山奈素色谱
2.8 回收率试验
精密称取已知含量的样品(批号:20121006,平均装量:20.252 6 g/包)10.0 g 9份置锥形瓶中,每份分别加入对照品混合溶液(重新配制)0.8 m L,0.8 m L,0.8 m L,1.0 m L,1.0 m L,1.0 m L,1.2m L,1.2m L,1.2m L(槲皮素浓度为0.247mg/m L,山奈素浓度为0.222 mg/m L)水浴加热将其蒸干。按2.2.2方法制备。按2.1项下分别进样10μL,记录色谱图,测定槲皮素和山奈素的峰面积,经换算后,计算槲皮素和山奈素的回收率,结果见表1。
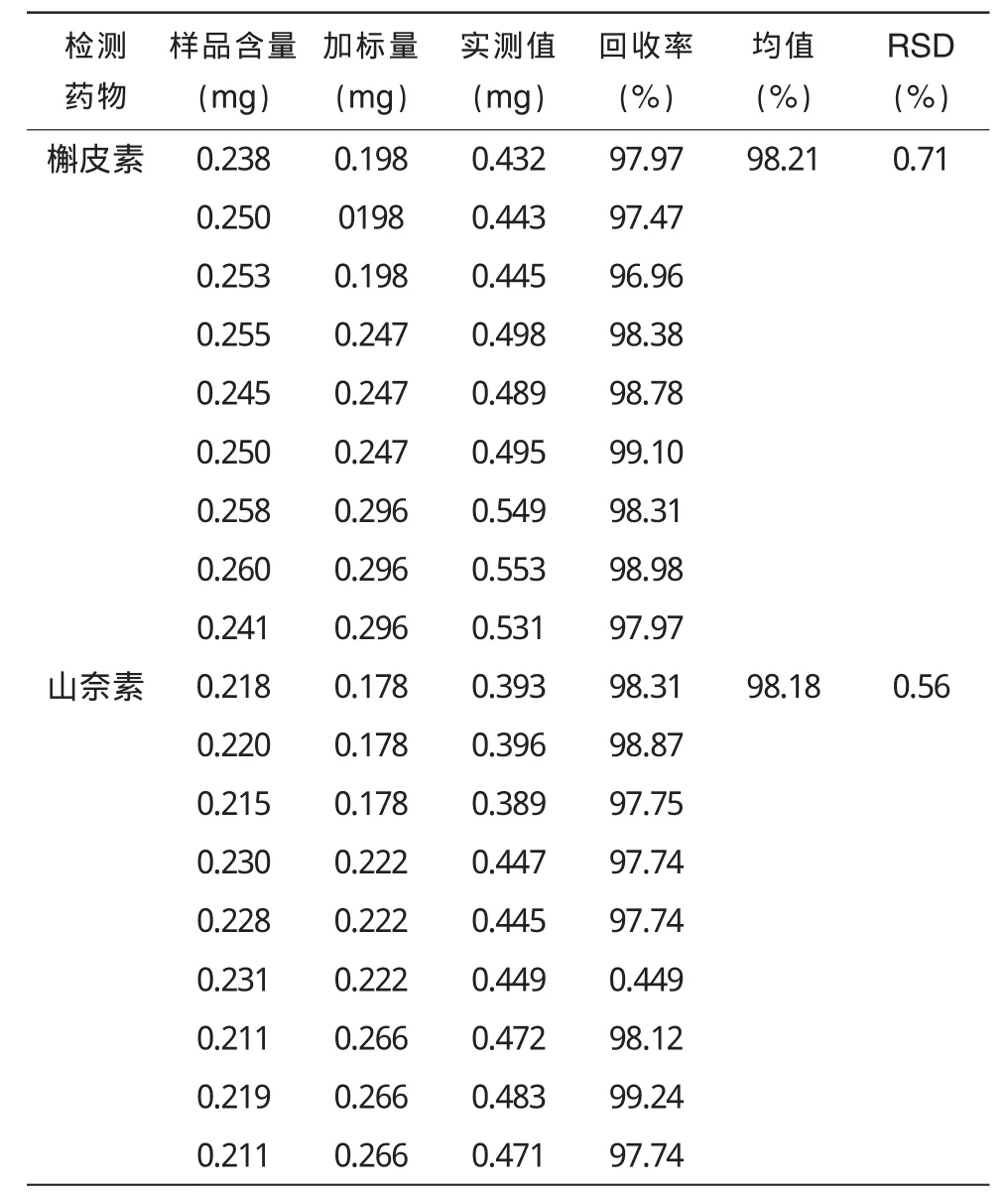
表1 回收试验结果(n=9)
2.9 样品含量测定
将3批不同批号的利胆消石颗粒按2.2.2方法制备,进样10μL,测定峰面积,按外标法计算含量。结果见表2。
3 讨论
3.1 以80%甲醇为溶剂,通过高效液相色谱DAD检测器扫描,发现槲皮素和山奈素这两种对照品溶液均在360 nm波长处有最大吸收,因此确定360 nm为检测波长。
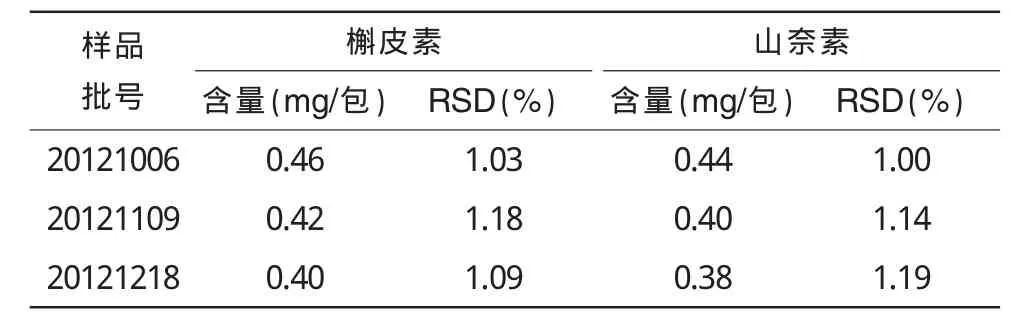
表2 样品含量测定结果(n=3)
3.2 试验中以文献[1]提供的色谱条件甲醇-0.4%磷酸(50∶50)为基础,改变流动相的比例甲醇-0.4%磷酸(45∶55),通过试验摸索,利胆消石颗粒中各组分能够较好分离,该条件适合利胆消石颗粒的含量测定。
3.3 本试验采用HPLC同时测定利胆消石颗粒中槲皮素和山奈素的含量,具有方法简便,重复性好,准确且专属性较强的优点,具一定的实际意义。
[1]国家药典委员会.中华人民共和国药典(2010年版)一部[S].北京:中国医药科技出版社,2010:204.
[2]杨燕飞.HPLC测定金胆片中山柰素和槲皮素的含量[J].中成药,2005,27(11):1263-1265.
[3]温梅云,钟球,钟鸣.HPLC法测定通淋颗粒中槲皮素山奈素的含量[J].国际医药卫生导报,2007,13(4):86-88.
[4]郭美玲,孙佳玲,孙公国.HPLC法测定北合欢中槲皮素和山奈素的含量[J].中国药事,2011,25(7):647-649.
[5]赵艳丽,黄亦琦,胡珊梅,等.HPLC测定全蚕粉中槲皮素和山奈素的含量[J].中国实验方剂学杂志,2012,18(18):95-97.
[6] 丁立新,李春英,孙启芬.高效液相法测定小叶金钱草中槲皮素和山奈素的含量[J].黑龙江医药科学,2009,32(5):17-18.
[7]阎婷,金宪涵,王盈.HPLC测定金钱草中槲皮素和山奈素的含量[J].中华中医药学刊,2009,20(6):624-625.
[8]张集盘,叶国梁,石晶萍,等.RP-HPLC测定金钱草中槲皮素和山柰素两种黄酮成分的含量[J].江苏药学与临床研究,2005,13(1):31-33.
[9]杜勇,李琰,张小茜.金钱草质量标准的研究[J].中国中药杂志,2006,31(5)438-440.
Content Determ ination of Quercetin and Kaempferol in Lidan XiaoshiGranules by HPLC
Liu Yi(Huaihua Municipal Food and Drug Inspection Institute,Hunan Huaihua 418000,China)
Objective:To establish a HPLC method for the content determ ination of quercetin and kaempferol in lidan xiaoshi granules.M ethods:DIKMA-C18(4.6 mm×250 mm;5μm)column was used w ith the mobile phase of methanol-0.4%phosphoric acid solution(45∶55),the flow ratewas 1.0m L/min,the detection wavelength was at 360 nm and the column temperature was at 30℃.Results:A good linear relationship of quercetin and kaempferol was w ithin the range of 0.988~98.8μg/m L(r=0.999 8)and 0.979~97.9μg/m L(r=0.999 7)respectively,and the average recovery of quercetin and kaempferolwas 98.21%and 98.18%(RSD was 0.71%and 0.56%).Conclusion:Themethod is simple and accurate,which can be used for the quality control of lidan xiaoshigranules.
Lidan XiaoshiGranules;Quercetin;Kaempferol;Content Determ ination;HPLC
10.3969/j.issn.1672-5433.2015.01.006
2014-06-27)
刘译,男,副主任药师。研究方向:食品药品检验。E-mail:442959621@qq.com

