脑梗死可逆性血管增多及静脉充盈早现一例
吴雄枫,李子付,洪 波,张永巍
1 病例介绍
患者,女性,66岁,因“突发意识不清3 d”于2015年5月15日就诊于长海医院脑血管病内科。患者3天前(2015-05-12)行双下肢静脉曲张微创手术,术后观察3 h,未给予药物治疗,中午出院下楼梯后突发胸闷不适、面色苍白、恶心呕吐、大小便失禁,继而意识不清,无牙关紧闭、肢体抽搐。立即在长海医院急诊就诊,测血压65/40 mmHg,考虑低血压休克,转入急诊重症监护病房抢救,行心肺复苏、静脉补液、多巴胺升压等治疗,5 h后意识转清,生命体征逐渐平稳,但出现言语不能,听不懂别人说话,烦躁不安,右侧肢体力弱,尚可抬举,无大小便异常。2 d后(2015-05-14)行头颅计算机断层扫描(computed tomography,CT)示左侧额颞顶叶大面积脑梗死,为进一步治疗收住脑血管病内科。
既往“双下肢静脉曲张”病史5年,分别于2015年5月7日、12日2次在我院血管外科行手术治疗,手术部位情况良好。否认心脏病、高血压病、糖尿病、肝炎、结核等史。无食物及药物过敏史,无毒物接触史,无烟酒嗜好。
入科查体:体温36.8℃、脉搏62次/分、呼吸21次/分、血压121/78 mmHg(右)、118/75 mmHg(左)。心、肺、腹查体无异常。神经系统查体:神志清楚,混合性失语(完全性运动性失语、不完全性感觉性失语),颅神经检查未见异常,右侧上下肢远近端肌力3级,左侧上下肢肌力5级,肌张力正常,左侧共济运动正常;双侧深、浅感觉正常。右侧Babinski征(+)、Chaddock征(+),颈软,脑膜刺激征(-)。美国国立卫生研究院卒中量表(National Institutes of Health Stroke Scale,NIHSS)评分7分。
辅助检查:实验室检查(2015-05-14):血、尿、便常规未见明显异常。D-二聚体:8.87 μg/ml(0~0.5 μg/ml)、纤维蛋白原:4.1 g/L(2~4 g/L)、纤维蛋白降解产物:23.32 μg/ml(0~6μg/ml),低密度脂蛋白胆固醇:2.75 mmol/L,高密度脂蛋白胆固醇:1.5 mmol/L,总胆固醇:4.62 mmol/L,甘油三酯:2 mmol/L;血糖:5.9 mmol/L;同型半胱氨酸:19 μmmol/L(0~10 μmmol/L)。自身免疫抗体全套未见异常。
心脏彩超(2015-05-14):左室舒张功能正常,射血分数(ejection fraction,EF)61%。
头颅CT(2015-05-14):左侧额颞顶叶大面积脑梗死(图1A)。
颅脑磁共振成像(magnetic resonance imaging,MRI)(2015-05-18):左侧额颞顶叶急性脑梗死(图2A、图2B)。
头颅计算机断层扫描血管造影(C T angiography,C TA)及灌注成像(C T perfusion imaging,CTP)(2015-05-18):左侧大脑中、后动脉及其分支明显增多增粗、扭曲,并左侧颅内浅静脉及静脉窦早显,致左额颞顶叶密度欠均匀,其供血区呈相对高灌注,考虑动静脉瘘可能性大(图3A);左侧大脑半球脑梗死,可能伴少许渗血灶(图1B)。
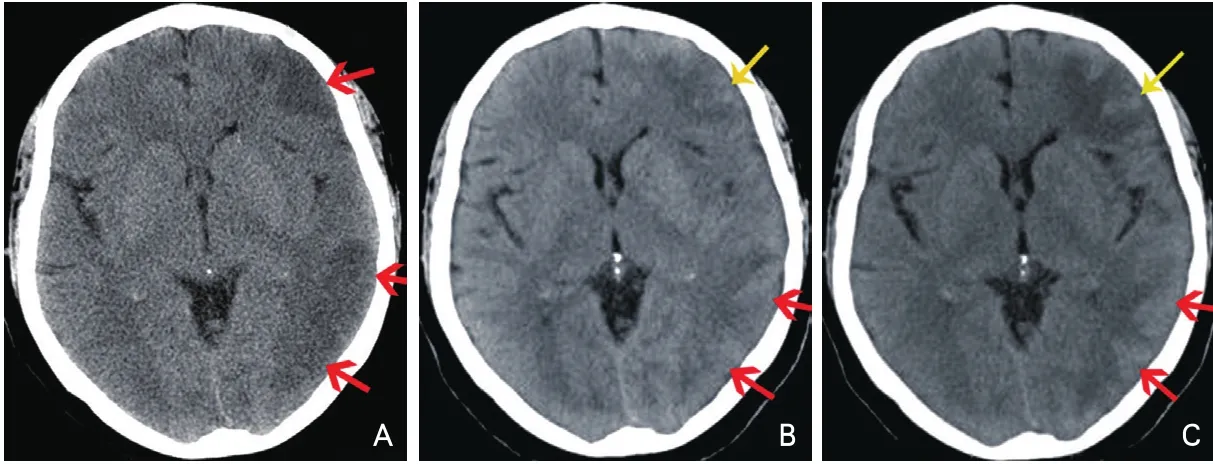
图1 患者头颅计算机断层扫描
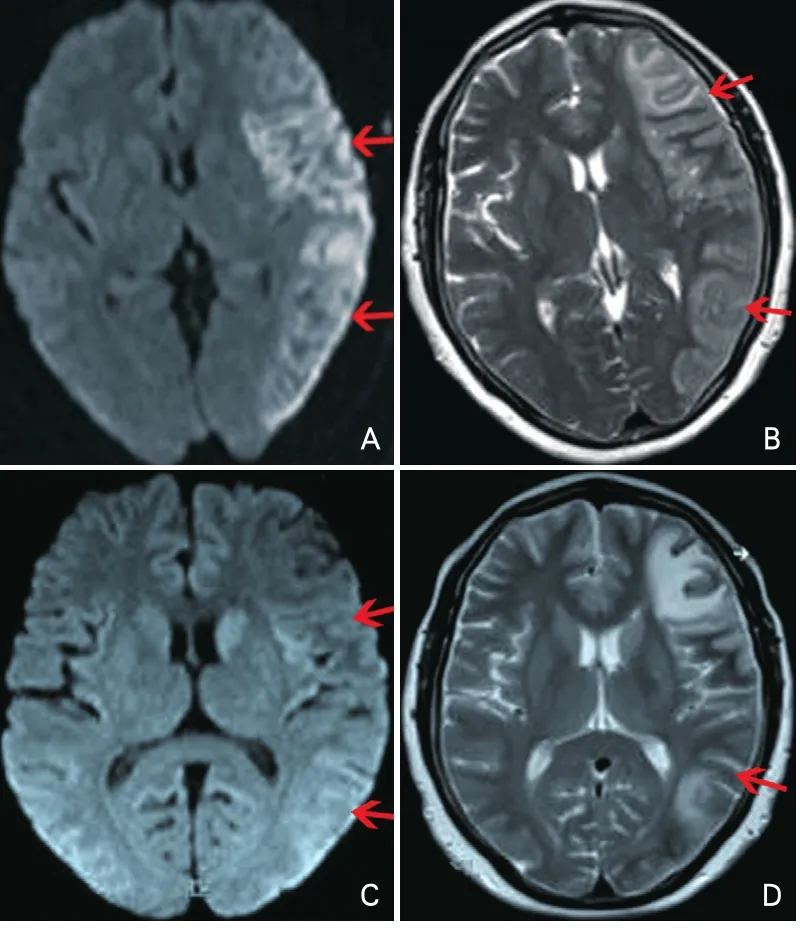
图2 患者颅脑磁共振成像
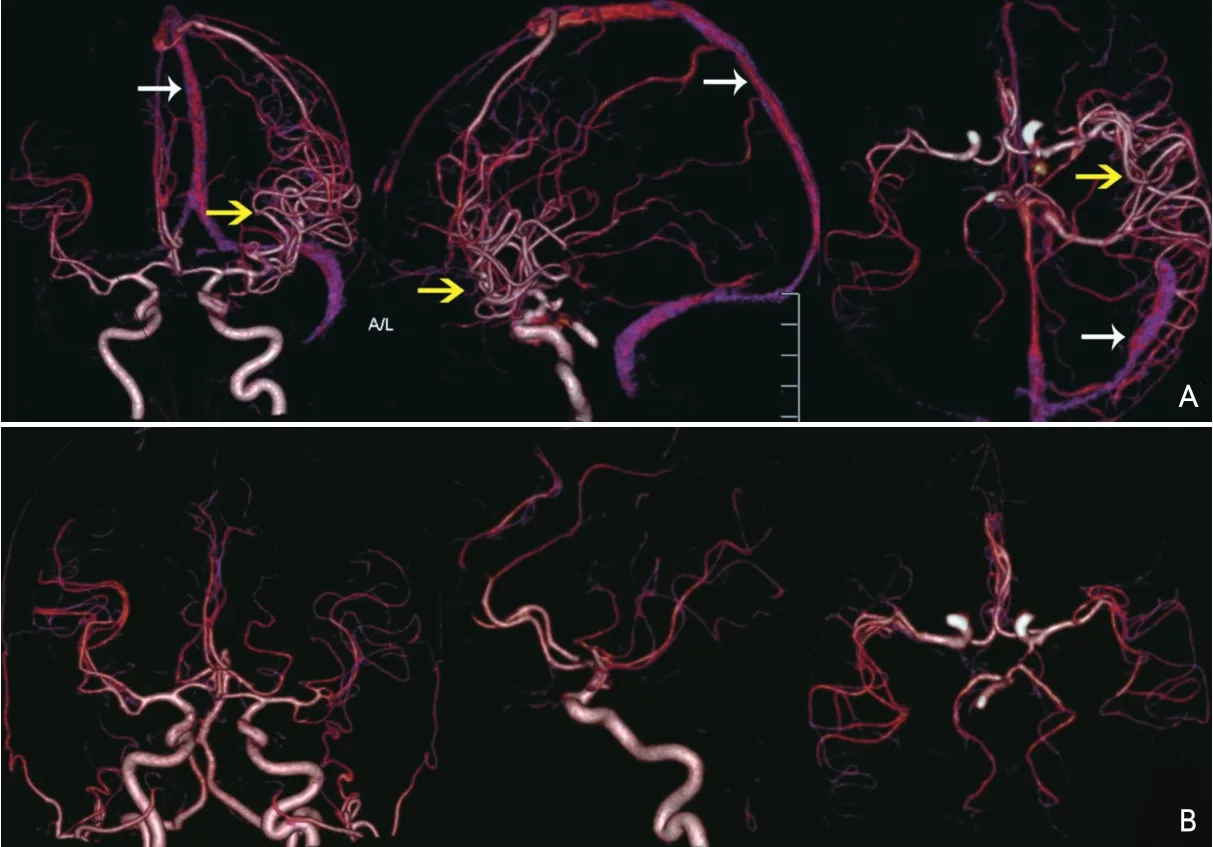
图3 头颅计算机断层扫描血管造影
肺动脉CTA(2015-05-22):肺动脉CT增强造影未见明显异常;两肺炎症,建议治疗后复查;两下肺背侧稍许间质性改变;双侧胸膜增厚。
动态心电图(2015-05-29):窦性心律;Ⅱ°Ⅰ型房室传导阻滞(24小时记录到4次)。
入院诊断:
脑梗死
左侧大脑中动脉供血区
大动脉粥样硬化性(TOAST)
双下肢静脉曲张术后
诊疗经过:按照脑梗死TOSAST分型标准[1],考虑患者为大动脉粥样硬化性,根据2014美国心脏学会/美国卒中学会卒中和短暂脑缺血发作二级预防指南[2],予入院后阿司匹林(100 mg,每天一次)和氢氯吡格雷(75 mg,每天一次)抗血小板、瑞舒伐他汀(10 mg,每天一次)调脂稳定斑块治疗,完善血检验和危险因素筛查及血管评估。发病7天头CTA及CTP检查(图3A、图4A)提示动静脉瘘可能。由于CT提示梗死区域内有渗血,根据欧洲协作急性卒中研究(European Cooperative Acute Stroke Study,ECASS)出血转化的CT分型标准[3],以及患者神经功能缺损未见加重及无头痛等表现,考虑为脑梗死出血转化HI-1型,治疗上停用阿司匹林,改为氯吡格雷单抗。为进一步排除动静脉瘘可能,于发病第9天行全脑数字减影血管造影术(图5),术中发现左侧大脑中动脉分支明显增多,染色不均匀,成团簇样改变,毛细血管显影,未发现瘤样改变和动静脉瘤或畸形。治疗2周,患者右侧肢体肌力逐渐改善,NIHSS评分降至3分。为查看颅内渗血吸收情况及血管异常情况,于发病15 d复查头颅CTA及CTP(图1C、图3B、图4B)示左侧额颞顶叶脑梗死并少量渗血,较1周前好转,双侧血管对称,左侧大脑中动脉分支血管形态恢复正常,左侧大脑半球由高灌注状态转变为轻度缺血。发病18 d时,患者语言及右侧肢体肌力较入院时改善,神经系统查体:神志清,完全性运动性失语,右侧上下肢肌力5-级,双侧病理征未引出。NIHSS评分3分。改良Rankin量表(modified Rankin Scale,mRS)评分1分,遂予出院。
出院诊断:
脑梗死伴出血转化(HI-1型)
左侧完全前循环(OCSP分型)
大动脉粥样硬化性(TOAST分型)
低灌注
双下肢静脉曲张术后

图4 头颅计算机断层扫描灌注成像

图5 患者DSA成像
2 讨论
静脉充盈早现(early venous filling)是脑梗死患者脑血管造影的一种影像学表现,多发生在颅内大血管急性闭塞后,其发生机制可能是缺血后的血管显著扩张,造影剂快速通过血管导致,提示局部血液循环增加,脑组织过度灌注状态[5-6],曾被称为“奢侈灌注(luxury perfusion)”[6-7]。
随着脑血管造影检查的普及,这方面的研究逐渐增加[8-9],而颅内可逆性血管增多及静脉充盈早现,同时出现奢侈灌注,并有详尽影像学报道者,国内少见。本病例详细描述了这一现象的发生、发展、治疗及转归,通过影像随访,可全面观察到脑梗死后出现的极为罕见的病理生理过程。
在临床中静脉早显常提示梗死后出血转化、脑血管调节受损、不可逆性脑梗死等病理生理可能[7]。对于前循环具有更高的指导意义,敏感度可达94.9%,特异性达81%,但对预测后循环的指导价值有限[7]。静脉早显具体分为丘脑纹状体和脑皮质静脉充盈两类,研究表明前者脑出血的发生率较高[11-13]。但其是否为预测出血转化相对独立的风险因素,及其持续时间的长短对出血转化的发生率有何影响尚不明确[7]。它一旦发现,尤其在脑深穿支血管供血区域,则高度提示出血转化可能,应避免动脉溶栓等治疗,并监控血压[11]。本病例为脑皮质静脉充盈,存在脑梗死出血转化,因渗血量少,为HI-1型[3],故未停用抗血小板药物,且复查渗血有吸收,患者预后良好。
按照TOAST标准[1]探讨本例病因机制,考虑为大动脉粥样硬化性、低灌注亚型。尽管影像学检查并无颅内外大血管的闭塞或程度≥50%狭窄的发现,但患者有下肢静脉手术史,病程中有血压下降、意识丧失、失语等症状体征,且颅脑CT及MRI检查发现有广泛大脑皮质损害。进一步完善的肺动脉、主动脉CTA等检查排除了下肢静脉血栓导致的肺栓塞或胸主动脉夹层等。而脑血管造影发现静脉充盈早现及“奢侈灌注”,更加佐证了早期颅内大血管急性闭塞的存在,遗憾的是患者因病情原因,第一次的颅内血管检查已是发病7 d时,若能更早,如发病1~3 d时行头颅CTA检查,可能会有大血管闭塞或狭窄的直接发现。

图6 iFlow彩色编码血流图[4]
1 Adams HP Jr, Bendixen BH, Kappelle LJ, et al.Classification of subtype of acute ischemic stroke. Definitions for use in a multicenter clinical trial. TOAST. Trial of Org 10 172 in Acute Stroke Treatment[J]. Stroke, 1993, 24:35-41.
2 Kernan WN, Ovbiaqele B, Black DM, et al.Guidelines for the prevention of stroke in patients with stroke and transient ischemic attack:a guideline for healthcare professionals from the American Heart Association/American Stroke Association[J]. Stroke,2014, 45:2160-2236.
3 Fiorelli M, Bastianello S, von Kummer R, et al.Hemorrhagic transformation within 36 hours of a cerebral infarct:relationships with early clinical deterioration and 3-month outcome in the European Cooperative Acute Stroke Study I (ECASS I)cohort[J]. Stroke, 1999, 30:2280-2284.
4 吴一娜, 杨鹏飞, 叶汇, 等. 彩色编码成像技术及其在脑血管疾病中的临床应用[J]. 中国卒中杂志, 2013,8:69-73.
5 Gursoy K, Kankaya Y, Uysal A, et al. Dealing with the venous congestion of free flaps:venous catheterization[J]. J Craniofac Surg, 2008,19:1645-1647.
6 Lassen NA. The luxury-perfusion syndrome and its possible relation to acute metabolic acidosis localised within the brain[J]. Lancet, 1966, 2:1113-1115.
7 Dorn F, Kuntze-Soderqvist A, PoppS, et al. Early venous drainage after successful endovascular recanalization in ischemic stroke - a predictor for final infarct volume?[J]. Neuroradiology, 2012, 54:745-751.
8 Zaidat OO, Yoo AJ, Khatri P, et al. Recommendations on angiographic revascularization grading standards for acute ischemic stroke[J]. Stroke, 2013, 44:2650-2663.
9 Shibata K, Uchiyama S, Takeuchi M, et al. A case of paradoxical cerebral embolism with ‘spectacular shrinking deficit’[J]. Rinsho Shinkeigaku, 1997,37:649-652.
10 Sakamoto M, Taoka T, Iwasaki S, et al. Detection of early venous filling in gliomas on MRI: preliminary study by 2D time-resolved dynamic contrastenhanced MR angiography with echo-sharing technique[J]. Magn Reson Imag, 2001, 19:1193-1201.
11 Ohta H, Nakano S, Yokogami K, et al. Appearance of early venous filling during intra-arterial reperfusion therapy for acute middle cerebral artery occlusion:a predictive sign for hemorrhagic complications[J].Stroke, 2004, 35:893-898.
12 马翊竑, 张海东, 齐军, 等. 动脉溶栓中静脉充盈早现与溶栓并发脑出血的关系[J]. 卒中与神经疾病, 2014,21:225-227.
13 毛森林, 马翊竑, 姚海乾, 等. 急性脑梗死患者动脉溶栓中静脉充盈早现与脑出血发生的关系研究[J]. 疑难病杂志, 2014, 13:900-903.

