高效液相色谱-蒸发光散射器法测定芪芳气血颗粒中黄芪甲苷含量
吴高芬
(湖南省岳阳市食品药品检验所,湖南 岳阳 414000 )
芪芳气血颗粒收载于国家药品标准(试行) [WS -5804 (B-0804)-2002],由黄芪、当归、熟地黄等9 味药材组方,具有益气补血的功效。原标准用薄层扫描测定黄芪甲苷的含量,该方法受展开环境等诸多因素影响,且需显色后扫描,结果不稳定[1],重复性也难以达到要求。为确保产品质量,笔者采用高效液相色谱-蒸发光散射器(HPLC-ELSD)法对产品中黄芪甲苷的含量进行测定,现报道如下。
1 仪器与试药
Waters Alliance 2695 型高效液相色谱仪,包括e2695 溶剂管理系统,2424ELS Detector Empower 工作站(美国Waters 公司);XS-105 型电子天平(上海梅特勒-托利多公司,精密度为0.01mg)。乙腈为色谱纯;水为纯化水;黄芪甲苷对照品(中国食品药品检定研究院,批号为110781-201314,含量为95.8%);芪芳气血颗粒(恒拓集团广西圣康制药有限公司,批号为130201)。
2 方法与结果
2.1 色谱条件
色谱柱:Ultimate XB-C18柱(250 mm×4.6 mm,5 μm);流动相:乙腈-水(34 ∶66)[2];流速:0.9 mL/min;漂移管温度:65 ℃;增益:40;数据率:1 PPS;空气压力:20.0 psi(1 psi=6.895 kPa);柱温:30 ℃。
2.2 溶液制备
精密称取黄芪甲苷对照品12.38 mg,置25 mL 容量瓶中,加甲醇至刻度,制成每1 mL 含0.5 mg 的对照品溶液。精密称取本品15 g(约1 袋),精密加水50 mL 使溶解[3],用水饱和的正丁醇振摇,提取4 次,每次40 mL,合并正丁醇提取液,正丁醇提取液用浓氨试液[4]洗涤2 次,每次40 mL,弃去洗涤液,正丁醇液蒸干,残渣用甲醇溶液并转移至5 mL 容量瓶中,加甲醇至刻度,摇匀,滤过,取续滤液作为供试品溶液。按芪芳气血颗粒处方比例取缺黄芪的方中其他药材制成阴性样品,再按供试品溶液制备方法制成阴性对照品溶液。
2.3 方法学考察
阴性干扰试验:分别取2.2 项下3 种溶液20 μL,按拟订色谱条件进样测定,记录色谱图。结果显示,供试品溶液色谱中,在与对照品溶液色谱相同保留时间处有一致的色谱峰,阴性对照品溶液色谱无此吸收峰,见图1。
线性关系考察:精密吸取对照品溶液5,10,15,20,25 μL,按拟订色谱条件进样测定。以黄芪甲苷进样量的自然对数(X)为横坐标、峰面积的自然对数(Y)为纵坐标进行线性回归,得回归方程Y=1.470 3 X+4.432 5,r=0.999 6( n=5)。结果表明,黄芪甲苷进样量在2.37 ~11.86 μg 范围内与峰面积的线性关系良好。
精密度试验:精密吸取同一对照品溶液10 μL,连续进样6 次,测定峰面积积分值。结果的RSD 为0.57%(n=6),表明仪器精密度良好。
稳定性试验:精密吸取同一供试品溶液(批号为130201),分别于0,3,6,9,12,24 h 时进样测定峰面积。结果的 RSD 为0.83%(n=6),表明供试品溶液在24 h 内稳定。
重复性试验:取芪芳气血颗粒(批号为130201),依法平行制备供试品溶液6 份。精密吸取10 μL 注入高效液相色谱仪,计算黄芪甲苷的含量。结果平均含量为每袋1.41 mg,RSD 为1.32%(n=6),表明方法重复性良好。
加样回收试验:精密称取已知含量的样品(批号为130201,每袋含量为1.41 mg)7.5 g,加入上述对照品溶液1.5 mL,精密加水50 mL 使溶解,依法制备同一质量浓度的供试品溶液6 份,进样测定,计算回收率。结果见表1。
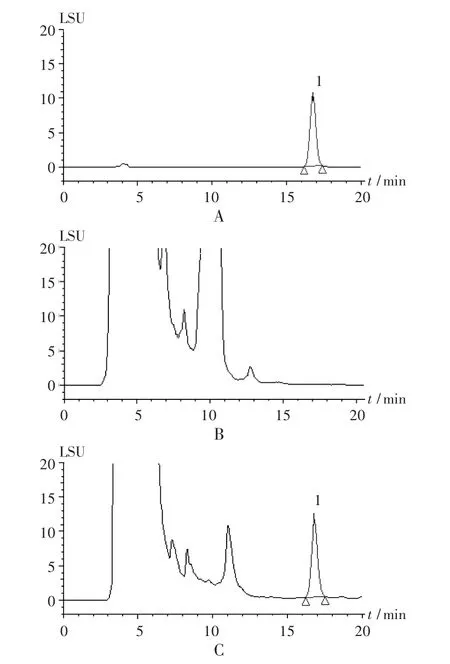
图1 高效液相色谱图
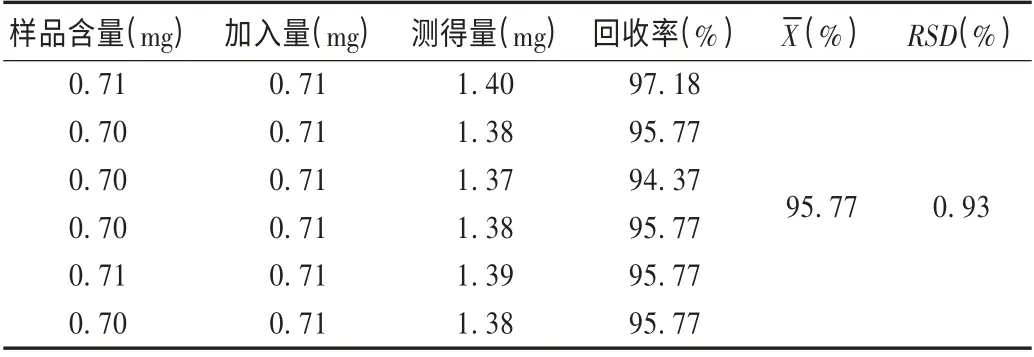
表1 黄芪甲苷加样回收试验结果(n=6)
2.4 样品含量测定
取3 批样品,按拟订色谱条件进样测定含量。结果批号为130201,130301,130401 的样品中黄芪甲苷含量分别为每袋1.41,1.32,1.38 mg。
3 讨论
蒸发光散射器为质量型检测器[5],适用于仅有末端吸收[6]或无紫外吸收的皂苷类化合物的测定,不受官能团的影响,不受流动相溶剂干扰,前处理简单,分离度高,回收率高,是目前测定黄芪甲苷含量较好的方法,故选择HPLC-ELSD 测定芪芳气血颗粒中黄芪甲苷的含量,并优化漂移管温度、气流速、增益、数据率等因素对峰形的影响,有效保证测定方法的灵敏度及准确性。
黄芪甲苷为环菠萝蜜烷型四环三萜类皂苷。皂苷在含水丁醇或戊醇中溶解度较好[7],且样品中的黄芪甲苷已被提取,直接加水溶解,用水饱和的正丁醇提取,且正丁醇提取液一般不含单糖、多糖等杂质,便于分析。
曾采用浓氨试液(每次40 mL,2 次)与氨试液[5](每次40 mL,2 次)及1%氢氧化钠溶液[8](每次20 mL,4 次)洗涤正丁醇提取液,结果同体积的浓氨试液及1%氢氧化钠溶液提取黄芪甲苷的量较氨试液约多1 倍。在碱性环境下,黄芪皂苷Ⅰ和Ⅱ向黄芪甲苷Ⅳ转化[9]。在一定碱性范围内,碱性越强,黄芪皂苷Ⅰ和Ⅱ向黄芪甲苷Ⅳ转化越完全。
[1] 李镜友,陈 军,罗巧红,等. HPLC-蒸发光散射检测法测定益气温阳胶囊中黄芪甲苷的含量[J] . 中医药导报,2009,15(7):86.
[2] 李 毅,王 颖,张廷模. 活血散结合剂中黄芪甲苷的含量的测定[J]. 时珍国医国药,2011,22(3):769.
[3] 丁水平,马宝瑕,张 锐. 黄芪甲苷在黄芪及制剂质控中的应用[J].中国药师,2001,4(5):361
[4] 国家药典委员会. 中华人民共和国药典(一部)[M]. 北京:中国医药科技出版社,2010:790 -791.
[5] 唐德智,莫 迎. 高效液相色谱-蒸发光散射检测法测定小儿健脾开胃合剂中黄芪甲苷的含量[J]. 中国药业,2010,19(6):22.
[6] 匡海学. 中药化学[M]. 北京:中国中医药出版社,2003:240.
[7] 李 飞,周洪雷,杜昊忱,等. 高效液相色谱-蒸发光散射检测法测定心脑补益口服液中黄芪甲苷的含量[J]. 中国药业,2011,20(5):16.
[8] 吴永平,徐永梅,曹 园,等.HPLC-ELSD 法测定黄芪提取物中黄芪甲苷的含量[J]. 中成药,2001,23(9):674.
[9] 汪 祺,张聿梅,戴 忠,等. 黄芪中皂苷类成分的特征薄层图谱鉴别[J] . 中国药事,2011,23(12):1 229.

