刺槐豆多糖纳米硒的制备及表征
高义霞, 周向军, 袁毅君, 鲜鹏杰
(天水师范学院 生命科学与化学学院,甘肃 天水 741001)
硒是人体生命中必需的重要微量元素,具有增强机体免疫能力、抵抗自由基损伤、防病和调节甲状腺机能等多种功能[1-3]。然而硒及其化合物对人体有效和中毒剂量范围非常窄[4],因此需通过有机硒化物或纳米硒的形式来降低其毒性。纳米硒生物吸收性高,能高效清除自由基[5-6],且毒性比无机硒和天然有机硒低,活性比无机硒和天然有机硒高,从而克服了无机硒有效与中毒剂量十分接近而难以预防的缺点[7-9],是一种有效的补硒药物。纳米硒的合成方法有抗坏血酸还原法、表面活性剂法、微乳液法、蛋白质模板法、聚合物模板法、超声化学法、温度控制法和电化学法[10-11]等。抗坏血酸(VC)将亚硒酸(H2SeO3)中的 Se(IV)还原为 Se0后,此时硒不稳定,极易团聚,如聚合体一旦超过纳米尺度,其生物活性大大降低,因此需要对纳米硒粒子表面进行修饰以防止聚集。刺槐豆多糖是刺槐种子胚乳部分焙炒后热水抽提而成,常用于食品增稠剂、持水剂等,主要含有甘露糖和半乳糖[12],但因相对分子质量大、黏度高、溶解度低等限制了其临床应用[13]。研究发现,壳聚糖、阿拉伯胶等多糖可作为模板用于合成纳米硒[14],且单质硒微粒的形成和聚集易受到糖分子的调控[15]。因此在发生氧化还原反应前加入刺槐豆多糖,其便吸附、包裹在初始形成的硒晶体表面,一方面阻止了粒子之间相互结合、团聚,使纳米硒稳定存在于溶液中,另一方面可减缓或控制粒子的生长,使产生的纳米硒形成多种形貌。本研究中以刺槐豆多糖为软模板制备纳米硒,生成的纳米硒具有良好的生物活性和广泛用途,有效地提高了硒的生理功能。
1 实验器材
1.1 材料及试剂
刺槐豆胶(食品级,分子质量为300 ku,黏度3 700 mPa·s,主要含有甘露糖及半乳糖),甘肃弘诺科技贸易有限公司产品。抗坏血酸,Sigma公司产品。Savege液:氯仿与正丁醇以4∶1的体积比混合。亚硒酸等其他试剂均为分析纯。
1.2 仪器
722型可见分光光度计,上海欣茂仪器有限公司制造;UV-2450型紫外光谱仪,日本岛津公司制造;RE-2000B旋转蒸发器,上海亚荣生化仪器厂制造;D2F-6021型真空干燥箱,上海精宏实验设备有限公司制造;TGL-20M高速台式冷冻离心机,湘仪离心机仪器有限公司制造;JSM-6701F冷场发射型扫描电镜,日本电子光学中心制造。
2 实验方法
2.1 刺槐豆多糖的制备
参照高义霞方法[16]进行。
2.2 纳米硒的制备
取一定量的亚硒酸、刺槐豆多糖溶液置于25 mL的比色管中,混合均匀后静置片刻,加入一定量抗坏血酸溶液,加水稀释至刻度,振摇混合均匀,将反应混合液置于不同温度水浴中或超声波环境中一定时间,使H2SeO3中Se4+还原为Se0,并在刺槐豆多糖模板上生长至一定的形貌[17]。
2.3 表征手段
利用紫外光谱法表征刺槐豆多糖为软模板的纳米硒溶液的粒度变化;扫描电镜(SEM)和X射线衍射(XRD)分别测定最佳制备纳米硒工艺条件下反应产物的形貌、粒度大小及形态。
3 结果与分析
3.1 紫外光谱
图1是不同溶液的全扫描吸收光谱,作为制备纳米硒的反应背景,可知VC最大吸收峰在265 nm处,刺槐豆多糖在此处无吸收峰。单纯刺槐豆多糖、VC或两者的混合液在大于400 nm的可见光区均无吸收,说明在该条件下无红色纳米硒生成。以刺槐豆多糖为介质的总反应体系中,在400~600 nm处有较强的吸收,峰值较宽,说明该条件下生成了大量的红色纳米硒,但溶液中含有未消耗的反应物及中间产物,此结果与SEM表征结果 (见图2)一致。
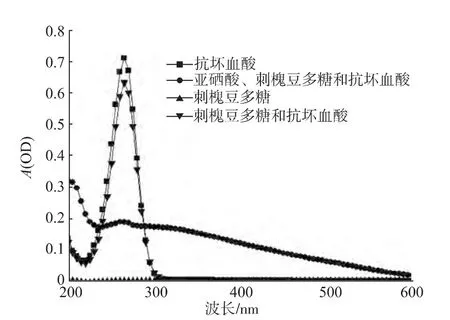
图1 不同溶液的吸收光谱Fig.1 Absorption spectra of different solutions

图2 H2SeO3、刺槐豆多糖和VC混合物的SEM分析Fig.2 SEM analysis mixture of H2SeO3,locust bean polysaccharides and VC
据测定胶体溶液的双波长法[18],胶体粒径参数

式(1)中, A1、 A2分别为波长 λ1、 λ2处的吸光值。
固定波长λ1、λ2,当吸光值比值A2/A1不变时胶体粒径不变,生成的纳米硒粒径均匀,处于稳定状态。为避开VC的吸收且使测定方便,试验选择410nm和490 nm作为纳米硒测定波长,并以A410/A490作为表征纳米硒粒度随时间变化的依据[19]。
3.2 反应物浓度对纳米硒的影响
固定 H2SeO3浓度为 0.1 mmol/L,VC浓度为0.1 mmol/L,改变刺槐豆多糖质量分数,40℃反应4 h,考察其对纳米硒的影响,结果见图3(a)。随刺槐豆多糖质量分数的增加,吸光值呈明显增大趋势,当刺槐豆多糖质量分数为0.1‰时,吸光值基本保持不变,但A410/A490开始降低;当刺槐豆多糖质量分数为0.2‰时,A410/A490维持在1.7左右,说明此时纳米硒颗粒稳定,故刺槐豆多糖质量分数选择0.2‰。固定H2SeO3浓度为0.01 mmol/L,刺槐豆多糖质量分数为0.2‰,改变VC浓度,40℃反应4 h,考察其对纳米硒形成的影响,结果见图3(b)。随着VC浓度的增加,吸光值逐渐增大,当VC浓度为0.05 mmol/L时,吸光值最大且趋于平稳,但此时A410/A490为1.68,且持续增加;当VC浓度为0.1 mmol/L,A410/A490稳定在1.77,说明此时纳米硒粒度均匀稳定,因此选择 VC 浓度为 0.05~0.1 mmol/L。 理论上按 n(VC)/n(H2SeO3)=2∶1 计量关系发生氧化还原反应,但稍过量的VC能提供还原性介质,使晶核生长速度加快,同时起稳定纳米硒的作用[20-21]。 n(VC)/n(H2SeO3)=5∶1~10∶1 为宜,本试验则选择 5∶1。
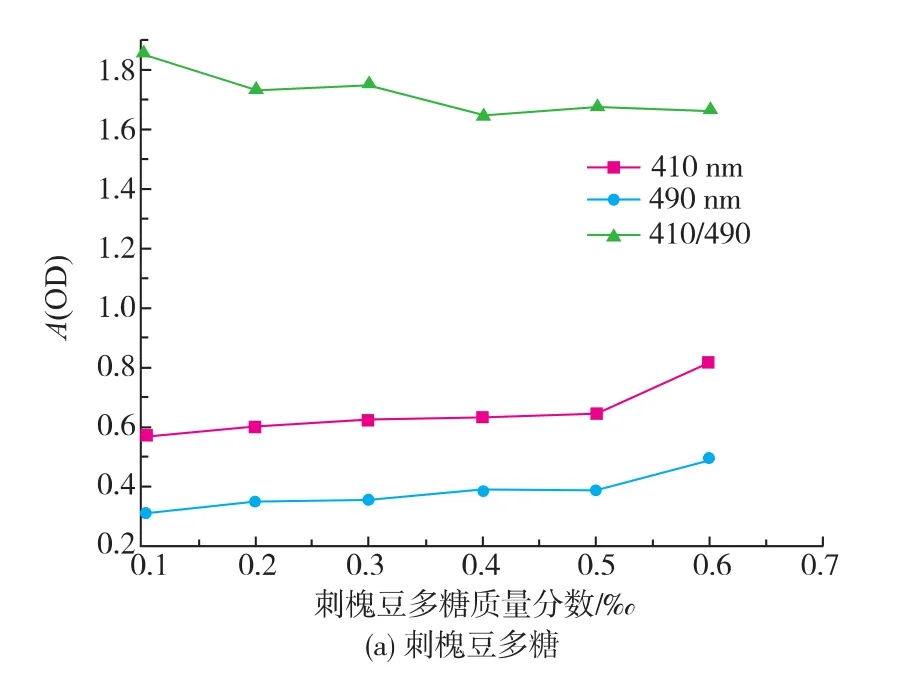

图3 刺槐豆多糖质量分数及VC浓度对纳米硒的影响Fig.3 Effects of locust bean polysaccharides and VC concentration on nano-selenium
3.3 不同温度下反应时间对纳米硒的影响
固定H2SeO3浓度为0.01 mmol/L,刺槐豆多糖质量分数为0.2‰,VC浓度为0.05 mmol/L,考察20、40、60℃和80℃下不同时间对纳米硒的影响,结果见图4。 由图 4(a)和(b)可知,随反应时间的延长,两者反应物吸光值不断增加,2 h后均趋于稳定,A410/A490分别维持在1.76和1.8左右,说明此时纳米硒稳定;和20℃相比,40℃生成物吸光值更高,说明该条件下反应较为迅速充分。由图4(c)可知,60℃条件下,反应混合物吸光值随时间的增加而明显增大,5 h后吸光值增加程度减缓,但反应4 h后,A410/A490下降明显,说明此时纳米硒稳定程度开始降低。由图4(d)可知,80℃条件下,吸光值随时间的延长呈急剧增加趋势,4 h后逐步趋于平稳,但A410/A490一直明显降低,说明该条件下形成的纳米硒有增大、团聚趋势[22],不适合本试验。试验中发现,在较高温度下,随着时间的延长,溶液颜色加深,说明纳米硒颗粒随温度升高有定向生长趋势,形成了其它形貌[23-24]。综合考虑40℃和60℃吸光值及A410/A490,从节省能源等因素综合考虑,选择40℃反应4 h作为纳米硒制备条件。


图4 不同温度下反应时间对纳米硒的影响Fig.4 Effects of reaction time on nano-selenium under different temperature
3.4 扫描电镜表征
在上述筛选出的条件,即刺槐豆多糖质量分数为 0.2‰,n(VC)/n(H2SeO3)为 5∶1,40 ℃反应 4 h,制备的反应产物经离心后在室温条件下放置一个月仍为红色,溶液中无沉淀,进行SEM分析,结果见图5,可知此条件下制备的纳米硒为球状分子,粒径约在95~100 nm,颗粒粒度大小均一、分散均匀。
3.5 X射线衍射分析
以质量分数0.2‰刺槐豆多糖为分散体系,VC和 H2SeO2(两者摩尔比 5∶1)40 ℃水浴反应 4 h,制得纳米硒刺槐豆多糖分散乳液,冷冻离心、旋转蒸发得纳米硒溶液,-20℃冷冻干燥至恒质量,取固体粉末进行X射线衍射分析,并与刺槐豆多糖衍射图比较。

图5 最佳条件下反应产物的SEM分析Fig.5 SEM analysis of Reaction product under the optimal conditions
图6为1和2两个样品在2°≤2θ≤85°范围内的XRD分析图。
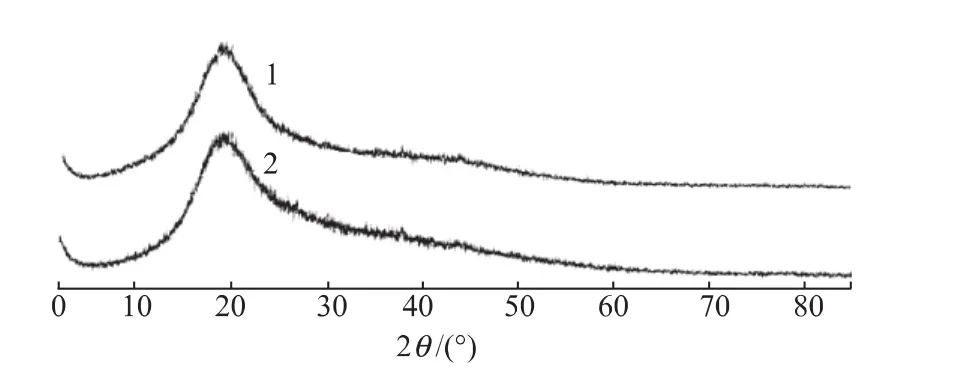
图6 反应产物和刺槐豆多糖的XRD分析Fig.6 XRD analysis of Reaction product and Locust bean polysaccharides
结果表明:样品2有X衍射峰,说明刺槐豆多糖是杂多糖,如糖蛋白质,因为均多糖不能形成晶体,为无定型粉末;由图与样品1的衍射峰对比可知,两种物质峰形及位置相同,说明样品1中没有结晶态物质,即以刺槐豆多糖为模板生成的纳米硒非晶态亦为无定型粉末。
4 结语
通过控制实验条件,以刺槐豆多糖为模板,用抗坏血酸还原亚硒酸的方法制备纳米硒。当抗坏血酸和亚硒酸摩尔比为5∶1,刺槐豆多糖质量分数为0.2‰,40℃反应4 h后可得红色均匀的纳米硒颗粒,其粒度大多在95~100 nm,分散相对均匀,X衍射显示其为非晶态无定型粉末。纳米硒具有硒和刺槐豆多糖的双重功效,有望在营养和疾病防治方面获得进一步应用。
[1]罗海吉,吉雁鸿.硒的生物学作用及其意义[J].微量元素与健康研究,2000,17(2):70-72.LUO Haiji,JI Yanhong.Biological function and its significance of selenium[J].Studies of Trace Elements and Health,2000,17(2):70-72.(in Chinese)
[2]Rayman M P.The importance of selenium to human health[J].Lancet,2000,356(9225):233-241.
[3]李曦,刘义,吴军,等.微量热法研究硒对砷在大肠杆菌生长中的联合作用[J].高等学校化学学报,2003,24(1):91-94.LI Xi,LIU Yi,WU Jun,et al.Microcalorimetric study of the associated action of selenium to arsenic on the growth of Escherichia coli[J].Chemical Journal of Chinese Universities,2003,24(1):91-94.(in Chinese)
[4]门晓媛,王一飞,郑文杰,等.纳米硒化裙带菜多糖的制备及其体外抗CVB3病毒作用研究[J].中国卫生检验杂志,2005,15(10):1153-1155.MEN Xiaoyuan,WANG Yifei,ZHENG Wenjie,et al.The synthesis of selenium nanoparticles with polysaccharides from undaria pinnatifida(charv) suringer and its antivirus effects on CVB3 in vitro[J].Chinese Journal of Health Laboratory Technology,2005,15(10):1153-1155.(in Chinese)
[5]Gao X Y,Zhang J S,Zhang L D.Hollow sphere selenium nanoparticles:their in-vitro anti hydroxyl radial effect[J].Advanced Materials,2002,14(4):29-293.
[6]Huang B,Zhang J S,Hou J W,et al.Free radical scavenging efficiency of nano-se in vitro[J].Free Radical Biology Medicine,2003,35(7):805-813.
[7]Zhang J S,Gao X Y,Zhang L D,et al.Biological effects of a nano red elemental selenium[J].Bio-Factors,2001,15(l):27-38.
[8]Zhang J S,Wang H L,Bao Y P,et al.Nano red elemental selenium has no size effect in the induction of seleno-enzymes in both cultured cells and mice[J].Life Sciences,2004,75(2):237-244.
[9]韩晶,郭雄,吴翠艳,等.硫酸软骨素纳米硒可抑制T-2毒素诱导的大骨节病软骨细胞凋亡[J].南方医科大学学报,2013,33(2):225-229.HAN Jing,GUO Xiong,WU Cui-yan,et al.Nano-Se-Chondroitin sulfate inhibits T-2 toxin-induced apoptosis of cultured chondrocytes from patients with Kashin-Beck disease[J].Journal of Southern Medical University,2013,33(2):225-229.(in Chinese)
[10]Byron G,Brian M,Andrew G,et al.A sonochemical approach to the synthesis of crystalline selenium nanowires in solutions and on solid-supports[J].Advanced Materials,2000,14(23):1749-1752.
[11]Byron G,Brian M,Bryan C,et al.Synthesis and characterization of uniform nanowires of trigonal selenium [J].Advanced Functional Materials,2002,12(3):219-227.
[12]高义霞,周向军,王风霞,等.刺槐豆多糖硒酸酯的制备及表征[J].食品工业科技,2012,33(14):288-290.GAO Yixia,ZHOU Xiangjun,WANG Fengxia,et al.Preparation and characterization of selenium-polysaccharides of locust bean[J].Science and Technology of Food Industry,2012,33(14):288-290.(in Chinese)
[13]孟春,郭养浩,石贤爱,等.海藻多糖生物活性及分子修饰[J].中国生物工程杂志,2004,24(3):35-39.MENG Chun,GUO Yanghao,SHI Xianai,et al.The physiological effect and molecular modification of algae polysaccharides[J].China Biotechnology,2004,24(3):35-39.(in Chinese)
[14]Lin Z H,Chris W C R.Evidence on the size-dependent adsorption spectral evolution of selenium nanoparticles[J].Materials Chemistry and Physics,2005,92(2):591-594.
[15]郑文杰,黄亮,杨芳,等.降解裙带菜多糖对纳米硒的形成与稳定作用[J].高等学校化学学报,2007,28(2):208-211.ZHENG Wenjie,HUANG Liang,YANG Fang,et al.Formation and stabilization of selenium nano-particles in aqueous solution of undaria pinnatifida charv.suringer polysaccharide[J].Chemical Journal of Chinese Universities,2007,28 (2):208-211.(in Chinese)
[16]高义霞,周向军,张继,等.罗望子多糖模板法制备纳米硒[J].林产化学与工业,2011,31(3):5-10.GAO Yixia,ZHOU Xiangjun,ZHANG Ji,et al.Preparation of nano-selenium using tamarind polysaccharides as template[J].Chemistry and Industry of Forest Products,2011,31(3):5-10.(in Chinese)
[17]王红艳,张胜义,刘明珠,等.壳聚糖模板法制备纳米硒[J].应用化学,2004,21(8):788-792.WANG Hongyan,ZHANG Shengyi,LIU Mingzhu,et al.Synthesis of selenium nanoparticles in the presence of chitosan template[J].Chinese Journal of Applied Chemistry,2004,21(8):788-792.(in Chinese)
[18]Gao H W.Molecular dynamics simulations and the rheology of fluids[G].Proceedings of 4th Asian Chemical Congress.Beijing:Chinese Chemical Society,1991:372.
[19]王红艳,张胜义,郝洪文,等.羧甲基纤维素钠模板法制备纳米硒[J].功能材料,2004,35(2):259-261.WANG Hongyan,ZHANG Shengyi,HAO Hongwen,et al.Synthesis of selenium nanoparticles by sodium carboxymethyl cellulose template[J].Journal of Functional Materials,2004,35(2):259-261.(in Chinese)
[20]温金凤,金花,崔胜云.壳聚糖为负载的纳米硒的制备[J].延安大学学报:自然科学版,2007,33(1):37-40.WEN Jinfeng,JIN Hua,CUI Shengyun.Preparation and characterization of nanoselenium loaded on the chitosan[J].Journal of Yanbian University:Natural Science Edition,2007,33(1):37-40.(in Chinese)
[21]李志林,滑鹏敏.十二烷基硫酸钠模板法制备纳米硒[J].无机盐工业,2009,41(7):32-34.LI Zhilin,HUA Pengmin.Preparation of nanosized selenium by sodium dodecyl sulfate template method [J].Inorganic Chemicals Industry,2009,41(7):32-34.(in Chinese)
[22]王红艳,张莉,张胜义,等.纳米硒的制备及表征[J].淮北煤炭师范学院学报,2004,25(3):36-39.WANG Hongyan,ZHANG Li,ZHANG Shengyi,et al.Synthesis and characterization of selenium nanoparticles[J].Journal of Huaibei Coal Industry Teachers College,2004,25(3):36-39.(in Chinese)
[23]史宏伟.纳米硒和硒化镉制备方法研究[D].合肥:安徽大学,2005.
[24]滑鹏敏.纳米硒的制备与应用[D].石家庄:河北大学,2009.

