应用CLSI C28-A3文件建立妊娠期甲状腺功能相关指标的参考区间*
苏汉文,李栋,顾剑,李艳,范翠芳(武汉大学人民医院:.检验科;.妇产科,武汉 430060)
2011美国甲状腺学会在《Thyroid》上发表《妊娠和产后甲状腺疾病的诊治指南》[1],对妊娠期甲状腺功能亢进症的诊治进行了详细的指导。2012年5月中华医学会内分泌学分会和围产医学分会联合编撰中国《妊娠和产后甲状腺疾病的诊治指南》,指南均强力推荐“建立本单位或本地区妊娠早、中、晚期特异的血清甲状腺功能指标参考值”,作为妊娠甲状腺功能诊断的指导。本研究参照美国临床实验室标准化委员会文件《临床实验室如何确定、建立和验证参考区间;批准指南-第3版》(CLSI C28-A3)的要求,建立本实验室妊娠期血清甲状腺激素参考区间,为临床医生评价妊娠期孕妇甲状腺功能状况提供依据。
1 材料与方法
1.1 材料来源血清标本来自2012年4月至2013年5月在武汉大学人民医院妇产科进行孕检的妇女共445例,平均年龄(25.5±4.58)岁。孕早期为1~12周、孕中期为13~27周、孕晚期为28~40周。依据美国临床生化研究院(NACB)的标准[2],妊娠期参考值来自下述人群:(1)妊娠妇女标本至少120例;(2)排除抗甲状腺过氧化物酶抗体(TPOAb)阳性者;(3)排除有甲状腺疾病个人和家族史者;(4)排除可见或可触及的甲状腺肿者;(5)排除服用药物者(雌激素类除外)。
1.2 标本采集用BD 含血清分离胶采取静脉血3mL,3000 r/min 离心5min。4h内完成测量。当天不能完成测量者分离血清,-20℃冻存,30d内检测。
1.3 标本检测血清游离三碘甲状腺原氨酸(FT3)、血清游离甲状腺激素(FT4)、促甲状腺激素(TSH)、TPOAb检测使用Siemens Advia Centaur XP化学发光免疫分析仪及其配套试剂和校准品。FT3、FT4、TSH 使用BIO-RAD 免疫复合质控品;TPOAb采用Siemens试剂配套质控品,在保证检测系统正常的情况下每个样品检测1次。TPOAb采用Siemens试剂说明书提供的参考区间(1~60IU/mL),大于60IU/mL 视为阳性。
1.4 统计学处理使用SPSS17.0软件进行数据存储、统计分析和正态性检验。
2 结果
2.1 离群值的处理对所有实验数据观察发现,存在5个疑似离群点,按照CLSI C28-A3文件要求,将其与邻近点的差值(D)与数据全距(R)相除,D/R值分别为0.389,0.342,0.337,0.351,0.301。前4个数据D/R值大于1/3,予以剔除,后一个数据D/R值小于1/3,故不认为该点为离群点,保留其测定数据。最后441个数据纳入统计,其中孕早期130例,孕中期165例,孕晚期146例,均符合CLSI C28-A3文件要求最低120例的标准。
2.2 妊娠早、中、晚期血清FT4、FT3、TSH 水平分布做441名孕妇妊娠早、中、晚期血清FT4、FT3、TSH 检测结果频数分布图,进行正态性分析,结果FT3为正态分布,FT4接近正态分布,TSH 为偏态分布。见图1、2、3。
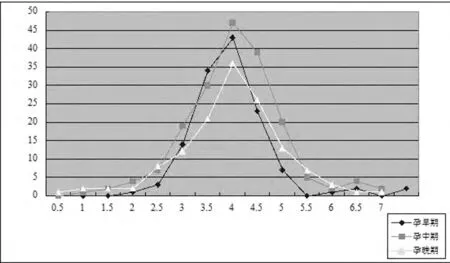
图1 孕早、中、晚期血清FT3水平频数分布图
2.3 妊娠期FT3、FT4、TSH 孕期参考值的确定妊娠各期血清FT4和TSH 水平不符合正态分布,可采用百分位法表示,参考值选择95%的可信区间,采用2.5th为下限、97.5th为上限,统计孕早、中、晚期血清FT4、FT3、TSH 参考区间。建立孕早期FT3、FT4、TSH 参考区间分别为3.25~5.78、11.80~21.20pmol/L、0.03~4.52mIU/L;孕中期FT3、FT4、TSH 参考区间分别为3.05~5.10、10.60~17.70pmol/L、0.05~4.50mIU/L;孕晚期FT3、FT4、TSH 参考区间分别为3.14~5.12、9.30~16.70pmol/L、0.47~4.55 mIU/L。孕早、中、晚期孕妇血清FT4和TSH 水平差异较大,其参考区间不能互相替代。

图2 孕早、中、晚期血清FT4水平频数分布图

图3 孕早、中、晚期血清TSH 水平频数分布图
2.4 妊娠各期血清FT3、FT4、TSH 参考区间的验证按CLSI C28-A3文件要求,选取妊娠各期正常孕妇各20例,用相同检测系统分别检测血清FT3、FT4、TSH 水平,与本研究建立的参考区间进行比较,结果均在本参考区间范围内。
3 讨论
妊娠与甲状腺疾病的研究是内分泌学和围产医学研究的热点。临床研究证实,妊娠期孕妇甲状腺激素水平的高低对胎儿大脑及全身发育有至关重要的影响[3-5]。对妊娠期甲状腺功能异常的孕妇进行早期治疗,可以减少甚至避免对胎儿脑发育的损伤[6]。本研究结果表明,随着孕周的增加,FT4水平呈现下降趋势;且TSH 水平比非妊娠妇女的TSH 水平低,一方面可能与妊娠期母体在雌激素刺激下肝脏合成甲状腺素结合球蛋白(TBG)增加,清除减少,影响血清中FT4水平有关;另一方面人绒毛膜促性腺激素(hCG)α亚基与TSH 结构同源,高水平的hCG 能结合并激活TSH 受体,引起妊娠期一过性高甲状腺素血症,增多的甲状腺激素负反馈抑制TSH 分泌使血清TSH 水平降低[7]。可见妊娠期妇女甲状腺激素具有独特的生理变化,普通成人标准已不适合妊娠期妇女,同时甲状腺疾病诊治对实验室检测结果的依赖性较强,妊娠期甲状腺功能相关项目参考区间的确定至关重要[8]。因此各实验室应该根据自己所在地区,所用实验仪器和方法,建立不同孕期的参考区间,以降低对妊娠妇女甲状腺功能异常的漏诊和误诊率,从而为临床诊治提供可靠依据。
本研究参照CLSI C28-A3文件指南,建立本实验室妊娠甲状腺功能相关指标的参考区间。孕早期FT3、FT4、TSH 参考区间分别为3.25~5.78、11.80~21.20pmol/L、0.03~4.52 mIU/L;孕中期FT3、FT4、TSH 参考区间分别为3.05~5.10、10.60~17.70pmol/L、0.05~4.50mIU/L;孕晚期FT3、FT4、TSH 参考区间分别为3.14~5.12、9.30~16.70pmol/L、0.47~4.55mIU/L。并对参考区间进行了验证,为本参考区间的临床应用奠定了理论基础。但本研究的局限性为单中心,参考个体涵盖面不够广泛。根据CLSI C28-A3文件的要求,若能进行多中心研究,则能获取更客观的参考值数据,降低了地区性差异的影响,这样得到的参考区间更加客观有效,对临床医生的指导意义更大。因此,后续研究中可考虑采用多中心联合研究,尽可能使统计结果反映更广泛群体的真实状态。
[1]Stagnaro-Green A,Abalovich M,Alexander E,et al.Guidelines of the American thyroid association for the diagnosis and management of thyroid disease during pregnancy and postpartum[J].Thyroid,2011,21(10):1081-1089.
[2]Stricker R,Echenard M,Eberhart R,et al.Evaluation of maternal thyroid function during pregnancy:the importance of using gestational age-specific reference intervals[J].Eur J Endocrinol,2007,157(4):509-514.
[3]陈桂山,杨有业,温冬梅,等.临床生化检验项目生物参考区间适用性验证探讨[J].中华检验医学杂志,2008,31(2):170-174.
[4]杨有业,张秀明.临床检验方法学评价[M].北京:人民卫生出版社,2008.
[5]Lazarus JH.Thyroid function in pregnancy[J].Br Med Bull,2011,97(2):137-148.
[6]康燕.孕妇甲状腺疾病对胎儿及新生儿的影响[J].实用儿科临床杂志,2011,26(2):80-82.
[7]于晓会,王薇薇,藤卫平,等.左旋甲状腺素治疗妊娠期亚临床甲减妇女对后代神经智力发育影响的前瞻性研究[J].中华内分泌代谢杂志,2010,26(11):921-925.
[8]范建霞,宋梦帆.妊娠期甲状腺功能特异性参考值的意义[J].中华围产医学杂志,2012,15(2):69-72.

