高级别胶质瘤术后放疗55例疗效及预后因素分析
黎 珊,洪金省,陈 君,张海荣,张纬建
(福建医科大学附属第一医院放疗科,福建 福州 350009;∗九江市肿瘤医院,江西 九江;#福建医科大学公共卫生学院,福建 福州)
神经胶质瘤简称胶质瘤,是最常见的颅脑恶性肿瘤之一。2012年中国肿瘤登记报告指出中国脑及中枢神经系统恶性肿瘤死亡率为3.87/10 万,位列十大高病死率肿瘤之第9 位[1]。欧洲肿瘤内科学会(European Society for Medical Oncology,ESMO)最新数据显示恶性胶质瘤每年发病率达3~5/10 万,发病率随着年龄的增长而增加,在50~60 岁间达到高峰[2]。其中高级别胶质瘤(HGG)占原发性脑肿瘤的35%~45%[3],占所有胶质瘤的77.5%[4]。HGG 恶性程度高,浸润性强,手术完整切除率低,多数情况下难完全切除,且单纯手术后几乎毫无例外地出现复发。术后放疗不但可以延长局部肿瘤复发间隔时间,而且术后放疗者具有明显的生存优势。因此,术后放疗是高级别胶质瘤的标准治疗手段。本研究回顾性分析了55 例高级别胶质瘤患者,旨在探讨影响胶质瘤术后放射治疗的疗效的预后因素。
1 临床资料
1.1 一般资料 选取福建医科大学附属第一医院肿瘤放射治疗科2009年10月至2013年7月间收治的高级别胶质瘤患者,接受手术及术后精确放疗的患者55 例,55 例患者有相关所需的完整资料。男性30 例,女性22 例。年龄<20 岁者18 例,≥40 岁者9例,≥20 且<40 岁者28 例,其中位年龄47 岁。根据2007年WHO 分级,Ⅲ级35 例,Ⅳ级20 例。术前有癫痫者18 例,无癫痫发作者37 例。
1.2 治疗方法
1.2.1 手术治疗 55 例均接受手术治疗。
1.2.2 放射治疗 所有患者均为术后首次接受放射治疗者。55 例患者均接受术后调强放射治疗(intensity modulated radiotherapy therapy,IMRT),其中38 例行术后同步放化疗,17 例在术后放疗过程中未配合替莫唑胺口服化疗。放疗采用6MVX 射线照射,仰卧位热塑面罩固定,术后残留病灶为GTV,术前病灶外扩2~3 cm 形成CTV,由GTV、CTV 外放0.3 cm 形成相应PTV。处方剂量:PTV-G 为60~70Gy,分割剂量1.8~2.4 Gy/次,5 次/周;PTV-C 为50~60 Gy,分割剂量1.7Gy~2.0Gy,5 次/周。
1.2.3 化学治疗 55 例患者均以放化疗联合治疗的方式,其中38 例患者中采用TMZ 75 mg(/m2·d)行同步放化疗,未行同步放化疗17 例。
1.3 随访 通过寄信、打电话和查阅病历相结合的方式进行随访,随访起止时间为2009年12月1日至2013年10月1日,随访时间1~48 个月,中位生存时间36 个月。
1.4 统计学处理 应用SPSS20.0 软件进行统计学分析。单因素分析采用Kaplan-Meier 法检验。多因素分析采用Cox 比例风险模型,以存活时间为非独立变量,选用逐步回归分析进行预后相关因素判断。
2 结果
2.1 随访及生存情况 55 例胶质瘤患者均获得随访,其中23 例死亡。55 例患者中1、2、3年生存率分别是49.0%,23.6%,7.3%,中位生存期为11 个月。
2.2 单因素分析 如图1所示,采用Kaplan-Meier 法对55 例患者总生存率进行单因素分析,其中病理分级(P=0.002)、年龄(P=0.001)是影响HGG 术后放疗生存率的重要因素,而性别(P=0.870)、是否行同步放化疗(P=0.999)、癫痫状态(P=0.243)对预后的影响不明显。55 例高分级脑胶质瘤患者不同因素生存分析如图。

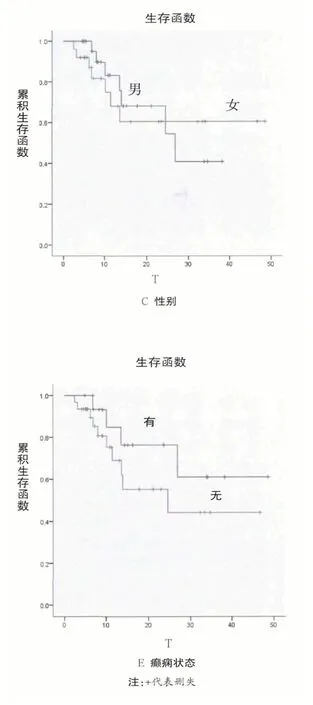
2.3 多因素分析 使用Cox 比例风险模型,采用回归分析结果显示:病理分级(P=0.019)、年龄(P=0.033)是影响患者的独立预后因素。
3 讨论

高级别胶质瘤(HGG)是脑原发性肿瘤中发病率最高、最难治疗的一类肿瘤。手术切除是治疗脑肿瘤的主要手段,术后配合放疗已作为常规治疗。星形胶质细胞瘤根据WHO 可分为星形细胞瘤(低度恶性)、恶性星形细胞瘤(间变性星形细胞瘤、Ⅲ级)、胶质细细胞瘤(Ⅳ级)。其中Ⅲ级星形细胞瘤平均生存期3.5年,Ⅳ级胶质母细胞瘤平均生存期15 个月,2年生存期仅27%[5]。结果中得出了一致的结论,单因素分析及多因素分析均提示Ⅳ级胶质瘤是影响预后的不良因素之一。
在年龄分组中,与年龄≥40 岁患者相比较,年龄<40 岁胶质瘤患者死亡风险明显降低,而<20 岁者获得更长的生存期,肿瘤复发的发生率降低。Smith等[6]的回顾性研究提示年龄较大的胶质瘤患者,即使病理分期为低级别,其恶性程度仍高于年轻患者。其原因可能是年轻胶质瘤患者耐受性较好,能较顺利的完成手术、放化疗疗程,接受规范化治疗的机会大,治疗后恢复较快,故这部分患者有较好的预后。
本组中,术前有癫痫发作的有19 例,无术前癫痫状态37 例,在单因素分及多析中可得知术前是否有癫痫状态对患者放疗预后无影响。部分学者曾[7]提出癫痫症状发作时间较早,有利于早期发现肿瘤,进而行手术切除,获得相好的预后。目前有关癫痫发作对恶性胶质瘤术后放疗预后的影响报道较少,未有有效的数据证明。
该分析中高级别胶质瘤术后行同步放化疗者共38 例,18 例在放疗期间未配合同步化疗,两组的对放疗无影响。Jeon 等[8]报道显示:高级别胶质瘤术后行同步放化疗及6 周期替莫唑胺化疗,取得了较好疗效,副作用轻,患者耐受性好。
综上所述,年龄、肿瘤分级为高级别胶质瘤的独立预后因素,如果进一步提高高级别胶质瘤的疗效,延缓胶质瘤复发时间及延长生存期,有待进一步大样本前瞻性研究的开展。
[1]Lecek TA,Propp JM,Stroup NE,et a1.Cbtrusstatistical report:Primary brain and central nervous system tumors diagnosed in the united statesin 2005-2009[J].Neuro Oncol,2012,14(5):1-49.
[2]Stupp R,Brada M,van den Bent MJ,et al.High-grade glioma:ESMO Clinical Practice Guidelines for diagnosis,treatment and follow-up[J].Ann Oncol,2014,29.
[3]殷蔚伯,余子豪,徐国镇,等.肿瘤放射治疗学[M].第4 版,北京:中国协和医科大学出版社,2008:1126-1127
[4]Central Brain Tumor Registy of the United States(CBTRUS).CBTRUSstatistical report:pimary brain and central nervous system tumors diagnosed in the United States in 2004-2006[J].Hinsdale:CBTRUS,2010.
[5]Ohgaki H,Kleihues P.Populmion-based studies on incidence,survival rates,and genetic alterations in astrocytieand oligodendroglial gliomas[J].JNeuropathol Exp Neurol,2005,64:479-489.
[6]Smith JS,Chang EF,Lamborn KR,et al.Role of extent of resection in the long-term outcome of low-grade hemispheric gliomas[J].J clin Oncol,2008,26:1338-1345.
[7]杨李轩,张弩,夏之柏.影响恶性胶质瘤生存预后的临床因素分析[J].中华神经医学杂志,2012,11(8):784-787.
[8]Jeon HJ,Kong DS,Park KB,et.al.Clinical outcome of concomitant chemoradiotherapy followed by adjuvant temozolomide therapy for glioblastaomas:single-center experience[J].Clin Neurol Neurosurg,2009,111(8):679-682.

