HPLC-MS-MS法测定降糖类中成药中非法添加物格列波脲
申国华,董培智,裴社强,郭景文,行江水(山西省食品药品检验所,山西太原 030001)
近年来,一些不法厂商在利益的驱动下,为了增强降糖效果,在降糖类中成药中非法添加各种降糖类化学药物[1]。因此,严厉打击中成药中非法添加化学药品的不法行为,建立快速准确检测方法尤为重要。但造假者的手段越来越隐蔽,甚至添加国内未上市的化学药物如格列波脲。格列波脲为磺脲类降糖药,它与甲苯磺丁脲、格列吡嗪、格列齐特、格列本脲、格列美脲、格列喹酮等又称为“磺脲类促胰岛素分泌剂”,它们有共同的降糖作用机理,即与胰腺β细胞膜上的磺酰脲受体结合,从而启动胰岛素的分泌来达到降糖的目的,它们的降糖优点各异,但毒副作用都差不多,仅仅是程度的不同而已;另一方面在结构上它们都以苯磺酰脲为主要官能团,其中格列波脲与其他几个格列类药物的区别在于它们各自所包含的基团不同,甲苯磺丁脲包含的是比较简单的丁胺,格列齐特包含的是环戊烷并吡咯烷的基团,格列吡嗪所包含的是甲基吡嗪酰胺和环己烷的两个基团,格列本脲所包含的是环己烷和2-甲氧基-5-氯本甲酰胺的两个基团,格列美脲包含的是对甲基环己烷和吡咯烷酮两个基团,格列喹酮包含的是环己烷和一个含异喹啉酮的基团,而格列波脲所包含主要是一个带四个手性分子桥环化合物,而其他几个药物很少含有手性结构。另一类降糖药是含苄基噻唑烷二酮类药品,主要代表为马来酸罗格列酮,盐酸吡格列酮等。
虽然本品未在国内批准上市,但在实际工作中已发现开始有不法分子添加此化学药品,但国家现行的降糖类非法添加化学药品标准规定的检验方法和检验项目不能检出此药品,而且国内外未见有关此药品的检测方法的报道[2-22]。因此,本实验建立了用于降糖类中成药中格列波脲初筛、定量和确证的方法。
1 仪器与试药
戴安U3000高效液相色谱仪,AL204-IC电子天平,Thermo LTQ-XL液质联用仪、ESI离子源;Agilent Eclipse Plus C18色谱柱 (4.6 mm×250 mm,5 μm);Dikma Spursil C18(150 mm × 2.1 mm,3 μm)柱;甲醇为色谱纯 (Dikma公司),水为纯化水,其余试剂均为分析纯;格列波脲 (Glibornuride),批号1113-082B1,纯度86.5%,购自加拿大TLCpharmachem公司;所用供试品为举报样品以及市场上随机购买样品。
2 检测条件
2.1 液质联用色谱条件 Dikma Spursil C18色谱柱(150 mm×2.1 mm,3 μm)柱;流动相为甲醇(A)-0.01 mol/L乙酸铵溶液 (B),梯度洗脱(0~10 min,5% ~95%A;10~11 min,95% ~5%A;11~20 min,5%A);柱温30℃;体积流量0.2 mL/min;进样体积10 μL。
2.2 质谱条件 质谱配有电喷雾离子源 (ESI),质谱检测参数:ESI+扫描,干燥气温度320℃,鞘气体积流量8L/min,辅助气体积流量3.3 L/min,喷雾电压4.5 kV,碰撞能量35 cid。扫描方式:一级质谱全扫描、二级质谱全扫描,扫描范围为100~1000 m/z。
2.3 液相定量条件 Agilent Eclipse Plus C18色谱柱 (4.6 mm ×250 mm,5 μm),流动相为甲醇(A)-0.01 mol/L乙酸铵溶液 (B),梯度洗脱(0~3 min,40%A;3.1~10 min,40% ~60%A;10.1~30 min,60%A;30.1~40 min,60% ~80%A;40.1 ~60 min,80%A;60.1 ~61min,80% ~40%A;61.1~80 min,40%A);柱温30℃;体积流量1 mL/min;二极管阵列检测器,波长范围190~400 nm;进样体积10 μL;理论塔板数应不低于3000。
3 方法与结果
3.1 对照品溶液的制备 精密称取对照品适量,加甲醇溶解,制成0.2 mg/mL的格列波脲对照品溶液。
3.2 供试品溶液的制备
3.2.1 固体制剂 取相当于一次口服剂量的供试品 (大蜜丸剪碎可加入适量硅藻土研磨),研细混匀,加三氯甲烷 20 mL,超声处理 (250 W,33 kHz)10 min,滤过,精密量取续滤液5 mL,水浴低温蒸干,残渣用甲醇定量转移至5 mL中,用甲醇定容,摇匀,即得。
3.2.2 液体制剂 取样品混匀,精密量取相当于一次口服剂量的供试品溶液,置分液漏斗中,用三氯甲烷振摇提取2次,每次20 mL,合并三氯甲烷液,水浴低温蒸干,残渣用甲醇定量转移至5 mL中,用甲醇定容,摇匀,即得。若样品溶液质量浓度过大,则应将其稀释至线性关系内质量浓度。
3.3 对照品及供试品溶液的色谱及对应紫外光谱结果。见图1、图2。
3.4 格列波脲的HPLC/MS/MS特征离子峰及质谱图 格列波脲对照品 [M+H+]m/z如下,一级质谱母离子为367;二级质谱分子离子碎片为349、170、196、152。见图3。
3.5 线性关系 精密量取“3.1”项下对照品溶液,分别稀释成从0.002 mg/mL至0.2 mg/mL范围内的梯度对照品溶液,测定色谱峰面积,以质量浓度为横坐标,积分面积为纵坐标,求得回归方程Y=217.88X+0.3245,r2=0.9998,可见在0.002~0.2 mg/mL范围内呈线性关系。
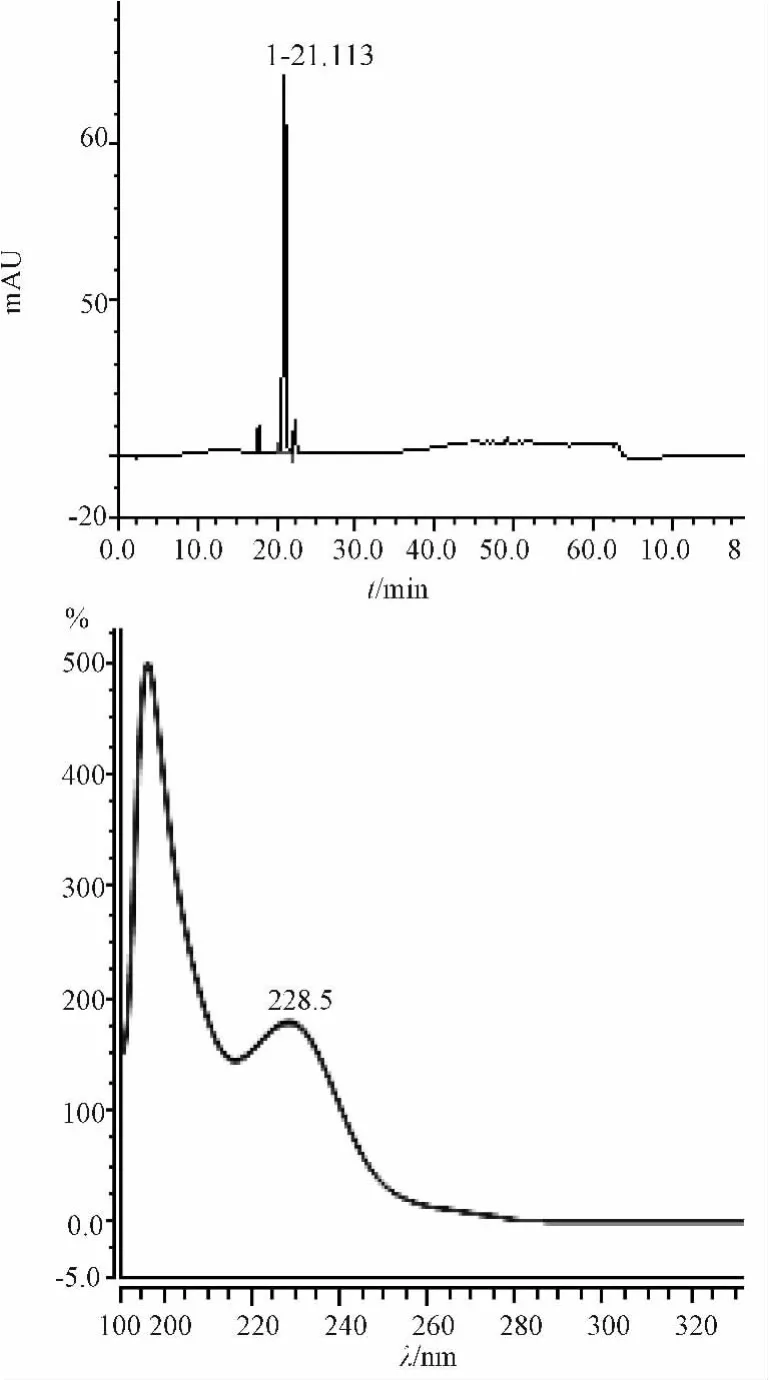
图1 格列波脲对照品色谱及对应紫外光谱图Fig.1 Reference Glibornuride chromatograms and the corresponding UV spectra
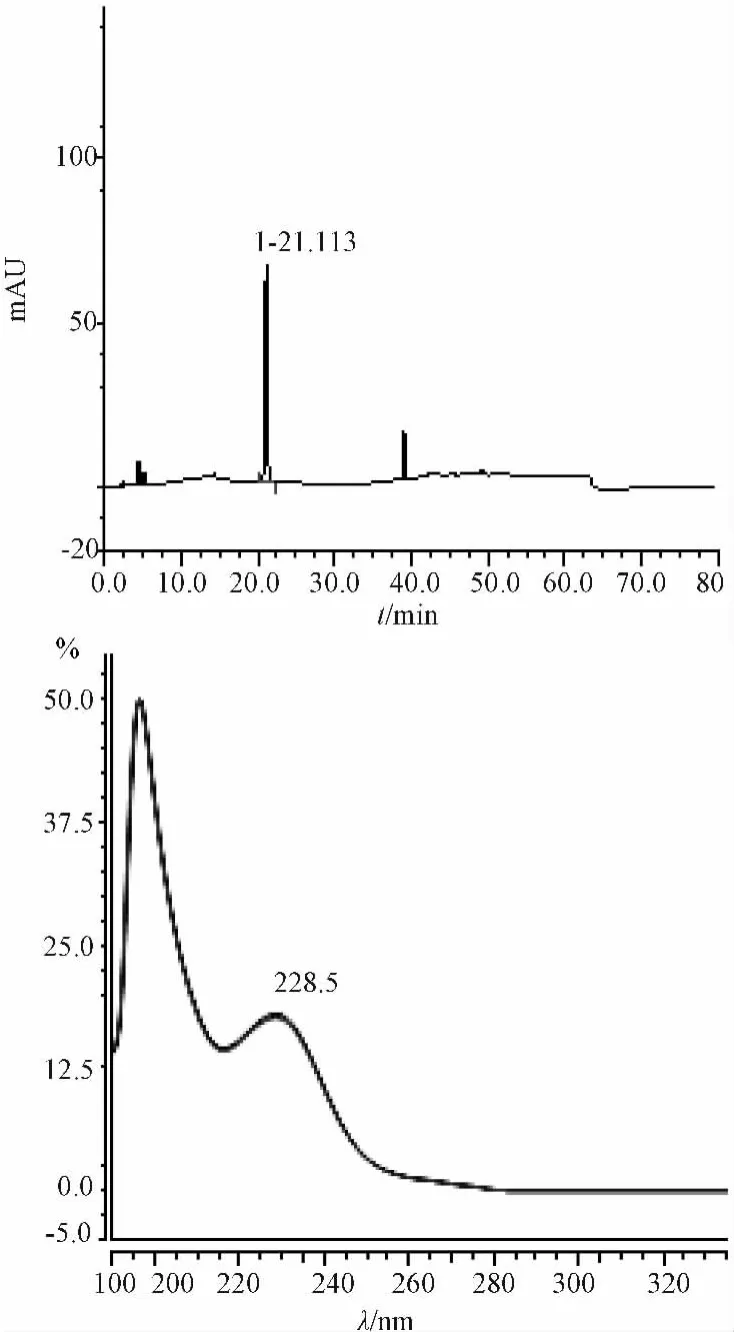
图2 供试品中格列波脲色谱及对应紫外光谱图Fig.2 Glibornuride chromatograms and ultraviolet spectrum of products in the corresponding
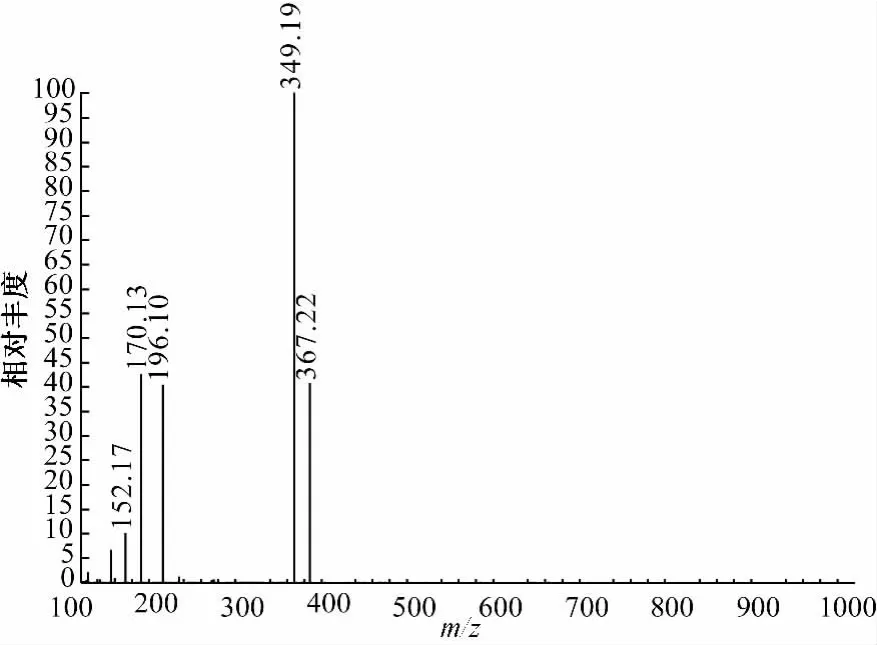
图3 格列波脲质谱图Fig.3 Glibornuride mass spectra
3.6 精密度试验 精密吸取同一格列波脲对照品溶液,重复进样6次,RSD为0.7%,表明仪器精密度良好。
3.7 定量限及检出限 以信噪比3倍的为检出限最低响应值,计算检出限为15.2 μg/g;以信噪比10倍的为定量限最低响应值,计算定量限为39.3 μg/g。
3.8 稳定性试验 取同一份供试品溶液,在制备后每隔2 h进一次样,结果表明供试品溶液在36 h内基本稳定。
3.9 回收率试验 采用加样回收法测定,精密称取上述已知含有量阳性样品 (消渴丸)9份,分别加入相当于线性范围内 (使最终的加样回收溶液中格列波脲的质量浓度在0.002~0.2 mg/mL线性范围内)3个不同量的对照品,按“3.2”项下供试品溶液制备方法制备,计算回收率,平均回收率为96.3%,RSD为1.0%。
3.10 耐用性试验 用两个品牌的液相 (戴安及岛津)以及两种品牌色谱柱 (安捷伦和Dikma)对测定结果均不影响,阳性样品及阴性样品检出结果一致。
3.11 专属性试验 在1批检出格列波脲的中成药样品中按照“2.3”项下条件测定,样品中出现与对照品保留时间相同的色谱峰,DAD光谱谱图均与相应的对照品一致,同条件下其余9种对照品有效分离,阴性样品没有干扰。见图4、图5。

图4 格列波脲与9种对照品色谱图Fig.4 Chromatogram of glibornuride and nine reference substances
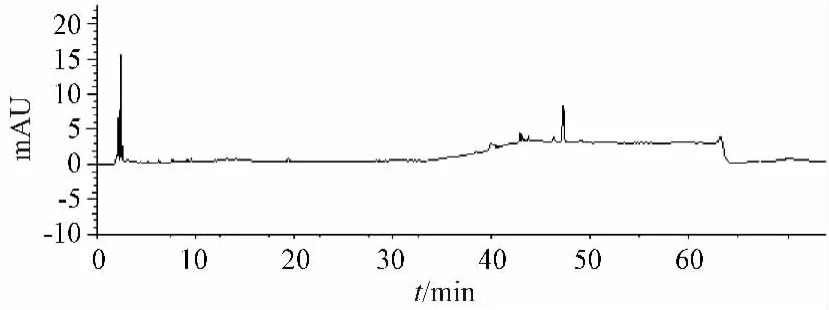
图5 阴性样品溶液色谱图Fig.5 Negative sample solution chromatogram
4 样品测定
按照所验证的方法对30多批次降糖类中成药(剂型包括胶囊、丸、口服液、片剂、颗粒剂)进行非法添加降糖类化学药品的快速筛查及确证定量,筛选出2批次阳性样品,含有量分别为5.8、3.5 mg/g。
5 讨论
5.1 本方法是在国家食品药品监督管理局药品检验补充检验方法和检验项目批准件 (批准件编号:2009029)检测方法基础上进行实验,这样可以在同一色谱系统条件下将10种化学药品成分进行有效分离,本实验检测波长定为235 nm,而非其最大吸收波长228 nm,是基于该方法通用的检测波长,可以提高分析效率;该方法中未将液体制剂的制备方法列入其中,而本实验对液体制剂的制备进行了补充完善;在进行质谱分析时,分别进行了ESI+、ESI-的方法考察,但 ESI-结果不佳,而ESI+结果则满意;通过研究证明,该方法准确可靠,能快速地对其进行筛查、定量测定及确证,为降糖药中非法添加化学药品又提供了一有力的技术支持。
5.2 本实验中涉及的中成药中非法添加化学药品格列波脲是“打非”过程中用“异常图谱法”意外发现,说明有些不法厂商对国家各类中成药中非法添加化学药品的检测标准非常了解,根据标准中的漏洞,添加一些检测标准中未列入的化学药品,即使检出也无判定依据,逃避监管。另一方面,因目前我国尚未批准格列波脲原料及相关制剂,但在市场中发现此化学药品的添加,说明有不法分子在非法合成此原料用于非法添加,有关部门正在积极查处。
5.3 本实验所用格列波脲对照品是从加拿大购进,国内尚无此对照,目前我们正努力实现格列波脲对照品的自给。
[1]国家食品药品监督管理局.2009029,降糖类中成药中非法添加化学药品补充检验方法[S].2009.
[2]张西如,姜建国.应用LC-MS联用技术检测生命糖安胶囊中添加的西药降糖成分[J].中成药,2009,31(3):418-420.
[3]许 琦,繆 刚,顾炳仁.HPLC法快速筛选降糖类中成药及保健品中非法加入的化学药品[J].中国现代药物应用,2010,4(9):1-2.
[4]彭碧燕,苏嘉珊,李阳羚.降糖类中成药、保健品添加多种降糖类化学药品的分析[J].海峡药学,2012,24(8):78-80.
[5]樊磊磊,刘乃强,李振国.UPLC-MS定性定量检测稳糖安胶囊中降糖类化学药品[J].中国实验方剂学杂志,2013,19(8):87-90.
[6]曹恒斌,袁玉梅.反相高效液相色谱法检测降糖类中药制剂及中药保健品中双胍类及磺酰脲类成分[J].医药导报,2010,29(10):1358-1360.
[7]刘福艳,李 军,谢元超,等.中成药中非法添加化学药品的现状与分析检测对策[J].中国药事,2008,22(12):1067-1069.
[8]李雪靖,潘 颖,郄素会.降糖中成药中非法添加化学药品的 HPLC法快速检测[J].河北医药,2008,30(6):882.
[9]王晓琦,田永庆,孙会昌,等.RP-HPLC检测治疗消渴症制剂中的多种磺酰脲类化学成分[J].中成药,2007,29(7):1011-1013.
[10]孙夏荣,李 丹,文红梅,等.LC-MS/MS法快速测定中成药与保健食品中非法添加20种化学成分研究[J].中国药师,2011,11(1):22-25.
[11]陈 静,张晓丹,周国华.快速筛查消渴类中成药中非法添加成分的HPLC-DAD数据库的建立[J].中国现代药物应用,2011,28(5):377-383.
[12]张晓丹,陈 静,伍晓勇.多次进样循环使用流动相HPLC-DAD法的建立及在快速筛查消渴类中成药中非法添加化学成分中的应用[J].药物分析杂志,2011,31(6):1088-1093.
[13]肖树雄,李杨杰.由降糖中成药和保健食品检验情况探索非法添加化学成分的系统快筛思路[J].药物分析杂志,2011,31(2):418-422.
[14]薛士荣.糖类中成药及保健品中添加化学药物的检测方法[J].海峡药学,2011,23(9):73-75.
[15]潘广洲,高国敬,傅 伟.两种快速检测降糖类中成药中添加磺酰脲类药物方法的比较[J].中国药业,2010,19(4):28.
[16]潘广洲,孙红刚.HPLC法检测降糖中成药添加磺酰脲类药物[J].现代中药研究与实践,2010,24(6):64-65.
[17]罗疆南,曹 玲,谭 力,等.LC-MS/MS法检测中药及保健品中非法添加的11种降糖类化学药物[C] //中国药学杂志岛津杯第九届全国优秀论文评选交流会.2009:269-272.
[18]殷 帅,吴公平,雷玉萍,等.液质联用法检测中成药和保健食品中添加辅助降血糖类药品的研究[J].药物分析杂志,2010,30(12):2400-2403.
[19]汪 祺,苏 晶,覃红萍,等.TLC法快速筛查降糖类中成药及保健食品中添加的11种化学药品[J].中国药事,2010,24(7):647-649.
[20]吴公平,雷玉萍,李荣玮,等.采用反相高效液相色谱法测定降糖类保健食品非法添加降糖化学药品检验方法的研究[J].中国现代医学杂志,2010,20(9):1380-1382.
[21]刘起忠,李慧义,杭太俊.中药降糖制剂中非法掺入的化学降糖药物成分的检测[J].中国现代应用药学杂志,2008,25(1):61-63.
[22]杨文红.降糖类中成药和保健品中非法添加化学物质的检测方法研究进展[J].今日药学,2009,19(5):55-57.

