外周血单核细胞HLA-DR/CD14分析的临床意义及其与降钙素原、C-反应蛋白、白细胞计数的相关性
熊小敏 ,李薇
1.广州军区 广州总医院检验科,广东 广州 510010;2.广州中医药大学,广东 广州 510405
近年研究表明,外周血单核细胞HLA-DR/CD14表达与临床疾病的感染及严重程度密切相关,其表达水平反映患者机体的免疫状态,可作为判断急重症疾病严重程度和预后的免疫指标[1-6]。我们将该指标应用于临床脓毒血症患者,并同步进行降钙素原(procalcitonin,PCT)、C-反应蛋白(C reactive pro⁃tein,CRP)、白细胞(white blood cells,WBC)计数等指标检测,比较脓毒血症患者与正常对照组外周血单核细胞表面HLA-DR/CD14的表达水平,并对各项指标间的相关性进行了分析。
1 资料与方法
1.1 研究对象与分组
选择2012-01~2013-07收入我院的ICU脓毒症患者47例,所选病例符合修订后的2010脓毒症、严重脓毒症、脓毒症休克诊断标准[7-8],根据感染病灶或细菌学检查结果判断是否存在感染,疾病严重程度依据APACHEⅡ[9]评分综合评估。根据HLA-DR/CD14的阈值结果[1-3],将<30%的患者视为重度感染并设为观察1组,共25例,其中男14例、女11例,平均年龄为63.88(29~93)岁;介于30%~49%之间的患者视为中度感染并设为观察2组,共22例,其中男16例、女6例,平均年龄59.91(25~96)岁。同期选择非感染引起炎症而住院的患者(包括强直性脊柱炎患者、血管炎患者、类风湿性关节炎患者等)设为观察3组,共10例,其中男6例、女4例,平均年龄55.9(17~93)岁。同期选择因其他疾病而住院的患者(包括高血压患者、2型糖尿病患者、冠心病患者、帕金森病患者等)设为观察4组,共18例,其中男13例、女5例,平均年龄60.33(16~92)岁。3、4组均依据脓毒症诊断标准[7-8]排除感染。正常对照组为同期健康体检者(肝肾功能、血脂四项、肿瘤标志物、心电图、X线胸片检查等物理检测均正常),共21例,其中男13例、女8例,平均年龄41.95(21~77)岁。
1.2 材料
CD14-FITC、HLA-DR-PE、小鼠IgG1-FITC、红细胞裂解液、FACSCantoⅡ流式细胞仪均购自BD Biosciences公司;Minividas全自动免疫荧光分析仪及配套试剂购自生物梅里埃公司;特种蛋白分析仪及配套试剂购自SIEMENS公司;XE2100血细胞分析仪及配套试剂购自广州宜德医疗器械有限公司。
1.3 标本采集
所有住院患者于治疗前采集EDTA-K3静脉抗凝血,用于检测HLA-DR/CD14及WBC;同步采集静脉血3 mL于干燥管中,待凝固后离心,血清用于PCT、CRP检测。
1.4 标本检测
1.4.1 HLA-DR/CD14检测 取抗凝全血各100 μL,分别加入测定、同型对照2管中,测定管加入20 μL HLA-DR-FITC、20 μL CD14-PE,同型对照管中加入20 μL小鼠IgG1-FITC、20 μL CD14-PE,混合后室温避光反应15 min;每管加入红细胞裂解液2 mL作用10 min,1000 r/min离心5 min,弃上清;每管加入2 mL PBS,1000 r/min离心5 min,弃上清;加入1 mL鞘液混匀后上机分析。
1.4.2 PCT检测 采用Minividas全自动免疫荧光分析仪及配套试剂,结合一步免疫测定夹心法和最终荧光检测法(ELFA)进行测定
1.4.3 CRP检测 采用特种蛋白分析仪及配套试剂,散射比浊法检测。
1.4.4 WBC检测 采用XE2100血细胞分析仪及配套试剂,流式细胞术检测。
1.5 结果分析
以CaliBRITE标准微球调节流式细胞仪PMT电压、荧光补偿、灵敏度,收集10 000细胞/管,以同型对照管CD14-PE/SSC散点图中CD14细胞群设门,小鼠IgG1-FITC/CD14-PE散点图确定阴性细胞区域,分析测定管HLA-DR FITC/CD14 PE散点图中右上象限HLA-DR/CD14阳性细胞百分率,结果以百分率表示。
PCT、CRP、WBC采用定量检测,记录具体数值。PCT正常参考范围为<0.05 ng/mL,CRP正常参考范围为<6.0 mg/L,WBC正常参考范围为3.5×109~9.5×109/L。
1.6 统计学分析
所有数据用SPSS13.0软件统计分析,结果用x±s表示。各组间指标比较采用计量资料多组数据方差分析,组内各指标间相关关系采用双变量相关分析;脓毒症患者2组间存活率采用独立样本2×2列联表资料的χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 各组数据均值及组间比较
选择单向方差分析(One-Way ANOVA)方法进行多组比较。对各组HLA-DR/CD14、PCT、CRP、WBC数据分别进行方差齐性检验,Levene检验方差不齐,P值均<0.05,因此选择方差不齐的多重比较方法Dunnett's T3,结果见表1。与正常对照组比较,1、2组各项指标与正常组间存在显著差异,P值均<0.01,有统计学意义;3组CRP与正常组CRP间存在显著差异,P<0.01,有统计学意义。与2组比较,1组除WBC外其他各项指标间均存在显著差异,P值均<0.01,有统计学意义。3、4组与1、2组各项指标间存在显著差异,P值均<0.01,有统计学意义。其他P值均>0.05,差异无统计学意义。
2.2 组内各指标的相关性比较
选择积矩相关系数(Pearson相关系数r)进行组内相关性比较。观察1组HLA-DR/CD14与PCT、CRP间存在显著负相关关系,与WBC间差异无统计学意义,r值分别为-0.911、-0.975、0.231,前两者P值均<0.01,后者P>0.05;观察2组HLA-DR/CD14与PCT、CRP间存在显著负相关关系,与WBC间差异无统计学意义,r值分别为-0.949,-0.915、-0.296,前两者P值均<0.01,后者P>0.05。其他指标比较P值均>0.05,不存在相关关系。
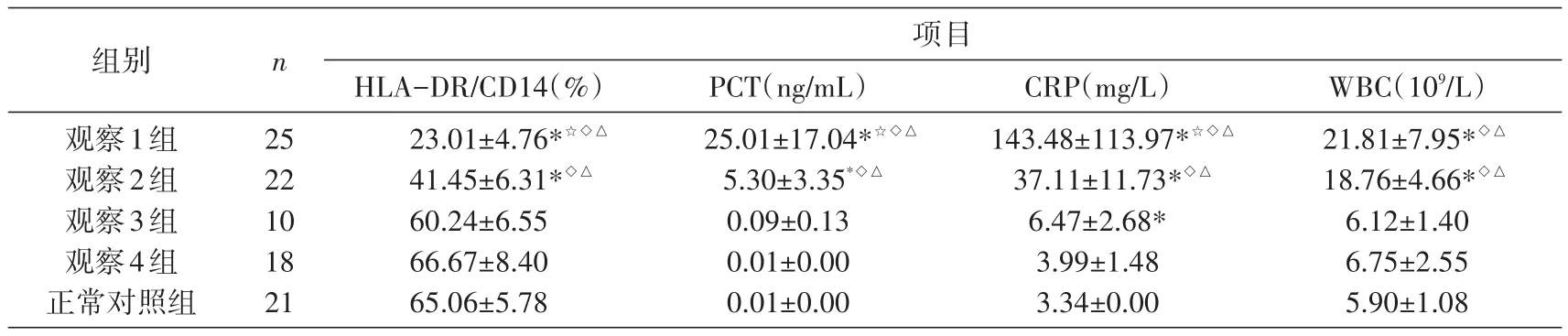
表1 各组检测项目结果分析(x±s)
2.3 脓毒症患者观察1、2组间存活率比较
设生存时间为28 d[5],存活率定义为观察组经历28 d后仍存活的可能性。脓毒症患者2组间存活率比较采用独立样本2×2列联表资料的χ2检验(Pearson χ2检验),结果见表2。经计算可得,自由度ν=1,查表可知χ20.05,1=3.84,本例χ2=7.74>χ20.05,1,可知P<0.05,说明2组的存活率具有显著性差异。观察1组的存活率为16.0%,观察2组的存活率为54.5%,可以认为观察2组的存活率比观察1组的存活率高。
2.4 脓毒症患者观察1、2组单核细胞表面HLADR/CD14表达的动态观察结果
对观察1、2组中10例脓毒症患者进行动态观察分析,发现其中5例患者经过积极治疗后指标仍未改善,并持续下降至16.96%±3.96%,直至死亡;另5例患者经治疗后指标逐渐上升至63.90%±10.88%,恢复至正常水平,临床症状同步改善直至治愈,与临床报道[1]相符。

表2 脓毒症患者2组间存活率比较
3 讨论
白细胞分化抗原14(CD14)是一种特异性的单核细胞、中性粒细胞和巨噬细胞表面标志物,属于细胞表面糖蛋白家族,作为白细胞表面分化抗原最早被发现,后续研究证实CD14是脂多糖(LPS)的细胞受体,在机体的免疫反应、表态性疾病、感染性疾病及多个系统的疾病发生、发展中起重要作用。CD14在生理状态下是单核/巨噬细胞的一种分化标志物,其表达在转录水平上受髓样细胞分化的调节;病理情况下,根据某些部位单核/巨噬细胞上CD14的特异性表达异常及血清中sCD14[10]的浓度异常来对疾病作出诊断,判断预后,指导临床。近年来有研究报道,外周血单核细胞表面HLA-DR/CD14表达率与感染及疾病的严重程度密切相关,可作为判断急重症疾病严重程度和预后的免疫指标[1,4-6]。
本研究表明,脓毒症患者(包括重度感染组和中度感染组)HLA-DR/CD14表达水平明显低于正常对照组,且与非感染炎症组、其他疾病组也存在明显差异,说明该2组患者机体存在感染,免疫状况异常,处于免疫抑制状态,与临床病情观察相符,且该2组患者PCT、CRP、WBC值均明显高于其他组,与其他3组比较,均存在显著性差异。研究结果显示,脓毒症患者无论重度感染或中度感染,HLA-DR/CD14表达水平与PCT、CRP结果存在显著负相关关系,说明HLA-DR/CD14表达水平下降时PCT、CRP升高;而与WBC结果间不存在显著性关系,HLA-DR/CD14表达水平下降时,重度感染组WBC存在升高的现象,中度感染组WBC存在降低的现象,说明HLADR/CD14表达水平下降时WBC有可能升高或降低。有研究报道,HLA-DR/CD14低于30%的患者经治疗后,若数值持续低下则存活率低,若数值升高至正常值或高于30%,免疫状态得以改善,病情得以控制,甚至好转出院;HLA-DR/CD14介于30%~49%的患者若经治疗后数值升高至正常值,病情得到控制,存活率较高,因此30%可设为临床判断患者病情严重程度及评估预后的阈值[1,3]。以28 d生存视为存活期观察,发现脓毒症患者中HLA-DR/CD14低于30%的重度感染组患者存活率为16.0%,介于30%~49%的中度感染组患者存活率为54.5%,2组存活率差异有统计学意义,可以认为中度感染组患者的存活率比重度感染组患者的存活率高。在对观察1、2组中10例脓毒症患者进行动态观察分析时发现,有5例死亡患者HLA-DR/CD14表达率经积极治疗后仍持续下降并低于30%,而另5例存活患者HLADR/CD14表达率经治疗后逐渐上升,恢复至正常水平,说明将HLA-DR/CD14阈值设为30%与临床疾病重症程度密切相关,与文献报道相符合,提示脓毒症患者具有免疫抑制特点,早期炎症介质增加,晚期则转变为免疫抑制状态[11]。HLA-DR/CD14表达水平低下提示患者处于免疫抑制状态,可作为感染性疾病免疫状态评价指标,用于临床感染性疾病患者的免疫状态评价、病程评估及诊疗评价[1-6]。
CRP、WBC作为实验室疾病辅助诊断的传统检测指标已应用于临床,当机体受到感染刺激后,CRP、WBC均有不同程度的变化,但特异性不强,各种原因引起的炎症反应也能使两者升高,但临床上仍进行检测证明这两者仍有重要的作用,可作为预警信号。近年来PCT作为较新的实验室感染指标,在脓毒血症的诊断中具有重要意义,然而临床上不可单一只用一个指标作为临床诊断指标,联合检测可更好地指导临床,无论是疾病诊断、病程监控还是预后。联合比较4项指标的相关文献较少,经组内各指标相关性比较可知,联合检测这4项指标有助于临床感染性疾病评估、诊疗观察,且动态观察HLA-DR/CD14表达率亦可监测患者疾病的发展,并对预后作出正确评估[1,6,10,12-19]。
[1]李薇,谢闻悦,张卫云,等.HLA-DR/CD14在外周血单核细胞中的表达及其临床意义[J].解放军医学杂志,2011,36(1):61-63.
[2]苏磊,周殿元,唐柚青,等.CD14+阳性细胞人白细胞DR抗原在脓毒症早期检测中的临床意义[J].中国危重病急救医学,2006,18(11):677-679.
[3]齐曼,夏成青,李文雄,等.外周血单核细胞膜CD14表达预测脓毒症患者预后的研究[J].中华临床医师杂志(电子版),2012,6(8):1993-1997.
[4]郭权,毕伟.白细胞分化抗原14的研究进展及意义[J].临床和实验医学杂志,2011,10(3):215-217.
[5]脓毒症免疫调理治疗临床研究协作组.乌司他丁、α1胸腺肽联合治疗严重脓毒症——一种新的免疫调理治疗方法的临床研究[J].中华医学杂志,2007,87(7):451-457.
[6]Prucha M,Zazula R,Müller M,et al.TREM-1 expression on monocytes is not a parameter specific for infectious etiology ofsystemicinflammatoryresponsesyndrome[J].PragueMed Rep,2011,112(3):205-215.
[7]李志军,王东强,田永超,等.2010德国脓毒症指南解毒—关于脓毒症的预防、诊断、治疗及后续护理[J].中国危重病急救医学,2011,23(5):257-262.
[8]Dellinger R P,Levy M M,Rhodes A,et al.Surviving sepsis campaign:international guidelines for management of severe sepsis and septic shock:2012[J].Crit Care Med,2013,41(2):580-637.
[9]Knaus W A,Draper E A,Wagner D P,et al.APACHEⅡ:a severity ofdisease classification system[J].CritCare Med,1985:1(10):818-829.
[10]Liu B.Chen Y X,Yin Q,et al.Diagnostic value and prog⁃nostic evaluation of Presepsin for sepsis in an emergency de⁃partment[J].Crit Care,2013,17(5):R244.
[11]Oberholzer A,Oberholzer C,Moldawer L L.Sepsis syndromes:understandingtheroleofinnateand acquired immunity[J].Shock,2001,16(2):83-96.
[12]李晓,石玉玲,李林海,等.动态监测血清降钙素原对多发伤患者并发脓毒症的诊断价值[J].生物技术通讯,2012,23(4):592-594.
[13]李政霖,祁恒旭,陈晓园.降钙素原指导脓毒血症患者抗感染治疗的研究[J].中国医药指南,2012,10(9):19-20.
[14]陈肇杰,冯广满,吴见欢,等.PCT和CRP检测在炎症诊断中的价值[J].贵阳中医学院学报,2012,34(6):52-54.
[15]杨素华,洪旭涛,林伟峰.联合检测血清PCT、CRP水平变化对脓毒症患者的诊断价值[J].中国卫生检验杂志,2012,22(12):2913-2915.
[16]杨清荣.C反应蛋白、红细胞和白细胞在内科感染性疾病的诊断价值分析[J].中国医药导报,2011,8(7):38-39.
[17]景正全,淡珂,陈晓艳,等.C反应蛋白联合白细胞检测在新生儿感染性肺炎中的临床价值评价[J].中国妇幼保健,2012,27:1490-1491.
[18]李建华,姜晓云.血清CRP和血常规检测在儿科中的应用[J].吉林医学,2012,33(1):151-152.
[19]陈宏础,王鸿利.全国临床检验操作规程[M].南京:东南大学出版社,2006:133.

