AuCl3-CuCl2/γ-Al2O3乙炔氢氯化催化剂的失活原因分析及再生性能研究
程晓光,赵基钢,王 雷,2,沈本贤
(1.华东理工大学化学工程联合国家重点实验室,上海 200237;2.天津大沽化工股份有限公司)
AuCl3-CuCl2/γ-Al2O3乙炔氢氯化催化剂的失活原因分析及再生性能研究
程晓光1,赵基钢1,王 雷1,2,沈本贤1
(1.华东理工大学化学工程联合国家重点实验室,上海 200237;2.天津大沽化工股份有限公司)
采用γ-Al2O3为载体通过浸渍法制备了AuCl3-CuCl2γ-Al2O3催化剂,考察其对乙炔氢氯化反应的催化性能,并用比表面积及孔径分析、扫描电镜、能谱仪、傅里叶变换红外光谱、电感耦合等离子体原子发射光谱等表征方法对催化剂的失活原因进行分析。结果表明:在温度150 ℃、压力0.1 MPa、空速120 h-1、V(HCl)∶V(C2H2)=1.05的工艺条件下,乙炔转化率达到97%以上,氯乙烯选择性达到99%以上,但反应3 h后催化剂活性迅速降低;催化剂表面积炭为其失活的主要原因。将失活催化剂在空气氛围、500 ℃下焙烧1 h后,其活性基本能恢复至新鲜催化剂水平,说明该催化剂具有优异的再生性能。
乙炔氢氯化 氧化铝 载体 失活 再生
我国石油资源短缺,合成聚氯乙烯的单体氯乙烯主要通过乙炔氢氯化反应合成,但该工艺采用剧毒且易升华损失的氯化汞催化剂,严重危害人体健康和污染环境,因此寻找一种非汞催化剂替代传统的汞催化剂已成为整个电石乙炔法PVC行业面临的一个亟待解决的问题。近年来,众多学者对Au基[1-6]、Pt基[7-9]甚至非金属[10]乙炔氢氯化反应催化剂等进行了研究,其中王声洁[11]开发的AuCl3-CuCl2/AC催化剂表现出优异的催化性能,虽然相比前人的研究结果,该催化剂的稳定性得到了改善,但由于以活性炭为载体,存在机械强度低、不能烧焦再生的缺点,使用王水洗涤的方法虽然可使其再生,但存在强腐蚀问题,很难实现催化剂的在线再生,从而提高了工业应用的成本,限制了催化剂的工业应用。经过试验筛选发现,以γ-Al2O3为载体的AuCl3-CuCl2γ-Al2O3催化剂对乙炔氢氯化反应表现出了优异的初始活性,但存在易失活的缺点。对其失活原因进行分析可以为开发高稳定性易再生的AuCl3-CuCl2γ-Al2O3乙炔非汞催化剂提供一定的指导作用。本课题以γ-Al2O3为载体制备AuCl3-CuCl2γ-Al2O3非汞催化剂,考察其对乙炔氢氯化反应的催化性能,并用比表面积及孔径分析、扫描电镜、能谱仪、傅里叶变换红外光谱、电感耦合等离子体原子发射光谱等表征方法对催化剂的失活原因进行分析。
1 实 验
1.1 催化剂制备
γ-Al2O3载体购自河南巩义宝来水处理材料厂。采用浸渍法制备AuCl3-CuCl2γ-Al2O3催化剂,制备方法参考文献[6]中制备AuCl3-CuCl2AC的方法。将一定量的HAuCl4·4H2O与CuCl2·2H2O分别溶解于去离子水中配成浸渍液,将10 g γ-Al2O3载体分别加入到一定浓度的HAuCl4(Au负载量1%)和CuCl2(Cu负载量10%)的混合溶液中,浸渍5 h,再于110 ℃下烘干,制得AuCl3-CuCl2γ-Al2O3催化剂。
1.2 催化剂表征
载体及催化剂的BET比表面积和孔结构等物理参数采用N2吸附方法在ASAP2020型化学吸附仪上测定,样品在573 K下真空干燥10 h,在77 K下进行吸附。新鲜和失活催化剂采用Nicolet 6700型傅里叶红外光谱仪(FT-IR)进行定性分析,样品研细至200目以上,采用KBr压片,扫描32次。试样的表面微观形貌采用NOVA NanoSEM450型超高分辨场发射扫描电子显微镜(SEM)分析,采用其附属的能谱仪(EDS)分析表面元素。Au和Cu含量采用美国Varian公司生产的710ES型电感耦合等离子体发射光谱仪(ICP-AES)进行测定。
1.3 催化剂性能评价
催化剂性能评价在固定床反应器中进行,取10 g催化剂置于内径为10 mm的不锈钢制固定床反应器恒温段内,两端非恒温段以石英砂封闭。HCl与C2H2原料气分别用5A分子筛和硅胶干燥。反应条件:反应温度150 ℃,反应压力0.1 MPa,空速120 h-1,V(HCl)∶V(C2H2)=1.05。反应前以50 mL/min通HCl气体2 h,对催化剂进行充分活化。反应后混合气体经冷却后用氢氧化钠溶液吸收,除去未反应的氯化氢,每隔一定时间用采气袋收集产品气并进行色谱分析。分析条件:柱温50 ℃,检测器温度180 ℃,汽化室温度180 ℃,升温速率10 ℃/min,进样量40 μL。催化剂的活性用乙炔转化率(XA)和氯乙烯选择性(SVCM)来评价。
XA=(1-φA)×100%
(1)
SVCM=φVCM(1-φA)×100%
(2)
式中:φA为剩余乙炔的体积分数;φVCM为产物中氯乙烯的体积分数。
2 结果与讨论
2.1 催化剂的活性
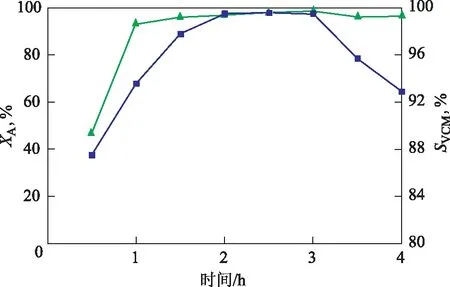
图1 新鲜AuCl3-CuCl2γ-Al2O3催化剂的催化性能■—乙炔转化率(XA); ▲—氯乙烯选择性(SVCM)
参照AuCl3-CuCl2/AC催化剂评价的工艺条件[6],考察AuCl3-CuCl2/γ-Al2O3新鲜催化剂对乙炔氢氯化反应的活性,结果见图1。由图1可见,在反应初期,随着反应时间的延长,乙炔转化率和氯乙烯选择性迅速增大,反应时间达到2 h时,乙炔转化率和氯乙烯选择性趋于稳定,乙炔转化率达到97%以上,氯乙烯选择性达到99%以上,反应3 h后催化活性开始出现明显的下降,催化剂寿命较短。
2.2 催化剂失活原因分析
2.2.1 BET表征 γ-Al2O3载体、新鲜催化剂与失活催化剂的比表面积及孔结构参数见表1。从表1可以看出:新鲜催化剂与γ-Al2O3载体的各参数基本一致,表明小粒径的AuCl3与CuCl2负载在γ-Al2O3载体的介孔孔道内,未产生大的团聚及架桥等现象,催化剂的孔道及比表面积基本无变化;失活后催化剂的各参数均有所降低,表明催化剂产生了孔道堵塞现象。
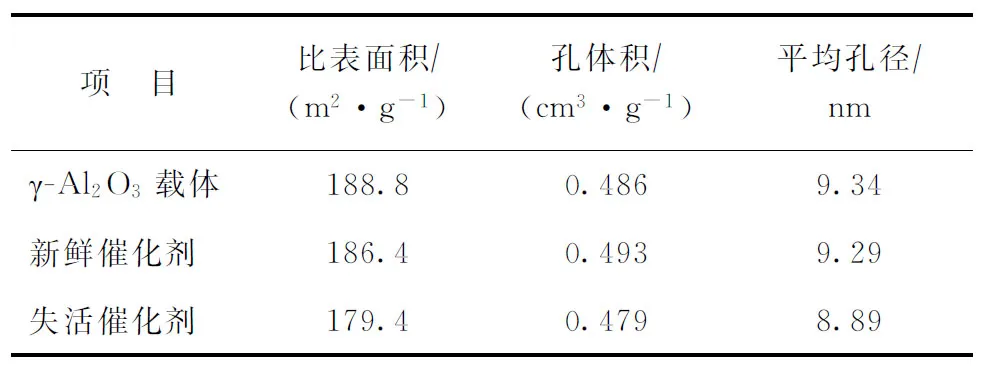
表1 催化剂的比表面积及孔结构参数
2.2.2 SEM-EDS表征 新鲜催化剂和失活催化剂的SEM照片见图2。由图2可见,新鲜催化剂表面的孔道较为丰富,未有堵塞现象;失活后催化剂表面覆盖了一层明显的积炭,呈“片状”结构,这与以活性炭为载体的AuCl3-CuCl2/AC催化剂表面的“丝状”积炭明显不同。选取片状积炭的一点进行EDS分析,结果见图3。由图3可以看出,积炭的主要元素为C和Cu,表明催化剂迅速积炭失活可能是因为活性组分中的Cu元素引起的,在Cu元素的周围乙炔容易发生催化聚合生成积炭。

图2 新鲜催化剂与失活催化剂的SEM照片
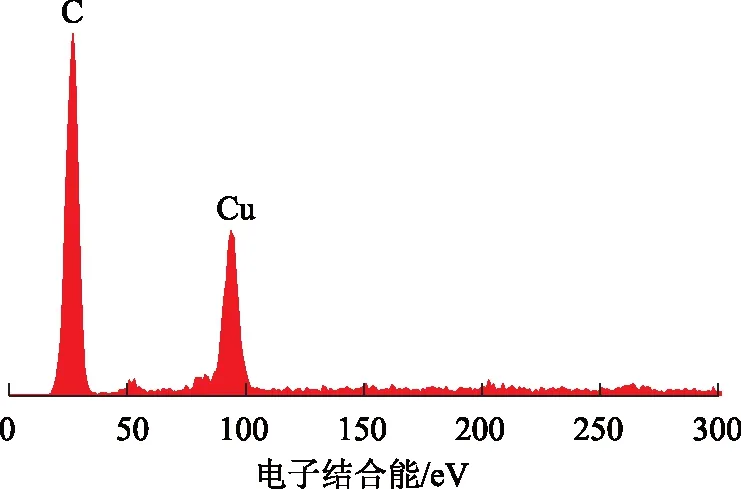
图3 失活催化剂积炭区域的EDS能谱
2.2.3 FT-IR表征 新鲜催化剂与失活催化剂的FT-IR图谱见图4。由图4可见,与新鲜催化剂相比,失活催化剂增加(或增强)了3个主要的吸收峰。其中,2 930 cm-1、2 850 cm-1处的峰分别归属为vs(CH2)和vas(CH2),1 404 cm-1处为饱和烷烃中C—H的面内弯曲振动峰,未出现属于不饱和烃类及C—Cl的吸收峰,表明失活催化剂表面的积炭主要为饱和链状烃类。
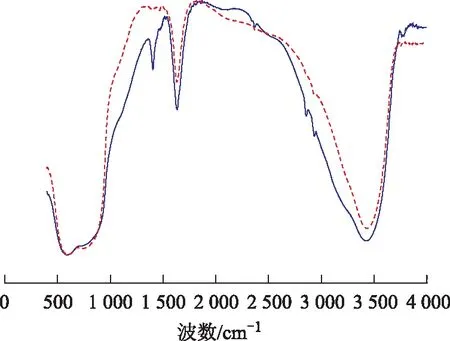
图4 新鲜催化剂与失活催化剂FT-IR图谱 —失活催化剂; —新鲜催化剂
2.2.4 ICP-AES表征 新鲜催化剂的AuCl3和CuCl2负载量(w)分别为0.89%和8.80%,而失活催化剂中AuCl3和CuCl2负载量(w)分别为0.81%和7.90%,其中主活性组分AuCl3负载量(w)仅下降0.08百分点,虽然助催化剂CuCl2负载量(w)下降0.9百分点,但对催化剂活性影响不大。这可能是因为γ-Al2O3对AuCl3有较强的吸附作用,可使后者稳定地负载在载体表面,而对CuCl2的吸附作用相对较弱,出现了助催化剂少量流失的现象。
2.3 催化剂再生
在空气氛围下,将失活后催化剂在500 ℃下焙烧1 h得到再生催化剂。再生催化剂表面的SEM照片见图5。从图5可以看出,失活催化剂表面的“片状”积炭(图2)已经基本除去,再生催化剂表面平滑,其形貌与新鲜催化剂(图2)基本相同。

图5 再生催化剂的SEM照片
在固定床反应器中考察再生催化剂催化乙炔氢氯化反应的活性,结果见图6。由图6可见,在反应初期,随着反应时间的延长,乙炔转化率和氯乙烯选择性迅速增大,反应时间达到1.5 h和2 h时,乙炔转化率和氯乙烯选择性分别达到最大值,为97%和99%,反应2.5 h后乙炔转化率出现明显的下降,这与新鲜催化剂作用下的变化规律基本一致。表明该催化剂表面的积炭在500 ℃下能充分烧去,使活性中心重新暴露出来,该催化剂具有很好的再生性能。普遍认为Au基乙炔氢氯化反应催化剂的活性组分主要为Au3+,催化剂再生后活性的恢复也表明Au3+的还原不是催化剂失活的主要原因。
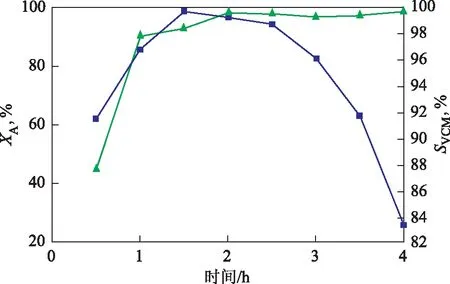
图6 再生催化剂的催化性能■—乙炔转化率(XA); ▲—氯乙烯选择性(SVCM)
3 结 论
在温度为150 ℃、压力为0.1 MPa、空速为120 h-1、V(HCl)∶V(C2H2)=1.05的工艺条件下,AuCl3-CuCl2γ-Al2O3催化剂具有很高的活性,乙炔转化率达到97%以上,氯乙烯选择性达到99%以上,但该催化剂寿命很短,反应3 h后活性迅速降低。对比分析失活催化剂与新鲜催化剂发现,该催化剂的失活原因主要为Cu元素引起的表面积炭覆盖了活性中心,而未出现活性组分的流失与Au3+的还原现象,这为该催化剂的再生提供了可能。失活催化剂在空气氛围、500 ℃下焙烧1 h可恢复到新鲜催化剂的活性水平,该催化剂具有很强的再生性能。
[1] Nkosi B,Coville N J,Hutchings G J,et al.Hydrochlorination of acetylene using gold catalysts:A study of catalyst deactivation[J].Journal of Catalysis,1991,128(2):366-377
[2] Conte M,Carley A F,Hutchings G J.Reactivation of a carbon-supported gold catalyst for the hydrochlorination of acetylene[J].Catalysis Letters,2008,124(34):165-167
[3] Conte M,Carley A F,Attard G,et al.Hydrochlorination of acetylene using supported bimetallic Au-based catalysts[J].Journal of Catalysis,2008,257(1):190-198
[4] Wang Shengjie,Shen Benxian,Song Qinglei.Kinetics of acetylene hydrochlorination over bimetallic Au-CuC catalyst[J].Catalysis Letters,2010,134(12):102-109
[5] Huang Chaofeng,Zhu Mingyuan,Kang Lihua,et al.Active carbon supported TiO2-AuCl3AC catalyst with excellent stability for acetylene hydrochlorination reaction[J].Chemical Engineering Journal,2014,242:69-75
[6] 程晓光,赵基钢,王雷,等.表面含氧基团对AuCl3-CuCl2C双组分非汞催化剂催化性能的影响[J].高等学校化学学报,2014,35(3):582-588
[7] Mitchenko S A,Khomutov E V,Shubin A A,et al.Mechanochemical activation of K2PtCl6:Heterogeneous catalyst for gas-phase hydrochlorination of acetylene[J].Theoretical and Experimental Chemistry,2003,39(4):255-258
[8] Mitchenko S A,Krasnyakova E V,Mitchenko R S,et al.Acetylene catalytic hydrochlorination over power catalyst prepared by pre-milling of K2PtCl4salt[J].Journal of Molecular Catalysis A:Chemical,2007,275(12):101-108
[9] Mitchenko S A,Khomutov E V,Shubin A A,et al.Catalytic hydrochlorination of acetylene by gaseous HCl on the surface of mechanically pre-activated K2PtCl6salt[J].Journal of Molecular Catalysis A:Chemical,2007,275(12):101-108
[10]Li Xiaoyan,Wang Yang,Kang Lihua,et al.A novel,non-metallic graphitic carbon nitride catalyst for acetylene hydrochlorination[J].Journal of Catalysis,2014,311:288-294
[11]王声洁.乙炔氢氯化非汞催化反应制取氯乙烯单体研究[D].上海:华东理工大学,2010
DEACTIVATION AND REGENERATION OF NON-MERCURY CATALYST AuCl3-CuCl2γ-Al2O3
Cheng Xiaoguang1, Zhao Jigang1, Wang Lei1,2, Shen Benxian1
(1.StateKeyLaboratoryofChemicalEngineering,EastChinaUniversityofScienceandTechnology,Shanghai200237;2.TianjinDaguChemicalCo.,Ltd.)
A non-mercury AuCl3-CuCl2γ-Al2O3catalyst was prepared by impregnation method using γ-Al2O3as support.The catalytic properties for acetylene hydrogen chloride reaction were explored in a fixed bed reactor.The catalyst was characterized by SEM-EDS, FT-IR, inductively coupled plasma atomic emission spectrum and BET analysis to see the reason for catalyst deactivation.The results show that acetylene conversion reaches more than 97% and the vinyl chloride selectivity is more than 99% under the conditions of a temperature of 150 ℃, a pressure of 0.1 MPa, a WHSV of 120 h-1, a volume ratio of HCl to C2H2equaling to 1.05∶1.However, the high activity can only keep for 3 h.The analysis found that the carbon deposit on the catalyst surface is the main reason for the deactivation.It proved that the catalyst activity can be recovered to the fresh level after regeneration in air for 1 h at 500 ℃.
acetylene hydrogen chloride; alumina; support; deactivation; regeneration
2014-05-27; 修改稿收到日期: 2014-07-20。
程晓光,硕士研究生,主要从事乙炔氢氯化反应非汞催化剂新型载体研究工作。
赵基钢,E-mail:zjg@ecust.edu.cn。
中央高校基本科研业务费专项资金资助项目(WA1214003)和天津市滨海新区塘沽科技发展专项资金资助项目(2012STHB04-01)。

