分子内叠氮酰氯的Schmidt反应合成(R)-苯并吲哚里西定*
李晓静,王宝娟,康晓艳,顾培明,李学强
(宁夏大学 宁夏天然药物工程技术中心 化学系 宁夏能源化工重点实验室,宁夏 银川 750021)
·快递论文·
分子内叠氮酰氯的Schmidt反应合成(R)-苯并吲哚里西定*
李晓静,王宝娟,康晓艳,顾培明,李学强
(宁夏大学 宁夏天然药物工程技术中心 化学系 宁夏能源化工重点实验室,宁夏 银川 750021)
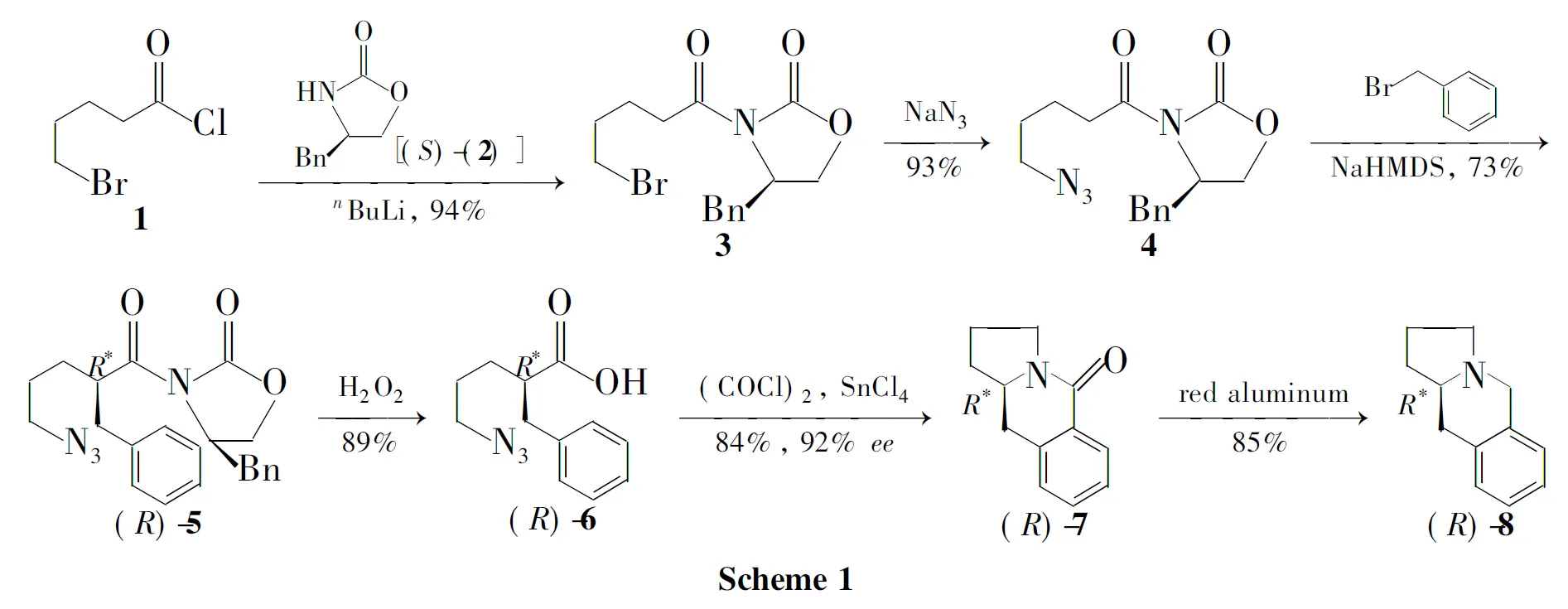
5-溴戊酰氯与手性助剂(S)-4-苄基-2-噁唑烷酮经酰胺化反应制得手性酰胺(3);3与叠氮钠反应得烷基化前体(4);以苄溴为烷基化试剂,碱辅助在酰胺羰基邻位引入苄基高立体选择性地制得手性酰胺[(R)-5],dr>99/1。用H2O2脱除(R)-5中的助剂结构单元得多米诺反应的前体手性叠氮羧酸[(R)-6];用草酰氯预处理(R)-6,原位制得叠氮酰氯,随即以四氯化锡来实现分子内Schmidt反应,苯环原位捕获重排中间体合成内酰胺[(R)-7],92%ee;用红铝还原(R)-7合成了(R)-苯并吲哚里西啶,收率85%,总收率40.6%,其结构经1H NMR,13C NMR和IR确证。
Schmidt反应;苯并吲哚里西定;合成;叠氮;立体化学
苯并吲哚里西定(8)结构在自然界中广泛存在,是很多具有重要生理活性的生物碱的关键子结构,研究人员对其进行了比较深入的合成研究[1-5]。
本课题组一直致力于使用叠氮基团进行的Schmidt反应研究[6-8],并首次报道了羧酸与烷基叠氮发生的新型的Schmidt反应[6],通过芳环对中间体进行捕获,成功制备了消旋体的苯并内酰胺结构单元,并以此反应对生物碱Antofine的消旋体进行了合成尝试[7]。
手性中心的立体控制构建是天然产物与药物合成中的重要内容,而一旦立体中心得以建立,往往需要考虑在进一步的化学转化中能够保持其构型。特别是立体中心位于羰基邻位的底物,很容易在较强的酸性或碱性条件下发生消旋化。在酰氯的Schmidt重排反应中,其迁移基团的立体构型能否保持对于制备手性的酰胺产物是关键。
本文首次探讨叠氮羧酸底物在发生Schmidt反应过程中,其羧基邻位的立体化学的控制问题。研究结果表明在酰氯的Schmidt反应中烷基迁移基团的立体化学构型可以保持,以此最终成功制备高光学活性的8。5-溴戊酰氯(1)与手性助剂(S)-4-苄基-2-噁唑烷酮[(S)-(2)]经酰胺化反应制得手性酰胺(3);3与叠氮钠反应得烷基化前体(4);以苄溴为烷基化试剂,碱辅助在酰胺羰基邻位引入苄基高立体选择性地制得手性酰胺[(R)-5,dr>99/1];用H2O2脱除(R)-5中的助剂结构单元得多米诺反应的前体手性叠氮羧酸[(R)-6];用草酰氯预处理(R)-6,原位制得叠氮酰氯,随即以四氯化锡来实现分子内Schmidt反应,苯环原位捕获重排中间体合成内酰胺[(R)-7,92%ee];用红铝还原(R)-7合成了(R)-8(Scheme 1),收率85%,总收率40.6%,其结构经1H NMR,13C NMR和IR确证。
1 实验部分
1.1 仪器与试剂
SGW-2型自动旋光仪;Bruker 400MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);FT-IR-8400S型傅立叶变换红外光谱仪(涂膜)。
1,TCI;2,J&K;丁基锂,叠氮钠,二(三甲基硅基)氨基钠(NaHMDS),红铝和二氧六环,Acros;苄溴,双氧水,草酰氯和四氯化锡,aladdin;薄层层析板和柱层析硅胶,青岛海洋化工厂;其余所用试剂均为分析纯,其中溶剂使用前按标准方法除水。
1.2 合成
(1)3的合成
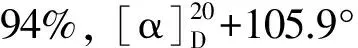
(2)4的合成

(3)(R)-5的合成

(4)(R)-6的合成
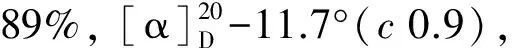
(5)(R)-7的合成

(6)(R)-8的合成
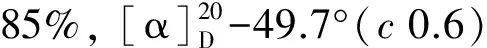
2 结果与讨论
2.16的合成
理论上,羧酸邻位的立体化学构建可以通过催化不对称烷基化的方法来构建,但一般情况下使用的羰基化合物为酯。这就需要在后续转化中,使用强碱来实现酯向羧酸的水解,在此过程中有可能导致羧酸邻位的手性中心消旋。为避免该问题,本文使用了手性助剂的策略,因为脱除噁唑烷酮是通过双氧水来实现的,在此过程中将有效避免了消旋化的发生。
2.2 Schmidt反应的立体化学
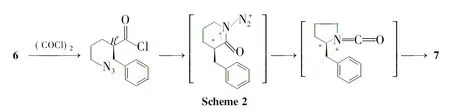
2辅助的烷基化反应产物5通过核磁检测,只发现单一构型产物,说明在此过程中立体化学得到了良好的控制。随即进行手性助剂的解离、原位酰氯化及Schmidt反应都有可能会对已经生成的立体化学中心产生影响。但最终我们检测到的酰胺产物7的ee值为92%,说明在这三步的转化过程中,只有4%的化合物发生了消旋化反应。通过比对最终还原产物8的旋光值,确定了酰胺7的立体构型为R,与引入的构型一致,说明在Schmidt反应过程中迁移基团的立体化学是基本得以保持(Scheme 2)。
3 结论
通过手性助剂——(S)-4-苄基-2-噁唑烷酮控制烷基化反应中新生成的羰基邻位碳的立体化学,成功制备了手性叠氮羧酸。然后通过原位制备的酰氯与烷基叠氮发生分子内的Schmidt反应,通过苯环对中间体处理,成功构建了手性酰胺结构。最后通过还原酰胺合成了天然产物中广泛存在的(R)-苯并吲哚里西定。
[1] Brenzovich,W E Jr,Benitez D,etal.Gold-catalyzed intramolecular aminoarylation of alkenes:C-C bond formation through bimolecular reductive elimination[J].Angew Chem Int Ed,2010,49:5519-5522.
[2] Cui M,Wang K,Wang Q,etal.Concise synthesis of benzoindolizidine derivatives and bioactivity evaluation[J].Lett Org Chem,2008,5:98-102.
[3] Osornio Y M,Miranda L D,Cruz-Almanza R,etal.Radical cyclizations to quinolone and isoquinolone systems under oxidative and reductive conditions[J].Tetrahedron Lett,2004,45:2855-2858.
[4] Pearson W H,Walavalkar R.Synthesis of (±)-tylophorine by the intramolecular cycloaddition of an azide with anω-chloroalkene[J].Tetrahedron,1994,50:12293-12304.
[5] Newcomb M,Esker J L.Facile production and cyclizations of amidyl radicals[J].Tetrahedron Lett,1991,32:1035-1038.
[6] Gu P,Kang X Y,Sun J,etal.Intramolecular schmidt reaction of acyl chlorides with alkyl azides:Rapid access to fused polycyclic nitrogen-containing heterocycles via a multistep one-pot transformation[J].Org Lett,2012,14:5796-5799.
[7] Gu P,Sun J,Kang X Y,etal.A formal metal-freeN-arylation via the Schmidt reaction of aromatic aldehydes with an azido amine[J].Org Lett,2013,15:1124-1127.
[8] Yi M,Gu P,Kang X Y,etal.Total synthesis of (±)-antofine[J].Tetrahedron Lett,2014,55:105-107.
[9] MacDonald M,Velde D V,Aubé J.Effect of progressive benzyl substitution on the conformations of aminocaproic acid-cyclized dipeptides[J].J Org Chem,2001,66:2636-2642.
[10] Garclía D,Foubelo F,Yus M.Reductive ring-Opening of phthalan and isochroman:Application to the stereoselective synthesis of tetrahydroisoquinolines and tetrahydrobenzazepines[J].Eur J Org Chem,2010,2893-2903.
Synthesisof(R)-benzoindolizidinebyIntramolecularSchmidtReactionofω-AzidoAcylChloride
LI Xiao-jing, WANG Bao-juan,KANG Xiao-yan,GU Pei-ming,LI Xue-qiang
(Ningxia Key Laboratory of Energy Sources &Engineering,Department of Chemistry,Ningxia Engineering Research Center for Natural Medicines,Ningxia University,Yinchuan 750021,China)
The chiral amide(3)was prepared by amidation of 5-bromopetanoyl chloride with the chiral auxiliary (S)-(-)-4-benzyl-2-oxazolidinone.The azido carboxylic acid[(R)-6] was synthesized by reaction of 3with sodium azide,then introducing of benzyl and removel of the auxiliary.Treatment of (R)-6with oxalyl chloride followed with stannic chloride gave the benzo fused lactam[(R)-7] in good yield with 92%ee.(R)-benzoindolizidine with the yield of 85% was synthesized by reudction of (R)-7with red aluminum.The total yield was 40.6%.The structure was confirmed by1H NMR,13C NMR and IR.
Schmidt reaction;benzoindolizidine;synthesis;azide;stereochemistry
2014-03-20
国家自然科学基金资助项目(21062014)
李晓静(1988-),女,汉族,宁夏石嘴山人,硕士研究生,主要从事有机合成的研究。Tel.0951-2062274,E-mail: lixiaojing0111@163.com
李学强,教授,E-mail: lixq@nxu.edu.cn
O626.3;O621.3
A
1005-1511(2014)05-0647-04

