香芍疏肝口服液质量标准研究
★ 毕晓黎 彭丽诗 李素梅
(1.广东省中医药工程技术研究院 广东 广州 510095;2.广州中医药大学 广东 广州 510405)
香芍疏肝口服液由香附、白芍、柴胡等中药组成,具有疏肝解郁、利胆和胃、理气健脾、燥湿化痰的功效。在临床上常用于肝气不疏、脾胃壅滞导致的慢性胃炎、胃溃疡、胆囊炎、胆囊结石等疾病。为了更好地控制其内在质量,保证临床用药安全有效,本文采用薄层色谱法对处方中的香附、白芍和柴胡进行了定性鉴别,采用高效液相色谱法对处方中所含的芍药苷进行了含量测定。
1 仪器与试药
1.1 仪器 Agilent 1200高效液相色谱仪(美国);DAD检测器;CAMAG TLC SAMPLER 4型全自动薄层点样仪(瑞士);CAMAG Reprostar 3型薄层成像系统(瑞士);Mettler XS205DU电子分析天平(瑞士);KQ5200 DE型数控超声波清洗器(昆山);电热恒温水浴槽(上海);DHG-9070A型电热恒温鼓风干燥箱(上海)。
1.2 试药 香附对照药材(批号:121059-200706)、白芍对照药材(批号:120905-200508)、柴胡对照药材(批号:120992-200504)、芍药苷对照品(批号:110736-201035)均购于中国药品生物制品检定所;香芍疏肝口服液(批号:120907、120908、1210909,由广东省第二中医院制剂室提供)。
2 薄层色谱定性鉴别
2.1 香附定性鉴别 取本品10mL,加乙酸乙酯振摇提取2次,每次30mL,合并乙酸乙酯液,蒸干,残渣加甲醇1mL溶解作为供试品溶液。另取对照药材2g,加水30mL,微沸30min,滤过,同法制成对照药材溶液。取缺香附药材的阴性样品,同供试品溶液制备法制成香附阴性对照溶液。照薄层色谱法(《中国药典》2010年版一部附录Ⅵ B)试验,吸取上述三种溶液各10μL,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-异丙醇-甲酸(7∶3∶0.1∶0.1)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,105℃加热约3min,放置5min后置紫外光灯(365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,阴性对照无干扰,见图1。
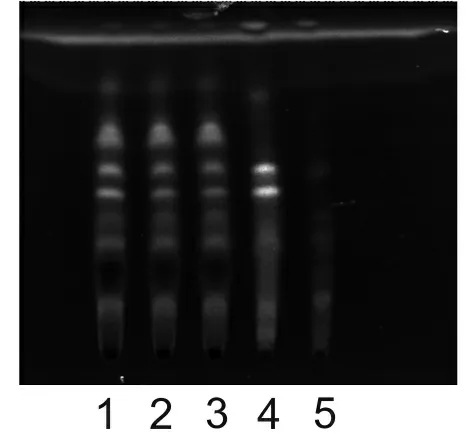
1~3、供试品溶液;4、香附对照药材溶液;5、香附阴性对照溶液
2.2 白芍定性鉴别 取本品5mL,加于大孔树脂柱(内径1cm,高10cm),先加水100mL洗脱,弃去洗脱液,后用20%乙醇100mL洗脱,收集洗脱液,蒸干,残渣加甲醇1mL使溶解,作为供试品溶液。另取白芍对照药材1g,加水20mL,煮沸30min,滤过,滤液浓缩至5mL,同法制成对照药材溶液。再取芍药苷对照品,加甲醇制成每1mL含1mg的溶液,作为对照品溶液。取缺白芍药材的阴性样品,同供试品溶液制备法制成白芍阴性对照溶液。照薄层色谱法(《中国药典》2010年版一部附录Ⅵ B)试验,吸取对照品溶液和对照药材溶液各5μL,供试品溶液和阴性对照溶液各10μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,在105℃加热至斑点清晰。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点,阴性对照无干扰,见图2。
2.3 柴胡定性鉴别 取本品20mL,加水饱和正丁醇振摇提取2次,每次30mL,合并正丁醇液,再用氨试液洗涤2次,每次30mL,弃去氨试液,合并正丁醇液,蒸干,残渣加甲醇1mL溶解即得。另取1g对照药材,同法制得对照药材溶液。取缺柴胡药材的阴性样品,同供试品溶液制备法制成柴胡阴性对照溶液。照薄层色谱法(《中国药典》2010年版一部附录Ⅵ B)试验,吸取上述三种溶液各10μL,分别点于同一硅胶G薄层板上,以正丁醇-乙酸乙酯-稀氨水(1→10)(4∶1∶5)上层溶液为展开剂,另槽用氨水饱和,展开,取出,晾干,喷以1%对二甲氨基苯甲醛的10%硫酸乙醇溶液,105℃加热至斑点清晰,置紫外光灯(365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,阴性对照无干扰,见图3。
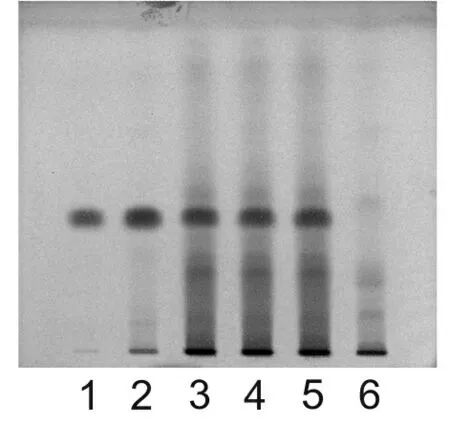
1、芍药苷对照品溶液;2、白芍对照药材溶液;3~5、供试品溶液;6、白芍阴性对照溶液
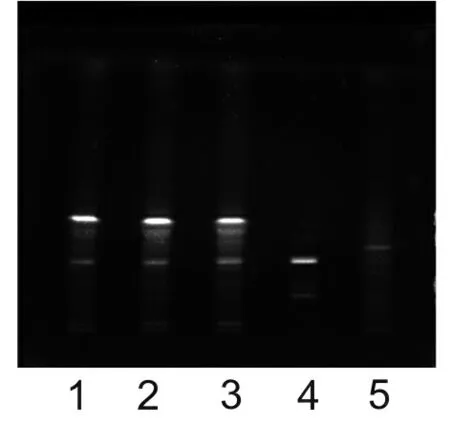
1~3、供试品溶液;4、柴胡对照药材溶液;5、柴胡阴性对照溶液
3 芍药苷含量测定
3.1 色谱条件 色谱柱:Agilent Extend C18柱(4.6mm×250mm,5μm);流动相:甲醇-0.2%磷酸水溶液(35∶65);检测波长:230nm;流速:1.0mL/min;柱温:25℃。理论板数按芍药苷峰计算应不低于2000。
3.2 对照品溶液的制备 精密称取芍药苷对照品适量,加甲醇制成每1mL含115.4μg的溶液,即得。
3.3 供试品溶液的制备 精密量取本品5mL,水浴蒸干,残渣用甲醇定容至10mL,微孔滤膜(0.45μm)滤过,取续滤液作为供试品溶液。
3.4 阴性对照溶液制备 按处方比例,取缺白芍的其他各味药,按制备工艺制成白芍阴性样品,再按“3.3”项下方法制成白芍阴性对照溶液。
3.5 测定 分别精密吸取上述对照品溶液、供试品溶液、白芍阴性对照溶液各10μL,注入液相色谱仪,在上述色谱条件下测定,见图4。结果显示,在上述色谱条件下,芍药苷与其他峰分离度较好,阴性对照无干扰。
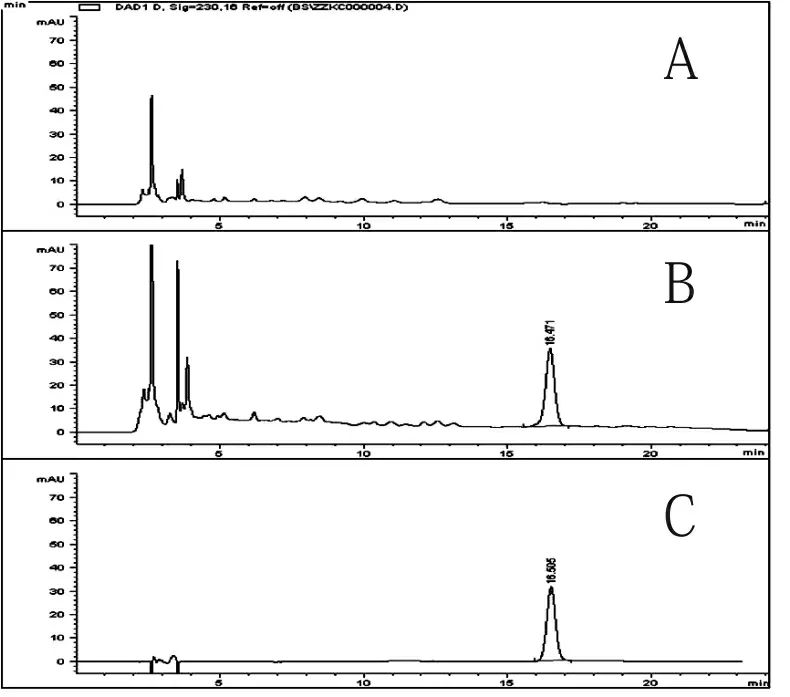
A.白芍阴性对照溶液;B.供试品溶液;C.芍药苷对照品溶液
3.6 线性关系考察 精密吸取芍药苷对照品溶液(115.4μg/mL)2,4,6,8,10μL进行测定,按上述色谱条件测定峰面积,并以峰面积(Y)对芍药苷含量(X)进行回归,得标准曲线:Y=23.5629X+1.0045,r=0.9999,表明芍药苷在0.2308~1.1540μg范围内线性关系良好。
3.7 精密度试验 精密吸取芍药苷对照品溶液(115.4μg/ml)10μL注入液相色谱仪,重复进样6次,测得其峰面积RSD值为0.35%,表明仪器精密度良好。
3.8 重现性试验 取供试品(批号:120907)5份,分别按照“3.3”项下方法制备供试品溶液,并按照上述色谱条件进行测定,结果芍药苷平均含量为0.2051mg/mL,RSD=0.87%,表明该方法重现性好。
3.9 稳定性试验 分别精密吸取同一份供试品溶液(批号:120907),分别于0,2,4,8,12h进样10μL,按“3.1”项下色谱条件进行测定,结果芍药苷峰面积RSD=0.69%,表明供试品溶液在12h内稳定性良好。
3.10 加样回收试验 精密称取9份已知含量的样品(批号:120907),分别精密加入一定量的芍药苷对照品,按“3.3”项下供试品制备方法处理,按“3.1”项下色谱条件进行测定,计算回收率,结果见表1。
3.11 供试品测定结果 分别精密吸取对照品溶液与供试品溶液各10μL,注入液相色谱仪,测得三批样品中芍药苷的含量,结果见表2。
4 讨论
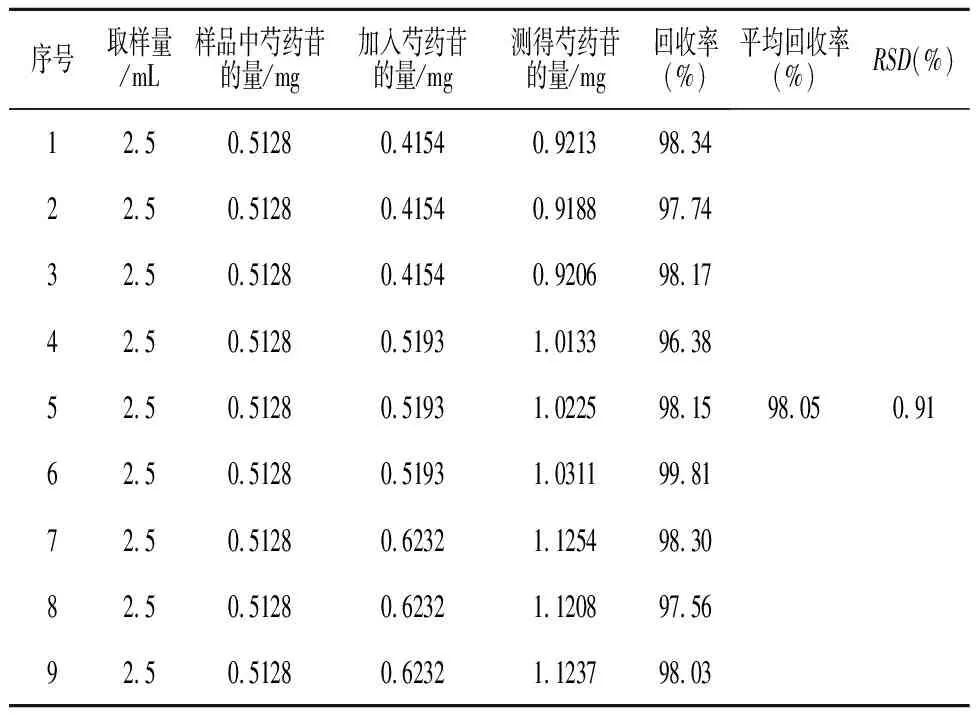
表1 芍药苷加样回收率试验结果(n=9)

表2 样品含量测定结果(n=3)
4.1 对方中香附进行薄层鉴别时,按照药典中香附的TLC鉴别方法[1],但由于香芍疏肝口服液的制备工艺为水提,而α-香附酮为脂溶性物质,难以提取出来,故供试品色谱中与对照品色谱无对应斑点。在参考文献中多种鉴别方法后[2,3],采用上述方法进行鉴别,且结果斑点清晰,分离效果好,且阴性无干扰。
4.2 对方中白芍进行薄层鉴别时,按照药典中白芍的鉴别方法[1],结果背景较深,拖尾严重,无法清晰鉴别,故参考了文献中多种方法[4,5],对供试品进行进一步的纯化处理,结果斑点清晰,分离度高,且阴性无干扰。
4.3 对方中柴胡进行薄层鉴别时,按照药典中柴胡的鉴别方法[1],发现阴性有干扰,在参考文献中多种鉴别方法后[6],采用上述方法进行鉴别,结果方法可行,且阴性无干扰。
4.4 芍药苷的含量测定方法,是在参考文献中芍药苷的多种含量测定方法之后[7],再对流动相进行调整而建立的,通过方法学验证,该法准确、可靠,可作为香芍疏肝口服液中苦芍药苷的含量测定方法。
4.5 本文所建立的方法操作简便、灵敏度高、准确可靠、重现性好,可作为香芍疏肝口服液的质量控制方法。
[1]国家药典委员会.中国药典﹒一部[S].北京:中国医药科技出版社,2010:241,96,263.
[2]翁燕,刘志辉.痛经合剂质量标准研究[J].中国中医药信息杂志,2011,18(8):52-54.
[3]阿古拉,张兆旺,王芳.慈航软胶囊质量标准研究[J].中成药,2009,31(7):1 044-1 048.
[4]高展,孙玉侠,阚红玉,等.养血清脑颗粒质量标准研究[J].广东药学院学报,2011,27(5):483-488.
[5]沈洁,任世禾.复方银杏叶胶囊质量标准的研究[J].上海中医药杂志,2007,41(6):79-81.
[6]叶延程,赵良存.乳康胶囊质量标准研究[J].中国实验方剂学杂志,2012,18(13):125-128.
[7]谢清春,吕竹芬,陈燕忠.补肺活血胶囊中芍药苷的含量测定[J].中药材,2012,35(8):1 335-1 336.

