miRNA-30b纳米粒转染对甲状腺未分化癌细胞系TA-K细胞生物学特性的影响
姚廷敬,张 晖,彭德峰,朱正志,马小开,周 锐,朱金海,崔 振,王岩岩
甲状腺未分化癌是甲状腺中少见的恶性肿瘤,发病率不超过甲状腺癌的5%,但病死率却占甲状腺癌的50%,甲状腺未分化癌恶性程度高、预后差、死亡率高给患者的生活质量带来的具大的威胁[1],因此,对于甲状腺未分化癌的研究将为临床诊治、判断预后等提供充足的理论基础;microRNA是一类非编码的小分子RNA,其通过在转录后水平与靶分子的mRNA结合达到调控蛋白表达的目的,在以往的研究中已证实microRNA几乎参与了肿瘤的发生、发展、转移等所有生物学活动[2],但是当前对于microRNA与甲状腺未分化癌的研究仍相对较少。因此本研究旨在通过纳米粒转染技术,以探究miRNA-30b对甲状腺未分化癌细胞系TA-K细胞生物学特性的影响。
1 材料与方法
1.1材料 异佛尔酮二异氰酸酯、氯仿、聚醚酰亚胺(PEI)购至上海伍林化工有限公司;miRNA-30b序列、Caspase-3上下游引物由上海生工公司合成;TA-K细胞购至上海索莱宝生物科技有限公司;Lipofectamine 2000转染试剂购至Invitrogen公司;Survivin(Biolegend)抗体购于上海科谨生物科技公司。
1.2方法
1.2.1miRNA-30b纳米粒的制备 将mPEG与过量的异佛尔酮二异氰酸酯(IPDI)溶于氯仿,经过催化、沉淀、干燥等得到异氰酸醋单端基聚乙二醇,然后将其加入至含PEI的氯仿中,加热、沉淀,过滤、干燥得到PEG-PEI嵌段共聚物;化学合成miRNA-30b序列,将PEG-PEI纳米共聚物与miRNA-30b复合形成负载miRNA-30b的PEG-PEI纳米粒。Annexin V/PI试剂盒(法国国际免疫公司)。流式细胞仪(FACScan型美国BD公司)。
1.2.2miRNA-30b纳米粒转染TA-K细胞 应用脂质体在lipofectamine2000条件下转染miRNA-30b纳米粒至甲状腺未分化癌细胞系TA-K细胞,其方法如下:细胞铺板含血清2 ml,密度为90%~95%,每孔细胞,使用250 ul无血清培养基(如OPTI-MEM I培养基)稀释4.0 ugmiRNA-30b纳米粒,轻轻混匀;和稀释的Lipofectamine 2000,室温放置20 min。将6孔板中的旧营养液吸出,用无血清培养基清洗2次。加入2 ml无血清配养基。直接将复合物加入到每孔中,摇动培养板,轻轻混匀。
1.2.3miRNA-30b纳米转染后TA-K细胞凋亡程度的检测 使用Annexin V/PI法检测TA-K细胞的凋亡程度,取2×106个细胞加入5 μl FITC-Annexin V及5 μl PI(浓度250 μg/ml),混匀置冰浴暗处温育10 min,PBS洗2遍,流式细胞仪分析;光源为488 nm氩离子激光器,FITC受激发后发绿色荧光,PI发红色荧光,每份标本收集10 000个细胞,然后在Macintosh650计算机上用相关软件分析数据。
1.2.4miRNA-30b靶基因的预测、验证及功能研究 在microRNA靶点预测数据库(miR.org)中预测miRNA-30b的靶点,发现Survivin是miRNA-30 b潜在的生物学靶点;转染miRNA-30 b纳米粒收集RNA后,使用RT-PCR方法检测survivin,上游引物为5-ggaccaccgcatctctacat-3、下游引物为3-tccagctccttgaagcagaa-5,反应程序设置为:预变性95 ℃ 10 min,95℃ 15 s,60 ℃ 30 s,72℃ 60 s,30个循环,最后72℃ 10 min延伸;收集转染miRNA-30b后的TA-K细胞,裂解并收集蛋白用Western-blot方法检测Caspase-3的蛋白表达水平,步骤如下:SDS-PAGE电泳分离蛋白,转膜后加入人Caspase-3抗(按合适稀释比例用0.01M PBS稀释,液体必须覆盖膜的全部),4℃放置12 h以上后用PBS分别洗膜4次,每次5 min,后加入辣根过氧化物酶偶联的二抗(按合适稀释比例用0.01 M PBS稀释),平稳摇动,室温2 hr,弃二抗,PBS分别洗膜4次,每次5 min,加入显色液,进行显色反应,在凝胶成像仪扫描成像;β-actin为对照组。
1.3统计学方法 对于转染miRNA-30b及空白脂质体后TA-K细胞凋亡比例及survivin的表达水平的分析,先用Shapiro-Wilk Test 及Levene' s Test判断2组数据是否正态分布及方差是否齐性,满足正态分布及方差齐性后采用均值±标准差进行表示子宫肿瘤的体积,并采用配对样本t检验检验判断两者间差异是否具有统计学意义,否则使用非参秩合检验;以上所有统计过程均在SPSS18.0中完成,检验水准均为0.05。
2 结果
2.1miRNA-30b纳米粒对于TA-K细胞凋亡的影响 在本研究中,我们转染了不同浓度的miRNA-30b纳米粒(50 nM、100 nM、200 nM)进入TA-K细胞中,通过Annexin V/PI法检测2组中、凋亡细胞比例是否有统计学差异;正常细胞FITC及PI均低染,凋亡细胞FITC高染而PI低染,死亡细胞FITC及PI均高染,所以我们对FITC阳性、PI阴性的细胞进行流式分析统计发现,结果如表1所示,在转染miRNA-30b纳米粒后,TA-K细胞的凋亡比例显著上调,并随着转染浓度的增加,TA-K细胞凋亡比例也随之上调,说miRNA-30b能够促进TA-K肿瘤细胞的凋亡。见表1。
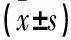
表1 转染miRNA-30b后TA-K细胞与对照组的凋亡比例比较
注:*为转染miRNA-30b纳米粒后与对照组比较,2组间凋亡细胞比均成正态分布、方差齐性,使用两独立样本t检验。
2.2miRNA-30b靶点的预测与RT-PCR验证 通过在miRNA.org靶点预测数据库中发现,miRNA-30b与Survivin的3-UTR区可以特异性结合,而Survivin是细胞凋亡过程中的抑制凋亡因子,故推测miRNA-30b可能通过负向调控Survivin的表达促进TA-K细胞的凋亡;随后,我们对miRNA-30b与Survivin的靶向关系进行了验证,首先转染不同浓度的miRNA-30b进入TA-K细胞后使用RT-PCR的方法检验Survivin的表达水平,如表2所示,转染miRNA-30b后TA-K细胞的Survivin的表达水平显著低于对照组,且随着miRNA-30b浓度的增加,Survivin的表达也逐渐下降。见表2。
表2 转染miRNA-30b后TA-K细胞与对照组的Survivin表达水平的比较
注:*为转染miRNA-30b纳米粒后与对照组比较,Survivin表达水平成正态分布、方差齐性,独立样本t检验。
2.3miRNA-30b靶点Survivin的western-blot验证 miRNA与靶点之间的相互作用主要体现在蛋白水平上,所以蛋白水平的改变也是检测两者靶向关系的金标准;按上述方法,转染miRNA-30b(200nM)进入TA-K细胞中,于72 h收集蛋白,进行western-blot检测,如图1所示,在转染miRNA-30b纳米粒后TA-K细胞中的survivin蛋白表达水平显著下调,说明Survivin确实是miRNA-30b的生物学靶点。
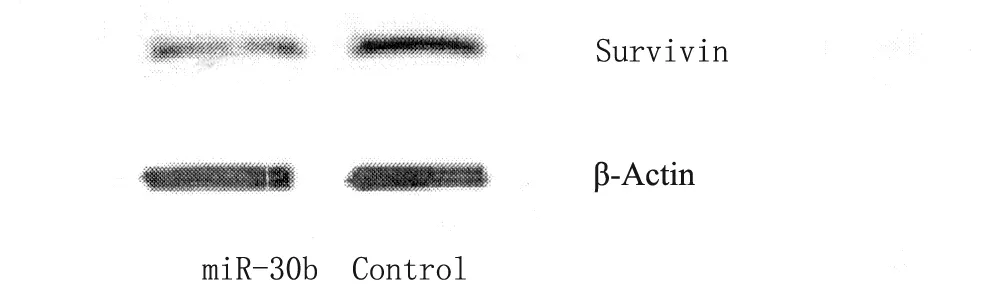
Figure: the result of Western Blot图1 Western blot结果
3 讨论
甲状腺未分化癌是甲状腺中较为少见的恶性肿瘤,发病率较低,但恶性程度高、病死率高。甲状腺未分癌通常病程发展迅猛,确诊时已侵犯周围的组织器官,如气管、食管、血管、肌肉等,且有一半左右的患者在诊断时已有远处转移,此时即使给予积极的治疗,仅少患者能够长期生存,大部分患者在短时间内死亡,一般从确认到死亡中位生存期仅4~8个月[3-4]。由于甲状腺未分化癌手术、放疗、化疗疗效均较差,所以探讨甲状腺未分化癌的具体发病机制以及探索新的治疗策略对于甲状腺未分化癌十分重要。
microRNA,是一类内源性的短序列非编码RNA,其主要功能是在转录后水平参与靶基因的调控,它几乎参与机体所有的生物学活动,被认为是肿瘤表观遗传学中的重要一环;尽管近来随着肿瘤生物学的发展,人们对肿瘤的发生、发展的理解得到了不断的加深,但是对于其具体的发病机制还不是十分清楚,当前仍缺少能被广泛接受的、十分有效的肿瘤标记物用于甲状腺未分化癌的诊断、治疗以及预后判断[5];在甲状腺未分化癌中存在许多异常表达的microRNA,这些microRNA参与了肿瘤的生长、分化、浸润以及转移等过程,而这些异常microRNA的发现为进一步研究该类肿瘤提供了新的思路,某些特异的microRNA也将成为肿瘤诊疗的新的策略。
本研究中,我们发现转染了miRNA-30b纳米粒后TA-K细胞的生物学特性发生改变,即TA-K细胞凋亡增加,且随着纳米粒的转染浓度的增加,凋亡的比例也随之增加;因此,本研究证实,miRNA-30b可以促进TA-K肿瘤细胞的凋亡;而对于miRNA-30b促进肿瘤细胞凋亡的具体机制,我们发现Survivin在该过程中发挥着重要作用,同样在转染miRNA-30b后,TA-K细胞内的Survivin的表达水平显著下调,随后Western blot检查证实在蛋白水平上miRNA-30b可以负向调控Survivin的表达;所以,miRNA-30b可以通过下调Survivin的表达促进TA-K细胞的凋亡。Survivin是凋亡抑制蛋白家族的新成员,Survivin具有肿瘤特异性,只表达于肿瘤和胚胎组织,且与肿瘤细胞的分化增殖、浸润转移以及预后密切相关[6],本研究中使用的miRNA-30b可以很好作用于TA-K细胞中Survivin分子,为临床治疗甲状腺未分化癌提供了新的思路。此外,在当前的一些研究中,已经证实miRNA-30b在其它肿瘤如食管癌、胶质瘤中表达均显著异常,在食管癌中研究发现miRNA-30b的表达水平显著下调,说明在食管癌细胞中miRNA-30b表达低于正常组织,其促进肿瘤细胞凋亡的作用减弱可能是导致肿瘤生成的重要原因之一[7];而在胶质瘤中,研究发现miRNA-30b与Trail诱导的肿瘤细胞凋亡有关[8],进而说miRNA-30b与肿瘤细胞凋亡密切相关。
本研究发现miRNA-30b可以通过作用Survivin促进TA-K细胞的凋亡,这一现象也为将来甲状腺未分化癌的临床治疗提供了新的思路,而对于miRNA-30b在甲状腺未分化癌中具体作用机制仍需要进一步阐明。
【 参 考 文 献 】
[1] Dackiw AP.Anaplastic thyroid cancer[J].Cancer Treatment Research,2010,153:75-84.
[2] Bushati N,Cohen SM.MicroRNA functions[J].Annu Rev Cell Devl Biol,2007,23:175-205.
[3] Baroli A,Pedrazzini L,Lomuscio G,et al.Anaplastic thyroid carcinoma.Practical aspects of multimodal therapy and data emerging from a 40-year experience at a single Italian institution[J].Minerva Endocrinol,2010,35(1):9-16.
[4] Deshpande HA,Roman S,Sosa JA.New targeted therapies and other advances in the management of anaplastic thyroid cancer[J].Curr Opin Oncol,2013,25(1):44-49.
[5] Gomes CC,de Sousa SF,Gomez RS.MicroRNAs:small molecules with a potentially role in oral squamous cell carcinoma[J].Curr Pharm Des,2013,19(7):1285-1291.
[6] Rodel F,Sprenger T,Kaina B,et al.Survivin as a prognostic/predictive marker and molecular target in cancer therapy[J].Curr Med Chem,2012,19(22):3679-3688.
[7] Liu SG,Qin XG,Zhao BS,et al.Differential expression of miRNAs in esophageal cancer tissue[J].Oncol Lett,2013,5(5):1639-1642.
[8] Quintavalle C,Donnarumma E,Iaboni M,et al.Effect of miR-21 and miR-30b/c on TRAIL-induced apoptosis in glioma cells[J].Oncogene,2013,32(34):4001-4008.

