肾脏炎性肌纤维母细胞瘤1例并文献复习
李泽宇,王伟刚,周洪澜,王远涛,傅耀文
(吉林大学第一医院 泌尿系统疾病诊治中心,吉林 长春130021)
炎性肌纤维母细胞瘤(inflammatory myofibroblastic tumor,IMT)被世界卫生组织定义为“由分化的肌纤维母细胞性梭形细胞组成的,常伴大量浆细胞和( 或) 淋巴细胞的一种肿瘤”,属于软组织肿瘤中的间叶性肿瘤[1]。IMT以肺部多见,在泌尿生殖系统中以膀胱IMT多见,肾脏IMT极为罕见[2]。2012年8月我科收治了1例女性肾脏IMT患者,现报道如下。
1 临床资料
1.1 病历资料
患者,女,48岁,因“检查发现左肾占位1个月”于2012年8月19日入院。无特殊症状。查体:贫血貌,左肾区叩痛阳性。血常规:白细胞2.85×109/L,血红蛋白56 g/L,血小板67×109/L;尿常规:白细胞20.1/HPF,红细胞2.5/HPF;凝血常规:凝血酶时间19.4s,凝血酶原时间14.0 s,国际标准化比值1.21,凝血酶原时间比值1.22,凝血酶原活动度69%,纤维蛋白原1.55 g/l;乙肝表面抗原197.260IU/ML,乙肝e抗原0.299S/CO,乙肝e抗体0.110S/CO,乙肝核心抗体18.210S/CO。腹部彩超:左肾上极实质内见一等回声实质性肿物,大小约1.4 cm×1.1 cm,边界不清,向肾表面凸出,其内无血流信号。MRI:左肾上极见类圆形混杂信号影,大小约2.6 cm,T1WI呈稍低、低信号,T2WI呈高、稍低信号,边缘模糊。肾脏增强CT:左肾上极可见一大小约1.6 cm×2.9 cm的低密度影,与左侧膈肌、腹膜分界欠清,增强扫描略有强化,呈相对低强化影。患者既往“乙型病毒性肝炎”病史20余年,左侧季肋部外伤史13年。
1.2 治疗经过及术后病理
患者临床诊断为:左肾肿瘤、乙型病毒性肝炎、肝硬化、脾功能亢进。给予输血、抗病毒、保肝及纠正凝血等治疗后,在全麻下行后腹腔镜下左肾根治性切除术,术中见左侧肾脏上极一大小约2 cm×1.5 cm×1.0 cm的肿瘤,与腰大肌和腹膜、脾脏粘连明显,术后切开左肾,见肿瘤呈淡褐色,切面实性,质略硬。术后病理:炎性肌纤维母细胞瘤(图1)。免疫组化(图2):Ki-67(+5%),Desmin(局灶弱+),SMA(部分+),Vimentin(+),ALK(—),S-100(—)。术后患者恢复顺利,随访7个月,未见肿瘤复发及转移。

图1 病理切片:a.HE×100;b.HE×200
病理可见短梭形瘤细胞呈束状或编织状排列,未见明显核分裂象,伴有大量浆细胞及淋巴细胞浸润。
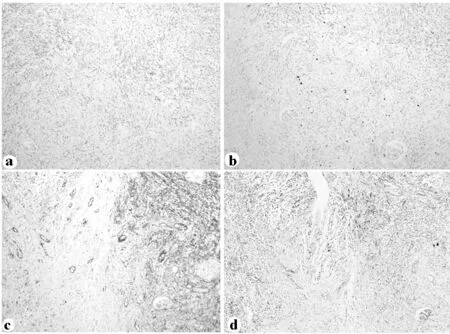
图2 免疫组化(×100)
a.肿瘤细胞Desmin呈阳性表达;b.肿瘤细胞Ki-67呈阳性表达;c.肿瘤细胞SMA呈阳性表达;d.肿瘤细胞Vimentin呈阳性表达。
2 讨论
IMT最早被发现于肺部,当时被认为是修复炎症后的病变,而非真性肿瘤,但随着相关遗传学和分子生物学的进展,如ALK融合基因及非整倍体瘤细胞的发现,并对大量的肺外组织器官IMT的临床、病理、预后进行研究,IMT逐渐被认为是一种真性肿瘤。IMT好发于儿童与青少年,部分呈侵袭性增长,可局部复发或转移[3]。
2.1 病因及发病机制
肾脏IMT的病因及发病机制目前尚不是很清楚,随着相关研究的不断深入,ALK基因融合在IMT的发生发展过程中扮演着重要角色。ALK基因位于2p23,编码一种大小为200kDa的酪氨酸激酶受体,该受体属于胰岛素受体超家族,主要表达于正在发育的神经系统,在成人的神经系统很少表达[4]。目前已在多数IMT中检测出了ALK基因融合现象,当ALK基因与其配偶体基因融合后,其表达的ALK融合蛋白类似于配偶体的表达产物直接与该酪氨酸激酶的胞内催化域结合,从而使ALK受体的活性持续存在,持续发挥其抑制细胞凋亡的作用,致其恶性转化[5]。
值得注意的是,并不是所有IMT都表达ALK,亦有阴性表达。查阅相关文献,有将近50%的IMT不表达ALK融合蛋白,而在不表达ALK融合蛋白的IMT中部分可见非整倍体瘤细胞,有些IMT的ALK阴性且非整倍体瘤细胞也为阴性。研究认为ALK阴性但有非整倍体瘤细胞的IMT可能意味着其生长更具有侵袭性, ALK阴性且非整倍体瘤细胞也为阴性的IMT可能意味着不同的发病机制,或者存在还尚未发现的其他的基因融合[3,5,6]。
对于本病例,其ALK阴性,可能意味着其发病机制更为复杂,需要进一步的研究。该患者有乙型病毒性肝炎和左侧季肋部外伤病史,且乙型病毒性肝炎病程较长,已发展为肝硬化、脾功能亢进、凝血功能障碍,这些因素都可能在本例肾脏IMT的发生及发展中起到了重要作用。
2.2 临床表现与组织病理
肾脏的IMT的临床表现是多种多样的,Kapusta等曾对发生于肾实质(4例)、肾盂(6例)、肾周软组织(2例)的共12例IMT进行总结,其中2例表现为腰腹部疼痛,1例表现为无痛性全程肉眼血尿,1例表现为伴有肾积水的肾盂输尿管连接处狭窄,8例无相应临床症状[7]。本例患者亦无相应临床症状,为偶然发现。
在大体标本上,IMT可表现为局限性或多结节性,质地硬,颜色为白色或黄褐色,切面可为轮生状,肉质样,纤维性变样或粘液胶冻样,在大多数病例中,表面可见出血和坏死区[8]。关于其组织病理学特点,Coffin等将其分为三类:(1)梭形的肿瘤细胞穿插于水肿及粘液样变的间质中;(2)肿瘤细胞常排列规则,在梭形的肿瘤细胞之间见浆细胞浸润,其他炎性细胞常成堆聚集;(3)梭形的肿瘤细胞稀疏,大量浆细胞和淋巴细胞浸润于胶原纤维之间[9]。本病例属于Coffin描述的第二种类型(如图1)。
2.3 临床诊断
对于肾脏IMT的诊断,根据患者的病史、体征及相关的辅助检查结果,术前难以确诊。其影像学表现缺乏特异性,尤其难与肾细胞癌鉴别,容易被误诊。Bektasa等2007年曾经报道一例被误诊为肾细胞癌的病例[10]。而经CT引导下穿刺活检,由于组织较少,阳性率较低,故其确诊主要依靠术后病理及免疫组化[11]。
2.4 治疗方法及预后
当前IMT被认为是真性肿瘤,低度恶性,有复发和转移的风险,所以肾脏根治性切除术为目前首选的治疗方案,且术后预后多良好,即使有不手术而使用激素治疗有效的报道[12]。Kapusta等曾对发生于肾脏不同部位的8例IMT患者进行随访,8例患者均行根治性肾切除术,随访时间为1-17年,均未复发[7]。Erics等曾报道一例侵及结肠,并且与腰大肌和十二指肠分界不清的肾细胞癌合并IMT的病例,行根治性肾切除术和右半结肠切除术,术后随访12个月,未见复发[6]。免疫组化ALK阳性与否可能与患者的预后有一定的关系,因为有学者报道,部分ALK阳性的患者预后较好[6,13]。
随着ALK融合基因的发现,针对它的靶向治疗将带来新的治疗思路,如酪氨酸激酶抑制剂,以病毒为载体的RNA干扰技术等[4]。尤其对那些孤立肾或者肾功能不全的患者,此种治疗方法更具有意义,相信在不久的将来定能实现。
参考文献:
[1]Fletcher CDM,Unni KK,Mertens F.World Health Organization classification of tumoursPathology and genetics of tumours of soft tissue and bone [M].Lyon:IARC Press,2002:48.
[2]Harik LR,Merino C,Coindre JM,et al.Pseudosarcomatous myofibroblastic proliferations of the bladder:a clinicopathologic study of 42 cases [J].Am J Surg Pathol,2006,30(7):787.
[3]Gleason BC,Hornick JL.Inflammatory myofibroblastic tumours:where are we now[J].J Clin Pathol,2008,61(4):428.
[4]Kelleher FC,McDermott R.The emerging pathogenic and therapeutic importance of the anaplastic lymphoma kinase gene [J].European Journal of Cancer,2010,46(13):2357.
[5]Coffin CM,Patel A,Perkins S,et al.ALK1 and p80 Expression and Chromosomal Rearrangements Involving 2p23 in Inflammatory Myofibroblastic Tumor [J].Mod Pathol,2001,14(6):569.
[6]Chan JK,Cheuk W,Shimizu M.Anaplastic Lymphoma Kinase Expression in Inflammatory Pseudotumors[J].Am J Surg Pathol,2001,25(6):761.
[7]Kapusta LR,Weiss MA,Ramsay J,et al.Inflammatory Myofibroblastic Tumors of the Kidney A Clinicopathologic and Immunohistochemical Study of 12 Cases [J].Am J Surg Pathol,2003,27(5):658.
[8]Gupta P,Dhingra KK,Singhal S,et al.Inflammatory myofibroblastic tumour of the kidney with a papillary adenoma[J].Pathology,2010,42(2):193.
[9]Coffin CM,Watterson J,Priest JR,et al.Extrapulmonary inflammatory myofibroblastic tumor (inflammatory pseudotumor):A clinicopathologic and immunohistochemical study of 84 cases [J].Am J Surg Pathol,1995,19(8):859.
[10]Bektasa S,Okuluc E,Kayigilc O,et al.Inflammatory myofibroblastic tumor of the perirenal soft tissue misdiagnosed as renal cell carcinoma [J].Pathol Res Pract,2007,203(6):461.
[11]Gwynn ES,Clark PE.Inflammatory myofibroblastic tumor associated with renal cell Carcinoma[J].Urology,2005,66(4):880.
[12]Williams ME,Longmaid HE,Trey G,et al.Renal failure resulting from infiltration by inflammatory myofibroblastic tumor responsive to corticosteroid therapy[J].Am J Kidney Dis,1998,31(6):E5.
[13]Chun YS,Wang L,Nascimento AG,et al.Pediatric inflammatory myofibroblastic tumor:anaplastic lymphoma kinase (ALK) expression and prognosis [J].Pediatr Blood Cancer,2005,45(6):796.

